1. DEFINICIÓN DEL SHOCK
El shock se define como una alteración de la circulación que provoca una inadecuada perfusión tisular generalizada, en la cual el aporte de oxígeno y nutrientes a nivel celular resulta insuficiente para satisfacer las demandas metabólicas de los órganos y tejidos.
El flujo sanguineo adecuado a los tejidos y las células requiere una bomba cardíaca eficaz, un volumen de sangre suficiente y una vasculatura adecuada. Si alguno de estos componentes se ve afectado, la perfusión a los tejidos se ve amenazada o comprometida.
Sin un diagnóstico e inicio de tratamiento precoz, el flujo sanguíneo inadecuado a las células da como resultado un estado de hipoxia y muerte celular, que progresará a disfunción orgánica, y finalmente a la muerte.
Un tercio de los pacientes que se admiten en una unidad de cuidados intensivos, ingresan en estado de shock. Y pese a los avances actuales en medicina, la mortalidad puede llegar a ser de hasta un 50%. Hasta el momento, la única variable que ha mostrado ser consistente en la disminución de la mortalidad, independientemente de la causa del shock, ha sido el reconocimiento y manejo precoz.
2. FISIOPATOLOGÍA Y FASES DEL SHOCK
El shock progresa a lo largo de un continuo y puede identificarse como temprano o tardío según los signos, sintomas y la gravedad general de la disfución orgánica que se haya producido. Cuanto antes se inicien las intervenciones a lo largo de este continuo, mayores serán las probabilidades de supervivencia del paciente.
Independientemente de la causa inicial que lo haya producido, ciertas respuestas fisiológicas son comunes a todos los tipos de shock. El cuerpo, responde a este estado mediante la activación del sistema nervioso simpático, y la instauración de una repuesta endocrina, hipermetabólica e inflamatoria.
En la evolución del shock se pueden distinguir tres fases:
2.1. Fase de shock compensado, caliente o pre shock
Esta etapa inicial se caracteriza por la aparición de mecanismos compensatorios que tienen por objetivo contrarestar la disminución de la perfusión tisular. Estos mecanismos pueden permitir que un adulto sano permanezca asintomático a pesar de haberse reducido un 10% el volumen circulante efectivo.
La disminución del volumen circulante efectivo, indistintamente de la causa que lo produzca, produce una disminución de la presión arterial (PA) y del gasto cardiaco (GC). Estas alteraciones, y su repercusión en la aparición de hipoxia tisular, son detectadas por baroreceptores y quimioreceptores situados en el arco aórtico y seno carotídeo, que alertan al sistema nervioso central para contrarestar esta situación. En consecuencia, se desencadena una respuesta simpático- adrenérgica que conduce a:
- La liberación de catecolaminas endogenas, producidas por la estimulación de la medula suprarenal, para tratar de preservar la perfusión de órganos vitales (corazón y sistema nervioso) a expensas de una vasocontricción de órganos no vitales (piel, músculo, riñón, tubo digestivo y área esplácnica).
- El incremento de la actividad simpática, produciéndose una mayor contractibilidad y frecuencia cardiaca para mantener el GC.
A su vez, los riñones regulan la PA activando el eje renina-angiotensina-aldosterona. La renina, producida por el riñón, es una enzima necesaria para generar angiotensina II, que produce un incremento de la PA por su efecto vasoconstrictor. Esta estimulación del mecanismo renina- angiotensina y la vasocontricción resultante, conducen indirectamente a la liberación de aldosterona desde la corteza suprarrenal, que promueve la retención de sodio y agua (produciendo hipernatremia). Este incremento de sodio, estimula la liberación de hormona antidiurética o vasopresina por parte de la hiposis, que actua en la resorción de agua a nivel renal. Como resultado de este mecanismo compensador se obtiene un mayor volumen circulante e incremento de la PA.
Además de los mecanismos compensatorios descritos, se produce un incremento de la frecuencia respiratoria (taquipnea) por activación simpática, en respuesta a la necesidad de incrementar el oxígeno en las células y compensar la acidosis metabólica resultante de la hipoperfusión. Esta taquipnea facilita la eliminación del exceso de dióxido de carbono (CO2), pero incrementa el PH de la sangre y a menudo causa una alcalosis respiratoria compensatoria.
Desde el punto de vista clínico, a pesar de una PA normal o ligeramente disminuida o aumentada por los mecanismos compensatorios, el paciente muestra numerosos signos clínicos que indican una perfusión inadecuada de los órganos. Podemos hallar: taquicardia, taquipnea, vasocontricción periférica con frialdad y palidez cutánea, sequedad de mucosas, debilidad muscular, oliguria y el paciente puede experimentar un cambio en el estado de ánimo, sintiéndose ansioso o confundido.
Si en este momento se actua contra la causa y se utilizan unas medidas terapéuticas adecuadas, el pronóstico para el paciente es más favorable que en las etapas posteriores.
2.2. Fase de shock descompensado o shock instaurado
Durante esta fase los mecanismos compensatorios descritos son insuficientes, la presión arterial media (PAM) cae por debajo de los límites normales y se empieza a disminuir el flujo a órganos vitales, apareciendo signos y sintomas de disfunción orgánica. Aunque todos los sistemas órganicos sufren de hipoperfusión en esta etapa, ocurren diversos acontecimientos que perpetúan el síndrome de shock.
Función celular normal y alteraciones a nivel celular
Las células necesitan oxígeno y glucosa para generar energía (ATP) a través del metabolismo aerobio, que posteriormente se metaboliza en agua y CO2. Si la causa del shock no se soluciona y persiste el estado de hipoperfusión e hipoxia celular, se pone en marcha una vía alternativa para generar energia apareciendo el metabolismo anaerobio, en ausencia de oxígeno, en el que la glucosa se metaboliza en forma de lactato.
El metabolismo anaerobio resulta menos eficiente, y lleva a la acumulación del ácido láctico como producto final tóxico, que debe eliminarse de la célula y transportarse al hígado para su conversión en glucosa y glucógeno. Ésta acumulación de ácido lactico, y la disminución de su metabolización por parte del hígado en el estado de shock, conduce a la aparición de alteraciones en el PH apareciendo acidosis metabólica e hiperlactacidemia, que agrava la situación del paciente.
A causa del bajo rendimiento energético y el entorno intracelular ácido, producido por el metabolismo anaeróbio, cesa la función celular normal dando paso a las siguientes alteraciones:
- La célula se hincha y la membrana celular se vuelve más permeable, permitiendo que tanto los electrolítos como el líquido se filtren hacia el interior, produciéndose un edema celular.
- La bomba de sodio y potasio se altera, favoreciendo la entrada de sodio y agua, y la salida de potasio.
- Las estructuras celulares, principalmente las mitocondrias (encargadas de la respiración celular), se dañan y se produce la muerte de la célula.
Alteraciones metabólicas
El cuerpo moviliza las reservas de energía y aumenta el consumo de oxígeno, para dar respuesta a las mayores necesidades metabólicas de los tejidos y las células, que se encuentran insuficientemente perfundidas.
En estados de estrés se liberan catecolaminas endogenas, glucagón, cortisol y mediadores inflamatorios bioquímicos, que provocan un incremento de la glicemia (a partir de la gluconeogénesis) y resistencia a la insulina para movilizar la glucosa para el metabolismo celular. Ante la falta de glucosa disponible para el metabolismo celular, el glucógeno almacenado en el hígado se convierte en glucosa a partir de la glucogenolisis, para satisfacer las necesidades metabólicas, incrementando la concentración de glucosa en sangre.
Nos encontramos en una situación en la que el metabolismo celular está deteriorado y esta respuesta contínua al estrés termina por agotar las reservas de glucógeno, conduciendo a la disfunción orgánica.
Cambios en la microcirculación y alteración en la coagulación
Por un lado, la función autorreguladora de la microcirculación falla en respuesta a los mediadores bioquímicos liberados por las células, lo que incrementa la permeabilidad capilar. A nivel capilar se produce además una relajación de los esfínteres precapilares, produciendose un escape de líquido de los capilares sanguineos hacia el intersticio, dando lugar a la aparición de edema instersticial (tercer espacio) y disminucion del retorno venoso.
Por otro lado, la acidosis produce una disfunción y lesión endotelial y celular significativa. En consecuencia, se activa la respuesta inflamatoria a la lesión y se produce una liberación de mediadores proinflamatorios y antiinflamatorios, que activan el sistema de coagulación en un intento por restablecer la homeostasis. En la situación de shock, la cascada de coagulación es superproductiva realizando una regulación al alza. Se producen pequeños coágulos que se alojan en la microcirculación de los tejidos, apareciendo trombosis microvascular, que dificultarán la distribución del flujo sanguineo a nivel de los capilares, agravándose la hipoperfusión celular.
La coagulación intravascular diseminada (CID) puede presentarse como causa o complicación del shock. El daño tisular producido, la respuesta inflamatoria generada y la trombosis microvasuclar secundaria, pueden conducir a la aparición de la CID. En esta afección, el sangrado y la coagulación generalizados ocurren simultáneamente. Pueden aparecer equimosis (hematomas) o hemorragias en la piel (petequias). Los tiempos de coagulación son prolongados, y los factores de coagulación y las plaquetas se consumen y precisan reemplazo para lograr la hemostasia.
Depresión miocárdica
El corazón con exceso de trabajo se vuelve disfuncional. La propia hipoperfusión del corazón, y el acumulo de mediadores bioquímicos y sustancias generadas por la muerte celular, conducen a la aparición de disfunción cardíaca a medida que progresa el shock.
En esta fase del shock, desde el punto de vista clínico nos encotraremos hipotensión clínica, la cual se define como una PA sistólica < 90 mmHg, una disminución en la PA sistólica de 40 mmHg en referencia a la presentada al principio del episodio o una presión arterial media (PAM)
2.3. Fase de shock irreversible o fallo orgánico
La etapa del shock irreversible representa el punto a lo largo del continuo del shock en el cual el daño de los órganos es tan grave que se vuelve irreversible, no hay respuesta al tratamiento y el paciente no puede sobrevivir, desarrollando un fallo multisistémico y finalmente la muerte.
Desde el punto de vista clínico podemos encontrar anuria e insuficiencia renal aguda, disminución de la contractibilidad y aparición de bradicardia a causa de la disfunción cardiaca, y un empeoramiento del estado de consciencia encontrándonos agitación, obnubilación y finalmente la aparición del estado de coma.
3. ETIOLOGÍA DEL SHOCK
Cualquier causa que afecte a los mecanismos que mantienen la circulación normal, pueden conducir a la aparición de shock. Existen cuatro factores principales que pueden conducir a su aparición:
- Disminución del volúmen circulante efectivo: shock hipovolémico.
- Obstrucción del flujo sanguineo: shock obstructivo.
- Disfunción vasomotora, con incapacidad para mantener el tono vascular y aparición de vasodilatación patológica secundaria: shock distributivo (séptico, neurogénico, anafiláctico).
- Fallo de la bomba cardíaca: shock cardiogénico.
El shock puede estar producido por uno de estos factores o por la combinación de varios. Por ejemplo, el paciente en situación de shock séptico inicialmente presenta disfunción vasomotora, pero a menudo tiene un componente hipovolémico (por la disminución de la ingesta oral, vomitos, diarreas) y/o cardiogénico (a causa de la disfunción miocárdica secundaria a la sepsis) a medida que se instaura y evoluciona el shock.
4. CLÍNICA COMÚN DEL SHOCK
El temprano reconocimiento del cuadro y la intervención precoz han demostrado disminuir la morbimortalidad del shock. Por ello, aunque en algunos pacientes el cuadro clínico sea grave y en otros leve e incluso asintomático en estadios muy iniciales, es muy importante detectar signos tempranos de shock por medio de la exploración física.
Los signos clínicos típicos iniciales, teniendo en cuenta los mecanismos compensatorios que se ponen en marcha tras iniciarse el shock, incluyen la taquicardia (que puede estar o no asociada a hipotensión), la taquipnea (para expulsar el dióxido de carbono producto del metabolismo anaerobio) y la aparición de signos de hipoperfusión que se pueden apreciar a través de las “tres ventanas” corporales, resultantes de los mecanismos compensatorios:
- Cutanea (por vasoconstricción periférica): piel fría, pálida y diaforética.
- Renal: oliguria, con una diuresis <0,5 ml/kg/h.
- Neurológica: nerviosismo, inquietud.
Existen signos y síntomas comunes en todos los tipos de shock, a medida que se producen alteraciones en los diferentes sistemas.
4.1. Alteraciones en el sistema nervioso central (SNC)
Entre el 15 y el 25% del gasto cardíaco está dirigido al cerebro, para mantener un adecuado flujo sanguineo cerebral (FSC). El cerebro tolera cambios de la presión arterial, regulándose el FSC para proteger el tejido cerebral de caídas o elevaciones bruscas de presión. Sin embargo, estas autorregulaciones solo se producen si la PAM se encuentra entre 60-150 mmHg.
Teniendo en cuenta que los mecanismos compensatorios tienen por objetivo conservar la perfusión en órganos vitales como el SNC, podemos encontrarnos en los momentos iniciales del shock, en los que la disminución de la presión arterial esta compensada, a la persona consciente pero con cambios en el estado de ánimo con aparición de ansiedad o confusión.
A medida que el shock progresa y se instaura, apareceran signos de hipoperfusión cerebral por un deterioro del flujo de sangre al cerebro, y el estado mental se vera afectado. Nos encontraremos alteraciones en el nivel de consciencia tales como agitación, confusión y delirio, empeorando hacia la obnubilción, letargia y finalmente el estado de coma. Una hipotensión marcada y prologanda puede producir una isquemia global, que dará lugar a una encefalopatía hipóxica e incluso a la muerte cerebral.
Cabe destacar que los paciente hipertensos crónicos pueden presentar síntomas incluso con presiones arteriales normales.
4.2. Alteraciones en el sistema cardiocirculatorio
Taquicardia: Desde el momento inicial del shock, a causa de los mecanismos compensatorios fisiológicos, se produce taquicardia (habitualmente >100 latidos por minuto, lpm) por activación del sistema nervioso simpático, con el objetivo de preservar el GC.
A medida que el shock evoluciona, la taquicardia incrementa llegando a ser superior a los 150 lpm. Además, el paciente puede presentar arritmias, dolor torácico e incluso sufrir un infarto agudo de miocardio (IAM), por la falta de un suministro adecuado de sangre al propio corazón.
En la fase del shock irreversible, aparecerá la bradicardia, a causa del agotamiento de los mecanismos compensadores y la aparición de depresión miocárdica por un corazón extenuado e hipoperfundido.
Cabe destacar que en el shock neurogénico encontraremos bradicardia desde el momento inicial, por la abolición del sistema nervioso simpático, y la dominancia del parasimpático en consecuencia.
Hipotensión: La perfusión tisular y la perfusión de órganos depende de la PAM. La PAM debe superar los 65 mmHg para garantizar que las células reciban el oxígeno y los nutrientes necesarios, con el objetivo de metabolizar la energia necesaria para mantener la vida.
La presión arterial como tal no es sinónimo de shock, y por tanto la ausencia de hipotensión no excluye el shock. Depender de ella como indicador exclusivo dará lugar a un retraso en su reconocimiento, ya que los mecanismos compensatorios evitan la caída de la presión arterial sistólica (PAS) hasta pérdidas del 30-40% del volumen vascular.
En la etapa inicial del shock, muchas veces existe normotensión e incluso hipertensión, propia de la adrenergia inicial compensatoria. Cuando la presión arterial está disminuida, el shock ya esta instaurado.
A medida que se instaura el shock, y los mecanismos compensatorios son insuficientes, se produce hipotensión arterial, que puede ser absoluta (PAS 40 mmHg sobre la PA sistólica basal).
La hipotensión relativa explicaría en parte porque podría estar un paciente en shock a pesar de tener una tensión arterial normal o alta. Esto podría ocurrir por ejemplo en aquellos pacientes con hipertensión arterial sistémica como enfermedad de base, en los que unas cifras de tensión arterial consideradas “normales” o dentro de rango, para ellos supone una disminución importante de sus cifras habituales, presentando signos y síntomas de shock.
4.3. Alteraciones pulmonares
En las fases iniciales del shock la frecuencia tiende a la taquipnea. Ésta aumenta en respuesta a la necesidad de incrementar el oxígeno en las células, eliminar el exceso de CO2 producido por el metabolismo anaeróbico y en compensación por la acidosis metabólica. Como resultado, a menudo causa una alcalosis respiratoria compensatoria.
A medida que se instaura el shock, la respiración se vuelve rápida y superficial, escuchándose incluso estertores en los campos pulmonares.
La disminución del flujo sanguíneo pulmonar en este punto, hace que disminuyan los niveles de oxígeno arterial (hipoxemia) e incrementen los de dióxido de carbono (hipercapnia). La hipoxemia y los mediadores bioquímicos producen una intensa respuesta inflamatoria y vasoconstricción pulmonar, empeorando la hipoperfusión capilar pulmonar y la hipoxemia en consencuencia.
Ante esta situación se produce una lesión pulmonar aguda (LPA) por diferentes mecanismos. Por un lado, los alvéolos hipoperfundidos dejan de producir surfactante (sustancia producida en el pulmón que permite la adecuada apertura de los alvéolos pulmonares y la respiración), produciéndose un colapso de los alvéolos. Por otro lado, los capilares pulmonares comienzan a filtrarse, causando edema pulmonar, alteraciones en la difusión y colapso alveolar adicional. A medida que la LPA continúa, la inflamación intersticial y la fibrosis son consecuencias frecuentes, lo que lleva a la aparición del síndrome de dificultad respiratoria aguda (SDRA).
Por tanto como podemos ver que las alteraciones de la función pulmonar van desde cambios compensatorios en respuesta a la acidosis metabólica, hasta un síndrome de distrés respiratorio del adulto (SDRA) con manifestación clínica de un edema pulmonar no cardiogénico.
4.4.Alteraciones renales
La diuresis se debe cuantificar mediante el sondaje vesical. Se considera normal si es > 1 ml/kg/h, disminuida entre 0,5-1 ml/kg/h y oliguria <0,5 ml/kg/h. La oliguria es la manifestación más común del compromiso renal en el shock.
En las fases iniciales se produce una disminución de la diuresis por varios motivos. Por un lado, como se ha detallado anteriormente, a causa de los mecanismos compensatorios se produce una vasocontricción de órganos “no vitales” como el riñon para preservar la circulación en los que se consideran vitales (SNC y corazón). La vasocontricción renal produce una disminución del flujo sanguineo renal, y en consecuencia una disminución del filtrado glomerular con una menor producción de diuresis. Por otro lado, se produce una reabsorción de sodio y agua por acción de la aldosterona y la hormona antidiurética, contribuyendo a la disminución del gasto urinario.
En el shock instaurado, cuando la PAM cae por debajo de 65 mmHg, la tasa de filtracion glomerular de los riñones no se puede mantener, produciéndose cambios drásticos en la función renal. Se produce una lesión renal aguda (LRA) que se caracteriza por un incremento de los niveles de urea y creatinina en sangre, desequilibrios hidroelectrolíticos y acidobásicos, y la pérdida de la regulación hormonal renal de la PA. Se produce una disminución de la diuresis, encontrándonos oliguria ( <0,5 ml/kg/h).
En fases avanzadas, en las que la hipoperfusión ha sido prolongada, encontramos insuficiencia renal aguda con anuria por el daño producido.
4.5.Alteraciones en la piel
Se puede distinguir dos tipos de alteracion en la piel según el tipo y la fase del shock en la que nos encontremos:
- Piel caliente, roja y seca, con relleno capilar normal: encontraremos estas características en la piel en las fases iniciales del shock distributivo por accion de la vasodilatación periférica producida (por pérdida del tono simpático en el shock neurogénico, o por la liberación de mediadadores bioquímicos de las células que producen vasodilatación en el shock séptico).
- Piel fría, pálida y humeda: en el shock hipovolémico, cardiogénico, obstructivo y en la fase fría del shock distributivo, nos encontraremos estas características en la piel. Se deben al efecto de los mecanismos compensatorios que producen vasoconstricción periférica, disminuyendo la perfusión de la piel, dirigiendo la sangre desde la periferia hacia los órganos vitales. A su vez se produce sudoración por activación de las glándulas sudoríparas por parte del sistema nervioso simpático.
A medida que se compromete la perfusión de la piel, en fases más avanzadas pueden aparecer tonos cianóticos y livideces, con llenado capilar lento.
4.6. Alteraciones hepáticas
Una vez el shock se instaura, el menor flujo sanguíneo al hígado afecta la capacidad de las células hepáticas para relizar sus funciones, encontrando las siguientes alteraciones:
- Funciones metabólicas: el paciente tiene menor capacidad para metabolizar fármacos y productos de desecho del metabolismo, como el ácido láctico. Además, se alteran las actividades metabólicas incluidas la gluconeogenesis y la glucólisis.
- Funciones fagocíticas: el paciente se vuelve más suceptible a las infecciones, debido a que el hígado no filtra las bacterias de la sangre.
El paciente desarrolla ictericia, a causa del incremento de las enzimas hepáticas y la bilirrubina.
4.7. Alteraciones gastrointestinales
Los efectos locales de la perfusión inadecuada, producida desde el inicio del shock, pueden conducir a la aparición de úlceras por estrés en la mucosa gástrica y a la isquemia con necrosis en el intestino delgado, pudiéndose producir hemorragias gastrointestinales.
La isquemia gastrointestinal además, conduce a la translocación bacteriana y disfunción orgánica, favoreciendo el paso de las toxinas bacterianas al torrente sanguineo a través del sistema linfático. Estas toxinas pueden causar, además de infección, depresión cardíaca, vasodilatación, incremento de la permeabilidad capilar y una respuesta inflamatoria intensa con la activación de mediadores bioquímicos adicionales.
5. TIPOS DE SHOCK
5.1. Tipos de shock según su perfil hemodinámico
La perfusión de los tejidos depende del gasto cardíaco y del tono vascular (resistencias vasculares sistémicas). Un descenso de uno de los factores da lugar a la respuesta fisiológica compensadora de incrementar el otro para mantener la homeostasis.
El gasto cardíado depende de la frecuencia cardíaca y del volumen sistólico, y este a su vez de la precarga, la contractibilidad y la poscarga. Las alteraciones en cada uno de estos parámetros condicionarán cambios en los demás, que se traducen en una presentación clínica y unos perfiles hemodinámicos característicos para los diferentes tipos de shock.
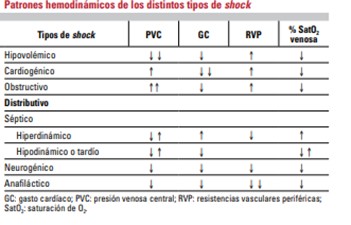
Ilustración 1 Perfiles hemodinámicos según el tipo de shock
Fuente: Medicine. 2018; 12 (52): 3066-75
- Shock con bajo gasto cardiaco o hipodinámico: En el shock hipovolémico, cardiogénico y obstructivo la disminución del transporte del oxígeno se debe a una disminución del flujo cardiaco. Nos encontramos con un perfil de shock en el que el gasto cardíaco esta disminuido, y para compensarlo se incrementan las resistencias vasculares periféricas.
- Shock con gasto cardíaco elevado o hiperdinámico: Por el contrario, en el shock distributivo del tipo séptico en su fase inicial/ shock caliente las resistencias vasculares periféricas se ven disminuidas por la vasodilatación massiva que caracteriza a este tipo de shock, incrementándose el gasto cardíaco.
A medida que se instaura el shock, presenta un perfil hemodinámico hipodinámico como el resto de shocks.
5.2. Tipos de shock según su etiología
Teniendo en cuenta la causa que lo produce, y los diferentes mecanismos que conducen a su presentación, el shock se clasifica en los siguientes tipos.
SHOCK HIPOVOLÉMICO
El shock hipovolémico se define como un estado de insuficiencia circulatoria aguda causado por una disminución brusca o rapidamente progresiva del volumen intravascular (sangre, plasma o agua y electrólitos).
La disminución del volúmen circulante efectivo que se produce, da como resultado una disminución del retorno venoso de la sangre al corazón y una posterior disminución del llenado ventricular. La disminución del llenado ventricular causa una reducción del volúmen sistólico (cantidad de sangre expulsada del corazón), y un descenso del gasto cardíaco en consecuencia. Cuando el gasto cardíaco disminuye, se produce una caída de la presión arterial y los tejidos no pueden perfundirse de una manera adecuada iniciándose el shock.
Se trata de uno de los shocks más frecuente y una de las principales causas de muerte en pacientes quirúrgicos y en pacientes politraumatizados.
Etiología
El líquido corporal está contenido en los compartimentos intracelular (representa 2/3 del agua corporal) y extracelular. El líquido extracelular del cuerpo se encuentra en uno de los dos compartimentos: intravascular (dentro de los vasos sanguineos) o intersticial (rodeando los tejidos, siendo de tres a cuatro veces mayor que el intravascular). El volumen intravascular puede reducirse tanto por la pérdida, como por el intercambio de líquidos entre los compartimentos intravascular e intersticial.
Se puede classificar el shock hipovolémico en dos grandes subtipos, en función del elemento principal que se ve afectado: hemorrágico (con pérdida hemática principalmente, además de plasma, agua y electrolíticos) y no hemorràgico (con pérdida exclusiva de plasma, agua y electrolítos).
Shock hipovolémico hemorrágico
El shock hipovolémico hemorrágico es el tipo de shock hipovolémico más frecuente. Puede clasificarse a su vez en traumático o no traumático, según su mecanismo causal.
- Shock hipovolémico hemorrágico de origen traumático
Las hemorragias traumáticas son causa directa del 30-40% de las muertes en pacientes que han sufrido un politrauma, y la segunda causa de muerte tras las afectaciones del sistema nervioso central. El 36% de los pacientes fallecen in situ por situaciones de exanguinación.
En el paciente traumático, la causa principal de situación de shock es la hipovolemia, siendo el shock hipovolémico hemorrágico el más frecuente. Sin embargo, se tiene que tener presente que pueden coexistir los diferentes tipos de shock en función de las afectaciones que presente derivadas del trauma, como por ejemplo: shock neurogénico (por afectación medular), shock cardiogénico (por afectación cardiaca como puede darse en una contusión cardiaca), shock obstructivo (por taponamiento cardíaco, neumotórax a tensión producido por fracturas costales, etc) o shock séptico (por un cuadro infeccioso de las propias heridas infectadas).
Podemos encontrarnos tanto hemorragias internas (rotura esplénica o lesión/rotura de grandes vasos secundarias al traumatismo, laceraciones, fracturas de huesos largos (femur) o esponjoso (pelvis), etc) como hemorragias externas (heridas de arma, traumatismos penetrantes en abdomen o torax, etc), en función del traumatismo que se haya producido.
- Shock hipovolémico hemorrágico de origen no traumático
Las causas más frecuentes son:
- Sangrado gastrointestinal superior e inferior (sangrado por varices, sangrado de gastropatia hipertensiva portal, úlcera péptida, diverticulosi).
- Sangrado de etiología vascular (fístula aortoentèrica, rotura de aneurisma aórtico abdominal, tumor que erosiona un vaso sanguineo importante).
- Hemorragia espontanea por el uso de anticoagulantes (en el caso de INR por encima de los niveles terapeuticos por interacciones medicamentosas) o por coagulopatias.
- Hemorragias intra y post operatorias.
- Hemorragias de origen obstétrico- ginecológica (atonia uterina, placenta previa, embarazo ectópico, etc).
Shock hipovolémico no hemorrágico
Cuando la causa de la hipovolemia es la pérdida de volúmen plasmático, agua y electrolitos, nos encontramos con el shock hipovolémico no hemorrágico. Las causas más frecuentes son:
- Pérdidas cutaneas/ pérdidas insensibles: paciente gran quemado, síndrome de Stevens- Johnson, necrólisis epidérmica tóxica, isolación, pirexia.
- Pérdidas gastrointestinales: diarreas, vómitos, fístulas o drenajes.
- Pérdidas renales: diuresis inducida por medicamentos, diuresis osmótica, transtornos endocrinos como la diabetes insipida, por secreción inadecuada de ADH, y el hipoaldosteronismo.
- Pérdidas del tercer espacio: pancreatitis, cirrosis, obstrucciones intestinales y ascitis.
Clinica
La pérdida del volumen intravascular puede ser inicialmente silente, por acción de los mecanismos compensatorios fisiológicos, encontrándonos evidencia de shock cuando hay una reducción en el volumen intravascular de un 15-30%, lo que representa una pérdida aproximada de 750-1500 ml de sangre en una persona de 70 kg.
La clínica variará según la causa desencadentante, el volúmen y la velocidad con que se pierdan los líquidos corporales y la respuesta individual a la agresión.
En el caso de pérdidas menores del 20% encontraremos hipotensión postural, piel fría, retraso en el relleno capilar y reducción de la presión de pulso. Cuando las pérdidas se encuentran entre el 20-40% aparece hipotensión, taquicardia, oliguria, sensación de sed y alteraciones mentales. En pérdidas superiores al 40% se observan manifestaciones de shock tales como hipotensión, taquicardia, taquipnea, oliguria, letargia, etc.
En el shock hipovolémico de causa no hemorrágica, podemos encontrarnos además signos de deshidratacion como sensación de sed intensa, aspecto de la lengua seca, ojos hundidos y signo de pliegue cutaneo positivo.
En el caso del shock hipovolémico de causa hemorrágica, la gravedad del cuadro dependerá de la cantidad de sangre perdida y la rapidez con la que se haya producido. Se clasifica en cuatro grados de gravedad, en los que encontraremos signos y síntomas que nos pueden orientar de la cantidad de sangre perdida.

Ilustración 2 Clasificación del shock hemorrágico según la pérdida hemática
Tabla adaptada de la fuente: Critical Care. 2004; 8 (5): 373-381
SHOCK CARDIOGÉNICO
El shock cardiogénico se define como un estado de insuficiencia circulatoria aguda causado por un fracaso agudo de la bomba cardíaca.
Se presenta cuando la capacidad del corazón para contraerse y bombear sangre se ve afectada, generalmente como consecuencia de una disminución de la contractibilidad miocárdica, comprometiéndose el gasto cardiaco. Cuando el volúmen sistólico y la frecuencia cardíaca disminuyen o se vuelven erráticos, la presión arterial baja y la perfusión tisular se reduce.
A causa de la insuficiente perfusión coronaria el corazón se debilita, afectando su capacidad de bombeo, el ventrículo izquierdo no expulsa completamente su volumen de sangre durante la sístole y se acumula líquido en los pulmones dando lugar a la aparición de congestión pulmonar.
Etiología
Las causas del shock cardiogénico se conocen como coronarias o no coronarias.
Causas coronarias
- Infarto agudo de miocardio (IAM): es la causa más frecuente, siendo necesaria al menos la necrosis del 40-50% de la masa ventrícular izquierda para provocarlo. Los pacientes que experimentan un IAM de la pared anterior, tienen mayor riesgo de choque cardiogénico debido al daño potencialmente extenso al ventrículo izquierdo ocasionado por la oclusión de la arteria coronaria descendente anterior izquierda.
Los factores de riesgo que se relacionan con el desarrollo de shock cardiogénico tras un IAM son: edad avanzada, IAM previo, antecedentes de hipertensión arterial o diabetes mellitus, enfermedad coronaria multivaso, presión arterial sistólica inferior a 120 mmHg, frecuencia cardíaca superior a 90 lpm, fallo cardíaco al ingreso, IAM con elevación de ST y bloqueo de rama izquierda.
Un 7% de los pacientes que sufren un IAM desarrollan shock cardiogénico, lo que conlleva una mortalidad muy elevada (40-50%).
Tras sufrir un IAM, podemos encontrar complicaciones mecánicas que pueden conducir a la aparición de shock cardiogénico, como son: insuficiencia mitral aguda por rotura de musculo papilar, rotura del septo interventricular, rotura de la pared libre del ventrículo, taponamiento por rotura de pared o efusión hemorrágica.
Causas no coronarias
Entre las causas de origeno no coronario que pueden conducir al shock cardiogénico encontramos, afecciones que estresan el miocardio como son:
- Hipoxemia grave
- Acidosis
- Hipoglucemia
- Hipocalcemia
- Neumotórax a tensión
Además de estados que provocan una función ineficaz del miocardio:
- Miocardiopatias (miocardiopatía avanzada, miocardiopatía hipertrófica obstructiva)
- Valvulopatias (estenosis o insuficiencia aórtica y mitral)
- Taponamiento cardíaco
- Arritmias (taquiarritmias, bradiarritmias)
- Miocarditis
- Contusión miocàrdica
- Bypass cardiopulmoar prolongado
- Tóxicos (fármacos que inducen depresión cardíaca)
Clínica
Desde el punto de vista hemodinámico el shock cardiogénico se caracteriza por la aparición de:
- Taquicardia con pulso débil/ filiforme (habitualmente alrededor de 90-110 lpm).
- Hipotensión arterial (PA sistólica <90 mmHg o PAM <65 mmHg o reducción de 30 mmHg respecto al nivel basal en pacientes hipertensos).
Signos y síntomas debido al bajo débito cardíaco como:
- Disnea, ortopnea
- Taquipnea, respiración superficial
- Fatigabilidad
- Disminución progresiva de la capacidad funcional
- Dolor torácico, secundario a la isquemia coronaria
- Arritmias (bradicardia extrema por bloqueo auriculoventricular u otros episodios arrítmicos)
- Síncope
- Aparición de edemas en zonas distales (pies y manos)
En este último punto, si el fallo es predominantemente izquierdo encontraremos clínica respiratoria, por congestión pulmonar (disnea, taquipnea, estertores y sibilantes), y si es predominantemente derecho encontraremos alteraciones en la circulación como ingurgitación yugular, reflujo hepatoyugular e hipotensión sin congestión pulmonar.
Además, aparecen signos de hipoperfusión tisular debido a la disminución del gasto cardíaco y a la vasoconstricción compensadora:
- Piel fría, pálida o cianótica
- Diaforesis, piel pegajosa
- Relleno capilar disminuido
- Oliguria
- Nerviosismo e inquietud
Cuando se realiza una monitorización más invasiva encontramos los siguientes datos:
- Gasto cardíaco reducido con un índice cardiaco disminuido (<1,8 L/min/m2 sin soporte o <2-2,2 L/min/m2 en presencia de soporte).
- Presión venosa central alta (PVC >15 mmHg).
- Presión de enclavamiento de arteria pulmonar alta (PCP > 15 mmHg) .
- Resistencias vasculares sistémicas (RVS) elevadas (>1500 dinas x seg x cm xm2).
SHOCK OBSTRUCTIVO
El shock obstructivo se define como un estado de insuficiencia circulatoria aguda causado por una obstrucción mecánica del flujo sanguíneo en el circuito cardiovascular. En este tipo de shock existe una patología subyacente que provoca un impedimento mecánico, que no permite el llenado o el vaciamiento adecuado del corazón, lo que lleva a una reducción del gasto cardíaco. En consecuencia se produce una disminuciñon de la presión arterial y de la perfusión sistémica.
Fisiopatológicamente se puede considerar similar al shock cardiogénico, produciéndose una disminución del gasto cardíaco además de un incremento en las presiones de llenado (PVC, PCP) y en las resistencias vasculares sistémicas (RVS).
Etiología
Este impedimento mecánico no depende de una alteración intrínseca del miocardio. Las causas que principalmente lo provocan son:
- Taponamiento cardíaco
- Pericarditis constrictiva
- Neumotorax a tensión
- Tromboembolismo pulmonar masivo
Clínica
Todos ellos cursan con hipotensión, ingurgitación yugular e intensa hipoxia. Sin embargo, aparecerán otros signos y sintomas dependiendo del cuadro clínico que lo cause.
Taponamiento cardiaco
Los hallazgos más frecuentes son:
- Disnea
- Triada de Beck; ingurgitación yugular, disminución de los ruidos cardiacos e hipotensión.
- Signo de Kusmaull (la inspiración incrementa la ingurgitación venosa).
- Pulso paradójico (descenso de la presión arterial sistólica (>10 mmHg) durante la inspiración).
Pericarditis constrictiva
Presentan sígnos y síntomas de insuficiencia cardiaca derecha, sin signos de insuficiencia cardiaca izquierda (o muy leves):
- Ingurgitación venosa yugular marcada
- Hepatomegalia
- Edemas periféricos
- Ascitis
- Derrame pleural
- Roce pericárdico
- Signo de Kussmaul
Neumotorax a tensión
Sospecharemos de él en el caso de traumatismos, heridas torácicas, ventilación mecánica, y cuando se presenten los siguientes signos y síntomas:
- Dolor torácico: se presenta de forma aguda, pudiendo tener características pleuromecánicas, y acompañándose con frecuencia de un cuadro vegetativo.
- Disnea: de inicio súbito, con una evolución progresiva.
- Taquipnea
- Tos seca
- Ruidos respiratorios ausentes o disminuidos
- Desviación traqueal hacia el lado normal
- Venas del cuello distendidas
Tromboembolismo pulmonar masivo
Los hallazgos pueden ir desde síntomas inespecíficos hasta claros signos de insuficiencia cardíaca derecha o intensa hipoxia.
Los signos y síntomas más frecuentes son:
- Taquipnea (>20 respiraciones/ minuto)
- Disnea
- Dolor torácico tipo pleurítico
- Tos
- Taquicardia (>100 lpm)
- Síncope
- Pudiendo encontrar con menor frecuencia: hemoptisis, signos de TVP, fiebre y cianosis.
SHOCK DISTRIBUTIVO
El tono vascular está determinado por mecanismos reguladores centrales, como ocurre en la regulación de la presión arterial y por mecanismos reguladores locales, como la demanda de oxígeno y nutrientes en los tejidos. La capacidad de los vasos sanguíneos para contraerse ayuda a retornar la sangre al corazón, contribuyendo al retorno venoso.
El shock distributivo se produce por una vasodilatación sistémica profunda. Esta vasodilatación arterial y venosa masiva puede ser causada por una pérdida de tono simpático o una liberación de mediadores bioquímicos de las células que provocan vasodilatación, produciéndose en consecuencia un acúmulo del volumen intravascular en los vasos sanguíneos periféricos.
La dilatación arterial reduce la resistencia vascular sistémica, e inicialmente en respuesta a los mecanismos compensatorios podemos encontrar un gasto cardíaco alto, tanto por la disminucion de la poscarga (causada por la disminución de la resistencia vascular sistémica) como por el mayor esfuerzo del músculo cardíaco para mantener la perfusión, incrementándose la frecuencia cardiaca, ante una vasculatura incompetente. Encontrándonos en el shock caliente inicial un perfil hemodinámico hiperdinámico, con aumento del gasto cardiaco.
Sin embargo, este desplazamiento anómalo del volumen intravascular hacia la periferia causa hipovolemia relativa, debido a que no regresa suficiente sangre al corazón, disminuyéndose el retorno venoso. La disminución del retorno venoso produce una reducció del volúmen sistólico y un descenso del gasto cardíaco, que produce a su vez una disminución de la presión arterial. Teniendo como resultado una perfusión tisular inadecuada y, una vez instaurado, nos encontramos el shock en su fase fría con un perfil de shock hipodinámico.
Los mecanismos que conducen a la vasodilatación inicial en el shock distributivo, proporcionan la base para una subclasificación del shock distributivo en tres tipos: anafiláctico, neurogénico y séptico. Siendo el shock séptico la causa más frecuente.
SHOCK ANAFILÁCTICO
El shock anafiláctico se define como un estado de insuficiencia circulatoria aguda causado por una reacción alérgica grave. Esto ocurre cuando los pacientes que ya han producido anticuerpos frente a una sustancia (antígeno), que el organismo identifica como extraña, desarrollan una reacción sistémica antígeno- anticuerpo.
Esta respuesta corresponde a las reacciones de hipersensibilidad tipo 1, mediada por la inmunoglobulina E (IgE) y se producen de la siguiente manera:
Ante una primera exposición a esta sustancia, el cuerpo que la detecta como extraña produce anticuerpos (IgE). Estos anticuerpos se fijan en la superficie de los mastocitos y los basófilos, produciéndose la sensibilización a este alérgeno.
Cuando se produce una nueva exposición, el antígeno se une a su IgE específico y conduce a la degranulación de los mastocitos y basófilos, dando lugar a la liberación de potentes mediadores vasoactivos (histaminas, prostaglandinas, factores quimiotácticos, leucotrienos, factos activador de plaquetas) que causan la activación de plaquetas, eosinófilos y neutrófilos. Como resultado se produce una respuesta inflamatoria anormal, pérdida del tono vascular con vasodilatación generalizada e incremento de la permeabilidad capilar produciéndose edema intersticial.
Estos mediadores vasoactivos, estan implicados además en las alteraciones que caracterizan a la anafilaxia: cambios en la permeabilidad vascular, la rubicundez, la urticaria, el angioedema, la hipotensión y la broncoconstricción.
Estas reacciones tempranas, se acompañan de una reacción de fase tardía o reacción de “rebote” 4-10 horas después de la reacción alérgica inicial. Y en el caso que los mediadores químicos se continúen liberando, puede darse una reacción retardada que dura hasta 24 horas.
Etiología
Los factores desencadenantes más frecuentes son:
- Fármacos: antibióticos (penicilina, betalactamicos, sulfas), contrastes radiológicos, alopurinol, anestésicos (lidocaína, procaína), vacunas, hormonas (insulina, vasopresina, hormona adrenocorticotrópica), bloqueantes neuromusculares, AINEs, ácido acetilsalicílico (AAS), etc.
- Alimentos: frutos secos, leche de vaca, mariscos, pescado, huevos, soja, trigo, etc.
- Picaduras de insectos: abejas, avispas, hormigas y otros himenópteros.
- Otros: latex, estímulos físicos como el ejercicio y el frío, y otros agentes farmacéuticos como los antígenos utilizados en las pruebas cutáneas.
Los antibióticos y los contrastes radiológicos causan las reacciones anafilácticas más graves.
Estos factores desencadenantes varían en función de la edad, siendo más frecuentes en unas franjas u otras:
- Fármacos: población adulta y ancianos.
- Alimentos: niños, adolescentes y adultos jovenes.
- Picaduras de insectos: adultos.
Por orden de prevalencia, los órganos diana afectados son los siguientes:
- Piel y membranas mucosas (80-90% de los episodios): produciendose eritema localizado o difuso, prurito, erupción, urticaria y/o angioedema.
- Sistema respiratorio (70% de los episodios): encontrándonos prurito y congestión nasal, estornudos, prurito u opresión en la garganta, tos, aparición de sibilancias y/o disnea.
- Tracto gastrointestinal (30-40% de los episodios): aparecen náuseas, vómitos, calambres y/o diarrea.
- Sistema cardiovascular (10-45% de los episodios): podemos encontrar hipotensión (que puede ir acompañada de síncope), taquicardia y/o arritmias cardiacas.
- Sistema nervioso central (10-15%): se puede producir cefalea, convulsiones y/o cambios en el estado mental.
- Otros, menos frecuentes: contracciones uterinas, disminución del tono de los esfínteres, pérdida de visión, zumbido en los oídos y/o muerte inminente.
Clínica
La anafilaxia tiene tres características definitorias:
- Inicio agudo de los síntomas.
- Presencia de dos o más síntomas incluyendo: compromiso respiratorio, reducción de la presión arterial, malestar digestivo e irritación de piel y mucosas.
- Compromiso cardiovascular de minutos a horas tras la exposición al antígeno.
La gravedad de la reacción anafiláctica se relaciona con la rapidez con la que progresen los síntomas, el tipo de antígeno, la vía de entrada y los órganos que resulten afectados. Se pueden producir desde reacciones leves, moderadas a graves con compromiso vital.
Los signos y síntomas de anafilaxia pueden presentarse dentro de los 2-30 minutos tras la exposición al antígeno, sin embargo, algunas reacciones pueden no desarrollarse durante varias horas. El tiempo desde la exposición al antígeno hasta el inicio de los síntomas es un buen indicador de la gravedad de la reacción, siendo mayor la gravedad de la reacción a mayor rapidez de inicio.
El tiempo de aparición de los síntomas difiere además según la causa que lo produzca, siendo más temprano en la exposición a fármacos (5-10 minutos) y en las picaduras de insectos (10-15 minutos), frente a los alimentos que lo presenta de manera más tardía (25-35 minutos).
En las reacciones sistémicas leves el inicio de los síntomas se produce dentro de las primeras 2 horas tras la exposición, pudiendo encontrar:
- Hormigueo periférico
- Sensación de calor
- Sensación de plenitud en boca y garganta
- Congestión nasal
- Tumefacción periorbitaria
- Prurito
- Estornudos
- Lagrimeo
En las reacciones sistémicas moderadas el inicio de los síntomas es el mismo que en la reacción leve, pudiendo encontrar sintomatología leve además de:
- Rubicundez
- Calor
- Ansiedad
- Prurito
En las reacciones graves/ shock anafiláctico, con un inicio abrupto de la sintomatología descrita, podemos encontrar:
- Compromiso neurológico con aparición de confusión e incluso pérdida de la consciencia
- Broncoespasmo
- Angioedema afectación de las vías respiratorias o laringe con disnea
- Saturación de hemoglobina (SatHb) igual o <92% (94% en niños)
- Tos
- Sibilancias
- Cianosis
- Inicio rápido de hipotensión
- Disfagia
- Cólicos abdominales
- Vómitos
- Diarrea
- Convulsiones
- Hipotonía
- Puede evolucionar a paro cardíaco
SHOCK NEUROGÉNICO
El shock neurogénico se define como un estado de insuficiencia circulatoria aguda causado por una interrupción de la vía autonómica por encima de la sexta vertebra torácica (T6), en la que se produce una pérdida total del tono simpático y una respuesta parasimpática sin oposición impulsada por el nervio vago.
La estimulación simpática hace que el músculo liso vascular se contraiga. Por el contrario, la estimulación parasimpática hace que el músculo liso vascular se relaje o se dilate.
El paciente, tras el traumatismo o la causa que haya conducido a la aparición de shock neurogénico, experimenta una abolición de la actividad simpática, con un predominio de la parasimpática.
Esta estimulación parasimpática predominante causa una disminución drástica en la resistencia vascular sistémica, con pérdida del tono vascular tanto arterial como venoso, produciendose vasodilatación. Pese a que el volumen sanguineo es adecuado, éste volumen se desplaza a causa de tener la vasculatura dilatada, produciendose una acumulacíón de sangre en la periferia, ocasionando un estado relativo de hipovolemia. En consecuencia disminuye el retorno venoso, el gasto cardíaco y la presión arterial, produciéndose una perfusión tisular insuficiente.
Además de la afectación en la vasculatura, la estimulación parasimpática produce una disminución de la frecuencia y contractibilidad cardiaca, con la consiguiente repercusión hemodinámica y una disregulación de la temperatura.
Etiología
Entre las causas que lo pueden producir encontramos:
- Lesiones de la medula espinal, con afectación por encima de T6: causa más frecuente.
- Lesiones en el SNC
- Anestesia aquídea
- Acción depresora de fármacos (antihipertensivos, barbitúricos, etc)
- Falta de glucosa (reacción a la insulina por ejemplo)
- Síncope vaso vagal
- Síndrome de Guillain- Barre
- Mielitis transversa y otras neuropatias
Clínica
El shock neurogénico puede tener una evolución prolongada, por ejemplo en la lesión de la médula espinal, o corta, como ocurre en los síncopes o desmayos. En este tipo de shock el sistema simpático no puede responder a los factores estresantes del cuerpo, por tanto las propiedades clínicas son signos de la estimulación parasimpática, que se caracteriza por:
- Hipotensión (TAM
- Bradicardia (FC
- Disregulación térmica
- Piel seca, roja y tibia/ caliente
- Signos de hipoperfusión como oliguria y alteraciones en el estado mental (confusión).
- Una vez monitorizado encontraremos el GC disminuido con caída de las resistencias vasculares sistémicas.
6. SEPSIS Y SHOCK SÉPTICO
En las últimas décadas se ha llevado a cabo una cantidad importante de investigación, dirigida a reducir la morbilidad y mortalidad relacionada con la sepsis y el shock séptico.
En 1991 tuvo lugar la primera conferencia de consenso por parte del American College of Chest Physicians y la Society of Critical Care Medicine, en la que desarrollaron una amplia serie de definiciones relacionadas con los síndromes sépticos (sepsis como una respuesta inflamatoria sistémica (SIRS), sepsis grave y shock séptico) que podrían mejorar la capacidad de los médicos de diagnosticar, supervisar y tratar la sepsis y otros aspectos relacionados con ésta.
En el año 2004 se publicó la primera edición de las guías de práctica clínica, dirigidas al tratamiento de la sepsis grave y el shock séptico, de la Campaña sobreviviendo a la sepsis (CSS).
Desde entonces, en los años 2008, 2012, 2016 (sepsis 3) y nuevamente en el 2018, expertos en cuidados críticos han reevaluado sistematicamente la investigación y proporcionado recomendaciones de prácticas clínicas, con base a la evidencia, para el tratamiento agudo de los pacientes con sepsis y shock séptico.
El desarrollo y la implementación de protocolos, centrados en la prevención, la detección temprana y el tratamiento de pacientes con sepsis, han reducido la mortalidad de los pacientes hospitalizados.
6.1. Definición y diagnóstico de la sepsis y el shock séptico
Según las definiciones del Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3) Task Force, realizado en el año 2016, la sepsis se define como un “síndrome clínico caracterizado por una disfunción orgánica que pone en peligro la homeostasis y es secundaria a una respuesta anormal y exagerada del huésped frente a una infección”.
La severidad de la sepsis es estratificable en función del número y/o grado de afectación que se produzca en los órganos afectados. Este grado de disfunción orgánica puede reconocerse de manera objetiva mediante diferentes scores y criterios clínicos. La reciente revisión de la definición de sepsis, recomienda el uso de la escala SOFA (Sequential Organ Failure Assesment) como elemento descriptivo de la repercusión sistémica.
La escala SOFA esta diseñada específicamente para la sepsis. Se trata de un sistema sencillo que se puede evaluar a lo largo de la evolución del paciente, que incluye la valoración de la función de los 6 órganos o sistemas siguientes, a través de los siguientes criterios en cada uno de ellos:
- Sistema nervioso central: valor de la escala de Glasgow
- Sistema respiratorio: mediante gases arteriales, cociente de PaO2/FiO2 (PaFi)
- Sistema cardiovascular: PAM y uso de cualquier vasopresor
- Función hepática: valor de bilirrubina sérica
- Sistema hematológico: recuento de plaquetas
- Función renal: valor de creatinina sérica y/o gasto urinario
Se asignan puntuaciones de 0 a 4 a cada uno de los sitemas u órganos. Denominándose “disfunción” cuando se asignan 1 o 2 puntos, y “fallo o insuficiencia” cuando alcanza la puntuación de 3 o 4, proporcionando un total de puntuación de 0 a 24. Se considerará que existe disfunción orgánica, cuando el paciente presente una variación aguda de 2 o más puntos en el SOFA, considerándose la puntuación basal 0 a menos que el paciente tuviera una disfunción previa a la infección. Cuanto mayor es la puntuación, mayor es el riesgo de morbimortalidad del paciente.
Pese a su sencillez, la escala SOFA presenta una desventaja para los pacientes que se encuentran fuera de la unidad de cuidados intensivos (UCI), ya que son necesarios datos de laboratorio para su valoración. Por este motivo, se introdujo una evaluación abreviada de disfunción órganica con la escala quick SOFA (qSOFA) o SOFA rápido.
Este modelo tiene un valor predictivo similar al SOFA, pero aplicado a pacientes que no se encuentran ingresados en una UCI con sospecha de infección, y se puede realizar a pie de cama mediante la valoración de 3 variables clínicas:
- Alteración del nivel de consciencia (Glasgow <15)
- Frecuencia respiratoria (igual o > 22 respiraciones por minuto)
- Cifras de la tensión arterial sistólica (igual o <100 mmHg)
Cada variables es valorada con 1 punto, una puntuación de qSOFA >2 puntos sugiere el desarrollo de sepsis, e identifica a pacientes con mayor riesgo de ingreso en UCI y mortalidad. Pese a que el qSOFA es altamente específico para identificar pacientes graves, no es diagnóstico de sepsis, siendo necesario calcular el SOFA para confirmar difunción orgánica.
El shock séptico es la causa más común de shock, y el tipo más común de shock distributivo. Se define como una “subcategoría de la sepsis en la que las alteraciones circulatorias y del metabolismo celular son lo suficientemente profundas como para aumentar considerablemente la mortalidad”. En esta última Conferencia de consenso se redefinieron los criterios clínicos de shock séptico:
- Hipotensión arterial, como un estado de fallo circulatorio agudo, con una PAM
- Necesidad de soporte con fármacos vasopresores para mantener PAM.
- Elevación del ácido láctico >2 mmol/l pese a una adecuada reanimación con fluidoterapia.

Ilustración 3 Quick SOFA (qSOFA) y criterios de shock séptico
Fuente: Medicine 2018; 12 (52): 3066-75
6.2. Epidemiología de la sepsis y el shock séptico
La sepsis y el shock séptico representan una de las principales causas de morbimortalidad en el mundo, mas de 30 millones de personas sufren de sepsis en todo el mundo cada año, lo que resulta en un potencial de 6 millones de muertes. Cifras que pueden estar infraestimadas, ya que no se disponen de informes de países con bajos recursos. Encontrar y tratar de manera agresiva la fuente de infección y restaurar rápidamente la perfusión tisular son intervenciones importantes que pueden impactar positivamente en el resultado clínico.
Pese a los avances que se han producido en la medicina, la incidencia tanto de sepsis como de shock séptico ha continuado aumentando, situándose la incidencia de sepsis en los países industrializados entre 200 y 400 casos/ 100.000 habitantes/ año.
Su letalidad se encuentra alrededor del 20-30%. Ésta viene determinada por factores no modificables (características del paciente, foco de la infección, microorganismo responsable del episodio) y por factores modificables, siendo los de mayor importancia el tiempo en restaurar la perfusión tisular y la adecuación en el manejo del foco séptico (tiempo transcurrido hasta el inicio del tratamiento antibiótico, adecuación de la cobertura antibiótica empírica y drenaje del foco séptico si precisa).
La supervivencia es de un 80% si el tratamiento se instaura en la primera hora, disminuyendo a menos del 50% a partir de la cuarta hora y limitada a un 15-20% si transcurren doce horas.
6.3. Factores de riesgo de la sepsis y el shock séptico
El número de ingresos hospitalarios relacionados con la sepsis se ha triplicado en la última decada, según la Surviving Sepsis Campaign del 2016. Los factores de riesgo que contribuyen a la creciente incidencia de la sepsis son:
- Extremos de edad (65 años): Nos encontramos con una población envejecida, y en el caso de los adultos mayores el riesgo es debido a la disminución de reservas fisiológicas, el envejecimiento del sistema inmunitario, la existencia de enfermedades concominantes y, a menudo, la presentación inespecífica de la infección
- Inmunodepresión
- Desnutrición proteico- calórica
- Enfermedades crónicas: como la diabetes, hepatitis, VIH, enfermedad renal crónica, cáncer, enfermedad pulmonar obstructiva crónica, cirrosis u obstrucción biliar, fibrosis quística, insuficiencia cardiaca congestiva u obesidad.
- Cirugías emergentes o múltiples
- Procedimientos invasivos y dispositivos médicos permanentes
- Alteración de las barreras naturales: a causa de un traumatismo, lesión quirúrgica, quemadura, enterocolitis, cateterismo o intubación.
6.4. Etiología de la sepsis y el shock séptico
El 70% de las sepsis son de origen comunitario, siendo clave una adecuada educación para que las personas busquen asistencia médica sin demora, para prevenir muertes innecesarias y discapadidad. El resto corresponde a las infecciones adquiridas en el hospital o relacionadas con la asistencia sanitaria. Las afecciones adquiridas en el hospital, se originan con mayor frecuencia en los pulmones (neumonía), en las vias urinarias (urosepsis) y en el torrente sanguineo (bacteriemia). Otras infecciones que se pueden producir incluyen las intraabdominales y las infecciones de heridas.
Según los datos del informe Envin 2019, las infecciones que se encontraron con mayor frecuencia en uci son: la neumonía asociada a ventilación mecánica (29,99%), seguida de la infección urinaria relacionada con sonda uretral (29,03%) y la bacteriemia, siendo en el 12,72% de los casos secundaria a infección de catéter.
Desde el punto de vista microbiológico, las bacterias gramnegativas han sido tradicionalmente los microorganismos implicados con mayor frecuencia en el desarrollo de la sepsis (58,41% según el informe Envin 2019). Sin embargo, hay una creciente incidencia de infecciones causadas por bacterias grampositivas (29,84%), víricas y micóticas (11,07%), que tambien pueden causar sepsis.
Según el informe Envin 2019, los microorganismos más frecuentes, aislados en las principales infecciones intra UCI, son:
- Bacterias gramnegativas: Escherichia coli (15,01%), Pseudomonas aeruginosa (13,64%) y Klebsiella pneumoniae (7,46%).
- Bacterias grampositivas: Staphylococcus epidermidis (7,95%), Enterococcus faecalis (6,58%), Stapylococcus aureus (5,54%) y Enterococcus faecium (3,53%).
- Hongos: Candida albicans (6,1%).
Los pacientes en estado crítico con sepsis y/o shock séptico, al igual que los pacientes neutropénicos, tienen una predisposición a la infección con organismos resistentes. Siendo necesario el inicio rápido del tratamiento antibiótico eficaz para prevenir el aumento de la mortalidad y otros desenlaces clínicos adversos.
6.5. Fisiopatología de la sepsis
Cuando los microorganismos invaden los tejidos del cuerpo, atravesando las barreras epiteliales (piel o mucosas), el huésped exhibe una respuesta inmunitaria. Si la respuesta inflamatoria secundaria es adecuada, la infección se controla y los microorganismos y/o sus toxinas son neutralizados o eliminados. En cambio, cuando la respuesta inflamatoria es inadecuada, como ocurre en la sepsis, ésta puede llegar a perpetuarse por mecanismos moleculares que la tornan excesiva e incontrolada, afectando a órganos distantes del foco infeccioso inicial.
La sepsis y el shock séptico forman parte de un proceso complejo, en el cual intervienen factores propios de los microorganismo y sus endotoxinas, del huésped (como el papel de los macrófagos y neutrofilos en la liberación de mediadores de la respuesta inflamatoria como las citoquinas, quimiocinas e icosanoides) y otras sustancias producidas por células del organismo (como los radicales libres de oxígeno y el peróxido de hidrógeno) que causan daño celular por ser capaces de lesionar las membranas celulares y producir la necrosis.
La sepsis es fundamentalmente una patología inflamatoria, mediada por la activación del sistema inmunitario, la cual provoca la activación de citoquinas y mediadores bioquímicos que producen una vasodilatación sistémica arterial y venosa profunda, causando una disminución de las resistencias vasculares sistémicas, hipotensión por hipovolemia relativa (por acumulo de la sangre en la periferia) e hipoperfusión tissular como resultado.
Además de la alteración en el tono vascular, se produce una disfunción de la barrera endotelial, a causa de la ruptura de las estructuras que mantienen la integridad del endotelio, por adhesión de plaquetas y neutrófilos, y liberación de mediadores inflamatorios e intermediarios oxidativos entre otras sustancias, produciendo una alteración en la permeabilidad vascular. Como resultado, nos encontramos con una fuga de líquido vascular (proteínas y plasma) a través de la barrera endotelial comprometida hacia el espacio extravascular, produciéndose el denominado tercer espacio.
Aunque la respuesta inflamatoria sistémica temprana se ha considerado el sello distintivo de la sepsis, se produce además una inmunosupresión desde el principio de la respuesta a la sepsis por parte del huésped. Lo que conlleva a la aparición de complicaciones infecciosas, con un cambio hacia la infección por organismos oportunistas.
Además de la activación de la respuesta pro y antiinflamatoria, se producen alteraciones en vías no inmunológicas, como es en la coagulación. El estado anticoagulativo normal dentro de la vasculatura se encuentra interrumpido. Se produce una activación del sistema de la coagulación, secundario a la respuesta inflamatoria y las citoquinas, que favorece la agregación de plaquetas, leucocitos y eritrocitos y el depósito de fibrina en los capilares, formandose microtrombos a nivel de la microcirculación, que contribuyen a la isquemia tisular. Produciéndose además un consumo inapropiado de factores de coagulación que puede conllevar a la aparición de hemorragias.
El desequilibrio de la respuesta inflamatoria y las cascadas de fibrinólisis y coagulación se consideran elementos críticos en la devastadora progresión fisiológica que se produce en los pacientes que cursan con sepsis.
6.6. Afectación en los diferentes órganos
La sepsis es un trastorno sistémico, que puede afectar a todos los órganos del cuerpo, probablemente debido a las citoquinas y los mediadores que se liberan a la circulación general durante el inicio del trastorno.
La sepsis es una enfermedad tiempo dependiente, a más tiempo se produce más hipoperfusión y disfunción de órganos. Si no se controla la infección en las fases iniciales, aparecerán manifestaciones de disfunción multiorgánica entre las que podemos encontrar:
Disfunción respiratoria
La sepsis es la causa más frecuente de fallo respiratorio. Esto se debe al daño que se produce a nivel de las membranas de los capilares alveolares, causado por los mediadores de la inflamación. Este daño en la estructura pulmonar, que produce un aumento de la permeabilidad vascuclar y lesión endotelial, se traduce en la aparición de edema pulmonar. Afectándose la capacidad del pulmón para ser ventilado (afectando a la complianza) y el intercambio gaseoso, produciéndose hipoxemia.
El fallo respiratorio puede dividirse en:
- Fallo respiratorio hipoxémico: En este tipo de fallo encontramos una presión arterial de oxígeno (PaO2)
- Fallo respiratorio hipercápnico: En este tipo de fallo encontramos una presión arterial de dióxido de carbono (PaCO2) > 50 mmHg, causado por la debilidad de la musculatura respiratoria que es generada por una disfunción diafragmática.
- Síndrome de distrés respiratorio agudo (SDRA): el SDRA en la sepsis se produce a causa de la respuesta inflamatoria mal regulada. En ésta, se produce una inadecuada acumulación y activación de neutrófilos y plaquetas con activación de las vías de la coagulación, adhesión de células endoteliales y epitealiales, que producen mediadores proinflamatorios que ocasionan un incremento en la permeabilidad vascular y alveolar.
Los criterios diagnósticos para definir el SDRA son:
- Tiempo de inicio: desarrollo dentro de la primera semana del inicio de la clínica o aparición o empeoramiento de los síntomas respiratorios.
- Radiografía de tórax: presencia de opacidades bilaterales no justificables por derrame, atelectasia pulmonar lobar o pulmonar o nódulos.
- Origen del edema: fallo respiratorio no causado por insuficiencia cardíaca o sobrecarga de fluidos.
- Hipoxemia: se valora la PaFi que es la relación entre la PaO2 y la fracción inspiratoria de oxígeno (FiO2), con este criterio puede clasificarse según la gravedad en leve (PaFi 200-300), moderada (PaFi 100-200) y grave (PaFi <100).
La principal infección de origen respiratorio es la neumonía, siendo la infección más frecuente (40% del total de infecciones).
Fallo hemodinámico
La hipotensión es el hallazgo típico en pacientes que cursan con sepsis y shock séptico. El shock séptico es un síndrome complejo que se caracteriza por un fallo grave del sistema hemodinámico, asociado con alteraciones de la función cardíaca, redistribución del flujo sanguíneo y alteraciones en la microcirculación.
Depresión miocárdica: La afectación miocárdica en este contexto es secundaria a los productos proinflamatorios liberados por la respuesta inflamatoria (diversas citoquinas, óxido nítrico) que alteran tanto la contractibilidad como la relajación miocárdica, además de la propia hipoperfusión del miocardio por el proceso séptico. Ocasionando una depresión miocárdica caracterizada por dilatación biventricular y disminución de la fracción de eyección. Esta disfunción es transitoria, con resolución tras 7-10 días desde su aparición, aunque en algunos casos se puede prolongar.
Fallo metabólico
La sepsis se caracteriza por la existencia de un estado hipercatabólico, con un consumo acelerado de todas las reservas energéticas del organismo, que conduce al desarrollo de un estado de malnutrición que compromete más el sistema inmunitario.
Es frecuente la hiperglicemia, producida por los siguientes mecanismos:
- Estimulación de la gluconeogénesis.
- Disminución en la liberación de insulina e incremento de la resistencia a ésta.
- La hiperglicemia anula la función de los neutrófilos y produce un incremento de la expresión de las moléculas de adhesión en las células endoteliales.
Fallo renal
Debido al estado de hipotensión e hipoperfusión se produce una insuficiencia renal prerrenal. La hipoperfusión mantenida produce necrosis tubular aguda, causando una insuficiencia renal aguda, siendo una de las principales causas de morbilidad inducida por sepsis.
Este síndrome clínico se define por los siguientes marcadores de disfunción renal:
- Incremento de las cifras de urea y creatinina
- Caída del filtrado glomerular
- Disminución del ritmo diurético
Se puede reducir la incidencia de insuficiencia renal en la sepsis con una reanimación agresiva y el uso de un volumen apropiado en el trastorno.
Fallo hepático
La hipoperfusión hepática causa inicialmente un descenso de la síntesis de proteínas y un menor aclaramiento de ácido láctico e hiperglicemia. En fases más avanzadas, disminuyen los depósitos de hidratos de carbono, causando hipoglicemia.
La lesión hepática produce un aumento rápido de las concentraciones de transaminasas, más tardío de los niveles de bilirrubina, además de una alteración del tiempo de protombina.
La disfunción hepática es común en la sepsis y el shock séptico, y se debe a la necrosis centrolobulillar del hígado, secundaria a la mala perfusión hepática.
Disfunción gastrointestinal
Se producen una serie de alteraciones a nivel gastrointestinal que dificultan la administración de alimentos por vía digestiva: náuseas, vómitos, mayor residuo gástrico, íleo paralítico, ulceración de la mucosa intestinal y malabsorción de nutrientes y hemorragias (gastropatía hemorrágica aguda y úlceras agudas por estrés).
Además, la hipoperfusión intestinal produce la disfunción de las células endoteliales y la pérdida de su función de barrera protectora, evitando el paso a la circulación portal de los microorganismos que residen habitualmente en el tubo digestivo, por ruptura de la barrera istestinal. La hipoperfusión y la reperfusión intestinal ocasionan la liberación masiva de numerosos mediadores de la inflamación, que fomentan la disfunción multiorgánica.
Coagulopatía
Un 35% de los pacientes que desarrollan sepsis, pueden complicarse con la aparición de coagulación intravascular diseminada (CID). Ésta se produce por una compleja interacción entre la respuesta inflamatoria y procoagulante del huésped frente a la infección.
La CID puede presentarse en una de sus dos formás clínicas: con hemorragias en múltiples sitios o, por el contrario, con trombosis de vasos sanguíneos pequeños y medianos. En el caso de la CID secundaria a sepsis predomina la coagulación, siendo mínima la fibrinolisis, lo que condiciona una clínica representada por el fracaso orgánico más que por la hemorragia.
El progreso de la CID supone un consumo de factores de coagulación y plaquetas, a causa de la trombosis generalizada, lo cual condiciona una coagulopatía de consumo que a su vez justifica el sangrado en estadíos más avanzados.
Encefalopatía séptica
Se trata de una encefalopatía metabólica difusa, con manifestaciones inespecíficas que pueden ir desde un estado de intranquilidad y disminución del nivel de consciencia, hasta una agitación incontrolable y coma.
Un 70% de los pacientes con sepsis pueden desarrollar esta encefalopatía, aunque en muchos de estos la alteración del estado mental podría estar justificada por la hipoxemia e hipotensión propia del proceso.
Insuficienciasuprarrenal
Inicialmente se produce un aumento del uso de los lípidos almacenados para la síntesis de esteroides. A medida que progresa la sepsis, disminuye dicha síntesis progresando a un estado de insuficiencia suprarrenal secundaria.
6.7. Clínica
Desde el punto de vista clínico, el shock séptico puede clasificarse en dos fases:
Fase de shock caliente o hiperdinámico: las alteraciones clínicas que se producen son consecuencia de la respuesta del organismo a las endotoxinas y la vasodilatación generalizada que producen y los mecanismos de compensación.
- Alteración del estado mental (confusión o agitación)
- Hipotensión arterial (PAM 40 mmHg en personas hipertensas respecto a sus cifras habituales) con respuesta a líquidos
- Taquicardia, con pulsos saltones
- Taquipnea, con alcalosis respiratoria e hipocapnia (PaCO2
- Diuresis mantenida o disminuida con oliguria (<0,5 ml/kg/h)
- Hipertermia y fiebre (>38ºC), con escalofrios
- Piel caliente y enrojecida
- Relleno capilar normal
- Aparición de alteraciones del aparato digestivo como: nauseas, vómitos, diarrea o disminución de la motilidad gástrica
- Hiperglicemia y resistencia a la insulina
- Con la monitorización hemodinámica invasiva se puede evidenciar un perfil hiperdinámico, con gasto cardíaco elevado y resistencias vasculares sistémicas disminuidas.
Fase de shock frío o hipodinámico: a medida que progresa la sepsis y el shock se instaura, los tejidos se vuelven menos perfundidos y acidóticos, la compensación comienza a fallar y se empiezan a evidenciar signos de disfunción orgánica.
- Mayor afectación del SNC con depresión neurológica (estupor, coma)
- Hipotensión arterial, refractaria a líquidos y drogas vasoactivas
- Mayor taquicardia
- Mayor taquipnea, con respiraciones superficiales
- Descenso más marcado de la diuresis, con aparición de oligoanuria
- Temperatura dentro de rango o hipotermia (<36ºC)
- Piel fría, pálida y sudada
- Presencia de piel moteada, cianosis y/o livideces
- Hipoglicemia
- Con la monitorización hemodinámica invasiva se puede evidenciar un perfil hipodinámico, con bajo gasto cardiaco.
- Signos de disfunción orgánica de los diferentes sistemas: SDRA, insuficiencia renal aguda, trastornos de la hemostasia con aparición de CID, trastornos metabólicos con aparición de ácidosis láctica, etc.
En ausencia de un tratamiento eficaz se agravan las manifestaciones del shock y de la disfunción multiorgánica,pudiendose producir la muerte.
6.8. Manejo hemodinámico en la fase inicial
El manejo hemodinámico en la fase inicial, se realiza en base a los siguientes objetivos de reanimación:
- PAM igual o >65 mmHg
- Presión venosa central (PVC) entre 8-12 cmHg
- Ritmo diurético igual o >0,5 ml/kg/hora
- Saturación venosa central (svcO2) igual o >70%
- Aclaramiento de los niveles de lactato.
6.9. Criterios de gravedad
Son un resumen de todo lo mencionado anteriormente:
- PAM
- Débito urinario <0,5 ml/kg/h, con elevación de la creatinina en sangre
- Cifras de lactato >2 mmol/l y en ascenso
- Plaquetopenia <100.000/ml
- Afectación respiratoria con relación PaO2/ FiO2
- Alteración del estado mental
6.10. “Hour-1 Surviving Sepsis Campaign bundle of Care”
La sepsis y el shock séptico, como se ha descrito, se consideran emergencias médicas, motivo por el cual el tratamiento y la reanimación deben iniciarse inmediatamente, siguiendo las directrices de la Surviving Sepsis Campaign.
En el año 2016 se clasificaron las intervenciones que se tenian que llevar a cabo teniendo en cuenta el progreso de la patología, especificándose los cuidados que se debian realizar antes de la primera, tercera y sexta hora desde su inicio o diagnóstico. En el año 2018, tras la revisión de la evidencia científica recogida hasta el momento, se combinaron las medidas terapéuticas establecidas creando un único paquete, con la intención de iniciar la reanimación y el manejo inmediatamente.
Las medidas propuestas por la Surviving Sepsis Campaign son:
- Medición del lactato sérico: Si el lactato se encuentra >2 mmol/l, debe realizarse nuevas mediciones para guiar la reanimación con fluidos, con el objetivo de normalizar sus niveles.
- Obtener hemocultivos: su obtención debe realizarse antes del inicio de la terapia antibiótica, con el objetivo de identificar el/los patogeno/s causantes del cuadro séptico. Sin que suponga una demora, superior a 45 minutos, en el inicio de la terapia antibiótica por su obtención.
- Administración de antiobióticos de amplio espectro: se recomienda iniciar el tratamiento endovenoso con antibióticos de la manera más precoz, tras confirmarse a sepsis y/o el shock séptico, en el plazo máximo de una hora. Se iniciará un tratamiento antibiótico empírico de amplio espectro, con la administración de uno o más antimicrobianos intravenosos, con el objetivo de cubrir todos los posibles patógenos.
- Administración de líquidos: la reanimación temprana y efectiva con líquidos es esencial para la estabilización de la hipoperfusión tisular causada por la sepsis o el shock séptico. Se administrará al menos 30 ml/kg de solución cristaloide por vía intravenosa, dentro de las primeras 3 horas. Y posteriormente a la resucitación inicial, los fluidos adicionales se administrarán mediante una reevaluación del estado hemodinámico, en función de las necesidades del paciente.
- Administración de vasopresores: en el caso de que la presión arterial no se restablezca con la reanimación inicial con líquidos, se iniciará la administración de vasopresores dentro de la primera hora con el objetivo de alcanzar una PAM >65 mmHg.
7. SINDROME DE DISFUNCIÓN ORGANICA MULTIPLE (SDOM)
El síndrome de disfunción orgánica múltiple (SDOM) se refiere a la disfunción progresiva de órganos en un paciente enfermo, de tal manera que la homeostasis no puede mantenerse sin una intervención clínica para apoyar la función continua del órgano. Se trata de otra fase en la progresión de los estados de shock.
Puede ser una complicación de cualquier forma de shock, pero se observa con mayor frecuencia en los pacientes con sepsis. El mecanismo preciso por el que se produce se desconoce, pero suele presentarse con frecuencia hacia el final del continuo del shock séptico, cuando la perfusión tisular no se puede restaurar de manera eficaz.
El fallo orgánico normalmente se inicia a nivel pulmonar, siguiéndole la inestabilidad cardiovascular, así como el fallo de los sistemas hepático, digestivo, renal, inmunológico y nervioso central. Esta secuencia de disfunción del órgano puede variar en función de la enfermedad primaria del paciente y las comorbilidades existentes antes de experimentar el shock.
Pese a que no es posible predecir el SDMO, se pueden utilizar las herramientas de evaluación clínica de la gravedad, como el SOFA o el APACHE, para anticipar el riesgo del paciente de disfunción orgánica y mortalidad. La disfunción de un sistema orgánico se asocia con un 20% de mortalidad, siendo almenos del 60% si fallan más de cuatro órganos.
La edad avanzada, la desnutrición y las enfermedades coexistentes parecen incrementar el riesgo de desarrollar SDMO en los pacientes con enfermedades agudas.
La prevención continúa siendo la principal prioridad en el control del SDMO.
8. DIAGNOSTICO DEL SHOCK
Un paciente con sospecha de shock constituye una emergencia médica, de la misma manera que lo es un politraumatismo o un infarto agudo de miocardio.
El diagnóstico del shock es principalmente clínico, basado en la observación de los signos y síntomas que presente el paciente, los datos obtenidos mediante la monitorización de éste y los datos de laboratorio, mediante la medición de los parámetros analíticos más directamente relacionados con el proceso. Todo ello ayudará a determinar la intesidad del cuadro y la posible causa subyacente.
8.1. Datos clínicos, hemodinámicos y bioquímicos
Es importante el reconocimiento precoz del shock, dado que su reversibilidad y morbimortalidad dependen del estadio evolutivo en que se encuentre en el momento del diagnóstico. Para ello inicialmente se obtendrá una historia clínica del paciente (alergias, patologías de base, tratamiento habitual, etc) y se realizará una exploración física meticulosa en la busqueda de datos clínicos y hemodinámicos mediante la monitorización que, juntamente a datos bioquímicos, confirmen el estado de shock.
- Datos clínicos: presencia de signos de hipoperfusión en las 3 ventanas corporales: neurológica (inquietud, irritabilidad, ansiedad, confusión, desorientación y somnolencia), renal (oliguria) y cutánea (piel fría, pálida y diaforética).
Pueden hallarse signos que nos puedan orientar del tipo de shock: presencia de hemorragias, vómitos o diarreas y sequedad de piel y mucosas (shock hipovolémico); disnea, dolor torácico, palpitaciones, soplos cardíacos e ingurgitación yugular (shock cardiogénico); tonos apagados, pulso paradójico e injurgitación yugular (shock obstructivo); disnea, angioedema, obstrucción de vía aerea, erupción cutanea generalizada, prurito (shock anafilático); disnea, fiebre y síntomas de localización de la infección (shock séptico), entre otros muchos signos.
- Datos hemodinámicos: desde los momentos iniciales del shock nos encontraremos con la presencia de taquicardia, asociada o no a hipotensión. Es importante recordar que en estadíos iniciales, en los cuales actuan los mecanismos compensadores del shock, la presión arterial puede estar conservada. A medida que se instaura el shock, y los mecanismos compensatorios son insuficientes, se produce hipotensión arterial. Por tanto la ausencia de hipotensión no excluye el shock, de hecho cuando la presión arterial está disminuida el shock ya esta instaurado.
- Datos bioquímicos: hiperlactacidemia >2 mmol/l.
En el caso de la sepsis y shock séptico, como se ha descrito anteriormente, las escalas de valoración qSOFA y SOFA contribuyen en su diagnóstico.
8.2. Pruebas complementarias
El diagnóstico inicial se completará con pruebas analíticas, electrocardiograma y estudios de imagen, según la sospecha etiológica y la estabilidad clínica del paciente, con el objetivo de orientar el grado de afectación del paciente y descubrir el origen del shock.
Analítica sanguínea
Bioquímica sanguínea:
- Ionograma: valoración de niveles de glucosa plasmática e iones. Podemos encontrar trastornos electrolíticos en el sodio y potasio en pacientes con fallo renal y acidosis metabólica (hiperpotasemia).
En el caso de shock hipovolémico no hemorrágico (secundario a vómitos, diarrea o tercer espacio), podemos encontrar alteraciones como hiponatremia, hipocloremia, hipocalcemia e hipopotasemia.
La hiperglicemia y la resistencia a la insulina son alteraciones habituales en pacientes sépticos. Pudiendo encontrar también hipoglicemia en el caso de fallo hepático.
- Función renal: valoración de los niveles de urea y creatinina, su elevación implica una insuficiencia renal secundaria a la hipoperfusión renal.
La urea puede verse incrementada además por hemorragia gastrointestinal, deshidratación (como puede ocurrir en el shock hipovolémico no hemorrágico), fiebre y sepsis.
- Función hepática: valoración de los niveles de transaminasas (aspartato aminotransferasa AST, alanina aminotransferasa ALT) y bilirrubina. Con aumento de transaminasas en el fallo hepático, siendo la alteración de los niveles de bilirrubina con hiperbilirrubinemia más tardía.
- Marcadores cardiacos: podemos encontrar niveles elevados de troponina I, CPK-MB (isoenzima MB de la creatininfosfoquinasa) y mioglobina en el shock cardiogénico de causa coronaria, por isquemia miocárdica. También pueden incrementar los niveles de péptidos natriuréticos (BNP o NT-proBNP) en el caso de insuficiencia cardíaca, como causa o consecuencia del shock, por estiramiento de las células de la aurícula.
Hemograma:
- Hematocrito, niveles de hemoglobina y recuento de hematíes: la deshidratación puede producir un incremento en el valor del hematocrito, por hemoconcentración, como ocurre en el shock hipovolémico no hemorrágico.
La disminución en los valores de hematocrito y hemoglobina indican la presencia de sangrado en el shock hipovolémico hemorrágico, pese a que en las fases iniciales suele haber normalidad en estos parámetros. Se tiene que tener presenta la posibilidad de hemodilución de la muestra por una fluidoterapia intensiva en la reanimación con líquidos.
- Fórmula leucocitaria: podemos encontrar leucocitosis con predominio de neutrófilos, con desviación a la izquierda en procesos bacterianos, o leucopenia en el shock séptico. Siendo posible encontrar aumento de leucocitos y del porcentaje de neutrofilos en otros tipos de shock como el hipovolémico.
Eosinofília en los casos de anafilaxia (shock anafiláctico).
- Plaquetas: podemos encontrar una reducción en el número de plaquetas (plaquetopenia/ trombocitopenia) por diversas causas: por consumo en el shock hemorrágico, por CID (más a menudo en el shock o tras un traumatismo severo) y por transfusiones de concentrados de hematíes.
Estudio de coagulación:
- TP, TTPa y D- dímero: el aumento en los tiempos de protrombina (TP), la prolongación del tiempo de tromboplastina activada (TTPa) y la disminución del nivel de fibrinógeno pueden ser consecuencia de una coagulopatía poshemorrágica o postransfusional en el shock hipovolémico hemorrágico.
El incremento del TP y la prolongación del TTPa pueder indicar insuficiencia hepática.
La aparición de plaquetopenia con disminución del fibrinógeno, aumento del TP, prolongacion de TTPa y la aparición de D- dímero sugieren el desarrollo de una CID.
Un incremento en la concentración de D- dímero no es un signo específico del tromboembolismo pulmonar (TEP), ya que puede aparecer como se ha descrito en la CID.
Gasometría:
Dependiente de la situación clínica del paciente se obtendrá una gasometría arterial (ante la presencia de insuficiencia respiratorio y/o sospecha de hipercapnia) o como mínimo venosa, para conocer el pH, bicarbonato, exceso de bases y la determinación del lactato.
- Arterial: es una medida muy sensible del estado metabólico en el que se encuentra el paciente, pudiendo encontrar acidosis metabólica o mixta, con aumento del lactato. La presencia de acidosis metabólica con retención de CO2, es un dato que refleja la incapacidad del paciente para compensar el estado de acidosis.
En las fases iniciales de shock podemos observar alcalosis respiratoria, por hiperventilación, resultante del mecanismo compensatorio para eliminar el exceso de CO2 producido por el metabolismo anaerobio.
Además, puede aparecer hipoxemia debido al estado de shock.
- Venosa: es posible realizar la medición de la saturación de oxígeno de la hemoglobina (preferiblemente en sangre venosa central a nivel de la vena cava superior SvcO2), para determinar el consumo de oxígeno y la diferencia entre los valores arteriales y venosos de la presión parcial de dióxido de carbono (V-ApCO2).
Podemos encontrar una SvCO2 < 65% por alteración en el aporte de oxígeno a los tejidos y un incremento compensatorio de su extracción.
Una V-ApCO2 > 6 mmHg puede indicar la existencia de un aporte de oxígeno disminuido, incluso cuando los valores de SvCO2 son normales.
También es posible determinar el nivel de lactato en una muestra venosa.
Grupo sanguineo: realización de pruebas cruzadas para la administración de hemoderivados en el shock hipovolémico de causa hemorrágica y en aquellas situaciones que lo precisen.
En el caso de sospecha infecciosa: cultivos de sangre (hemocultivo), orina (urocultivo) y otras muestras según sospecha etiológica (esputo, abcesos, heridas). En pacientes con sospecha de sepsis o shock séptico, se deben obtener cultivos microbiológicos de todos los sitios que se consideren posibles fuentes de infección, antes del inicio del tratamiento antibiótico, siempre que no se demore el inicio de éste por la extracción de las muestras.
La esterilización de los cultivos puede darse en el plazo de minutos a horas tras la primera dosis de antibiótico adecuado, por ello la obtención de cultivos antes de la administración de antibióticos incrementa significativamente la obtención de cultivos, facilitando la identificación del patógeno causante.
La relación riesgo/ beneficio favorece la administración rápida de antibióticos, si no fuera posible obtener los cultivos. Se establece un periodo de 45 minutos como ejemplo de lo que no se consideraría una demora en el inicio del tratamiento antibiótico.
Estos cultivos pueden incluir, además de la sangre: orina, secreciones respiratorias, heridas, líquido cefalorraquídeo y otros líquidos corporales. Si los antecedentes o la exploración clínica indica origen anatómico de la infección claro, no es necesario realizar cultivos de otros sitios, salvo de sangre.
Se recomienda obtener dos conjuntos de cultivos de sangre (aerobio y anaerobio), pudiendo extraerse al mismo tiempo, ya que no se ha demostrado que la obtención de cultivos en sangre mejore cuando se realizan las extracciones secuenciales ni cuando coindicen con los picos de temperatura.
En pacientes que se sospeche de infección de cateter venoso, se debe obtener al menos un cultivo de sangre del catéter, junto a cultivos de sangre periférica obtenidos mediante punción.
Electrocardiograma de 12 derivaciones: El ECG estándar de 12 derivaciones puede ayudar a identificar alteraciones del ritmo y la conducción, hipertrofia cardíaca, pericarditis, desequilibrios electrolíticos, toxicidad por fármacos, isquemia e infarto agudo de miocardio (sitio y extensión).
El ECG habitual evalúa sólo el ventrículo izquierdo, si se busca valorar el ventrículo derecho, en busca de daño o disfunción, se puede realizar un ECG con derivaciones torácicas derechas, o un ECG con derivaciones posteriores si se busca daño miocárdico en la superficie posterior del corazón.
En el shock habitualmente se observa una taquicardia sinusal, pero pueden hallarse además alteraciones del ritmo, así como alteraciones del segmento ST y la onda T debido a las posibles alteraciones iónicas y metabólicas que se dan en los pacientes con shock, o secundarias a la existencia de isquémia cardíaca, siendo de especial interés en el shock cardiogénico de causa coronaria.
Radiografía de tórax o abdomen: la radiografía de tórax puede ayudar a evaluar los signos de insuficiencia cardíaca (cardiomegalia, edema pulmonar, congestión pulmonar), y las causas de la insuficiencia respiratoria (como el derrame pleural, neumotorax o SDRA, entre otros) y de la sepsis/ shock séptico (como la neumonía). De todos modos, una radiografía de tórax sola no puede descartar un problema cardíaco, pueden aparecen signos clínicos hasta 24-48h antes de que el problema aparezca en la radiografía.
Se puede realizar una radiografía de abdomen en el caso que se sospeche de perforación del tracto digestivo o íleo mecánico.
Ecocardiograma transtorácico, transesofágico, abdominal, venosa y ecocardiografía: Puede ser útil realizar ecografías torácicas o abdominales en aquellos casos en que se sospeche de hemorragia interna, patología intraabdominal, tercer espacio, etc.
La ecocardiografía puede ser útil para valorar la funcionalidad del corazón y la afectación cardíaca en cualquier tipo de shock, la respuesta al tratamiento instaurado, además de para establecer la causa del shock cardiogénico y obstructivo (miocardiopatías, alteración de la contractibilidad del miocardio, disfunción valvular, taponamiento cardíaco, etc).
La ecografía venosa puede ser de utilidad ante la sospecha de embolismo pulmonar.
Otras pruebas de imagen: La TC se solicita cuando los resultados obtenidos mediante la ecografía no son concluyentes, así como en el caso del shock de origen traumático, el cual precisa una valoración de un mayor número de órganos, en los que alguno de ellos no pueden ser valorados mediante la ecografía (como son los de localización retroperitoneal). Según la localizacion encontramos:
- TC craneal: ante sospecha de edema cerebral, lesiones postraumáticas o accidente cerebrovascular (AVC).
- TC de tórax: ante la sospehca de tromboembolismo pulmonar (angioTAC), disección de aorta o ruptura del aneurisma aórtico.
- TC abdominal: en la busqueda de focos infecciosos en caso de sepsis, entre otras utilidades.
9. MARCADORES DE HIPOPERFUSION
Tras el inicio del tratamiento, la intención de normalizar la perfusión tisular puede monitorizarse mediante la medición de la saturación venosa de oxígeno (SvO2) y, sobre todo, con la determinación seriada de los niveles de lactato.
9.1. Lactato sérico
El lactato es el producto final de la glucólisis anaerobia. Durante la hipoperfusión, el piruvato intracelular (molécula base para la producción de energía) se convierte en lactato para mantener la producción de energía (ATP), ante la falta de oxígeno.
La concentración normal de lactato en sangre es
En situaciones de shock, las cifras de lactato pueden verse incrementadas por un aumento en su producción, secundario al metabolismo anaerobio, y/o una disminución en su aclaramiento a nivel hepático, renal y músculo esquelético, a medida que el shock progresa y se produce el fallo circulatorio y la hipoxia tissular, produciéndose una acidosis metabólica.
El lactato es considerado un excelente marcador de hipoxia tisular y del metabolismo tisular, siendo un marcador de la evolución del shock.
En la sepsis y el shock séptico, las concentraciones de lactato tienen un valor pronóstico importante. Tanto el nivel inicial de lactato, el lactato máximo, su aclaramiento, como el tiempo que tarda en normalizarse, son predictivos de mortalidad, siendo mayor la mortalidad a mayor nivel de lactato, menor aclaramiento o normalización.
Un ascenso >2 mmol/l y especialmente >4 mmol/l en paciente con sepsis, con o sin hipotensión, se asocia a una mayor mortalidad y peor pronóstico. Por el contrario, su progresión decreciente, con mejora de las cifras y del aclaramiento, indicaría un tratamiento adecuado, y se corresponden con la recuperación de la hipoperfusión tisular. Un aclaramiento del lacatato >10% en las primeras seis horas y su normalización en las primeras 24-48h, se asocia a un aumento de la supervivencia.
9.2. Saturación venosa mixta de oxígeno (SvO2) y saturación venosa central de oxígeno (SvCO2)
Los tejidos corporales utilizan un 25% del oxígeno administrado durante el metabolismo normal. Sin embargo, durante acontecimientos estresantes como el shock, los tejidos consumen más oxígeno, produciéndose una disminución en la saturación venosa de oxígeno, como puede ocurrir en el shock hipovolémico, obstructivo y cardiogénico. En cambio en el shock séptico nos encontramos con la situación contraria, cuando a medida que avanza éste y se producen microtrombos en la microcirculación, nos encontramos con una maldistribución de la sangre por los tejidos que dificulta la obtención de oxígeno, pudiendo encontrar saturaciones venosas de oxígeno elevadas.
La saturación venosa de oxígeno, como marcador de hipoperfusión, se puede obtener
mediante el uso de un cateter central situado en la vena cava superior, obteniendo la saturación venosa central de oxígeno (SvcO2) o a través de un cateter alojado en la arteria pulmonar (Swan-Ganz), obteniendo la saturación venosa mixta de oxígeno (SvO2).
SvO2: Hace mención a la saturación de la hemoglobina en la arteria pulmonar proximal, siendo el mejor indicador de la adecuación del transporte de oxígeno (DO2). Su valor depende del volúmen minuto cardiaco, la demanda de oxígeno, la concentración de hemoglobina y la saturación de oxígeno, viendose disminuido en situaciones de bajo gasto, aumento del consumo de oxígeno, descenso de hemoglobina e hipoxemia.
Se considera una medida indirecta de la oxigenación tisular, ya que nos indica el grado de aporte de oxígeno tisular y del estado de perfusión. En patologías graves como el shock, su descenso se asocia a mal pronóstico, ayudándonos su monitorización a guiar las intervenciones terapéuticas.
La interpretación de la SvO2 es la siguiente:
- SvO2 65-75%: valores normales
- SvO2 <65%: disminución en la disponibilidad de oxígeno
- SvO2 cerca del 50%: oxigenación tisular alterada
- SvO2 >75%: alteración en el consumo de oxígeno (frecuente en la sepsis y shock séptico, por el daño celular producido).
SvcO2: Hace mención a la saturación de hemoglobina en la vena cava superior. De la misma manera que la SvO2, su valor depende del volumen minuto cardiaco, la demanda de oxígeno, la concentración de hemoglobina y la saturación de oxígeno.
Los valores de SvcO2 deben mantenerse >70%, pudiéndose utilizar en la práctica en pacientes graves en general, con cualquier tipo de shock, y en pacientes con insuficiencia cardiaca.
Vigilar el consumo de SvcO2 es una medida invasiva que permite evaluar con mayor precisión la oxigenación tissular en la fase compensatoria del shock, antes de que aparezcan alteraciones en los signos vitales secundarias a la perfusión tisular alterada.
La SvcO2 ha demostrado una buena correlación con la SvO2 (la SvcO2 sobreestima un 5%). En el manejo del estado de shock, se han marcado como objetivos valores de SvcO2 >70% y SvO2 >65%. Concretamente, una SvcO2 >70% ha demostrado disminuir significativamente la morbimortalidad intrahospitalaria.
9.3. Diferencia venoarterial de la presión de dióxido de carbono (CO2)
En condiciones fisiológicas, el contenido de dióxido de carbono venoso es mayor que el arterial, resultante de la producción de CO2 a nivel periférico, sumado al consumo de oxígeno y el metabolismo en general.
Niveles de P(v-a)CO2 >6 mmHg han demostrado ser de utilidad en la detección de hipoperfusión persistente, incluso cuando los valores de SvcO2 son normales.
10. TRATAMIENTO DEL SHOCK
El shock es una patología tiempo dependiente, empeorando la situación de hipoxia tissular a medida que éste progresa sin instaurar un tratamiento adecuado.
El tratamiento específico de cada uno de los tipos de shock se dirige a identificar y corregir su causa. El tratamiento general del shock, de manera común en todos los tipos, se dirige a mejorar la utilización del oxígeno por parte de los tejidos y restablecer la perfusión tisular, a través de los siguientes métodos:
- Apoyar el sistema respiratorio, para obtener una adecuada oxigenación sanguinea
- Optimizar el volumen intravascular, mejorando la precarga
- Apoyar la acción de bombeo del corazón
- Mejorar la capacidad del sistema vascular, optimizando de las resistencias vasculares
Además de realizarse otras intervenciones y terapias de soporte (soporte nutricional enteral temprano, control de la hiperglicemia, etc).
El objetivo principal es recuperar el metabolismo celular aeróbico, de la forma más precoz posible.
10.1. Tratamiento de la causa
El tratamiento específico de cada uno de los tipos de shock va dirigido a corregir su causa. El tratamiento inicial ira dirigido a tratar la causa en situaciones de riesgo vital (taponamiento cardíaco, neumotórax a tensión, etc) en las que existe la posibilidad terapéutica para realizarlo, o se optará por un tratamiento diferido mejorando en primer lugar las alteraciones producidas por el shock.
En función del shock y su causa, encontramos diferentes intervenciones a realizar para tratarlo:
- Shock hipovolémico de causa hemorrágica: la medida más importante es identificar y controlar rápidamente cualquier foco de hemorragia, tanto externa como interna, pudiéndo requerir compresión externa manual ante un sangrado externo, intervención quirúrgica en un sangrado interno o el uso de radiología intervencionista (angiografía), en los casos en los que el sangrado haya sido producido por daño vascular, para controlar la hemorragia.
- Shock cardiogénico: En el shock cardiogénico de causa coronaria, el paciente puede precisar tratamiento trombolítico (fibrinólisis), procedimientos coronarios percutaneos (angioplastia con colocación de stent) o quirúrgico para la revascularización coronaria, tratamiento con bomba de balón intraaórtico, uso de dispositivos de asistencia ventricular o la combinación de éstos.
En el shock cardiogénico de causa no coronaria, según la causa subyacente, puede precisar reemplazo de válvula cardíaca en el caso de valvulopatías, corrección de una arritmia, corrección de la acidosis y las alteraciones electrolíticas, entre otras.
En situaciones de edema pulmonar agudo asociado, es relevante el papel de la ventilación mecánica no invasiva por un lado, para tratarlo y revertir la insuficiencia respiratoria aguda producida y, por otro lado, como medida terapéutica para mejorar el fallo de la bomba cardiaca, ya que contribuye a la mejora de la mecánica cardiaca.
- Shock obstructivo: en función de la causa que lo haya desencadenado podemos encontrar diferentes intervenciones: drenaje torácico en el neumotórax a tensión, pericardiocentesis en el taponamiento cardiaco o el uso de trombolíticos en el tromboembolismo pulmonar masivo cuando existe inestabilidad hemodinámica.
- Shock distributivo de tipo anafiláctico: Además de las medidas generales aplicadas (manejo de la vía aerea, reposición de volemia, etc), precisa la administración de adrenalina intramuscular de manera inmediata, en una dilución de 1:1000, en el miembro superior o el muslo y en ocasiones mediante infusión endovenosa, para restablecer el tono vascular por su acción vasoconstrictora. La dosis en adultos va de 0,3-0,5 mg y en los niños de 0,01 mg/kg, pudiéndose repetir a los 5-15 minutos.
Además se administrarán otros fármacos como tratamiento adyuvante, vía endovenosa, como los antihistamínicos para revertir los efectos de la histamina, corticoesteroides o broncodilatadores para revertir el broncoespasmo, etc.
- Shock distributivo de tipo neurogénico: en el caso de estar producido por una lesión de la médula espinal, es preciso la estabilización de la lesión quirúrgicamente o, en el caso de ser consecuencia de la anestesia raquídea, mediante la colocación adecuada de ésta.
- Shock distributivo de tipo séptico: Además de las estrategias comunes, ante la sospecha de la existencia de un foco infeccioso sera necesario la administración de antibioticoterapia empírica precoz, a la espera de los resultados de los cultivos, siguiendo las directrices descritas en el apartado de sepsis y shock séptico.
Una vez identificado el patógeno causante, se desescalará la terapia antibiótica dirigiéndose a la sensibilidad del patógeno. En aquellos pacientes con sepsis, que no se identifique el patógeno causante (suele ser un tercio de los pacientes), la reducción de la antibioticoterapia se realizará gradualmente en función de la mejoría clínica que presente o la evidencia de resolución de la infección. Y en el caso en que se sospeche que no existe foco infeccioso, se suspendera la terapia antibiótica.
10.2. Tratamiento general del shock: soporte respiratorio (A,B)
De la misma forma que ocurre en otras situaciones críticas, la prioridad inicial en el shock es asegurar una función respiratoria adecuada, manteniendo la permeabilidad de la vía aérea y una ventilación y oxigenación adecuada.
Se procederá a la intubación endotraqueal si existe insuficiencia respiratoria severa con hipoxemia (PO2
Además de asegurar la vía aerea, previniendo la aspiración y el compromiso respiratorio posterior, y permitir una ventilación y oxigenación adecuada, el uso de la ventilación mecánica invasiva tiene el beneficio de disminuir la demanda de oxígeno de los músculos respiratorios y la postcarga del ventrículo izquierdo al incrementar la presión intratorácica.
Se tiene que prestar especial atención a los pacientes politraumatizados o polifracturados con posible lesion medular, especialmente a nivel cervical (C). En lesiones por encima de C5 es necesario el soporte ventilatorio por falta de una musculatura respiratoria eficaz (lesiones en C1-C2) o por una ventilación dependiente de los músculos accesorios (lesión C3-C4). En lesiones inferiores de C5 se producen parálisis de la musculatura intercostal y abdominal, precisando la mayoría de soporte respiratorio también.
Tras un trauma, en el caso que el paciente requiera ser intubado, debe realizarse un manejo como si tuviese una lesión medular a nivel cervical, asegurando la vía aérea con el mínimo movimiento de la columna cervical para no producir o empeorar posibles lesiones.
Durante la secuencia de intubación, debe prestarse atención a la hemodinamia del paciente, ya que se puede producir una disminución de la presión arterial y el gasto cardíaco, secundario a los efectos vasodilatadores y depresores miocárdicos propios de los fármacos utilizados para realizar la inducción anestésica (midazolam, propofol, etc).
Se instaurará oxígeno suplementario, mediante los diferentes metodos disponibles (cánulas nasales, mascarilla tipo venturi, terapia de alto flujo, ventilación mecánica no invasiva o invasiva, etc), según la necesidad del paciente para proporcionar una oxigenación óptima (spO2 >94% mediante pulsioximetría), valorando además la aparición o resolución de la hipercapnia en pacientes con patologías respiratorias de base (EPOC).
En el caso de la aparición de SDRA, se recomienda una ventilación protectiva mediante:
- Volumenes corriente más bajos, de 6 ml/kg del peso corporal previsto (PBW), en lugar de más altos
- Mayores frecuencias respiratorias (hasta 35 inspiraciones/ minuto), durante la reducción del volumen corriente, con el fin de mantener la ventilación por minuto
- Utilizar la PEEP más elevada que permita el pulmón, en lugar de la más baja, con el objetivo de reclutar unidades pulmonares para el intercambio gaseoso, vigilando la presión meseta de la vía aérea
- Mantener la presión meseta de la vía aérea inferior a 30 cmH2O
- Utilizar la FiO2 necesaria para mantener una oxigenación adecuada
- Utilizar maniobras de reclutamiento si lo precisa el paciente
- Utilizar la posición decúbito prono en lugar de decúbito supino, en pacientes con SDRA con proporciones de PaO2/FiO2 (PaFi) <150
10.3. Tratamiento general del shock: soporte circulatorio (C)
Una vez asegurada la función respiratoria, se inicia el soporte circulatorio con la reanimación con líquidos, con el objetivo de restaurar el volumen intravascular.
Durante esta reposición de líquidos es necesario un control de sus efectos en la mejora de la perfusión (producción urinarea adecuada, cambios en el estado mental, en la piel y en los signos vitales), vigilando además la posible aparición de efectos secundarios y complicaciones, derivadas de la fluidoterapia. Debe evitarse tanto la reanimación insuficiente, asociada con mayor incidencia de morbimortalidad, como la excesiva. La administración excesiva de líquidos puede causar sobrecarga cardiovascular (edema sistémico), edema agudo pulmonar (EAP), hipertensión intraabdominal (HIA), el síndrome compartimental abdominal (SCA) y síndrome de disfunción orgánica múltiple (SDMO).
Para ello, se siguen unas pautas en la reanimación de líquidos donde se establecen unos objetivos de PAM, indicaciones y contraindicaciones de los líquidos utilizados según el tipo de shock y la velocidad de infusión de éstos. Además, se realizará una monitorización hemodinámica para valorar la respuesta al tratamiento y guiar su transcurso. En los casos en que la hipotensión es severa o no presenta respuesta a la infusión de líquidos, y/o se produce afectación de la función cardíaca, se utilizarán fármacos vasoactivos e ionotrópos según precise el paciente.
Para la infusión de líquidos será necesario inicialmente canalizar dos vías venosas periféricas para obtener acceso vascular, preferiblemente de calibre grueso, ya que son más rápidas (hasta un 75% mayor respecto a catéteres centrales de igual diámetro) y accesibles. Posteriormente, puede ser necesario canalizar una vía central, para la infusión de fármacos vasoactivos y/o la monitorización de la respuesta al tratamiento.
Reposición de la volemia: tipos de líquidos
Los tipos de líquidos administrados y la velocidad de administración a la que se infunden varian en función del tipo de shock, pero en todos ellos se administran con el objetivo de mejorar la oxigenación cardíaca y tisular, que en parte dependen del flujo.
De la misma forma que se realiza con cualquier fármaco, la administración de los fluidos debe realizarse con precaución e igual grado de conocimiento de sus indicaciones, contraindicaciones y efectos adversos.
Los líquidos administrados pueden incluir los cristaloides, los coloides y los componentes sanguíneos. La principal diferencia entre los cristaloides y los coloides es el mecanismo que emplean para expandir la volemia. Los cristaloides utilizan la presión osmótica, producida por la diferencia de concentración de solutos entre dos fluidos, para producir el arrastre de agua. En cambio los coloides utilizan la presión oncótica, producida por la diferencia de concentración de proteínas entre dos medios, para producir el paso de agua.
En general los coloides presenta mayor potencia que los cristaloides en la expansión de volemia y duración de su efecto, pero estan sujetos a mayor riesgo de efectos secundarios que incluyen: reacciones anafilácticas severas, prurito, deterioro de la función renal y de la hemostasia. Por esto, y por no presentar ninguna ventaja en cuanto a la supervivencia, las soluciones coloides no se utilizan inicialmente en la reanimación del paciente crítico. Además, el uso de coloides sintéticos se encuentra limitado en determinados tipos de pacientes críticos (paciente politraumático sangrante por su potencial alteración de la coagulación el uso de almidones en el paciente séptico, etc).
Por tanto, la balanza se inclina hacia el uso de los cristaloides por no presentar reacciones alérgicas, no afectar directamente al sistema de coagulación, y por su bajo coste.
La elección del tipo de fluidoterapia dependerá del perfil del paciente. Actualmente los cristaloides (SF o soluciones balanceadas) se consideran una opción válida para iniciar la reanimación con fluidos en el paciente crítico, incluyendo a los pacientes con sepsis y shock séptico, vigilando estrechamente la aparición de acidosis hiperclorémica. En el caso de que se produzca hipercloremia por uso de SF 0,9%, con o sin acidosis metabólica asociada, se recomienda utilizar fluidos con menor cantidad de cloro como las soluciones balanceadas.
Los cristaloides que se emplean de manera habitual en la reanimación del shock hipovolémico incluyen el SF 0,9% y la solución de Ringer lactato.
En el caso de la sepsis y el shock séptico, se sugiere el uso de albumina junto a los cristaloides, tanto en la reanimación inicial como en el posterior reemplazo del volumen intravascular en aquellos pacientes que precisen grandes cantidades de cristaloides. Se debe restringir el uso de almidones en el paciente con sepsis y/o shock séptico, por asociarse con un mayor riesgo de muerte, y necesidad de tratamiento renal sustitutivo debido a que aumentan la incidencia de fracaso renal agudo.
Cristaloides
Los cristaloides son soluciones que contienen agua, electrolitos y/o azúcares en diferentes proporciones, determinando su tonicidad, permeables a la membrana capilar.
- El suero hiposalino (ClNa al 0,45%) es una solución hipotónica, que puede estar indicada en la deshidratación con hipernatremia, pero no como expansor plasmático.
- Las soluciones salinas hipertónicas (ClNa a 3,7-5%) presentan concentraciones electrolíticas mayores a las del plasma sanguíneo. Son expansoras en mayor medida, ya que producen el paso de agua desde el comportamiento intersticial al intravascular, asociándose su aporte a un incremento en la volemia de 9 a 10 veces el volumen infundido, aunque de corta duración (
Sin embargo, su utilización en la reanimación del paciente crítico está en fase de investigación, quiza con la excepción del paciente politraumatizado, pudiendo adminitrarse en paciente con shock y lesión cerebral traumática.
- La solución salina fisiológica (ClNa/ SF al 0,9%) es levemente hipertónica respecto al plasma sanguíneo, con mayores concentraciones de sodio y cloro, y tiene un pH ácido. Se trata de la solución más utilizada en la práctica clínica, imprescindible en la reanimación de pacientes politraumatizados con TCE.
Siempre que la función renal esté conservada, el exceso de cloro que presenta esta solución será eliminado por el riñon. Pero en situaciones en que se produce su acumulo, como la insuficiencia renal, aparece una de sus principales complicaciones, la acidosis hiperclorémica.
- Para evitar esta acidosis, se han desarrollado soluciones equilibradas/ balanceadas, en las que se han reducido las concentraciones de sodio, y especialmente de cloro, sustituyéndose este anión por lactato (Ringer lactato), acetato (Ringer acetato, no comercializado actualmente en nuestro país), malato (Isofundin) o gluconato (Plasmalyte).
El pH de estas soluciones es menos ácido que el del suero salino, siendo sus concentraciones de sodio y cloro más similares a las del plasma. Sin embargo, el Ringer Lactato es ligeramente hipotónico respecto al plasma, y ésta relativa hipoosmolaridad supone una limitación para su uso en la reanimación de pacientes que presentan riesgo de edema cerebral, desaconsejándose en personas con TCE y en otros pacientes neurológicos con riesgo de hipertensión intracraneal.
El efecto expansor de volumen que se logra con este tipo de soluciones balanceadas, es muy similar al del suero salino. Tras administrar 1 litro de solución, a los 30-45 minutos sólo permanece el 25% en el espacio intravascular, precisando la administración de 4 veces el déficit vascular.
Coloides
Los coloides són particulas de alto peso molecular dentro de soluciones transportadoras, incapaces de atravesar la membrana capilar, de tal manera que son capaces de incrementar la presión oncótica a nivel plasmático y retener agua en el espacio intravascular.
Producen efectos hemodinámicos más rápidos y duraderos que los cristaloides, precisándo además menos volumen. Sin embargo, además de ser más caros, los coloides pueden unirse y disminuir el calcio sérico ionizado, disminuir los niveles de inmunoglobulinas circulantes y comprometer más el déficit de volumen intravascular en lugar de restaurarlo.
Los coloides se dividen en naturales (albúmina) y sintéticos (gelatinas, almidones y dextranos).
- Albumina: como coloide natural, sintetizada por el hígado, se obtiene a partir del fraccionamiento de la sangre, lo que conlleva un elevado coste económico y un riesgo de transmisión de infecciones. En España y en general en Europa se utiliza preferentemente la albumina al 20%, con un contenido más bajo en cloro (20 mEq/L).
Los pacientes críticos presentan por lo general hipoalbuminemia secundaria a la malnutrición, la disfunción hepática, a pérdidas gastrointestinales o porque presentan un síndrome de disfunción capilar.
La albumina presenta múltiples efectos fisiológicos, muy relevantes en el enfermo crítico y de especial interés en el paciente en shock, incluyendo la regulación de la presión coloidosmótica, el transporte plasmático de fármacos, la capacidad estabilizadora de membranas debido a su acción “scavenger” de radicales libres, la capacidad antioxidante y la modulación del óxido nítrico.
La albúmina al 20-25% se considera el coloide más potente como expansor, siendo su capacidad expansora de 4 a 5 veces el volumen infundido, con una duración de acción de 24 horas.
Su uso se considera especialmente en la reanimación del paciente con shock séptico que no responde a la administración de cristaloides.
Debido a que puede incrementar la presión intracraneal, no debe emplearse en el paciente con TCE.
- Gelatinas: se obtienen modificando fibras del colágeno bovino. Tienen un peso molecular bajo, por lo que su vida media intravascular corta y su capacidad expansora es limitada.
El efecto adverso más temido con el uso de las gelatinas, es la posibilidad de reacción anafiláctica, mayor que la producida con el uso de los almidones.
- Almidones: se obtienen del maíz y de la patata. Existen diferentes preparaciones de uso clínico, con variaciones en su concentración (baja 3%, media 6%, alta 10%).
Su efecto expansor de volumen viene determinado principalmente por la concentración de la solución. Las soluciones al 6% tienen una capacidad de expansión del 100% o ligeramente superior, siendo del 130% en soluciones con concentraciones del 10%, debido a que atraen el agua desde el espacio intersticial al intravascular.
Su larga vida media, de hasta 36 horas, y su acumulación en los tejidos como la piel, el hígado o los riñones por sus características fisicoquímicas, explican la elevada tasa de efectos adversos asiciados a su uso, como el prurito (efecto secundario más frecuente) y especialmente el fracaso renal.
En el año 2013, tanto la European Medicines Agency como la Agencia Española de Medicamentos y Productos Sanitarios recomendaron no utilizar los almidones en pacientes críticos. Se recomienda no emplear dichas soluciones en la reanimación del paciente crítico, ya que su uso se asocia a una mayor morbimortalidad (desarrollo de insuficiencia renal).
- Dextranos: son una mezcla de polimeros de glucosa. Estan disponibles en dos preparaciones de diferentes pesos moleculares y concentraciones, pudiendose administrar una dosis máxima de 1,5 g/kg/día en ambas.
Dextrano 70 (6% concentración, peso molecular medio 70.000 Da): duración del efecto expansor de 5 horas, con eficacia expansora del 100%.
Dextrano 40 (10% concentración, peso molecular medio 40.000 Da): duración del efecto 3-4 horas, con eficacia expansora del 200%.
Este tipo de coloide se asocia con una incidencia considerable de efectos secundarios como reacciones alérgicas, diátesis hemorrágica y fracaso renal. Además de producir alteraciones en las pruebas de coagulación y dificultad en la realización de las pruebas de compatibilidad sanguínea. Se desconoce el mecanismo exacto del efecto antiplaquetario que producen estas soluciones.
En los últimos años, practicamente han caído en desuso.
Componentes sanguíneos
La administración de sangre (concentrados de hematies) y hemoderivados (plasma y plaquetas) se utilizan para reponer la pérdida de componentes celulares sanguíneos (hematíes y plaquetas) y factores de coagulación (plasma), con la finalidad de mejorar el aporte de oxígeno a las células mediante el aporte de hemoglobina, y luchar contra la hemorragia reponiendo los déficits de plaquetas y factores de coagulación.
Concentrados de hematies: cada unidad de concentrado de hematíes produce un incremento del 3% del hematocrito (Hto) o 1 gr/dl la hemoglobina (Hb), en un adulto de 70 kg.
La indicación de transfusión viene determinada por parámetros como la intensidad y velocidad de pérdida sanguínea, la sintomatología que presenta el paciente y la presencia de comorbilidades, juntamente con los niveles de hemoglobina.
Se realizará transfusión a aquellos pacientes que lo precisen como ocurre en:
- Pacientes con shock hemorrágico, cuando existe inestabiliad hemodinámica (grados III y IV)
- Pacientes con una hemorragia, una vez estabilizado hemodinámicamente, si presentan una Hb 7 g/dl dependiendo de la magnitud del sangrado, existencia de sangrado activo y comorbilidades (isquemia miocárdica, insuficiencia cardiaca, insuficiencia respiratoria, ancianos, etc).
- En la sepsis y shock séptico se recomienda la adminsitración de una transfusión de hematies cuando las cifras de Hb sean
Un aspecto a tener en cuenta con la transfusiones sanguineas es que estos productos hemáticos contienen una pequeña cantidad de citrato, para su adecuada conservación. Una vez realizada la transfusión, el citrato reduce los niveles de calcio iónico por su acción quelante, motivo por el cual se tiene que realizar una monitorización de los niveles de calcio iónico. El objetivo es mantener una normocalcemia iónica por sus importantes efectos en la contractibilidad cardiaca, el tono vascular y como cofactor de la coagulación.
Plaquetas: cada unidad de plaquetas produce un incremento en el recuento de entre 5.000-8.000 µ/l. Su administración está indicada en:
- Pacientes con recuentos
- Pacientes con sangrados con recuentos
- Pacientes con sangrados con recuentos
- Pacientes con recuentos plaquetarios normal con sangrado activo, cuando se sospecha de disfunción plaquetaria, como ocurre en la ingesta crónica de aspirina o en los trastornos plaquetarios congénitos
- En los casos de transfución masiva, se añadiran 2 unidades de plaquetas por cada 6 unidades de hematíes
- En la sepsis y el shock séptico se sugiere la transfusión profiláctica cuando el recuentos de plaquetas es 50.000 mm3 (50x109/l) se recomienda la transfusión en situaciones de hemorragia activa, ante la realización de una cirugía o un procedimiento invasivo.
Plasma fresco congelado (PFC): posee todos los factores de la coagulación. Puede transfundirse:
- Cuando hay deficiencia documentad de los factores de coagulación (incremento de TP o TTPa) y la presencia de hemorragia activa
- Antes de procedimientos quirúrgicos o invasivos
- En el caso de la transfusión masiva, se administrará 1 unidad de plasma fresco congelado por cada 5 unidades de hematíes.
- En la sepsis y el shock séptico se sugiere no utilizarlo para corregir las anomalías de la coagulación, en ausencia de hemorragia o procedimientos invasivos planificados.
Objetivos de PAM
Como se ha comentado anteriormente, la perfusión tisular y la perfusión de órganos depende de la PAM, que depende a su vez de la presión arterial sistólica y diastólica. El objetivo terapéutico es lograr una PAM >65 mmHg, especialmente en el paciente con shock séptico, ya que éste es el punto en el que la mayoría de los lechos vasculares pierden su capacidad de autorregulación local desde un punto de vista fisiológico.
La PAM debe ajustarse a la situación individual de cada paciente, teniendo en cuenta el tipo de shock y los antecedentes personales del paciente. Aquellos que tienen antecedentes de hipertensión arterial sistémica precisarán de cifras mayores de PAM para mantener una adecuada perfusión y prevenir la insuficiencia renal.
En función del shock, podemos encontrar situaciones especiales en las que se estipulan unos objetivos de PAM específicos.
- Reanimación hipotensiva/ hipotensión permisiva, en el paciente traumático con shock hemorrágico no controlado sin TCE asociado:
El 25% de los pacientes que han sufrido un politraumatismo grave desarrollan una coagulopatía inducida por el traumatismo (CIT), tras sufrir una hemorragia severa. La administración agresiva de soluciones cristaloides en la reanimación inicial, produce una hemodilución e induce a la dilución de los factores de coagulación, siendo una causa exógena de la CIT, favoreciendo la persistencia de la hemorragia, con un aumento de la mortalidad en consecuencia.
Para prevenir esta complicación, las actuales guías europeas para el control y el manejo del sangrado en el paciente traumático recomiendan iniciar la fluidoterapia con un uso inicialmente restrictivo, mediante la infusión de bolos pequeños de fluido para lograr cifras de PAs de 80-90 mmHg o una PAM de 40 mmHg hasta que sea posible iniciar la transfusión de hemoderivados o hasta lograr el control del sangrado, normalizando las cifras de presión arterial posteriormente.
La hipotensión permisiva esta contraindicada si el paciente tiene neurotrauama asociado y estaría contraindicada o debería ser utilizada con mucha cautela en pacientes exanguinados, moribundos, ancianos (por tener reserva cardiovascular disminuida) o en aquellos con patologias cardiovasculares crónicas (hipertensión arterial sistémica, enfermedades cerebrovasculares, estenosis de arteria carótida y neuropatías o claudicación intermitente grado III/IV).
De todos modos, la hipotensión permisiva no debería ser vista como una medida estática y protocolarizada para todos los pacientes politraumáticos. Se trata de un procedimiento que se adecua al contexto, dinámico e individualizado, que se adapta a la evolución y las necesidades que presenta el paciente.
- Reanimación hipertensiva en el paciente traumático con neurotrauma asociado (TCE grave o lesión medular) con deterioro neurológico, sin evidencia de hemorragia sistémica:
Como ya se ha comentado anteriormente, entre el 15 y el 25% del gasto cardíaco está dirigido al cerebro, para mantener un adecuado flujo sanguineo cerebral (FSC). El cerebro tolera cambios de la presión arterial, regulándose el FSC para proteger el tejido cerebral de caídas o elevaciones bruscas de presión, siempre que la PAM sea >60 mmHg en los casos de hipotensión sistémica.
Si el paciente tiene un neurotrauma asociado, ya sea por un TCE grave o por una lesión medular, la PAM debe ser igual o >80 mmHg, con el objetivo de mantener una adecuada presión de perfusión cerebral, evitando de esta manera lesiones neurológicas secundarias a isquemia. Una vez monitorizada la presión intracraneal, se ajustarán los niveles de PAM con el objetivo de asegurar la perfusión cerebral.
Reposición de la volemia: velocidad de infusión según el tipo de shock
Las causas de shock con hipovolemia presentan una buena respuesta a la reposición de volumen vascular, siendo menor la respuesta en aquellos con fallo de bomba u obstrucción al flujo. En función del shock, encontraremos unas velocidades y volúmenes de administración.
- Shock hipovolémico de causa no hemorrágica: para estabilizar la PAM, la infusión debe ser agresiva, con un promedio de 20-30 ml/kg (1-3 litros de cristaloides).
- Shock hipovolémico de causa hemorrágica: administración de 3 ml de solución cristaloide por cada mililitro de pérdida de sangre estimada (3:1), continuándose con hemoderivados en función de las necesidades del paciente (estado de coagulopatía, hemorragias importantes/ masivas, etc).
Debido a que la pérdida es principalmente hemática, la decisión de administrar sangre se basará en la falta de respuesta del paciente a la reanimación realizada con cristaloides, el volumen de sangre perdido, la necesidad de que la hemoglobina contribuya al transporte de oxígeno, teniendo en cuenta sus niveles, y a la necesidad de corregir la coagulopatía del paciente. En el caso de precisar una transfusión masiva, los pacientes presentan mejor respuesta cuando los hemoderivados se administran en una proporcion 1:1:1 (unidades de plasma, plaquetas y concentrado de hematies).
- Shock cardiogénico: la administración de líquidos debe ser cautelosa, controlándose de cerca para poder detectar signos de sobrecarga, mediante la realización de bolos de líquido endovenoso pequeños (como por ejemplo 250 ml de SF en 20 minutos), valorando la repercusión hemodinámica y ausencia de efectos perjudiciales.
- Shock obstructivo: en este tipo de shock la cantidad de líquidos que se necesita es menor, ya que al resolverse la causa subyacente (mediante la descompresión del neumotórax, la pericardiocentesis, etc) la PAM mejora.
- Shock distributivo tipo anafiláctico: puede precisar de la administración de cristaloides (SF 0,9%) de manera agresiva en los primeros minutos si existe hipotensión (hasta 1-2 litros) a la espera de que se recupere el tono vascular por acción de la adrenalina y la ayuda de fármacos vasopresores, para mantener la presión arterial y el estado hemodinámico normal.
- Shock distributivo tipo séptico: en la reanimación inicial con fluidos, deben administrarse almenos 30 ml/kg de solución cristaloide vía endovenosa, dentro de las primeras 3 horas. Posteriormente, los fluidos adicionales se guiarán mediante una reevaluación del estado hemodinámico.
Monitorización hemodinámica: monitorización inicial
La valoración hemodinámica es fundamental en el paciente crítico en situación de shock, tanto para obtener información que ayude al diagnóstico, como para la valoración de la respuesta al tratamiento instaurado. En este último punto, tras el aporte inicial de volumen, debe individualizarse la reposición de la volemia en función del tipo de shock y la respuesta hemodinámica obtenida.
La monitorización continuada es esencial en todo paciente en situación de shock, mediante un adecuado control hemodinámico, respiratorio y renal. El tipo de seguimiento variará en función del tipo de shock, y el estadio en el que se encuentre, oscilando desde simple y poco agresivo a complejo e invasivo. Dentro de la monitorización hemodinámica básica inicial se destaca:
- Frecuencia cardíaca (FC): como se ha explicado anteriormente, en el momento de ingreso y siempre que se considere oportuno se obtendrá un ECG de 12 derivaciones. Además, la monitorización continua del electrocardiograma nos dará información de utilidad que nos puede ayudar a discernir la causa del fallo hemodinámico (elevación ST, aparición de arritmias, etc).
- Presión arterial (PA): en el paciente crítico es esencial el conocimiento preciso de la presión arterial. El tiempo de hipotensión en las primeras horas de shock, puede presentar un efecto acumulativo en el desarrollo de fracasos orgánicos posteriormente, lo que justificaría la necesidad de realizar una medición frecuente y precisa de la PA. Ésta puede obtenerse de manera no invasiva mediante esfignomanometría especialmente en fases iniciales.
En los estados de shock, la estimación de la PA mediante el uso del esfignomanometro puede ser inexacta. Motivo por el cual puede ser conveniente el uso de la medición invasiva de la PA mediante la inserción de un cateter intraarterial, ya que además de ofrecer una medición más precisa y continua de la PA, permite el análisis latido a latido y la obtención de muestras.
- Saturación percutánea de oxígeno: las determinaciones de saturación de oxígeno arterial se realizarán mediante la medición de pulsioximetría. Teniendose en cuenta la posibilidad de que su medición sea poco precisa, e incluso poco fiable, en aquellas situaciones en que la hipoperfusión sea marcada, se recomienda una gasometría arterial para verificar los niveles de oxígeno sanguíneos.
- Diuresis: la medición de la diuresis es necesaria para valorar la perfusión renal, mediante sondaje vesical.
- Temperatura: la medición de la temperatura es importante tanto para discernir de qué tipo de shock se trata, como para valorar su posible causa (por ejemplo: shock caliente tipo séptico de causa infecciosa, etc).
- Medición de láctico sérico y/o SvcO2: a través de la analítica sanguínea, se realizará la valoración de al menos una variable que nos aporte información del estado de oxigenación global de los tejidos. Pudiendo obtener información del láctico sérico mediante la punción periférica, siendo necesario sin embargo un cateter venoso central alojado en vena cava para la medición de SvcO2.
En este momento inicial, la canalización de un acceso venoso central, con extremo distal en la vena capa superior, nos podría permitir infundir líquidos y drogas vasoactivas para la reanimación hemodinámica, obtener muestras para la medición de la SvcO2, además de poder monitorizar la presión venosa central (PVC).
- PVC: En el manejo inicial del shock, y en ausencia de otro tipo de variabes de valoración de dependencia de precarga y/o GC, la monitorización de la PVC puede ser de utilidad, utilizada junto con parámetros de evaluación adicionales como la producción de orina, la FC, la respuesta de la PA a los líquidos, etc.
Se trata de una medida estática utilizada tradicionalmente, que nos puede aportar información sobre el estado de la volemia. Los valores normales de PVC son de 8-12 mmHg.
Pese a las limitaciones que presenta en la predicción de la respuesta al aporte de volumen, los valores extremadamente bajos de PVC se pueden asociar con una volemia insuficiente, aceptándose que valores de PVC
Tras la reanimación inicial con líquidos, la administración de más líquidos vendrá determinada por las necesidades del paciente, realizando una revaloración frecuente del estado hemodinámico. Esta revaloración incluye las variables fisiológicas descritas anteriormente, una exploración clínica completa, así como otro seguimiento no invasivo o invasivo, según se encuentre disponible.
Monitorización hemodinámica: monitorización semi invasiva e invasiva en UCI
En los casos en que, pese a una resucitación inicial adecuada, se produzca una persistencia del shock con signos de hipoperfusión tisular transcurridas 3-6 horas, y en aquellos pacientes con fracasos orgánicos y/o comorbilidades susceptibles de interferir o empeorar durante la reanimación, sería oportuno realizar una mayor monitorización hemodinámica continua. Esta monitorización debería proporcionar información acerca del gasto cardíaco (GC) y sus determinantes:precarga/dependencia de precarga, contractilidad y poscarga.
El GC es un parámetro fundamental en la valoración hemodinámica del paciente crítico. Se refiere a la cantidad total de sangre bombeada por uno de los ventrículos en litros por minuto, siendo en un adulto en reposo de 4-6 L/min, variando en función de las necesidades metabólicas corporales.
Se considera un evaluador de la función cardíaca global, que nos puede proporciona información sobre la causa del shock y del fallo orgánico. Sin embargo, para la obtención de una información completa es necesario integrar el GC con otras variables hemodinámicas (precarga, poscarga, contractiblidad), signos biológicos y parámetros de oxigenación tisular.
A nivel de urgencias y en las valoraciones iniciales, se podría utilizar el ecocardiograma para obtener el GC de forma no invasiva, mediante la ecocardiografía transtorácica, o mínimamente invasiva, con el uso de la ecocardiografía transesofágica, ofreciendo además una amplia información hemodinámica (como la funcionalidad del corazón, la contractibilidad mediante la fracción de eyección ventricular izquierda (FEVI), la afectación cardíaca en cualquier tipo de shock, etc).
Entre las técnicas de monitorización más avanzada encontramos: las ténicas de dilución transpulmonar (PICCO) y la cateterización de la arteria pulmonar (Swan-Ganz), descritas a continuación.
Técnicas de dilución transpulmonar (sistema PiCCO)
Se trata de un método que realiza un análisis del contorno de la onda de pulso, basándose en la morfología de la curva de presión arterial.
Por un lado, permite realizar la medición del GC, precisando únicamente una línea arterial femoral y un cateter venoso central. Debido a que la mayoría de pacientes críticos precisan de estos dispositivos, se considera un método poco invasivo.
Por otro lado, mediante el análisis de la onda de presión de pulso que realiza, permite obtener el cálculo de volúmenes que ayudarán a una estimación de la precarga, la poscarga, la determinación de volúmenes intratorácicos y la cantidad de agua pulmonar extravascular.
Se considera de elección para guiar el manejo hemodinámico, especialmente en situaciones de sepsis y shock séptico, y para mejorar la función pulmonar y disminuir el tiempo de ventilación mecánica en el SDRA.
Proporciona, como se ha descrito, la siguiente información:
- Mediciones de flujos sanguíneos (GC): se realiza el cálculo del GC mediante termodilución transpulmonar. Precisa calibraciones del sistema cada 8h, y con mayor frecuencia en situaciones de inestabilidad hemodinámica, para obtener mayor precisión en los valores de GC obtenidos.
Estimación de la respuesta al volumen: Utiliza el análisis de la onda de presión de pulso para realizar el análisis del volumen sistólico (VS), lo que permite realizar el cálculo del porcentaje de variación en la presión de pulso (VPP) o en el área con la variación de volúmen sistólico (VVS). Ambos aportan información sobre el estado de la volemia del paciente, son parámetros muy sensibles de precarga e indican en qué punto de la curva de Frank-Starling se encuentra el paciente, proporcionando información de si va a tener o no respuesta al aporte de fluidos. Motivo por el cual se utilizan para dirigir el aporte de fluidoterapia y analizar la respuesta a ésta. En ambos casos los valores iguales o <10% indicarían poca variación y falta de respuesta al volumen.
- Mediciones de volúmenes: esta técnica permite calcular diferentes volúmenes de los compartimentos intravasculares, no presiones como ocurre en el CAP, así como el líquido extravascular a nivel pulmonar.
Estima la precarga a través de 2 parámetros: la medición del volumen global al final de la diástole (GEDV), con valores normales 680-800 ml/m2, que se define como la suma del volumen de sangre de las cuatro cavidades cardíacas, y el índice de volumen sanguíneo intratorácico (ITBV), con valores normales 850-1000 ml/m2, considerado como el volumen de sangre que hay en las cuatro cavidades cardíacas sumado a la sangre del lecho vascular pulmonar. Ëstos parámetros no presentan alteraciones con la ventilación mecánica.
Cuantificación del edema pulmonar y situación de la permeabilidad vascular: el agua pulmonar extravascular (ELWI), con valores normales de 3-7 ml/kg, mide el líquido que se encuentra fuera de los capilares pulmonar, tratándose de una medida de cuantificación del edema pulmonar. El índice de permeabilidad vascular pulmonar (PVPI), con valores normales de 1-3, nos indica el estado de los capilares pulmonares ayudándonos a determinar la causa del edema pulmonar. Un índice elevado (>3) orienta a una fuga capilar secundaria a un proceso inflamatorio (como podría ser el SDRA secundario a la sepsis), mientras que sus valores son normales existe una alta probabilidad que el edema sea de orígen cardíaco.
- Valoración de la contractibilidad y la poscarga: para valorar la relación entre el gasto cardíaco y la poscarga se obtiene la resistencia vascular sistémica (RVSI, con valores normales de 1700-2400 dyn x s x cm x m2), que nos informan del estado del tono vascular (siendo mayor en situaciones como el shock cardiogénico o menor en el shock distributivo), y de su efecto sobre la función cardíaca a través de la fracción de eyección global (GEF, 25-35%) y la contractibilidad del ventrículo izquierdo.
Como podemos comprobar, este método de monitorización proporciona tanto médidas estáticas (PVC, GEDV, EVLW, PVPI) como dinámicas (VVS, VPP).
Puede presentar limitaciones y problemas en la práctica clínica que reducen la precisión en la medición del GC como la amortiguación de la curva arterial, el cero insuficiente, la presencia de arritmias severas o el uso del balón intraaórtico de contrapulsación. El gran inconveniente que presenta, es que la mayoría de estos parámetros sólo serán fiables en pacientes sedados, en ventilación mecánica y sin arritmias graves.
Las complicaciones que puede presentar este tipo de técnica se encuentran relacionadas con el catéter (infección, trombosis, sangrado, daño vascular, etc).
Cateterización de la arteria pulmonar (CAP, Swan-Ganz)
El catéter de arteria pulmonar ha sido una herramienta ampliamente utilizada en los últimos 50 años, para la monitorización hemodinámica, herramienta en el diagnóstico y como guía del tratamiento. Se trata de un método de monitorización invasivo, ya que precisa la inserción de un cateter que, a través de su paso por las cavidades cardíacas derechas, queda alojado en su extremo distal en una ramificación de la arteria pulmonar.
La cateterización de la arteria pulmonar mediante el catéter Swan-Ganz estaría indicada únicamente en situaciones especiales, siendo útil para el manejo de condiciones circulatorias complejas como pueden ser el shock cardiogénico, la hipertensión pulmonar y pacientes sometidos a cirugía cardíaca. Su uso ha disminuido además con la disponibilidad de dispositivos menos invasivos.
Su uso permite valorar tres categorías de variables:
- Medidas de flujo sanguineo (GC): su medición se basa en la termodilución transcardíaca.
- Presiones intravasculares intratorácicas: teniendo en cuenta su posicionado a través del corazón derecho, permite obtener las siguientes presiones:
Presión aurícula derecha: se puede tomar de referencia como valor de PVC, ya que se asemeja a ésta, con valores normales 0-6 mmHg.
Presión de arteria pulmonar (PAP): con valores normales de 25/6-12 mmHg. Útil para valorar situaciones de HTA pulmonar.
Presión de enclavamiento de la arteria pulmonar/ presión capilar pulmonar (PCP, POAP): esta medición de obtiene mediante el inflado del balón del cateter. Tras su valoración debe desinflarse el balón de manera rápida para restablecer el flujo sanguíneo, ocluido por el procedimiento. Representa una estimación aproximada de la presión de la auricula izquierda (PAI), permite evaluar la precarga del ventrículo izquierdo y las resistencias pulmonares. Además ayuda en el diagnóstico de la causa de la hipertensión pulmonar y el edema pulmonar (cardiogénico/ no cardiogénico), considerándose un indicador de congestión pulmonar y riesgo de edema agudo de pulmón.
- Parámetros oximétricos: Además de la obtención de parámetros hemodinámicos, es posible obtener muestras a través del cateter para la saturación de oxígeno venosa central (SvcO2) por su extemo proximal y para la saturación de oxígeno mixta (SvO2) por su posición en la arteria pulmonar en su extremo distal.
La SvO2 se considera el mejor indicador aislado de la adecuación del transporte global de oxígeno (DO2), ya que representa la cantidad de oxígeno que queda en la circulación sistémica tras su paso por los tejidos.
Como podemos apreciar, proporciona principalmente variables estáticas (PVC, PAP, POAP).
El CAP se ha asociado a un aumento en el riesgo de infecciones (bacteriemia), fenómenos trombóticos (uso prolongado >48 h) y mayor riesgo de arritmias durante su inserción. Además de otras complicaciones como rotura del balón, infarto pulmonar, trombosis, arritmias, lesiones intracardíacas, etc.
Monitorización hemodinámica: respuesta y guía del tratamiento
La reanimación con fluidos debe ir monitorizada para valorar la respuesta en el paciente y sus efectos en la mejora de la precarga, además de la repercusión que tiene en el resto de parámetros hemodinámicos.
En todos los tipos de shock es necesario saber la capacidad de respuesta al volumen, con el objetivo de adecuar el tratamiento, para evitar la sobrecarga hídrica que conlleva la realización de una resucitación agresiva.
En situaciones de inestabilidad hemodinámica, indistintamente del tipo de shock que se trate, se distinguen dos tipos de pacientes: respondedores y no respondendores a volumen. Esta clasificación viene determinada por lo que se denomina “precarga- dependencia” derivada de la ley de Frank-Starling. En ella se describe que la relación entre la precarga y el volúmen sistólico es positiva de forma curvilínea (no lineal). Lo que se traduce en que a partir de un determinado nivel de precarga, la administración de fluidos no va a producir una mejora del volumen sistólico, causando sin embargo un aumento de las presiones intracardíacas sin ningún beneficio hemodinámico.
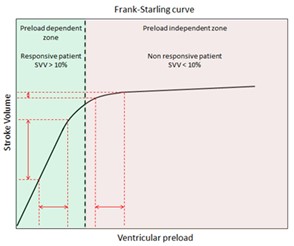
Ilustración 4 Curva Frank- Starling
Fuente: Wikimedia Commons
Parámetros estáticos La monitorización hemodinámica proporciona información tanto de la etiología como de la respuesta al tratamiento. Tradicionalmente se habían utilizado los parámetros estáticos, como la PVC, para guiar la fluidoterapia. En la actualidad se dispone de diferentes parámetros, gracias a los dispositivos de monitorización avanzada disponibles, que permiten valorar la precarga y la respuesta a la administración de volumen. Entre ellos encontramos parámetros estáticos y dinámicos.
Los parámetros estáticos proporcionan un valor absoluto de precarga y, pese a su limitación para predecir la respuesta a volumen, continúan empleándose en la práctica diaria como herramienta para decidir cúando administrarlo a un paciente, en especial la PVC. Entre los parámetros estáticos encontramos:
- La PVC o PEAP: pese a no considerarse buenos predictores de respuesta a volumen en pacientes con ventilación mecánica, en pacientes con respiración espontanea se acepta que valores de PVC
- Los volúmenes y áreas (como el GEDV): no se consideran buenos predictores de respuesta a volumen, ni en pacientes ventilados ni en pacientes con respiración espontanea, sin embargo los volúmenes proporcionan una mejor estimación de la precarga.
Parámetros dinámicos
A diferencia de los parámetros estáticos, los parámetros dinámicos de precarga- dependencia proporcionan una valoración funcional del rendimiento cardiaco ante modificaciones transitorias de la precarga, trazando una instantánea en movimiento del funcionamiento del corazón.
Por lo tanto, no realizan una estimacion de la precarga ni proporcionan información sobre la volemia, sino que cuantifican la respuesta cardiaca ante modificaciones de la precarga, permitiendo determinar en qué zona de la curva de Frank- Starling se encuentra el paciente.
Entre los parámetros dinámicos encontramos:
- VVS y VVP: La ventilación mecánica (VM) con presión positiva produce cambios cíclicos en el volúmen sistólico del ventrículo izquierdo, caracterizados por un incremento durante la inspiración y una disminución durante la espiración. La VVS determina el porcentaje de variación que se produce en el volúmen sistólico durante el ciclo respiratorio. De igual modo ocurre con la presión de pulso arterial, ya que se encuentra directamente relacionada con el volumen sistólico izquierdo.
La precarga- dependencia dependerá de la magnitud de estas oscilaciones, de tal forma que a mayor oscilación se preve mayor respuesta al aporte de fluidos. Por tanto, se considerará al paciente respondedor a volumen cuando presente VVS >10% y VVP >13%.
La VVS y la VVP tienen limitaciones en su uso, ya que sólo pueden utilizarse en pacientes con ventilación mecánica ventilados en modo controlado, preferiblemente con volúmenes tidal > 8 ml/kg de peso ideal, en ausencia de arritmias cardíacas y/o extrasístoles frecuentes y sin disfunción ventricular derecha asociada.
- Maniobra de la oclusión de la válvula espiratoria: durante la fase inspiratoria de la ventilación mecánica se produce un incremento de la presión intratorácica, disminuyendo en consecuencia el retorno venoso y la precarga del ventrículo derecho.
La maniobra de la oclusión de la válvula espiratoria consiste en realizar una pausa espiratoria de 15 segundos en los pacientes con VM, facilitándo el retorno venoso y aumentando la precarga, del mismo modo que lo haría una pequeña carga de volumen, valorando su repercusión en la presión de pulso arterial y el índice cardíaco (IC). Se considerará al paciente respondedor a volumen si se produce un aumento > 5% en alguno de los dos parámetros.
- Variaciones respiratorias de las venas cavas mediante ecocardiografia: en pacientes con VM tanto la existencia de variaciones respiratorias del diámetro de la vena cava inferior (>12%) como la colapsabilidad de la vena cava superior (>36%), predicen la respuesta favorable a los fluidos.
- Maniobra de elevación pasiva de piernas: se trata de un método sencillo y fiable para la valoración de la precarga- dependencia en pacientes con fracaso circulatorio. Útil tanto en pacientes con VM como en ventilación espontanea e incluso en aquellos con arritmias cardíacas.
Consiste en realizar una elevación de piernas, partiendo de la posición supina, en un ángulo de 45º durante al menos un minuto. Esta maniobra equivale a un test de aporte de volumen, con efecto transitorio, ya que se transfieren 300 ml aproximados procedentes de las extremidades inferiores hacia los vasos intratorácicos. Esta transferencia de sangre produce
un incremento del retorno venoso, la precarga cardiaca y si el paciente se encuentra en la zona de precarga- dependencia de la curva de Frank-Starling, experimentará un aumento del gasto cardiaco en los siguientes minutos, siendo máximo pasados 60-90 segundos de la elevación.
Por tanto, se considerará al paciente respondedor a volumen si experimenta un incremento igual o >10% del GC durante los primeros 60-90 segundos.
Las limitaciones de esta maniobra vienen determinadas por la situación clínica del paciente. Por un lado, su realización puede incrementar la presión intracraneal, por lo que no debe realizarse si hay riesgo de hipertensión intracraneal.
Por otro lado, su eficacia se ve disminuida en los pacientes con síndrome compartimental abdominal preexistente, ya que no es fiable si la presión intrabdominal está elevada. En el caso de que el paciente este conectado a ventilación mecánica debe vigilarse el riesgo de aspiración, minimizándolo con un adecuado vaciado gástrico y evitando bajar el tórax de los 0º. Además de existir otras circunstancias que pueden disminuir la respuesta al test como las medias de compresión elática, el shock hemorrágico y el shock cardiogénico.
- Carga de volumen (fluid challenge): la valoración de la respuesta a la administración de una determinada cantidad de volumen, pese no ser realmente un predictor, se ha utilizado ampliamente en la práctica clínica para valorar la eficacia y la seguridad de la respuesta al aporte de volumen.
Consiste en administrar un determinado volúmen (250-500 ml de cristaloide) en un tiempo rápido (10-20 minutos), valorando su repercusión en la hemodinamia del paciente. Se establecerían previamente unos valores de PAM como objetivo y de PVC como seguridad, y en el caso de que se alcanzaran o superaran estos límites, se pararía la adminisitración del volumen.
En la actualidad las medidas dinámicas se consideran de elección frente a las estáticas, para guiar la reanimación con fluidos, ya que han demostrado mejor precisión diagnóstica para predecir los pacientes que posiblemente respondan a una sobrecarga de líquidos.
Optimización de la PAM tras la reanimación con líquidos: uso de fármacos vasoactivos
Los fármacos vasoactivos pueden administrarse en todos los tipos de shock, para mejorar la estabilidad hemodinámica del paciente cuando los líquidos administrados no pueden mantener una PAM adecuada. Sin embargo, no deben utilizarse hasta asegurar una reposición adecuada de la volemia y la corrección de la acidosis que dificulta su acción.
Cuando se administran fármacos vasoactivos, debe realizarse una monitorización hemodinámica más exhaustiva con valoración de los signos vitales al menos cada 15 minutos hasta que se estabilicen, o más a menudo si lo precisa el paciente. Se recomienda la colocación de un catéter arterial a los pacientes que precisen vasopresores, tan pronto como sea posible, para poder realizar una monitorización continua de la respuesta a éstos.
No es conveniente demorar el inicio de fármacos vasoactivos, hasta la obtención de una vía central, como acceso venoso óptimo para su administración. En situaciones de urgencia, y mientras se obtiene la vía central, pueden administrarse los fármacos vasoactivos por un catéter periférico único, insertado en una vena del mayor calibre posible, en la extremidad superior en la que no se esté monitorizando la presión arterial de forma no invasiva. Ésta administración se realizará por un máximo de 6 horas, dado que aumenta el riesgo de complicaciones, ya que la infiltración y la extravasación de algunos fármacos vasoactivos pueden producir necrosis tisular y desbridamiento.
Podemos diferenciar los fármacos vasoactivos en aquellos con efecto predominane en las resistencias vasculares sistémicas:
- La noradrenalina es el fármaco vasopresor de elección para la optimización de la PAM, para todos los tipos de shock con hipotensión grave. Se trata de un agonista adrenérgico alfa 1, que incrementa tanto la tensión arterial sistólica como la diastólica, y en consecuencia en la PAM, mediante la vasocontricción periférica severa. A su vez incrementa el flujo sanguineo coronario, mejorando la función cardiaca indirectamente.
Tiene una actividad agonista beta modesta, que lo convierte en un vasocontrictor con pocos efectos ionotropos y cronotrópicos, útil en situaciones en los que la estimulación de la frecuencia cardíaca puede ser perjudicial. Pero, pese a que conlleva un menor riesgo de arritmias, cuando se utiliza como apoyo vasopresor de manera prolongada, puede tener un efecto tóxico directo sobre los miocitos cardíacos.
La velocidad de infusión de la noradrenalina se ajustará para alcanzar el objetivo de PAM deseado.
- La vasopresina o la terlipresina se utilizan como adyuvantes a la noradrenalina, para elevar la presión arterial en pacientes resistentes a la noradrenalina, o para disminuir las dosis de ésta cuando son elevadas.
- La adrenalina: droga de acción beta predominante en dosis bajas (0,015 a 0,1 µg/kg/min), produce un aumento en la frecuencia cardiaca, gasto cardiaco, volumen de eyección y las resistencias vasculares sistémicas, y alfa predominante en dosis mas altas (por encima de 0,1 µg/kg/min), produciendo una vasocontricción importante que causa un aumento de la presión arterial.
Indicada como droga de primera elección en el shock anafiláctico.
- Nitroglicerina: droga vasoactiva con efecto contrario a los descritos anteriormente, con acción vasodilatadora en la musculatura venosa, disminuyendo el retorno venoso y el consumo de oxígeno, reduciendo la PA. Reduce, además, la resistencia vascular coronaria, incrementa el flujo colateral y reduce la presión capilar pulmonar.
Estaría indicada como vasodilatador en casos concretos de shock cardiogénico y/o en casos de hipertensión pulmonar asociada.
- Nitroprusiato: droga vasoactiva de acción vasodilatadora, que afecta tanto a nivel venoso como arterial. Actua reduciendo la poscarga y la precarga cardiaca, entre otras funciones, y estaría indicado en situaciones concretas de shock cardiogénico con HTA.
En cuando a los fármacos vasoactivos con efecto predominante de la función cardíaca:
- La dobutamina es una catecolamina sintética, agonista selectiva de los receptores beta 1. Su acción produce un aumento de la frecuencia cardíaca, aumentan el volúmen sistólico y la contracción miocárdica, además de reducir las resistencias vasculares sistémicas (efecto beta 2), mejorando el gasto cardíaco. Produce por tanto una mejoría en la hemodinamia y cierta mejoría en los índices de perfusión (mejora clínica, disminución del lactato sérico y mejora de SvcO2), pero incrementa la demanda de oxígeno del corazón.
Teniendo en cuenta la acción que tiene sobre las resistencias vasculares sistémicas, es importante saber que en los pacientes con sepsis o shock séptico puede causar hipotensión severa y taquicardia, si se administra de manera precoz en situaciones de relleno vascular insuficiente.
Se recomienda en pacientes con shock cardiogénico con hipotensión asociada, en el shock séptico que cursa con disfunción miocárdica y en pacientes que muestren evidencia de hipoperfusión persistente, a pesar de recibir una sobrecarga de líquidos adecuada y el uso de fármacos vasopresores.
La dosis óptima de dobutamina varía entre 2,5-25 microgramos/kg/mn.
Terapias de soporte en el shock
Además de las medidas descritas, el tratamiento del paciente en estado de shock incluye las siguientes terapias de soporte.
Soporte nutricional enteral temprano
El soporte nutricional es un aspecto relevante en la atención de los pacientes que se encuentran en estado crítico.
El paciente en estado de shock puede requerir más de 3000 calorías diarias, debido al incremento de las tasas metabólicas que se produce durante el shock, ya que aumenta los requisitos de energía y los requisitos calóricos. La liberación de catecolaminas al inicio del shock, conduce a un rápido agotamiento de las reservas de glucógeno, satisfaciendo los requisitos de energía nutricional mediante la descomposición de la masa corporal magra. Éste echo comporta la pérdida de masa esquelética, incluso cuando el paciente presenta grandes reservas de tejido adiposo.
La pérdida de masa esquelética, sumada a la falta de administración de una cantidad adecuada de proteína a través de una nutrición adecuada, pueden causar dificultades para la desconexión del respirador, mayor debilidad general y prolongación en el tiempo de recuperación.
El soporte nutricional, vía enteral o parenteral, debe iniciarse lo antes posible.
La administración de nutrición parenteral puede garantizar el aporte calórico deseado, lo que supone una ventaja, especialmente cuando los pacientes pueden estar mal alimentados debido a intoleracias gastrointestinales. Sin embargo, su administración es más invasiva y se ha asociado a complicaciones como las infecciones.
Por el contrario, la nutrición enteral esta asociada a supuestos beneficios fisiológicos relacionados con el mantenimiento de la integridad intestinal y la prevención de la permeabilidad intestinal, la disminución de la respuesta inflamatoria, de especial interés en la sepsis y el shock séptico, además de la modulación de las respuestas metabólicas que pueden reducir la resistencia a la insulina, entre otros.
La implementación enteral temprana favorece la inmunidad mediada por el intestino, reduce la respuesta metabólica al estrés y mejora la morbilidad y mortalidad general del paciente.
Por estos motivos, la nutrición enteral se considera de elección, siempre que no exista contraindicación para su uso.
Control de la hiperglicemia mediante el uso de insulina endovenosa
Las recomendaciones actuales sugieren utilizar un objetivo máximo de glucemia de 180 mg/dl, sin fijar un objetivo inferior, exceptuando la hipoglucemia. Los pacientes con antecedentes médicos de diabetes e hiperglucemias crónica y/o insuficiencia renal terminal, pueden precisar rangos de glucemia más elevados.
El tratamiento debe evitar tanto la hiperglucemia como la hipoglucemia, además de las grandes variaciones e inestabilidades en sus niveles, ya que se han asociado a una mayor mortalidad.
Las últimas recomendaciones recogidas en la “surviving sepsis campaign” indican la necesidad de un enfoque protocolizado para el control de la glucemia de este tipo de pacientes en la UCI, en el cual se debería iniciar la administración de insulina endovenosa en aquellos pacientes que presenten dos niveles de glucemia consecutivos >180 mg/dl. Realizando una monitorización de los valores de glucemia cada 1-2 horas, hasta que los valores de glucemia y las tasas de infusión de insulina sean estables, realizándose posteriormente cada 4 horas.
Un aspecto a tener en cuenta en este tipo de pacientes es la posibilidad de obtener mediciones de glicemia erroneas, en aquellas que se obtienen con glucómetros utilizando sangre capilar, en situaciones de hipoperfusión marcada con afectación de zonas distales, derivadas del propio shock o del efecto de los fármacos vasopresores utilizados para su tratamiento. Siendo de elección en estos casos la obtención de sangre arterial para realizar la medición de glicemia.
Prevención de las úlceras gastoduodenales agudas y la hemorragia gastrointestinal
Los pacientes en estado crítico pueden presentar úlceras gastroduodenales agudas, asociándose a una importante morbilidad y mortalidad.
No se comprende con exactitud el mecanismo que lleva a su producción, pero se cree que podría estar relacionado con la interrupción del mecanismo de protección en contral del ácido gástrico, la presencia de hipoperfusión de la mucosa gástrica y/o duodenal, el incremento en la producción de ácido y las lesiones oxidativas producidas en el tracto digestivo. En este sentido, los factores más fuertes para predecir el riesgo de hemorragia gastrointestinal, en pacientes en estado crítico, son la ventilación mecánica (>48 horas) y la coagulopatía.
Se sugiere utilizar inhibidores de la bomba de protones o antagonistas de los receptos de la histamina 2, en aquellos casos en que se indique la profilaxis para las úlceras gastroduodenales aguad.
Solo debe realizarse profilaxis en presencia de factores de riesgo de hemorragía gastrointestinal, por lo que se evaluaran a los pacientes periodicamente para la identificación de estos factores y la necesidad de profilaxis.
Prevención de las trombosis venosas
Los pacientes que se encuentra en la UCI corren un mayor riesgo de sufrir trombosis venosa profunda (TVP) y embolia pulmonar (PE), con una incidencia del 10% y del 2-4% respectivamente.
Se ha descubierto que el uso de vasopresores, frecuente en los pacientes de UCI y especialmente en los que padecen shock séptico, es un factor de riesgo independiente para el desarrollo de la trombosis venosa profunda adquirida en la UCI.
Tanto la profilaxis farmacológica, mediante el uso de heparina de bajo peso molecular (LMWH) o heparinas no fraccionadas (UFH) en aquellos pacientes que no presenten contraindicaciones para el uso de estos agentes, como la profilaxis mecánica, mediante compresión neumática intermitente (IPC) y/o medias de compresión graduada (GCS) y/o la combinación de ambas, pueden ser opciones en el paciente crítico para la prevención de TVP.
En aquellos pacientes con contraindicación para el uso de la profilaxis farmacológica, como pueden ser los que presenten un alto riesgo de sangrado, plaquetopenia o coagulopatía, puede optarse por el uso de la profilaxis mecánica, siendo de elección la IPC.
BIBLIOGRAFIA
- Hinkle JL, Cheever KH. Enfermería medicoquirúrgica Volumen 1. 14ª Edición. Philadelphia: Wolters Kluwer; 2018
- Aragonés Manzanares R, de Rojas Román JP, Aguiar Flores E, Alcalá Peña MM, Alcalde Perez D, Aldana Díaz EM et all. Cuidados Intensivos: Atención integral al paciente crítico. España: Editorial Médica Panamericana S.A.; 2016
- Grupo de shock. Actualización en Shock: atención del paciente en shock en urgencias [internet]. 3ª edición. España: Bubok Publishing S.L; 2014 [citado 2021 Marzo 2]. Disponible en: actualizacion-de-manejo-del-paciente-en-shock-tercera-edicion.pdf (sborl.es)
- Navío Serrano AM, Abad Esteban F, Aguiló Mir S, Alonso Llasheras JE, Afonso Rivero D, Aragón Leal MA et all. Manejo del paciente en shock en urgencias [internet]. Barcelona: Edikamed S.L; 2011 [citado 2021 Marzo 2]. Disponible en: SHOCK2ED.pdf (grupodeshock.info)
- Camacho JM, Calvo C. Shock: etiología y diagnóstico. An Pediatr Contin. 2003; 1 (3): 119-24
- Avilés García M, Figueira Iglesias JC, Agrifoglio Rotaeche A, Sánches Sánchez M. Bacteriemia, sepsis y shock séptico. Medicine. 2018; 12 (52): 3066-75
- Yébenes JC, Lorencio C, Estebanc E, Espinosa L, Badia JM, Capdevilaf JA et all. Código Sepsis Interhospitalario en Catalunya: modelo organizativo territorial para la atención inciial al paciente con sepsis. Med Intensiva. 2020; 44 (1): 36-45
- Aboal J. Reposición de volumen: ¿Cristaloides o coloides?. Rev Esp Cardiol Supl. 2015; 15 (D): 15-19
- Banchón Alvarado JD, Camacho García DE, Fernández Saquicela CA, Villacís Nieto JM. Conceptos actuales de sepsis y shock séptico. Journal of America Health [Internet]. 2020 [citado 2021 Marzo 2]; 3 (2): 103-116. Disponible en: Conceptos actuales de sepsis y shock séptico | Journal of America health (jah-journal.com)
- Garnacho Montero J, Fernández Mondéjar E, Ferrer Roca R, Herrera Gutiérrez ME, Lorente JA, Ruiz Santana S et all. Cristaloides y coloides en la reanimación del paciente crítico. Med Intensiva. 2015; 39 (5): 303-315
- Levy M, Evans L, Rhodes A. The Surviving Sepsis Campaign Bundle: 2018 update. Intensive Care Med. 2018; 44: 925-928
- Vahdatpour C, Collins D, Goldberg S. Cardiogenic Shock. Journal of the American Heart Assocition [internet]. 2019 [citado 2021 Marzo 2]; 8. Disponible en: Cardiogenic Shock | Journal of the American Heart Association (ahajournals.org)
- Hotchkiss R, Moldawer L, Opal S, Reinhart K, Turnbull I, Vicent JL. Sepsis and septic shock. Nat Rev Dis Primers [internet]. 2016 [citado 2021 Marzo 2]; 2. Disponible en: Sepsis and septic shock - PubMed (nih.gov)
- Kislitsina O, Rich J, Wilcox J, Pham D, Churyla A, Vorovich E et all. Shock- Classification and Pathophysiological Priciples of Therapeutics. Current Cardiology Reviews. 2019; 15 (2): 102-113
- Hernández Palazón J, Fuentes García D, Burguillos López S, Domenech Asensi P, Sansano Sánchez TV, Acosta Villegas F. Análisis de la insuficiencia de órganos y mortalidad en la sepsis por peritonitis secundaria. Med Intensiva. 2013; 37 (7): 461-467
- Rodríguez Botoa G, Rivero Garvía M, Gutiérrez González R, Márquez Rivas J. Conceptos básicos sobre la fisiopatología cerebral y la monitorización de la presión intracraneal. Neurología. 2015; 30 (1): 16-22
- Romero Valdez JG, Pereira Q, Atilio Zini R, Canteros GE. Reacciones de hipersensibilidad. Revista de Posgrado de la Via Cátedra de Medicina [internet]. 2007 [citado 2021 Marzo 2]; 167: 11-16. Disponible en: Microsoft Word - 3_167.doc (unne.edu.ar)
- Sáez Lorenzo L, Sáez Lorenzo M, Sáez Martin V. Revisión y actualización de la fluidoterapia de reanimación en el paciente con shock hipovolémico de origen traumático. Rev enferm CyL. 2016; 8 (1): 3-23
- Carrillo Ramírez SC, Elguera Echavarría PA. Choque circulatorio. Estableciendo metas enla reanimación con líquidos. Acta Medica Grupo Ángeles. 2017; 15 (1): 78-82
- Alemparte Pardavila E, Aller Fernández V, Bouza Vieiro MT, Cortés Cañones JR, Galeiras Vázquez R, García Monge MJ et all. SHOCK: identificación y manejo [Internet]. A Coruña: Seteseis Comunicación Creatividade SL y Complexo Hospitalario Universitario A Coruña (CHUAC); 2011 [citado 2021 Marzo 2]. Disponible en: (PDF) SHOCK: Identificación y Manejo (researchgate.net)
- González Villavelázquez ML, García Gonzalez A. Traumatismo craneoencefálico. Revista Mexicana de Anestesiología. 2013; 36 (1): 186-193
- González Posada MA, Biarnés Suñe A, Naya Sieiro JM, Salvadores de Arzuaga CI, Colomina Soler MJ. Damage Control Resuscitation en el paciente traumático. Rev Esp Anestesiol Reanim. 2019; 66 (7): 394-404
- Narváez I, Canabal A, Martín C, Sánchez M, Moron A, Alcalá J et all. Incidencia y evolución de la miocardiopatía séptica en una cohorte de pacientes con sepsis y shock séptico. Med Intensiva. 2018; 42 (5): 283- 291
- Zariquiey Esteva G, Santa Candela P. A propósito de un caso: intervenciones enfermeras a una paciente con shock anafiláctico en la UCI. Enferm Intensiva. 2017; 28 (2): 80-91
- Sánchez D, Lara B, Clausdorff H, Guzmán A. Generalidades y manejo inicial del shock. ARS MEDICA Revista de Ciencias Medicas. 2018; 43 (3): 66-76
- López Cruz F, Reyes Barragán G, Tapia Ibáñez EX, Paz Cordero DC, Ochoa Morales X, Cano Esquivel AA et all. Choque hipovolémico. An Med (Mex). 2018; 63 (1): 48-54
- Galeiras Vázquez R, Ferreiro Velasco ME, Mourelo Fariña M, Montoto Marqués A, Salvador de la Barrera S. Actualización en lesión medular aguda postraumática. Parte 1. Med Intensiva. 2017; 41 (4): 237- 247
- Dave S, Cho JJ. Neurogenic Shock [internet].StatPearls Publishing; 2021 [citado 2021 Marzo 2]. Disponible en: Neurogenic Shock - StatPearls - NCBI Bookshelf (nih.gov)
- Rhodes A, Evans L, Alhazzani W, Levy M, Antonelli M, Ferrer R et all. Campaña para sobrevivir a la sepsis: recomendaciones internacionales para el tratamiento de la sepsis y el choque septicémico: 2016. Critical Care Medicine. 2017; 45 (3): 486-568
- Haseer Koya H, Paul M. Shock [internet] StatPearls Publishing; 2021 [citado 2021 Marzo 2]. Disponible en: Shock - StatPearls - NCBI Bookshelf (nih.gov)
- Velasco Zúñiga R. Shock. Unidad de Urgencias Pediátricas. Hospital Universitario Río Hortega Valladolid. 2020
- Sabatier C, Monge I, Maynar J, Ochagavia A. Valoración de la precarga y la respuesta cardiovascular al aporte de volumen. Med Intensiva. 2012; 36 (1): 45-55
- Diaztagle Fernández JJ, Rodríguez Murciaa JC, Sprockel Diaz JJ. La diferencia venoarterial de dióxido de carbono en la reanimación de pacientes con sepsis grave y shock séptico: una revisión sistemática. Med Intensiva. 2017; 41 (7): 401- 410
- Palencia Herrejón E, Bueno García B. Nuevas guías de práctica clínica de la «Campana˜ sobrevivir a la sepsis»: lectura crítica. Med Intensiva. 2013; 37 (9): 600-604
- Grupo de trabajo de sepsis. Documento de Consenso (SEMES-SEMICYUC). Recomendaciones del manejo diagnóstico-terapéutico inicial y multidisciplinario de la sepsis grave en los Servicios de Urgencias hospitalarios. Med Intensiva. 2007; 31 (7): 375-87
- Grupo de trabajo de enfermedades infecciosas y sepsis. Estudio nacional de vigilancia de infección nosocomial en servicios de medicina intensiva ENVIN HELICS Informe 2019 [Internet]. España: Sociedad Española de Medicina Intensiva Crítica y Unidades Coronarias (SEMICYUC); 2019 [citado 2021 Marzo 2]. Disponible en: ENVIN-UCI '14 (vhebron.net)
- Ochagavía E, Baigorri F, Mesquida J, Ayuela JM, Ferrándiz A, García X, et al. Monitorización hemodinámica en el paciente crítico. Recomendaciones del Grupo de Trabajo de Cuidados Intensivos Cardiológicos y RCP de la Sociedad Espanola ˜ de Medicina Intensiva, Crítica y Unidades Coronarias. Med Intensiva. 2014; 38 (3): 154-169
- Mateu Campos ML, Ferrándiz Sellés A, Gruartmoner de Vera G, Mesquida Febrer J, Sabatier Cloarec C, Poveda Hernández Y, et al. Técnicas disponibles de monitorización hemodinámica. Ventajas y limitaciones. Med Intensiva. 2012; 36 (6): 434-444
- Grupo código sepsis. Plan de asistencia a la sepsis de Galicia. CÓDIGO SEPSIS [Internet]. Galicia: Xunta de Galicia; 2018 [citado 2021 Marzo 2]. Disponible en: CODIGO_SEPSE_CASTELLANO_WEB.pdf (sergas.es)
- Bravo Jover R, Morcillo Huertas J, Candela AB, Marín Real S, Martínez Baltanás A, Pascual Pérez R. Sepsis en adultos. España: Fisterra; 2020 [citado 2021 Marzo 2]. Disponible en: Guía clínica de Sepsis en adultos (fisterra.com)
- Empendium. Manual panamericano de medicina interna. Shock [Internet]. Polonia: Empendium [citado 2021 Marzo 2]. Disponible en: Shock - Enfermedades cardiovasculares - Enfermedades - Medicina Interna Basada en la Evidencia (empendium.com)
- Gersch C, Heimgartner NM, Rebar CR, Willis LM. Enfermería medicoquirúrgica. 4ªed. Philadelphia: Wolters Kluwer; 2017
- Woodruff DW. Enfermería fácil: Enfermería del paciente en estado crítico. 4ªed. Philadelphia: Wolters Kluwer; 2016
- Picó A, Aranda López I, Sesmilo G, Toldos González O, Japón MA, Luque RM et al. Recomendaciones sobre el diagnóstico e informe anatomopatológico de los tumores neuroendocrinos hipofisarios. Consenso de expertos de la Sociedad Española de Endocrinología y Nutrición y de la Sociedad Española de Anatomía Patológica. Endocrilogía, Diabetes y Nutrición. 2020; 1-12
- Blanco Carrera C, Cabañas Durán M, Tasende Fernández C, Rubio García JA. Tirotoxiocosis e hipertiroidismo. Medicine. 2020; 13 (13): 718-26
- Espinosa de Ycaza AE. Mujer, corazón y tiroides. Rev Colomb Cardiol. 2018; 25 (S1): 42-48
- Caneo C, Aedo I, Riquelme MJ, Fardella C. Disfunción tiroidea y trastornos del ánimo: revisión del estado del arte. Rev Med Clin Condes. 2020; 31 (2): 122-129
- Tortosa F, Webb S. Aspectos novedosos en histopatología de la hipófisis. Endocrinol Diabetes Nutr. 2017; 64 (3): 152-161
- Ortiz Flores AE, Araujo Castro M, Pascual Corrales E, Escobar Morreale HF. Síndrome de secreción inadecuada de hormona antidiurética. Medicine. 2020; 13 (18): 1000-6
- García Martínez MA, Martínez de Lagrán Zurbano I, García de Lorenzo y Mateos A. Recomendaciones para el tratamiento nutrometabólico especializado del paciente crítico: respuesta metabólica al estrés. Grupo de Trabajo de Metabolismo y Nutrición de la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias (SEMICYUC). Med Intensiva. 2020; 44 (S1):15-18
- Rojas D. Manejo de los tumores de hipófisis. Rev Med Clin Condes. 2017; 28 (3): 409-419
- Trifu DS, Gil- Fournier Esquerra NG, Peláez Torres N, Álvarez Hernández J. Hipotiroidismo. Medicine. 2020; 13 (13): 727-34
- Pascual Corrales E, Araujo Castro M, Ortiz Florez AE, Escobar Morreale HF. Hipopituitarismo. Medicine. 2020; 13 (15): 856-64
- Díez JJ. Hipoparatiroidismo postquirúrgico: un trastorno de interés creciente entre los endocrinólogos. Endocrinol Diabetes Nutr. 2019; 66 (7): 399-401
- Muñoz Torrez M, García Martín A. Hiperparatiroidismo primario. Med Clin (Barc). 2018; 150 (6): 226-232
- Rodríguez Gómez IA, Bernabeu I, Guillín C, Casanueva FF. Hiperaldosteronismo e hipoaldosteronismo. Medicine. 2016; 12 (14): 787-94
- Iturregui Guevara M, Larrán Escandón L, López Tinoco C. Enfermedades de la secreción de aldosterona. Medicine. 2020; 13 (19): 1072-82
- Araujo Castro M, Pascual Corrales E, Ortiz Flores AE, Escobar Morreale HF. Eje hipotálamo hipofisario. Fisiología y patología. Medicine. 2020; 13 (15): 846-855
- Galofre Martínez MC, Daguer Menco A, Rodríguez Cantillo J, Ramos Villegas Y, Barciela E, Moscote Salazar LR. Disfunción tiroidea en el paciente crítico: fisiopatología, evaluación y manejo. Acta Colomb Cuid Intensivo. 2019: 1-6
- Pascual Corrales E, Araujo Castro M, Ortiz Flores AE, Escobar Morreale HF. Diabetes insípida. Medicine. 2020; 13 (18): 993-9
- Tasende Fernández C, Rodríguez Troyano MJ, Lallena Pérez S, Álvarez Hernández J. Bocio y enfermedad nodular. Medicine. 2020; 13 (13): 709-17
- Mateo Gavira I, Baena Nieto G, García García Doncel L, Torres Barea IM. Actualización sobre el manejo diagnóstico y terapéutico del feocromocitoma y el paraganglioma. Medicine. 2020; 13 (19): 1083-93
- Hinkle JL, Cheever KH. Enfermería medicoquirúrgica Volumen 2. 14ª Edición. Philadelphia: Wolters Kluwer; 2018
- Belda Hofheinz S, Del Villar Guerra P, Palacios Cuesta A. Cetoacidosis diabética. An Pediatr Contin. 2014; 12 (2): 55-61
- Serrano Carmona JL, Luna Aljama J, Parra Moreno MD. Abordaje de la Cetoacidosis diabética: a propósito de un caso. Rev Paraninfo Digital [Internet], 2015; 22 [citado 2021 Abril 2]. Disponible en: http://www.index-f.com/para/n22/178.php
- Adeyinka A, Kondamudi NP. Hyperosmolar Hyperglycemic Nonketotic Coma [Internet] StatPearls Publishing; 2021 [citado 2021 Abril 2]. Disponible en: Hyperosmolar Hyperglycemic Nonketotic Coma - StatPearls - NCBI Bookshelf (nih.gov)
- Ghimire P, Dhamoon AS. Ketoacidosis [Internet] StatPearls Publishing; 2021 [citado 2021 Abril 2]. Disponible en: Ketoacidosis - StatPearls - NCBI Bookshelf (nih.gov)
- García Martínez MA, Martínez de Lagrán Zurbano I, García de Lorenzo y Mateos A. Recomendaciones para el tratamiento nutrometabólico especializado del paciente crítico: respuesta metabólica al estrés. Grupo de Trabajo de Metabolismo y Nutrición de la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias (SEMICYUC). Med Intensiva. 2020; 44 (S1): 15-18
- Vaquerizo Alonso C, Bordejé Laguna L, Fernández Ortega JF. Recomendaciones para el tratamiento nutrometabólico especializado del paciente crítico: introducción, metodología y listado de recomendaciones. Grupo de Trabajo de Metabolismo y Nutrición de la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias (SEMICYUC). Med Intensiva. 2020; 44 (S1): 1-14
- Juan Díaz M, Mateu Campos ML, Sánchez Miralles A, Martínez Quintana ME, Mesejo Arizmendi A. Recomendaciones para el tratamiento nutrometabólico especializado del paciente crítico: monitorización y seguridad.Grupo de Trabajo de Metabolismo y Nutrición de la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias (SEMICYUC). Med Intensiva. 2020; 44 (S1): 44-51
- Savino P, Patiño JF. Metabolismo y nutrición del paciente en estado crítico. Rev Colomb Cir. 2016; 31: 108-27
- Valls Matarín J, del Cotillo Fuente M, Grané Mascarell N, Quintana S. Variación de la masa muscular y el peso en el paciente crítico. Enferm Intensiva. 2015; 26 (3): 86-91
- Vaquerizo Alonso C. Nutrición parenteral en el paciente crítico: indicaciones y controversias. Nutr Clin Med. 2017; 11 (1): 26-41
- Martín López JI, Rodríguez Delgado ME, López Torres G, Albendín García L. Estrategia nutricional y metabólica en el paciente séptico en Cuidados Intensivos. Revisión bibliográfica. Parainfo Digital. 2015; 22
- Zamora Elson M, Martínez Carmona JF. Ruiz Santana S. Recomendaciones para el tratamiento nutrometabólico especializado del paciente crítico: consecuencias de la desnutrición en el paciente crítico y valoración del estado nutricional.Grupo de Trabajo de Metabolismo y Nutrición de la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias (SEMICYUC). Med Intensiva. 2020; 44 (S1): 19-23
- Gutierrez G, Reines HD, Wulf-Gutierrez ME. Clinical review: Hemorrhagic shock. Critical Care. 2004; 8 (5): 373-381
