1. MEDICAMENTOS PELIGROSOS
1.1. Introducción
Las y los profesionales de Enfermería nos enfrentamos diariamente a distintos riesgos para la salud. Uno de ellos es la exposición a medicamentos peligrosos (en adelante MP).
A diferencia de otros productos químicos, los medicamentos se crean expresamente para unirse a las células y producir un efecto terapéutico. A veces, con el coste de efectos secundarios peligrosos que constituyen un sacrificio necesario para lograr el objetivo primario de sanar o paliar la situación del enfermo. Pero los profesionales son personas sanas que se exponen a un cóctel de fármacos que no necesitan y a sus efectos nocivos. Y, a diferencia de las personas enfermas, cuya exposición es limitada en el tiempo, la enfermería se expone, potencialmente, 230 días al año a estos fármacos durante toda su vida laboral.
Estas actividades se realizan en las salas del hospital. Incluso en el mejor de los casos, las condiciones de seguridad difícilmente evitan el riesgo de entrar en contacto con los MP. Algunas situaciones pueden dar lugar a contacto a través de la piel, no solo en la preparación y administración, sino también, con restos de medicamentos en superficies de trabajo o áreas contaminadas, manipulación de líquidos corporales o ropa de cama, acciones de descontaminación y limpieza de las zonas de preparación, etc.
Esta exposición ha sido un tema poco abordado desde el aspecto preventivo y, en todo caso, circunscrito a los medicamentos oncológicos en los servicios de Farmacia. Sin embargo, el resto de los profesionales de enfermería, tanto en hospitales como en atención primaria, manipulamos a diario medicamentos peligrosos desconociendo generalmente que lo son.
Aunque el grupo más importante de Medicamentos Peligrosos lo constituyen los antineoplásicos, actualmente se han incorporado otros medicamentos muy diversos que afectan a un amplio grupo de profesionales sanitarios y áreas clínicas. Los factores que condicionan el riesgo de exposición de los manipuladores incluyen:
• Peligrosidad intrínseca del medicamento por su potencial carcinogénico, teratogénico, genotóxico, toxicidad reproductiva y toxicidad sobre órganos a dosis bajas.
• Utilización de medidas de prevención: medidas técnicas (Cabina de Seguridad Biológica (CSB), sistemas cerrados de transferencia de medicamentos (SCTM), sistemas automatizados), medidas organizativas (procedimientos de limpieza, actuación ante derrames y mantenimiento, gestión de residuos y técnicas de manipulación) y medidas de prevención secundaria (Equipos de Protección Personal (EPI)).
• Estructura: recursos humanos (formación y capacitación, número de manipuladores), instalaciones (diseño y especificaciones técnicas, disponibilidad y tipo de CSB), utilización de SCTM en preparación y administración y disponibilidad de sistemas automáticos.
• Susceptibilidad del manipulador: alergia, embarazo, lactancia, edad reproductiva.
• Nivel de exposición: capacidad de penetración o absorción del medicamento, concentración, cantidad, duración y frecuencia de la manipulación, tipo de actividad, lugar y riesgo de exposición asociado. Los efectos sobre la salud de los Medicamentos Peligrosos están asociados a sus efectos terapéuticos y/o a sus efectos secundarios, que se admiten por ser menores o, en algunos casos, inevitables, como con los efectos cancerígenos asociados al uso de muchos citostáticos. Dichos efectos quedan justificados en los pacientes por presentar un balance beneficio/riesgo favorable, pero se deben evitar de manera radical en el personal sanitario y cuidadores para los que no existe beneficio clínico. Siguiendo la legislación vigente (ver el apartado correspondiente) se deben adoptar medidas que eviten o minimicen la exposición a Medicamentos Peligrosos y garanticen condiciones óptimas de trabajo y seguridad; las organizaciones sanitarias deben asegurar las medidas de prevención primaria colectiva, técnicas y organizativas, que deben anteponerse a las de protección individual.
1.2. Definición de medicamento peligroso
Desde la perspectiva de Salud Laboral, definimos MEDICAMENTO PELIGROSO como aquel fármaco que contiene un principio activo cuya potencial toxicidad representa un riesgo para la salud de los profesionales sanitarios que van a manipularlo.
Se consideran MEDICAMENTOS PELIGROSOS aquellos que son susceptibles de producir lesiones en el organismo de aquellas personas que, no siendo receptoras de los mismos, los manipulan de forma voluntaria para administrarlos o involuntaria por contacto accidental.
La peligrosidad de estos medicamentos supone un riesgo químico, sobre todo por la actividad carcinogénica, teratogénica, genotóxica y tóxica sobre el proceso reproductivo o sobre un órgano concreto a dosis bajas, o por tratarse de un nuevo fármaco similar a otros con este tipo de riesgos.
Se consideran MEDICAMENTOS PELIGROSOS los que presentan una o más de las siguientes seis características en seres humanos o animales:
1 carcinogenicidad.
2 Teratogenicidad u otra toxicidad del desarrollo.
3 toxicidad reproductiva.
4 evidencia de toxicidad grave en órganos u otra toxicidad en dosis bajas en modelos
animales o en pacientes tratados.
5 genotoxicidad.
6 estructura y perfiles de toxicidad de las nuevas medicinas que se han determinado
como peligrosas según los criterios anteriores.
NIOSH (National Institute for Occupational Safety and Health) clasifica los MP en:
Grupo 1: medicamentos antineoplásicos.
Grupo 2: medicamentos no antineoplásicos que cumplen al menos un criterio anterior.
Grupo 3: medicamentos que presentan riesgo para el proceso reproductivo y que pueden afectar a hombres y mujeres que están intentando concebir de forma activa, y mujeres embarazadas o en periodo de lactancia, pero que no comportan riesgo para el resto del personal.
Las vías de exposición más probables son la inhalación y el contacto/absorción a través de la piel, aunque también son posibles la ingestión accidental por contacto mano-boca y la inyección accidental a través del pinchazo con una aguja o lesión con objetos cortopunzantes.
Las exposiciones laborales a MP pueden inducir:
1) Efectos agudos como erupciones cutáneas.
2) Efectos crónicos como acontecimientos reproductivos adversos y
3) Anormalidades en cromosomas 5 y 7 y posiblemente cáncer.
Ante esta situación, las principales sociedades científicas implicadas, prepararon un Documento de Consenso, en enero de 2015, donde se analizó la situación y se propusieron una serie de recomendaciones, como la necesidad de revisar y analizar los puntos críticos para la prevención de exposición a MP de los profesionales sanitarios en las fases de preparación, transporte y administración.
En medidas de Prevención para su preparación y administración, todos los hospitales deberían tener un protocolo de medicamentos peligrosos donde nos indique la guía de MP, para saber manipular, reconstituir y administrar dichos medicamentos. Lo importe es proteger la salud de los trabajadores, disminuyendo la exposición a MP hasta el mínimo nivel razonablemente posible.
En septiembre de 2016, "El Instituto Nacional de Seguridad, Salud y Bienestar en el Trabajo" (INSSBT) publicó el documento técnico “Medicamentos peligrosos: Medidas de prevención para su preparación y administración”, en el que se recoge un listado de medicamentos y productos sanitarios que se comercializan en España es el siguiente:


Aquí tenéis el enlace de la guía por el ministerio. En este documento técnico se recogen recomendaciones de uso y medidas de prevención a adoptar para la manipulación segura de este tipo de medicamentos.
Además, el INSSBT pone a disposición del personal sanitario la base de datos INFOMEP, en la que se puede encontrar información sobre más de 2.400 medicamentos y especialidades relacionadas y recomendaciones para la preparación y administración: http://infomep.inssbt.es/
Otra de las guías que publico el Ministerio es: Guía de buenas prácticas para trabajadores profesionalmente expuestos a agentes citostáticos. Os dejo el enlace y el QR.
http://gesdoc.isciii.es/gesdoccontroller?action=download&id=26/03/2014-199edf956b

Los medicamentos que más comúnmente se identifican dentro de la categoría de medicamentos peligrosos suelen ser los citostáticos o antineoplásicos, pero también son medicamentos peligrosos los usados para otros fines de modo más frecuente y cuya aplicación es común en áreas de atención no especializada.
En la siguiente tabla podemos ver algunos de los medicamentos peligrosos de uso
más común clasificados en función de su grupo terapéutico:
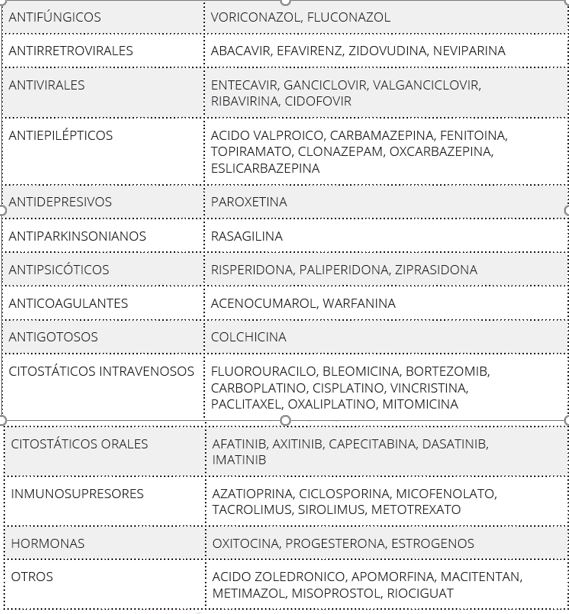
- VÍAS DE EXPOSICIÓN

Imagen 18 Fuente: Ilustraciones del Hospital General Universitario de Elda.
Algunos factores que pueden influir en la absorción a través de estas vías son:
• La pureza de los medicamentos que se manipulan.
• La frecuencia y duración del proceso en que se manejan.
• La formación (o su falta) del personal expuesto.
• El potencial de absorción de los propios medicamentos.
- EFECTOS SOBRE LA SALUD
Los efectos de la exposición pueden ser:
• Agudos: Tienen una duración de semanas a meses, produciéndose por efectos locales y perjudiciales por el contacto directo del medicamento con piel y mucosas.
Entre los efectos agudos de los medicamentos peligrosos se incluyen: mareos, náuseas, cefalea, dermatitis, problemas menstruales, etc.
• Crónicos: Su inicio de manera subclínica puede no resultar evidente hasta muchos
años después, haciendo difícil establecer conexión entre la exposición y la aparición
de la enfermedad. Entre los efectos crónicos más frecuentes encontramos:
Aumento de los efectos genotóxicos en los diferentes aparatos y sistemas del organismo: (pulmón, hígado, problemas auditivos, médula ósea, etc.), cáncer (entre muchos tipos de cáncer leucemia y linfomas), alteraciones fetales (malformaciones, abortos, bajo peso al nacer, etc.) y de la función reproductora (infertilidad temporal o permanente).
Los estudios muestran que las enfermeras expuestas a los fármacos citotóxicos tienen el doble de probabilidades de abortar y el personal hospitalario que maneja fármacos citotóxicos tiene tres veces más probabilidades de desarrollar cáncer.
Se ha demostrado un aumento del daño genético en las enfermeras, especialmente en las enfermeras de los hospitales de día, al ser el grupo que maneja la mayor cantidad de medicamentos durante el proceso de administración.
- MEDIDAS PREVENTIVAS A ADOPTAR
Plan de prevención de riesgos: La Evaluación de riesgos y la planificación de la acción preventiva.
La normativa señala que la prevención de riesgos laborales deberá integrarse en el sistema general de gestión de la empresa, tanto en sus actividades como en todos los niveles jerárquicos de la misma, a través de la implantación y aplicación de un plan de prevención de riesgos.
Este plan de prevención de riesgos laborales deberá incluir la estructura organizativa, las responsabilidades, las funciones, las prácticas, los procedimientos, los procesos y los recursos necesarios para realizar la acción de prevención de riesgos en la empresa.
• Evaluación de riesgos
La evaluación de riesgos es un documento que deberá recoger exhaustivamente todos las tareas y puestos de trabajo en los que los trabajadores y las trabajadoras van a estar en contacto con los medicamentos peligrosos. Como hemos señalado anteriormente, no solo el personal sanitario se considera expuesto, sino todas las personas que van a tener contacto con el tóxico desde que llega al lugar de trabajo hasta que se eliminan sus residuos.
La evaluación de riesgos determinará las medidas preventivas y la prioridad en su adopción en función de una matriz que cruza las variables: probabilidad de que ocurra un daño y la gravedad o severidad del mismo en caso de que ocurriera.
Es recomendable que la evaluación incluya un inventario de los medicamentos peligrosos existentes en el lugar de trabajo y de los puestos en los que se está en contacto con ellos de manera directa o indirecta.
Asimismo, será pertinente la elaboración y mantenimiento de un registro de trabajadores y trabajadoras que según la evaluación de riesgos hayan estado expuestos a medicamentos peligrosos o lo estén en la actualidad.
• Planificación de la acción preventiva
Si los resultados de la evaluación pusieran de manifiesto situaciones de riesgo, el empresario realizará aquellas actividades preventivas necesarias para eliminar o reducir y controlar tales riesgos. El empresario deberá planificar estas actividades priorizando en función de su peligrosidad y probabilidad, estableciendo el plazo para llevarlas a cabo, la designación de responsables y los recursos humanos y materiales necesarios para su ejecución.
Además, deberá asegurarse de la efectiva ejecución de las actividades preventivas incluidas en la planificación, efectuando para ello un seguimiento continuo y una comprobación de su eficacia
• Formación e información
La Ley de Prevención de Riesgos Laborales determina que la formación e información en materia de riesgos laborales es un derecho de los trabajadores y una obligación de los empresarios (arts. 18 y 19 LPRL).
Tanto esta norma como las relativas específicamente a la protección contra los riesgos derivados de la exposición a químicos indican que los trabajadores y las trabajadoras tienen derecho a recibir información sobre los riesgos generales y específicos para la seguridad y salud en el trabajo, así como de las medidas de protección y prevención a adoptar.
Por lo tanto, las plantillas deben recibir información y formación sobre la existencia de medicamentos peligrosos en sus lugares de trabajo, los riesgos que implica su uso y las medidas preventivas que se deben adoptar para su uso adecuado, incluyendo los procedimientos de trabajo preceptivo por personal cualificado.
• Vigilancia de la salud
El personal expuesto a medicamentos peligrosos debe estar controlado en un adecuado programa de vigilancia de la salud. Este incluirá reconocimientos específicos periódicos en función de los medicamentos que estén manejando en sus puestos de trabajo.
Para los medicamentos citostáticos específicamente, el Ministerio de Sanidad y Consumo elaboró el Protocolo de Vigilancia Sanitaria para trabajadores expuestos a Agentes Citostáticos:
http://www.mscbs.gob.es/ciudadanos/saludAmbLaboral/docs/Agentescitostaticos.pdf
que se deberá tener en cuenta a la hora de realizar la vigilancia de la salud a los grupos de profesionales expuestos a este tipo de medicamentos.
Os dejo el QR del protocolo:

El monitoreo biológico realizado de manera individual a cada trabajador o trabajadora consistirá, entre otras pruebas, en la realización de análisis para determinar la presencia de medicamentos peligrosos o sus metabolitos en sangre o en orina.
La vigilancia de la salud tiene una vertiente individual y una colectiva. Esta segunda implica la recolección y estudio de los datos de salud individuales para su análisis en conjunto y la utilización en la detección precoz de daños a la salud de la plantilla.
Los datos obtenidos en agregado de esta vigilancia de la salud nos permitirán hacernos una idea de la eficacia de las medidas preventivas adoptadas y nos permitirán adoptar las que sean pertinentes.
Con el objetivo de realizar una detección precoz de los posibles daños a la salud, se ofrecerá al trabajador o a la trabajadora la posibilidad de realizar una vigilancia de la salud individual específica, que podrá incluir la realización de pruebas médicas determinadas para tal fin.
La vigilancia se deberá realizar:
• Antes de la incorporación al puesto de trabajo.
• A intervalos periódicos durante la vida laboral.
• Después de alguna exposición aguda o daño para la salud.
• A la finalización de la relación laboral.
- MEDIDAS DE PREVENCIÓN: COLECTIVAS E INDIVIDUALES
La evaluación de riesgos de los diferentes puestos de trabajo y actividades desarrolladas dará como resultado la recomendación de llevar a cabo una serie de medidas para la adecuada gestión del riesgo derivado del uso de medicamentos peligrosos.
Según sean las características de cada medicamento, el modo de preparación del mismo y sobre todo el modo de administración y el lugar en el que esta se realice, habrá que adoptar unas medidas preventivas u otras.
No obstante, la normativa sobre exposición al riesgo químico establece una jerarquía en la adopción de estas medidas preventivas encaminadas a reducir la exposición:
• En primer lugar se tratará de sustituir, en la medida de lo posible, el medicamento peligroso por otro que implique menos riesgos para la salud. Los niveles umbral de exposición no pueden predecirse y, por lo tanto, debe evitarse el contacto con carcinógenos genotóxicos en la medida que sea posible.
• Si esto no fuera posible, será prioritario el trabajo utilizando procesos de trabajo cerrados, en los cuales el contacto con el medicamento peligroso sea el mínimo posible.
• Uso de equipos de aspiración general y de aspiración localizada, cabinas de seguridad biológicas, salas limpias.
• Medidas organizativas de manera que el tiempo de exposición y el número de personas trabajadoras expuestas sea el mínimo posible. La evolución científica y tecnológica, tanto en el tipo de fármacos que se usen como en las técnicas y procesos para su preparación y administración, deberá ser tenida en cuenta a la hora de marcarnos los objetivos y las medidas preventivas a adoptar en cada momento.
Por último:
• Uso de equipos de protección individual, como guantes, equipos de protección
respiratoria, gafas, bata, calzas, gorro, etc.
Miremos el gráfico de los equipos de protección necesarios (EPIS):

Imagen 18 Fuente: Ilustraciones del Hospital General Universitario de Elda.

Imagen 19 Fuente: Ilustraciones del Hospital General Universitario de Elda

Veamos el vídeo de colocación de las EPIS realizado por el hospital del bierzo.

Imagen 20 Fuente: Ilustraciones del Hospital General Universitario de Elda.
Veamos el vídeo de retirada de las EPIS realizado por el hospital del bierzo.

Riesgos en la preparación de los (MP) : Veamos en los gráficos

Imagen 21 Fuente: Ilustraciones del Hospital General Universitario de Elda.

Video preparación de medicamentos peligrosos con sistema Tevadaptor.

Imagen 22 Fuente: Ilustraciones del Hospital General Universitario de Elda
- VIAS DE ADMINISTRACIÓN. MEDIDAS GENERALES PARA LA ADMINISTRACIÓN DE MP
Vías de administración:
• Vía Oral.
• Vía Tópica.
• Vía Parenteral (subcutánea, intramuscular, intravenosa...).
• Otras vías (intratecal, inhalatoria, intraarterial y/o quimio embolización, intracavitaria).
Medidas Generales:
La administración del MP se realizará siguiendo las recomendaciones de las fichas técnicas y siempre según los protocolos o guías de cada centro:
• Lavado de manos antes y después del procedimiento.
• Uso de sistemas cerrados de transferencia para fármacos Grupo 1 y Grupo 2.
• Aplicar las máximas medidas de asepsia en la zona donde se realice la manipulación
para minimizar la contaminación.
• No comer, beber o masticar chicle. No llevar joyas ni maquillaje.
• Finalizada la administración de MP, desechar todo el material empleado y los residuos generados en el contenedor adecuado según apartado 5.
• Disponer de mobiliario adecuado para depositar el fármaco antes de ser usado. Usar mesas y superficies antideslizantes con topes para preparar la técnica y sillón o camilla para colocar al paciente. Todo el mobiliario será de materiales impermeables, fáciles de limpiar y serán limpiados después de su uso y siempre que se precise.
• Disponer de Kit de Derrames y conocer el procedimiento de actuación en caso deDerrames y la localización del Kit.
• Utilizar EPI’s recomendado, según tabla que se adjunta. ADMINISTRACIÓN VIA ORAL.
En la administración oral de MP, la elección de la presentación se realizará priorizando las formas sólidas completas (comprimidos, grageas y cápsulas) y las formas líquidas (jarabes y gotas). Si surge necesidad de fraccionar o machacar una forma sólida oral, deberá hacerse en el área acondicionada para ello.
Adoptar las medidas generales para todas las vías de administración de MP.
ADMINISTRACIÓN MP VÍA TÓPICA.
Presentación en forma de cremas, pomadas, ungüentos, bálsamos, parches y resto de presentaciones. Procedimiento de administración:
En la administración tópica de MP se tendrán en cuenta las mismas precauciones generales que para las formas farmacéuticas líquidas orales.
- Utilizar espátulas u otros productos de aplicación, que eviten el contacto con el producto
- Se utilizarán alfombras absorbentes por el anverso e impermeables y antideslizantes por el reverso antes de la administración. Después de la aplicación se cubrirá la superficie de piel tratada.
- Adoptar las medidas generales para todas las vías de administración MP.
6. ADMINISTRACIÓN MP VÍA PARENTERAL (SUBCUTÁNEA (SC), INTRAMUSCULAR
(IM), INTRAVENOSA (IV).
Procedimiento de administración:
• Usar formas farmacéuticas intactas, en viales monodosis con sistema de bioseguridad. De no ser así, se pautarán presentaciones precargadas y purgadas con sistemas cerrados de transferencia.
• En caso de precisar purgado, utilizar gasa estéril empapada en alcohol 70º, para impedir la formación de aerosoles y contaminación de superficies.
• Para evitar contaminar ropa de cama o sillón a la hora de administrar el fármaco, disponer de una alfombra absorbente por el anverso e impermeable y antideslizante por el reverso.
• En la administración por vía parenteral en ningún momento se desconectará la aguja o catéter de la jeringa; las conexiones deben ser LUER-LOCK que impida la desconexión accidental.
• Los MP vía parenteral vendrán preparados con sistema cerrado en jeringa ensamblada a la aguja destinada a su fin para así, evitar manipulación en la administración y no generar derrames, aerosoles, ni pinchazos accidentales.
• Siempre que sea posible la administración de MP por vía parenteral se realizará en espacios amplios con buena ventilación para minimizar la concentración de aerosoles y vaporización.
• Adoptar las medidas generales para todas las vías de administración MP.
7. ADMINISTRACIÓN VÍA INTRAVENOSA (IV).
Para minimizar al máximo el riesgo de derrames y cualquier otro incidente o accidente (pinchazos, roturas de bolsas, fugas...) que puedan provocar inhalación, ingestión y/o salpicaduras, habrá que utilizar:
- Recursos materiales
- Bombas de infusión
- volumétricas.
- Equipos de infusión.
- Dispositivos Cerrados o Sistemas cerrados de perfusión.
- Kit de derrames
- Mobiliario adecuado y seguro.
Bombas de infusión volumétricas:
Permiten la administración de los tratamientos a la velocidad deseada y con un sistema de alarma que permite detectar fallos durante la infusión.
Equipos de infusión:
Son los llamados equipos de goteo. Constan de:
• Un punzón perforador.
• Cámara de goteo.
• Tubuladura.
• Dispositivo que se introduce en la bomba volumétrica.
• Extremo distal con conexión LUER-LOCK.
Existen muchos tipos en el mercado pues se van adaptando a las características de las bombas volumétricas y a las necesidades requeridas tanto del fármaco (equipos de baja absorción) como del paciente (equipos con uno o varios puertos de acceso en su tubuladura).
Estos equipos de infusión o goteo se acoplan a los sistemas cerrados de administración de Fármacos.
Dispositivos cerrados o Sistemas de perfusión:
NIOSH (National Institute for Occupational Safety and Health, Estados Unidos) dio el nombre de CSTD (Closed System drug Transfer Devices) a los dispositivos para la transferencia de citostáticos y, en general, de principios activos de alta potencia o toxicidad, definidos como aquellos equipos que impiden de manera mecánica la entrada de contaminantes en el sistema y el escape de principios activos peligrosos fuera del mismo.
Hay diferentes tipos de sistemas cerrados para la administración de MP, que pueden acoplarse a las bombas de infusión según fueran necesario. Dichos sistemas cerrados de administración como mínimo deberán:
• Estar exentos de látex, DEHP y otros materiales que puedan desprender partículas en
contacto con este tipo de fármacos.
• Minimizar el número de maniobras de conexión/desconexión.
• Con puertos de conexión sin agujas.
• Disminuir el riesgo de goteo, derrame y aerosoles mediante válvulas antirreflujo.
• Sistema de una sola pieza o compacto que disminuya el número de productos necesarios para su funcionamiento.
• Hay sistemas cerrados de perfusión continua con multiconexión de material plástico y flexible en una sola pieza y sistemas de perfusión intermitente, (bioconectores), que son de material plásticos rígido en una sola pieza, provisto de una conexión luer-lock
hembra compatible con jeringa o sistema de perfusión estándar. La conexión distal debe ser tipo luer-lock macho, adaptable a agujas, catéteres y llaves de tres pasos convencionales.
Procedimiento de administración:
Se pueden utilizar dos técnicas; perfusión continua o administración en bolo:
- Cuando el fármaco se administre en bolo, se preparará en una jeringa adecuada para la aplicación directa, lo cual requiere la utilización de un sistema cerrado, especialmente diseñado para la administración de MP que evite el goteo, creación de aerosoles y desconexión accidental. En ningún momento de la administración se desconectará dicho sistema de la jeringa.
La administración se realizará a través de un bioconector, provisto de válvulas de seguridad cerradas tanto mecánicamente como microbiológicamente de tal forma que por una luz se administre el MP, y por la otra, suero limpio para purgar y lavar la vía. Una vez finalizada la infusión se procede a la limpieza de la superficie de la válvula por la que se ha infundido el MP con antiséptico adecuado, para eliminar cualquier residuo que pueda quedar, por mínimo que este sea.
- Para la perfusión continua de MP, se utilizan sistemas cerrados de perfusión, que garanticen la seguridad tanto del trabajador como del paciente.
El fármaco llegará al Servicio donde vaya a ser administrado conectado a una alargadera que haya sido previamente purgada en SFH con suero limpio o con otra solución inocua, para evitar derrame de MP durante el transporte o conexión al sistema de administración.
Llegado el momento de administrar el MP se insertará el extremo libre de la alargadera al puerto de acceso sin aguja del sistema cerrado de infusión. El sistema se eliminará como si fuera una sola pieza en el contenedor de MP según apartado 5 No se deben desconectar los fármacos utilizados.
El personal implicado en la técnica debe ser formado para asegurar la utilización adecuada de los sistemas cerrados para lograr un óptimo funcionamiento, y reducir al mínimo el riesgo de goteos, derrames o creación de aerosoles.
8. ADMINISTRACIÓN MP EN INFUSOR.
• Definición:
Dispositivo mono-uso que permite la administración de medicación en forma continua,
segura y sencilla, sin uso de baterías ni corriente eléctrica. Se usa para pacientes ambulatorios, en domicilio.
• Colocación del infusor:
- Se realizará preferiblemente en hospital.
- Educación sanitaria al paciente portador de infusor para evitar derrames, roturas.
- Adoptar las medidas generales para todas las vías de administración MP.
• Retirada del infusor:
Se puede realizar en: Hospital, Domicilio, Centro de Salud, Residencia Sociosanitaria.
Antes de retirar infusor, pinzar lo más cerca posible del conector mediante el uso de la pinza destinada a este fin para evitar fugas de MP.
Desechar Infusor con alargadera y aguja en bloque y todo el material utilizado (gasas, jeringas...) al contenedor de residuos MP.
Adoptar las medidas generales para todas las vías de administración MP.
Limpieza y desinfección.
La limpieza y desinfección son unas de las medidas preventivas básicas para evitar la exposición e incluyen varias etapas:
Desactivación: transforma el MP en un compuesto
- inerte o inactivo.
- Descontaminación: elimina los residuos de MP de las superficies.
- Limpieza: elimina contaminantes de las superficies.
Toda persona encargada de la limpieza del área de trabajo debe estar entrenada en los procedimientos adecuados para protegerse y evitar la contaminación del medio ambiente y adecuadamente formada.
9. NORMAS GENERALES.
- Limpiar siempre con guantes adecuados a la actividad que se esté desarrollando.
- Antes de iniciar la limpieza general recoger la materia orgánica (sangre y otros fluidos).
- Limpiar siempre que esté sucio.
- No barrer nunca, recoger la suciedad con mopa o protegiendo el cepillo con textil húmedo o tejido sin tejer.
- Limpiar las superficies con bayetas húmedas.
- El material de limpieza utilizado tiene que ser específico.
- No crear corrientes de aire que faciliten el desplazamiento de gérmenes.
- Utilizar productos de uso hospitalario aprobados por la Comisión de Expertos de cada centro.
- Dosificar el producto según las pautas establecidas.
- No mezclar productos incompatibles (ej.: hipoclorito sódico con aldehídos).
- Llevar siempre en el carro de la limpieza los envases originales tanto de detergentescomo de desinfectantes.
- No se recomienda fumigar ni utilizar sprays.
- El material utilizado para limpiar todo tipo de superficies (bayetas, fregonas, mopa…) ha de estar lo más escurrido posible. Dejar actuar el desinfectante sobre las superficies, no es necesario aclarar ni secar.
- El material utilizado para la limpieza debe dejarse limpio, desinfectado y bien escurrido en cada turno.
- Durante la manipulación de los productos de limpieza, el personal se protegerá para prevenir posibles riesgos (inhalación y/o salpicaduras sobre piel o mucosas) con equipos de protección individual (EPI).
- El personal de limpieza deberá utilizar las mismas medidas de protección que el personal sanitario, tanto en lo referente al vestuario como para la eliminación de los residuos generados siguiendo las normas de cada centro.
- Orden de limpieza: siempre será de arriba abajo, de dentro hacia afuera y de limpio a Sucio.
10. TRATAMIENTO DE EXCRETAS.
Las excretas de pacientes que hayan recibido determinados MP pueden contener restos de estos fármacos y/o de sus metabolitos hasta varios días después de su administración, por lo que se deben tomar medidas de prevención durante la manipulación de las mismas.
El riesgo es variable y, entre otros factores, estará determinado por el medicamento, vía de administración, dosis recibida, vía de eliminación, función renal o hepática del paciente. En general, para la manipulación de excretas de pacientes tratados con MP tipo 1 se recomienda el empleo de EPI durante un periodo mínimo de 48 horas.
Los EPI recomendados para protegerse son: guantes, bata impermeable con refuerzo en parte delantera y brazos, con puños ceñidos y atada atrás, desechables después de su uso. Se usarán mascarilla y gafas, o pantalla facial, en caso de que exista posibilidad de salpicaduras. En caso de vertido libre, trasvase o manipulación similar de excretas que pueda generar aerosoles en el lugar de trabajo, deberá utilizarse también mascarilla de protección respiratoria FFP3.
En el resto de MP se deberá acudir a la información contenida en la ficha técnica del medicamento.
11.GESTIÓN DE RESIDUOS
Bajo la denominación de residuos sanitarios, se recogen todos los generados en cualquier establecimiento o servicio en el que se desarrollen actividades de atención a la salud humana. En este sentido, el material sanitario debe considerarse residuo a partir del momento en que su utilidad o manejo clínico se dan definitivamente por concluidos.
Clasificación:
• Residuos de MP1
Este grupo de residuos se corresponde exactamente con el definido en la lista europea de residuos como Residuos de medicamentos citotóxicos y citostáticos (LER 180108*) y con la Clase IV del Protocolo para la gestión de residuos sanitarios generados en los centros sanitarios que incluye residuos sanitarios compuestos por restos de MP1.Se consideran residuos citostáticos los siguientes:
- Los restos de medicamentos citostáticos generados en la preparación y administración.
- El material utilizado en la limpieza de las zonas donde se lleva a cabo la manipulación, especialmente la preparación y administración de citostáticos.
- El material utilizado en la preparación y administración de citostáticos (agujas, jeringas, frascos, bolsas y sistemas de infusión).
- El material de protección de los manipuladores de citostáticos (ropa protectora desechable, guantes y mascarilla de protección respiratoria).
- El material procedente del tratamiento de derrames accidentales, incluidos los de excretas durante el periodo de vida activa del citostático. do el material que haya estado en contacto con ellos.
Su segregación se realizará en contenedores homologados, rígidos, de un solo uso, de color azul. Hay disponibilidad de contenedores de 30 y 60 litros de capacidad.

Imagen 23 Fuente: Ilustraciones del Hospital General Universitario de Elda.
Contenedores para residuos citostáticos.
Los residuos punzantes o cortantes generados como resultado de la administración de este tipo de medicamentos deben desecharse en los contenedores de punzantes identificados para residuos citostáticos. Algunos ejemplos de capacidades disponibles son 3, 5 y 10 litros

Imagen 24 Fuente: Ilustraciones del Hospital General Universitario de Elda.
Contenedores para residuos citostáticos punzantes.
• de MP2 y MP3
Como norma general, los MP orales se administrarán, siempre que sea posible, en dosis o presentaciones que eviten el fraccionamiento y por tanto la generación de restos de MP.
Los residuos que contengan restos de MP2 y MP3 (frascos, sistemas, ampollas, viales, jeringas...) se eliminarán en el contenedor azul de residuos peligrosos de medicamentos seleccionando el contenedor de menor tamaño posible, para ajustar su capacidad al volumen de producción de residuos. En muchos casos, será adecuado el uso de los contenedores de 3 o 10 litros.
Los EPI utilizados para la administración de MP2 y MP3, se eliminarán como residuo asimilable a urbano, salvo contaminación evidente (salpicadura, derrame...). Los EPI empleados en preparación, se eliminarán en el contenedor de residuos peligrosos de medicamentos.
El material empleado para la recogida de derrames (material absorbente, EPI...) se eliminará en el contenedor azul de residuos peligrosos de medicamentos.
Precauciones generales en la gestión de residuos
Es importante aplicar correctamente el cierre de los contenedores.
En el caso de contenedores para punzantes, es preciso ensamblar bien la tapa antes de su primer uso.
Durante su utilización, debe aplicarse el cierre provisional (girando la tapa cuando no se use) y el cierre definitivo una vez esté lleno (presionando la lengüeta.
Aplicación de los cierres provisional y definitivo del contenedor de punzantes.

Ensamblaje de la tapa del contenedor de punzantes.
Imagen 24 Fuente: Ilustraciones del Hospital General Universitario de Elda.
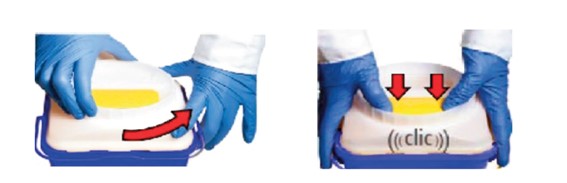
Aplicación de los cierres provisional y definitivo del contenedor de punzantes.

Imagen 25 Fuente: Ilustraciones del Hospital General Universitario de Elda.
Como norma general los contenedores deberán cerrarse cuando se hayan ocupado las 2/3 partes de su capacidad.
- No se debe superar el límite de llenado, con objeto de evitar accidentes y dificultades para cerrar los contenedores.
- Es preciso adecuar, en la medida de lo posible, la capacidad del contenedor a la cantidad de residuos generada, de modo que se establezca un equilibrio razonable entre frecuencia de retirada y aprovechamiento eficiente de su capacidad.
- Los envases en uso nunca se dejarán en zonas de paso o lugares que puedan dar lugar a tropiezos, y siempre se mantendrán alejados de cualquier fuente de calor.
- Es muy importante que en todos aquellos puntos donde se puedan administrar MP, retirar sistemas de infusión..., los responsables de solicitar el material prevean el suministro de los contenedores adecuados. La segregación de los residuos en los contenedores designados minimiza el riesgo de accidente y garantiza que sean gestionados de acuerdo con su peligrosidad.
- En cualquier caso, los filtros de alta eficacia de las cabinas de seguridad empleados en preparación de MP, al ser sustituidos se eliminarán como tales residuos. Para ello, habrán de depositarse en los contenedores establecidos o, en caso de no caber, en sacos o bolsas para residuos, de galga mínima 400, adecuadamente precintados y etiquetados para su identificación.

BIBLIOGRAFÍA
- Sandiumenge, A., Anglés, R., Martínez-Melgar, J. L., & Torrado, H. (2008). Utilización de bloqueantes neuromusculares en el paciente crítico. Med. intensiva(Madr.,Ed.impr.),69-76.Disponible en : https://www.medintensiva.org/es-pdf-13116128
- Illman, HL, Laurila, P., Antila, H., Meretoja, OA, Alahuhta, S. y Olkkola, KT (2011). La duración del bloqueo neuromuscular residual después de la administración de neostigmina o sugammadex en dos contracciones visibles durante la monitorización del tren de cuatro. Anestesia y analgesia , 112 (1), 63-68. 2011 Jan;112(1):63-8. Epub 2010 Oct 26 (PubMed) Disponible en: https://anestesiar.org/2011/bloqueo-neuromuscular-residual-tras-administracion-de-rocuronio-comparacion-sugammadex-neostigmina/
- Celis-Rodríguez, E., Birchenall, C., de la Cal, M. Á., Arellano, G. C., Hernández, A., Ceraso, D., & Rubiano, S. (2013). Guía de práctica clínica basada en la evidencia para el manejo de la sedoanalgesia en el paciente adulto críticamente enfermo. Medicina intensiva, 37(8),519-574Disponible en:https://www.medintensiva.org/es-pdf-S0210569113000855
- Sánchez, S. S., Vivas, A. M., Obregón, J. S., Ortega, M. R., Jambrina, C. C., Marco, I. L. T., & Jorge, E. C. (2009). Monitorización de la sedación profunda. El monitor BIS®. Enfermería intensiva, 20(4), 159-166.
- Sandiumenge, A. (2008). coordinador. Sedación, analgesia y bloqueo neuromuscular en el paciente crítico. Recomendaciones del Grupo de Trabajo de Analgesia y Sedación de la SEMICYUC. Med Intensiva, 32, 1-124.sedación, analgesia y bloqueo neuromuscular en el paciente crítico. Recomendaciones del Grupo de Trabajo de Analgesia y Sedación de la SEMICYUC Disponible en: https://www.medintensiva.org/es-vol-32-num-s1-sumario-X0210569108X60502
- Giustino V., Magdi Hanna, Giorgos Macheras et al. Analgesia multimodal en el dolor moderado a intenso: utilidad de una nueva combinación de dosis fijas de dexketoprofeno y tramadol. CMRO.2017.1:1-2
- Bermúdez-Guerrero, F. J., Gómez-Camargo, D., Palomino-Romero, R., Llamas-Bustos, W., & Ramos-Clason, E. (2015). Comparación de 3 pautas de sedación para pacientes sometidos a anestesia subaracnoidea. Ensayo clínico aleatorizado, simple ciego. Revista Colombiana de Anestesiología, 43(2), 122-128.
- Echeverry P, Jaramillo J. Sedación en anestesia regional [consultado 13 Abr 2018]. Disponible en: http://www.anestesiaweb2.com/archivos/sedacion.pdf
- Oseguera Oyuela, E. J. (2021). Errores comunes en la medicación (Doctoral dissertation, Granada, España).
- Guías para el etiquetado de medicamentos prescritos 2001 [Available from: https://www.fip.org/www/uploads/database_file.php?id=259&table_id=.
- Borges, A. L., Vázquez, P., FERNÁNDEZ, L. J., TANDRÓN, J. M. C., AGUILAR, H. A., RODRÍGUEZ, B. Y. B., & GARCÍA, L. M. M. (2002). Interacciones medicamentosas. Acta Farm. Bonaerense, 21(2), 139-148. Disponible: https://www.sefh.es/bibliotecavirtual/fhtomo1/cap214.pdf
- Gómez-Arnau, J. I., Otero, M. J., Bartolomé, A., Errando, C. L., Arnal, D., Moreno, A. M. & Domínguez-Gil, A. (2011). Etiquetado de los medicamentos inyectables que se administran en anestesia. Revista Española de Anestesiología y Reanimación, 58(6), 375-383.
- Anestesia SEdNeSe. Recomendaciones para el etiquetado de los medicamentos inyectables que se administran en anestesia 2011 [Available from: http://www.ismpespana.org/ficheros/Recomendaciones%20ETIQUETADO%20Enero%202011.pdf.
- Lao, G. C., Reyes, M. R., Turet, J. R., Dot, M. P., Muner, D. S., & Cabezas, C. L. (2020). Compatibilidad de los fármacos administrados en «Y» en las unidades de cuidados intensivos: revisión sistemática. Medicina Intensiva, 44(2), 80-87.
- Ramos, G., & Olivares, G. (2010). Uso racional de medicamentos: Una tarea de todos. División de políticas públicas saludables y promoción. Dpto. De Políticas Farmacéuticas Y Profesiones Médicas. Chile.
- Uso racional de medicamentos; una tarea de todos. Contenidos e información del uso racional para el personal técnico de la salud. https://www.minsal.cl/portal/url/item/8da19e5eac7b8164e04001011e012993.pdf
- Merino, P., Martín, M. C., Alonso, A., Gutiérrez, I., Álvarez, J., & Becerril, F. (2013). Errores de medicación en los servicios de Medicina Intensiva españoles. Medicina Intensiva, 37(6), 391-399.
- Oseguera Oyuela, E. J. (2021). Errores comunes en la medicación (Doctoral dissertation, Granada, España).
- Prevención de errores por confusión en los nombres de los medicamentos [Available from: http://www.ismp-espana.org/documentos/view/63.
- http://www.juntadeandalucia.es/agenciadecalidadsanitaria/observatorioseguridadpaciente/gestor/sites/PortalObservatorio/usosegurodemedicamentos/documentos/GPS_SIMILI. Portal uso seguro del medicamento.
- Barbagelata, E. I. (2016). Implementación de estrategias de prevención de errores en el proceso de administración de medicamentos: un enfoque para enfermería en cuidados intensivos. Revista Médica Clínica Las Condes, 27(5), 594-604.
- Ibarra, P., Galindo, M., Molano, A., Niño, C., Rubiano, A., Echeverry, P., & Sarmiento, R. (2012). Recomendaciones para la sedación y la analgesia por médicos no anestesiólogos y odontólogos de pacientes mayores de 12 años. Revista Colombiana de Anestesiología, 40(1), 67-74.
- Sakata, R. K. (2010). Analgesia y sedación en unidad de cuidados intensivos. Rev Bras Anestesiol, 60(6), 360-365.
- Palanca, I., Sánchez, A., & Elola, J. (2010). Unidad de cuidados intensivos: Estándares y recomendaciones. Ministerio de Sanidad y Política Social: Madrid, Spain.
- McGrane, S. y Pandharipande, PP (2012). Sedación en la unidad de cuidados intensivos. Minerva anestesióloga , 78 (3), 369-380.
- Martínez S.A., Cacho A.E. Monitorización de la Sedación en UCI. SEDAR.2018.
- Antuña MT, Fanjul RM. Sedoanalgesia en el Paciente Crítico; [Internet]. [citado 2018Abr20];Disponible: http://www.uninet.edu/cimc2000/conferencia/conf2/SED_ANALGESIA.htm
- Fernández V, Mora R, Sánchez MJ. Manual de Anestesia para procedimientos fuera de quirófano. Internet Medical Publishing. 2013; 106-114.
- Taboada, R. (2012). Sedación paliativa (parte I): Controversias sobre términos, definiciones y aplicaciones clínicas. Acta bioética, 18(2), 155-162.
- Carrilero López, C., & Tornero Sánchez, L. Desarrollo e implementación de un protocolo de sedación, analgesiaycontroldedelirioenUCI.2014Disponibleen:https://www.chospab.es/publicaciones/protocolosEnfermeria/documentos/9501e1fd429a179d533dce134799079b.pdf
- Mamani Aguilar, J. H. (2017). REMIFENTANILO-PROPOFOL VS KETAMINA, MEPERIDINA, MIDAZOLAM EN COLANGIOPANCREATOGRAFIA RETROGRADA ENDOSCOPICA BAJO SEDACION EN HOSPITAL OBRERO 2 (Doctoral dissertation, Residencia Medica-Anestesiología; RM. A.-001/17).
- Nevot, M. J. V. (2015). Evaluación del cumplimiento de un protocolo de prevención de Neumonía asociada a Ventilación mecánica en una UCI polivalente. Enfermería global, 14(2), 102-117. Disponible:http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S1695-61412015000200005&lng=es.
- Folco, C. P., & da Cruz, I. C. F. (2016). Lung injury associated with mechanical ventilator: systematic literature review for a clinical protocol. Journal of Specialized Nursing Care, 8(1).
- Del Prado Olmedo BM, Muñoz RAM. Cuidados de enfermería del paciente crítico: uso de escalas de sedoanelgesia. Rev Paraninfo [Internet]. 2013 Dic [citado 2018 Abr 13]; 18(2): 155-162. Disponible en: http://www.index-f.com/para/n19/135d.php
- Raurell Torredà, M., Burgos Cordón, A., Conejo Caravaca, A., & Corcuera Pastor, I. (2015). Evaluación de la sedación mediante la escala Richmond Agitation Sedation Scale en pacientes con ventilación mecánica de larga duración. Rev. Rol enferm, 533-538.
- Chamorro C., Romera M.A.Dolor y miedo en la UCI. Medicina Intensiva.2015.39(7):442-444.
- Celis, E., Salazar, F. V., Marrugo, V. T., Ortiz, G., & Dueñas, C. (2017). Revisión comparativa de las guías de sedación, analgesia y delirio en pacientes críticos. Acta Colombiana de Cuidado Intensivo, 17(2), 107-116.
- Robinson, B. R., Berube, M., Barr, J., Riker, R., & Gélinas, C. (2013). Psychometric analysis of subjective sedation scales in critically ill adults. Critical care medicine, 41(9), S16-S29. doi: 10.1097/CCM.0b013e3182a16879. Review. PubMed PMID:23989092.
- Mera, M. F., Solanas, M. C., Pinilla, M. D. C. V., Izquierdo, J. S., & López, E. A. (2014). ¿ Qué papel tiene enfermería en la valoración y manejo de la analgesia, sedación y delirio del paciente crítico con ventilación mecánica? Evidencia: Revista de enfermería basada en la evidencia, 11(47), 4. Disponible en: http://www.index-f.com/evidentia/n47-48/ev9246.php.
- Celis-Rodríguez, E., Birchenall, C., de la Cal, M. Á., Arellano, G. C., Hernández, A., Ceraso, D., & Rubiano, S. (2013). Guía de práctica clínica basada en la evidencia para el manejo de la sedoanalgesia en el paciente adulto críticamente enfermo. Medicina intensiva, 37(8), 519-574. Disponible: http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S0210-56912007000800003&lng=es.
- Gallardo-Hernández, A. G., Hernández-Pérez, A. L., Sánchez-López, J. A., Ordoñez-Espinosa, G., Islas-Andrade, S., & Revilla-Monsalve, C. (2016). Monitores de profundidad anestésica. Revista Mexicana de Anestesiología, 39(3), 201-204.
- PAPEL DE LA ENFERMERÍA EN LA SEDOANALGESIA DEL PACIENTE CRÍTICO, NPunto Volumen II. Número 16. Julio 2019 disponible: https://imotions.com/blog/wayt-is-egg/
- Herrera, J. G. D., Larios, C. G. S., & Carrillo, L. G. D. (2016). Prevalencia de dolorpostquirúrgico. Acta Médica Grupo Ángeles, 14(2), 84-89.
- Rosa-Díaz, J., Navarrete-Zuazo, V., & Díaz-Mendiondo, M. (2014). Aspectos básicos del dolor postoperatorio y la analgesia multimodal preventiva. Revista Mexicana de Anestesiología, 37(1), 18-26.
- Secretaria de Salud GdH. Guia "Uso seguro de medicamentos" [Available from: http://www.salud.gob.hn/doc/calidad/guiausosegurodelosmedicamentos.pdf. TUD_VALORADA.pdf.
- Sistema Nacional de Salud E. Sistema Español de Verificación de Medicamentos 2016[Available:https://www.aemps.gob.es/en/laAEMPS/eventos/industria/2016/docs/J-infodispositivos-seguridad/4-urzay.pdf
- Martín de Rosales Cabrera, A. M., López Cabezas, C., & García Salom, P. (2014). Diseño de una matriz de riesgo para la valoración de los preparados estériles en los centros sanitarios. Farmacia Hospitalaria, 38(3), 202-210.
- Pazos, A. (2003). Acciones de los fármacos I. Interacciones fármaco y receptor. Farmacología Humana, 4ª ed. Barcelona. Masson, 7-17.
- Florez J. Farmacología humana. Acciones de los fármacos I. Interacciones fármaco y receptor. 6ªEd. Barcelona: Elsevier 2013.
- Lorente del Río N. Montero Arroyo R, Martinez Trufero G, Manjón Fernández S et al. Acceso EIR: Conceptos fundamentales para la práctica enfermera Volumen 2. 7ª ed. Madrid: ENFO ediciones para FUDEN; 2015 p 207-340.
- De Gracia, M. M., Sánchez, A. A., & Cachá, A. A. (2015). Aplicabilidad y uso de los fármacos en el proceso de cuidados. In Prescripción enfermera en la terapéutica del cuidado: indicación, uso y dispensación de medicamentos y productos sanitarios en los cuidados generales (pp. 471-606). Enfo Ediciones.
- Compatibilidad de fármacosporvíaparenteraldisponible:https://www.cofb.org/c/document_library/get_file?uuid=fe601fcf-e69f-4b04-80c4-19d31def3da4&groupId=10136.En la pág. 54 encontrareis la página de la compatibilidades de los fármacos a color.
- Instituto para el Uso Seguro de los Medicamentos de España (ISMP) http://www.ismp-espana.org/noticias/view/124
- Oseguera Oyuela, E. J. (2021). Errores comunes en la medicación (Doctoral dissertation, Granada, España).
- Ojeda Vásquez, L. A. (2019). Detección, evaluación y caracterización de reacciones adversas a medicamentos y errores de medicación en la agencia privada step-therapy. Disponible en:https://www.sefh.es/bibliotecavirtual/fhtomo1/cap214.pdf
- Vásquez, L. A. O. (2019). Detección, Evaluación y Caracterización de Reacciones Adversas a Medicamentos y Errores de Medicación en la Agencia Privada Step-Therapy (Doctoral dissertation, Pontificia Universidad Católica de Chile (Chile).
- M.J.Otero R. Martín, M. D. Robles, C. Codina. Errores de medicación. Disponible en:https://www.sefh.es/bibliotecavirtual/fhtomo1/cap214.pdf
- Van de Beek, D., de Gans, J., Tunkel, A. R., & Wijdicks, E. F. (2006). Community-acquired bacterial meningitis in adults. New England Journal of Medicine, 354(1), 44-53.
- Durand, M. L., Calderwood, S. B., Weber, D. J., Miller, S. I., Southwick, F. S., Caviness Jr, V. S., & Swartz, M. N. (1993). Acute bacterial meningitis in adults--A review of 493 episodes. New England Journal of Medicine, 328(1), 21-28.
- Quagliarello, V. J., & Scheld, W. M. (1997). Treatment of bacterial meningitis. New England Journal of Medicine, 336(10), 708-716.
- Neurosurgery Working Party of the British Society for Antimicrobial Chemotherapy. Br 2000; 14:7. - NEJM 339: 868, 1998
- Manes, G., Uomo, I., Menchise, A., Rabitti, P. G., Ferrara, E. C., & Uomo, G. (2006). Timing of Antibiotic Prophylaxis in Acute Pancreatitis: A Controlled Randomized Study with Meropenem: CME. American Journal of Gastroenterology, 101(6), 1348-1353.
- Pederzoli, P., Bassi, C., Vesentini, S., & Campedelli, A. (1993). A randomized multicenter clinical trial of antibiotic prophylaxis of septic complications in acute necrotizing pancreatitis with imipenem. Surgery, gynecology & obstetrics, 176(5), 480-483.
- Brown, J. de Louvois, R. Bayston, P. D Lees, IK Pople, E. M. (2000). The management of neurosurgical patients with postoperative bacterial or aseptic meningitis or external ventricular drain-associated ventriculitis. British journal of neurosurgery, 14(1), 7-12.
- Dellinger, E. P., Tellado, J. M., Soto, N. E., Ashley, S. W., Barie, P. S., Dugernier, T.,& Utzolino, S. (2007). Early antibiotic treatment for severe acute necrotizing pancreatitis: a randomized, double-blind, placebo-controlled study. Annals of surgery, 245(5), 674.
- Isenmann, R, Runzi, M, Kron, M, et al. Prophylactic antibiotic treatment in patients with predicted severe acute pancreatitis: A placebo-controlled, double-blind trial. Gastroenterology 2004; 126:997.
- Namias, N., Solomkin, JS, Jensen, EH, Tomassini, JE y Abramson, MA (2007). Estudio aleatorizado, multicéntrico, doble ciego de eficacia, seguridad y tolerabilidad de ertapenem intravenoso versus piperacilina / tazobactam en el tratamiento de infecciones intraabdominales complicadas en adultos hospitalizados. Infecciones quirúrgicas ,8 (1), 15-28.
- Tellado, J. M., Sitges-Serra, A., Barcenilla, F., Palomar, M., Serrano, R., Barberán, J., ... & Prieto, J. (2005). Guidelines for the empirical antibiotic treatment of intraabdominal infections. Revista española de quimioterapia: publicación oficial de la Sociedad Española de Quimioterapia, 18(2), 179-186.
- De Cuidados, I. D. L. S., & de la SEDAR, C. GUÍAS DEL TRATAMIENTO ANTIBIÓTICO DE LAS PERITONITIS.
- Balter, MS, La Forge, J., Low, DE, Mandell, L., Grossman, RF y Grupo de trabajo de bronquitis crónica. (2003). Directrices canadienses para el tratamiento de las exacerbaciones agudas de la bronquitis crónica. Revista respiratoria canadiense , 10 (Suppl B), 3B-32B.
- Wilson, R., Jones, P., Schaberg, T., Arvis, P., Duprat-Lomon, I., & Sagnier, P. P. (2006). Antibiotic treatment and factors influencing short- and long-term outcomes of acute exacerbations of chronic bronchitis. Thorax, 61(4), 337-342.
- Snow, V., Lascher, S., & Mottur-Pilson, C. (2001). Evidence base for management of acute exacerbations of chronic obstructive pulmonary disease. Annals of internal medicine, 134(7), 595-599.
- Dimopoulos, G., Siempos, I. I., Korbila, I. P., Manta, K. G., & Falagas, M. E. (2007). Comparison of first line with second-line antibiotics for acute exacerbations of chronic bronchitis: a metanalysis of randomized controlled trials. Chest, 132(2), 447-455.
- Siempos, I. I., Dimopoulos, G., Korbila, I. P., Manta, K., & Falagas, M. E. (2007). Macrolides, quinolones and amoxicillin/clavulanate for chronic bronchitis: a meta-analysis. European Respiratory Journal, 29(6), 1127-1137.
- American Thoracic Society, & Infectious Diseases Society of America. (2005). Guidelines for the management of adults with hospital-acquired, ventilator-associated, and healthcare-associated pneumonia. American journal of respiratory and critical care medicine, 171(4), 388.
- Aarts, M. A. W., Hancock, J. N., Heyland, D., McLeod, R. S., & Marshall, J. C. (2008). Empiric antibiotic therapy for suspected ventilator-associated pneumonia: a systematic review and meta-analysis of randomized trials. Critical care medicine, 36(1), 108-117.
- Heyland, D. K., Dodek, P., Muscedere, J., Day, A., Cook, D., & Canadian Critical Care Trials Group. (2008). Randomized trial of combination versus monotherapy for the empiric treatment of suspected ventilator-associated pneumonia. Critical care medicine, 36(3), 737-744.
- Wolfe, J. E., Bone, R. C., & Ruth, W. E. (1977). Effects of corticosteroids in the treatment of patients with gastric aspiration. The American journal of medicine, 63(5), 719-722.
- Kadowaki, M., De mura, Y., Mizuno, S., Uesaka, D., Ameshima, S., Miyamori, I., & Ishizaki, T. (2005). Reappraisal of clindamycin IV monotherapy for treatment of mild-to-moderate aspiration pneumonia in elderly patients. Chest, 127(4), 1276-1282.
- Watkins, RR y Lemonovich, TL (2011). Diagnóstico y tratamiento de la neumonía adquirida en la comunidad en adultos. Médico de familia estadounidense, 83 (11), 1299-1306.
- Lim, W. S., Baudouin, S. V., George, R. C., Hill, A. T., Jamieson, C., Le Jeune, I., & Woodhead, M. A. (2009). BTS guidelines for the management of community acquired pneumonia in adults: update 2009. Thorax, 64(Suppl 3), 1-55.
- Mandell, LA, Marrie, TJ, Grossman, RF, Chow, AW, Hyland, RH y el grupo de trabajo de neumonía adquirida en la comunidad canadiense. (2000). Directrices canadienses para el tratamiento inicial de la neumonía adquirida en la comunidad: una actualización basada en la evidencia de la Sociedad Canadiense de Enfermedades Infecciosas y la Sociedad Torácica Canadiense. Enfermedades infecciosas clínicas, 31 (2), 383-421.
- Rubinstein, E., Kollef, M. H., & Nathwani, D. (2008). Pneumonia caused by methicillin-resistant Staphylococcus aureus. Clinical Infectious Diseases, 46(Supplement_5), S378-S385.
- Rodríguez, A., Mendia, A., Sirvent, J. M., Barcenilla, F., de la Torre-Prados, M. V., Solé-Violán, J.,& CAPUCI Study Group. (2007). Combination antibiotic therapy improves survival in patients with community-acquired pneumonia and shock. Critical care medicine, 35(6), 1493-1498.
- Gaspar Carreño, M., Achau Muñoz, R., Torrico Martín, F., Agún González, J. J., Sánchez Santos, J. C., Cercos Lletí, A. C., & Ramos Orozco, P. (2017). Desarrollo de un procedimiento para el manejo seguro de medicamentos peligrosos. Farmacia Hospitalaria, 41(2), 222-256.
- Unda-Urzáiz, M., Alonso-Herreros, J. M., Fernández-Gómez, J. M., Gaspar-Carreño, M., Cozar-Olmos, J. M., & Lleti, A. C. C. Preparación de medicamentos peligrosos HOSPITALARIA.
- Guía de buenas prácticas de preparación de medicamentos en servicios de farmacia hospitalaria. Dirección General de Cartera Básica de Servicios del SNS y Farmacia. Junio 2014.
- Instituto Nacional de Seguridad e Higiene en el Trabajo (INSST). NTP 612: Protección y promoción de la salud reproductiva: funciones del personal sanitario del servicio de prevención.INSHT.2004.Disponible en:http://www.insht.es/InshtWeb/Contenidos/Documentacion/Fichas-tecnicas/NTP/Ficheros/601a700/ ntp_612.pdf
- Instituto Nacional de Seguridad e Higiene en el Trabajo (INSST). NTP 915: Embarazo, lactancia y trabajo: Vigilancia de la salud. INSHT. 2011. Disponible en: http://www.insht.es/InshtWeb/Contenidos/
- MSSSI Guía de buenas prácticas de preparación de medicamentos en los servicios de Farmacia Hospitalaria. Ministerio de Sanidad, Servicios Sociales e Igualdad.Junio2014. http://www.msssi.gob.es/profesionales/farmacia/pdf/GuiaBPP3.pdf
- AMMTAS Guía de buenas prácticas para trabajadores profesionalmente expuestos a agentes citostáticos. Asociación Madrileña de Medicina del Trabajo en el Ámbito Sanitario (AMMTAS). Escuela Nacional de Medicina del Trabajo. Instituto de Salud Carlos III. Ministerio de Economía y Competitividad. Madrid, 2014.http://gesdoc.isciii.es/gesdoccontroller?action=download &id=26/03/2014-199edf956b
- National Institute for Health and Care Excellence. Intravenous fluid therapy. Intravenous fluid therapy in adults in hospital.Disponible en: https://www.nice.org.uk/guidance/cg1742015(Guideline Ref ID 38 CG174).
- Corcoran, T., Rhodes, JEJ, Clarke, S., Myles, PS y Ho, KM (2012). Estrategias perioperatorias de manejo de líquidos en cirugía mayor: un metaanálisis estratificado. Anestesia y analgesia , 114 (3), 640-651.
- Cecconi, M., Corredor, C., Arulkumaran, N., Abuella, G., Ball, J., Grounds, RM, y Rhodes, A. (2013). Revisión clínica: terapia dirigida por objetivos: ¿cuál es la evidencia en pacientes quirúrgicos? El efecto en diferentes grupos de riesgo. Cuidados intensivos , 17 (2), 1-15.
- Arnal, D., Bernardino, M., León, J. A., Velayos, C., Gómez, J. C., & Gilarranz, J. L. (1998). Atención por intoxicación etílica en un Servicio de Emergencia Médica prehospitalario en Madrid. Emergencias, 10, 381-7.
- Norberto Gamero, M. J., Martínez Álvarez, M., Postigo Mota, S., & Llerena Ruiz, A. (2000). Intoxicación por insecticidas organofosforados. Epidemiología y prevención. Rev. Rol enferm, 847-854.
- Larsen, L. C., & Cummings, D. M. (1998). Oral poisonings: guidelines for initial evaluation and treatment. American family physician, 57(1), 85.
- Nogué, S., Munné, P., SOYA, D., & Millá, J. (1998). Disponibilidad, utilización y coste de los antídotos en Cataluña. Medicina clínica, 110(16), 609-613.
- Ries, NL y Dart, RC (2005). Nuevos desarrollos en antídotos. Clínicas médicas , 89 (6), 1379-1397.
- Locatelli, C., Petrolini, V., Lonati, D., Butera, R., Bove, A., Mela, L., & Manzo, L. (2006). Disponibilità di antidoti nei servizi d’urgenza del Sistema Sanitario Nazionale e realizzazione della Banca Dati Nazionale degli Antidoti (BaNdA). Ann Ist Super Sanita, 42(3), 298-309.
- OMS, P. (1998). OIT: Directrices para la lucha contra las intoxicaciones. Programa internacional de seguridad de las sustancias químicas. Ginebra.
- Piñeiro G, Olivera R y Guindel C. Administración de medicamentos en pacientes con nutrición enteral mediante sonda. Nutr Hosp 2006; 21 (Supl. 4): 1-218.
- Gago A, Garzás MC, Calañas A y Molina MJ. Guía de administración de fármacos por sonda nasogástrica. Soporte CD-ROM 2005.
- Izco N, Creus N, Codina C y Ribas J. Incompatibilidades fármaco-nutrición enteral: recomendaciones generales para su prevención. Farm Hosp 2001; 25(1): 13-24.
- Gámez M, Clopés A, y cols. Importancia de las características físico-químicas de los fármacos para su administración por sonda nasoentérica o enterostomía. Farma Hosp. 1998; 22(3): 137-143.
- Hidalgo FJ, Delgado E, García D y cols. Guía de administración de fármacos por sonda nasogástrica. Farm Hosp. 1995; 19 (5): 251-258.
- Luna T, Sorní I, Goyache M y cols. Técnica para la administración de medicamentos por sonda nasogástrica. Farm hosp 1998; 22 (5) : 257-260.
- Goñi R, Sánchez L, baztán A y Asiain MC. Administración de fármacos por sonda digestiva. Enferm Intensiva 2001; 12 (2): 66-79.
- Organización Mundial de la Salud (OMS). Directrices para la lucha contra las intoxicaciones. Ginebra, 1998. p.57-67.
- Tenenbein M. Recent advancements in pediatric toxicology. Ped Clin North Am 1999; 46:1179-88.
- Ward RM, Bates BA, Benitz WE, Burchfield DJ, Ring JC, Wals RP, et al. Acetaminophen toxicity in children. Pediatrics 2001;108:1020-4.
- Munné P, Nogué S, Millá J. Antídotos ¿Cuándo y cómo utilizarlos? Edicomplet 1996:137-50. Disponible en: http://66.102.11.104/search.
- Noorkool, DM, Kirkpatrick, JN. Treatment of acute carbon monoxide poisoning with hyperbaric oxigen: a review of 115 cases. Ann. Emerg. Med. 1985; 14, 1168-1171
- Clinical Toxicologic Working Group of the Spanish Society of Pediatric Emergency Medicine Emergency Visits for Childhood 53 Área Sanitaria Ferrol Anexo: Antídotos e intoxicaciones en Atención Primari Poisoning: A 2-Year Prospective Multicenter Survey in Spain. Pediatric Emerg Care. 2006; 22:334-8. [Medline]
- Burillo-Putze G, Munne P, Dueñas A, Pinillos MA, Naveiro JM, Cobo J, et al. National multicenter study of acute intoxication in emergency departments of Spain. Eur J Emerg Med. 2003; 10:101 4. [Medline]
- American College of Emergency Physicians. Clinical policy for the initial approach to patients presenting with acute toxic ingestion or dermal or inhalation exposure. Ann Emerg Med. 1995; 25:570-85. [Medline]
- Riordan M, Rylance G, Berry K. Poisoning in children 1: general management. Arch Dis Child. 2002; 87:392-6. [Medline]
- Grupo de trabajo de intoxicaciones de la Sociedad Española de Urgencias de Pediatría Manual de intoxicaciones en Pediatría. Disponible en:http://www.seup.org/seup/grupos_trabajo/manualIntoxicaciones/manual_index.htm
- Belson MG, Simon HK. Utility of comprehensive toxicologic screens in children. Am J Emerg Med. 1999; 17:221-4. [Medline]
Shannon M. Ingestion of toxic substances by children. N Engl J Med. 2000; 342:186-91. [Medline]
- Wax PM, Cobaugh DJ. Prehospital gastrointestinal decontamination of toxic ingestions: a missed opportunity. Am J Emerg Med. 1998; 16:114-6. [Medline]
- Bond GR. The role of activated charcoal and gastric emptying in gastrointestinal decontamination: a state-of-the-art review. Ann Emerg Med. 2002; 39:273-86. [Medline]
- Kalil, AC, Metersky, ML, Klompas, M., Muscedere, J., Sweeney, DA, Palmer, LB, y Brozek, JL (2016). Manejo de adultos con neumonía adquirida en el hospital y asociada al respirador: guías de práctica clínica de 2016 de la Infectious Diseases Society of America y la American Thoracic Society. Enfermedades infecciosas clínicas, 63 (5), e61-e111.
- Torres, A., Niederman, M. S., Chastre, J., Ewig, S., Fernandez-Vandellos, P., Hanberger, H.& Wunderink, R. (2017). International ERS/ESICM/ESCMID/ALAT guidelines for the management of hospital-acquired pneumonia and ventilator-associated pneumonia: guidelines for the management of hospital-acquired pneumonia (HAP)/ventilator-associated pneumonia (VAP) of the European Respiratory Society (ERS), European Society of Intensive Care Medicine (ESICM), European Society of Clinical Microbiology and Infectious Diseases (ESCMID) and Asociación Latino Americana del Tórax (ALAT). European Respiratory Journal, 50(3).
- De la SEPAR, G. D. T. (2010). Neumonía adquirida en la comunidad. Nueva normativa de la Sociedad Española de Neumología y Cirugía Torácica. Arch Bronconeumol, 46(10), 543-558.
- Blanquer, J., Aspa, J., Anzueto, A., Ferrer, M., Gallego, M., Rajas, O., & Torres, A. (2011). Normativa SEPAR: neumonía nosocomial. Archivos de Bronconeumología, 47(10), 510-520.
- Barr, J., Fraser, G. L., Puntillo, K., Ely, E. W., Gélinas, C., Dasta, J. F., & Jaeschke, R. (2013). Clinical practice guidelines for the management of pain, agitation, and delirium in adult patients in the intensive care unit. Critical care medicine, 41(1), 263-306.
- Greenberg, S. B., & Vender, J. (2013). The use of neuromuscular blocking agents in the ICU: where are we now? Critical care medicine, 41(5), 1332-1344.
- Hunter, J. M., & Naguib, M. (2018). Sugammadex-induced bradycardia and asystole: how great is the risk? British journal of anaesthesia, 121(1), 8-12.
- Ortega, M. R., Jambrina, C. C., Vallhonrat, I. L., & Simón, I. F. (2014). Indications of dexmedetomidine in the current sedoanalgesia trends in the critical patient. Medicina Intensiva (English Edition), 38(1), 41-48.
- Clarett, M. (2012). Escalas de evaluación de dolor y protocolo de analgesia en terapia intensiva. Clínica y Maternidad Suizo Argentina Instituto Argentino Diagnóstico y Tratamiento.
- Torres, A., Niederman, M. S., Chastre, J., Ewig, S., Fernandez-Vandellos, P., Hanberger, H.& Wunderink, R. (2017). International ERS/ESICM/ESCMID/ALAT guidelines for the management of hospital-acquired pneumonia and ventilator-associated pneumonia: guidelines for the management of hospital-acquired pneumonia (HAP)/ventilator-associated pneumonia (VAP) of the European Respiratory Society (ERS), European Society of Intensive Care Medicine (ESICM), European Society of Clinical Microbiology and Infectious Diseases (ESCMID) and Asociación Latino Americana del Tórax (ALAT). European Respiratory Journal, 50(3).
- Barr, J., Fraser, G. L., Puntillo, K., Ely, E. W., Gélinas, C., Dasta, J. F.,& Jaeschke, R. (2013). Clinical practice guidelines for the management of pain, agitation, and delirium in adult patients in the intensive care unit. Critical care medicine, 41(1), 263-306.
- Greenberg, S. B., & Vender, J. (2013). The use of neuromuscular blocking agents in the ICU: where are we now? Critical care medicine, 41(5), 1332-1344.
- Hunter, J. M., & Naguib, M. (2018). Sugammadex-induced bradycardia and asystole: how great is the risk? British journal of anaesthesia, 121(1), 8-12.
- Romera MA et al. Indications of dexmedetomidina in the current sedoanalgesia trenes in the critical patient. Med Intensiva 2014;38(1):41-48.
- Alfonso J, Reis F. Dexmedetomidina: papel actual em anestesia en cuidados intensivos. Rev Bras Anestesiol. 2012;62(1).
- Atención M, Enfermería D. Experto Universitario en Cuidados Críticos y Reanimación. :1–13.
- Ateneo E El. Drogas vasoactivas en el paciente crítico. Med Intensiva. 2006;(2001).
- Langlois PL, Oliveira Figliolino LF de, Hardy G, Manzanares W. Farmaconutrición parenteral con selenio en la sepsis TT - Pharmaconutrition with parenteral selenium in sepsis. Med intensiva (Madr, Ed impr). 2014;38(3).
- Sylvia Mónica Amorós Cerdá A, Maqueda Palau M, Ribas Nicolau B, Arévalo Rubert MJ, Pérez Juan E. ADMINISTRACIÓN COMPATIBLE DE LA TERAPIA INTRAVENOSA CONTINUA EN EL PACIENTE CORONARIO CRÍTICO. Enferm Cardiol Año XX. 2013;
- Buil Lavilla P, Blanco García C. Errores De Medicación. Farm Clin. 1993;10(5):393-394+396.
- López C, Soy D, Guerrero L, Molas G, Anglada H, Ribas J. Compatibilitat fisicoquímica de fàrmacs administrats en perfusió contínua en les unitats de cures intensives. Circ Farm. 2011;69(4):37–56.
- PROTOCOL SEDACIO. Hospital Universitario Sant Joan de Reus
- Barbagelata I. De Administración De Medicamentos : Process : an Approach for Intensive Care Nursing. 2017;27(5):594–604.
- Castells Lao G, Rodríguez Reyes M, Roura Turet J, Prat Dot M, Soy Muner D, López Cabezas C. Compatibilidad de los fármacos administrados en «Y» en las unidades de cuidados intensivos: revisión sistemática. Med Intensiva. 2020;44(2):80–7.
- Chiva ED. Nociones básicas sobre Sedoanalgesia. 2019;
- Corbalan Trumbull G. Reacciones adversas a los medicamentos antimicrobianos. Rev Med Chil. 1977;105(12):944.
- García Batlle C, Pla Poblador R. Revisión de interacciones farmacológicas en un hospital general. Farm Hosp. 2002;26(2):110–8.
- Gonzalo Ramos N, Guillermo Olivares J. Uso racional de medicamentos: una tarea de todos. Subsecr Salud Publica; Minist Salud. 2014;50.
- Jiménez L, Fernández J. Interacción Medicamentosa. Acta Farm Bonaer [Internet].2009;21(2):139–48. Available from: http://www.latamjpharm.org/trabajos/21/2/LAJOP_21_2_2_2_3B9FQZINM4.pdf
- Merino P, Martín MC, Alonso A, Gutiérrez I, Álvarez J, Becerril F. Errores de medicación en los servicios de Medicina Intensiva españoles. Med Intensiva. 2013;37(6):391–9.
- Sospecha CON, Confirmado OD. Ingresan a Unidades De Cuidados Intensivos Con Sospecha O De Covid-19. 2020;19.
- Tineo Drove T, Razola Rincón R, Jiménez Peña P, Barrajón Sánchez M. J. Analgesia convencional frente a analgesia controlada por el paciente. Nurs (Ed española). 2008;26(1):56
- Alcaide García J, Gutiérrez Calderón V, Benavides Orgaz M. Capítulo 2. Fármacos anticonvulsivantes. Guía SEOM Uso los fármacos antiepilépticos en Oncol. 2006;37–56.
- Atención M, Enfermería D. Experto Universitario en Cuidados Críticos y Reanimación. :1–13.
- F. VNMAF, N. MGA, C. AA. Drogas Administradas Por Infusión Continua En Pacientes críticos. 2001;1–10.
- Ferrol REAS. Antídotos En Intoxicaciones. :3–56.
- INTRAMED. Analgesia, Sedación Y Relajación En El Paciente Critico. Libro Virtual Intramed. 2006;(2001):1–38. Monroy AM. Farmacología Cardiovascular Isbn 978-84-16861-16-3-1.
- Narbona Toledo C, Narbona Toledo F. Enfermería en la monitorización del Índice Biespectral Bis. Enfermería Docente [Internet]. 2010;10–3. Available from: http://www.juntadeandalucia.es/servicioandaluzdesalud/huvvsites/default/files/revistas/ED-092-05.pdf
- Ruiz J, Blanch L, Martín MC, Blanco J, Castillo F, Roca J, et al. Indicadores de calidad en el enfermo crítico. Vol. 32, Medicina Intensiva. 2008. 23–32 p.
- Estomatológicos AP, Estomatológicos AAP. Grupo a – Tracto Alimentario Y Metabolismo. :4–6.
- Muñoz M, Montalván L, Pérez A, García A, Gómez A. Fluidoterapia intravenosa en urgencias y emergencias. Univ Málaga [Internet]. 2009;1–30. Available from: http://www.medynet.com/usuarios/jraguilar/Manual de urgencias y Emergencias/fluido.pdf
- Nogué Xarau S. INTOXICACIONES AGUDAS Bases para el tratamiento en un servicio de urgencias. 2010;534. Available from: http://www.fetoc.es/asistencia/Intoxicaciones Agudas Protocolos 2010.pdf
- www.vademecum.es
- www.cima.aemps.es/cima/publico/home.html
(agencia española del medicamento y de productos sanitarios)
