1. RECORD ANATÒMIC I FISIOLÒGIC DEL SISTEMA ENDOCRÍ
Es compon de tres elements per desenvolupar les seves funcions: glàndules, hormones i receptors.
Glàndules
Es tracta d'un grup de cèl·lules o òrgans especialitzats que produeixen, emmagatzemen i secreten hormones i transmissors químics cap al torrent sanguini, amb l'objectiu de regular les funcions de l'organisme.
El sistema endocrí està compost per les glàndules hipòfisi, tiroide, paratiroide, suprarenals, pineal, pàncrees, tim i les gònades (ovaris i testicles).
Hormones
Són substàncies químiques secretades generalment per les glàndules endocrines, podent provenir a més de teixits especialitzats com els que es troben en el ronyó, aparell digestiu i els leucòcits. Aquests compostos integren i regulen les funcions corporals, en coordinació amb el sistema nerviós, actuant en llocs diana locals o distants.
Des del punt de vista estructural, les hormones poden classificar-se en tres tipus:
- Amines i aminoàcids: deriven de la tirosina, un aminoàcid essencial que es troba en la majoria de les proteïnes. Dins d'aquest grup trobem les hormones tiroïdals (T3 i T4), produïdes per la glàndula tiroide i les catecolamines (adrenalina, noradrenalina i dopamina), produïdes a la medul·la de les glàndules suprarenals.
A través de la seva unió als llocs receptors en les parets cel·lulars permeten fer canvis ràpids dins de la cèl·lula.
- Pèptids, polipèptids, proteïnes i glucoproteïnes: són compostos proteics, formats per molts aminoàcids connectats per enllaços peptídics. Dins d'aquest grup trobem hormones hipofisàries anteriors (somatotropina, tirotropina, corticotropina, folitropina, lutropina, hormona estimulant dels melanòcits i prolactina), hormones hipofisàries posteriors (hormona antidiürètica / vasopressina i oxitocina), hormones produïdes per la paratiroide (hormona paratiroïdal) i hormones pancreàtiques (insulina i glucagó).
Es tracten de molècules més complexes que presenten una resposta més lenta.
- Esteroides: deriven del colesterol. Dins d'aquest grup trobem hormones adrenocorticals (aldosterona i cortisol), secretades per l'escorça de les glàndules suprarenals, a més d'hormones sexuals (estrògens, progesterona i testosterona) secretades per les gònades.
A causa de la seva menor grandària i alta solubilitat en lípids penetren en les membranes cel·lulars interactuant amb els receptors intracel·lulars. Requereixen diverses hores per fer el seu efecte.
L'alliberament de les hormones es produeix com a resultat de l'estimulació d'una glàndula endocrina, però podem trobar diferents patrons d'alliberament en funció de l'hormona, com són:
- Corticotropina i cortisol: s'alliberen en resposta als cicles del ritme corporal, en forma de descàrregues ràpides i irregulars, presentant concentracions màximes en les primeres hores del matí.
- Hormona paratiroïdal i prolactina: s'alliberen de manera uniforme durant el dia.
- Insulina: presenta dos patrons d'alliberament, estable i esporàdica, en funció de les concentracions de glucosa.
En un estat fisiològic, la concentració d'hormones en el torrent sanguini es manté dins d'uns valors relativament constants.
La regulació hormonal es produeix mitjançant un mecanisme complex de retroalimentació negativa, per evitar la seva acumulació. En funció de les concentracions hormonals s'envia informació (retroalimentació) a les glàndules endocrines per augmentar o disminuir la seva producció i alliberament, amb l'objectiu de mantenir l'equilibri de l'organisme.
Receptors
Quan una hormona arriba al lloc diana, s'uneix a un receptor específic situat a la membrana cel·lular (polipèptids i algunes amines) o dins de la cèl·lula (esteroides i hormones tiroïdals).
Els receptors són molècules de proteïna que, en resposta a aquests estímuls hormonals, desencadenen canvis fisiològics específics en les cèl·lules diana.
2. ALTERACIONS A LA HIPÒFISI
La glàndula hipòfisi o pituïtària es troba a la cadira turca, una formació òssia situada a la superfície de l'os esfenoide a la base del cervell. Està revestida per duramàter, es troba delimitada a la part superior pel quiasma òptic i en les seves regions laterals pels sens cavernosos (esquerre i dret). Es troba dividida en dos lòbuls: hipòfisi anterior (adenohipòfisi) i posterior (neurohipòfisi).
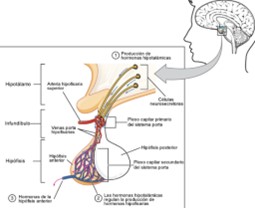
|
Il·lustració 5 Glàndula hipófisi Font: Wikimedia commons |
L’adenohipòfisi produeix les següents hormones:
- Prolactina (PRL)
- Hormona de creixement o somatotropina (GH)
- Corticotropina o corticotropina (ACTH)
- Hormona luteïnitzant o lutropina (LH)
- Hormona foliculoestimulant o folitropina (FSH)
- Hormona estimulant de la tiroide o tirotropina (TSH)
Aquestes hormones entren en la circulació general, sent transportades als seus òrgans diana.
La neurohipòfisi emmagatzema i allibera oxitocina i hormona antidiürètica o vasopressina (ADH), ambdues hormones sintetitzades a l'hipotàlem.
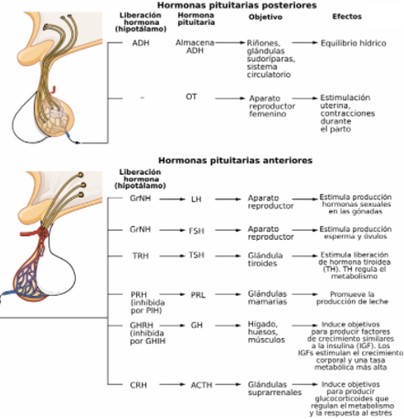
|
Il·lustració 6 Hormones hipofisàries Font: wikimedia commons |
Eix hipotàlem hipofisari
L'hipotàlem està situat a la base del crani, per sota del tàlem i per sobre del quiasma òptic i la glàndula hipofisària, amb la qual manté relacions tant anatòmiques com funcionals. Actua com a centre coordinador i integrador de múltiples funcions vitals entre les que es troben les relacionades amb el sistema endocrí (funció hipofisària).
La hipòfisi està connectada a l'hipotàlem per l'infundíbul o tija hipofisari, permetent rebre estímuls químics i nerviosos. D'una banda, l'hipotàlem connecta amb la neurohipòfisi a través de vies nervioses, podent estimular la secreció d'ADH i oxitocina. D'altra banda, regula les funcions de l'adenohipòfisi mitjançant altres hormones inhibidores i estimulants.
2.1. Hipopituïtarisme
L’hipopituïtarisme és la síndrome clínica causada per la deficiència total (panhipopituïtarisme) o parcial de les hormones produïdes en l'adenohipòfisi o emmagatzemades a la neurohipòfisi, conduint a l'aparició de patologies endocrines. Entre elles podem trobar: insuficiència suprarenal central, hipotiroïdisme secundari, hipogonadisme central, dèficit d'hormona de creixement i, amb menor freqüència, diabetis insípida.
Les causes més freqüents en persones adultes són els tumors hipofisaris, el tractament derivat dels mateixos (radiació cranial, cirurgia) i el dany cerebral secundari a un traumatisme cranioencefàlic. Però pot ser causat a més per:
- Infeccions: bacterianes, micòtiques, sífilis, tuberculosi, etc.
- Ús de fàrmacs: glucocorticoides, opiacis, anàlegs de la somatostatina, etc.
- Alteracions vasculars: infart hipofisari en el postpart (síndrome de Sheehan), hemorràgia subaracnoïdal, etc.
- Malalties infiltratives / inflamatòries: hipòfisi xantomatosa, hemocromatosi, etc.
- Malalties genètiques: hi ha diverses mutacions genètiques que participen en la cascada de diferenciació hipofisiària.
- Idiopàtica
- Altres: cadira turca buida.
L'aparició de deficiències hormonals sol seguir un patró seqüencial, amb un dèficit inicial d'hormona de creixement seguit de la disminució de gonadotropines, tirotropina i finalment corticotropina.
Manifestacions clíniques
Les manifestacions clíniques de l'hipopituïtarisme són variables i depenen de diversos factors, entre els quals es troben:
- L'etiologia
- El nombre i tipus d'eixos hormonals afectats i la seva intensitat
- L'edat d'aparició
- El temps d'instauració
Els pacients adults poden presentar signes o símptomes clínics relacionats amb els dèficits hormonals, com són:
- Dèficit d'ACTH (insuficiència suprarenal secundària): es tracta del dèficit més greu i pot produir compromís vital. Podem trobar signes i símptomes com: astènia, debilitat, hipoglucèmia, letargia, pèrdua de pes, anorèxia, nàusees, vòmits i diarrees.
- Dèficit de TSH (hipotiroïdisme central): presenta clínica similar a la de l'hipotiroïdisme primari com fatiga, debilitat, augment de la sensibilitat al fred, augment de pes, restrenyiment, sequedat a la pell, etc.
- Dèficit de LH i FSH (hipogonadisme hipogonadotropo): podem trobar en les dones amenorrea / oligomenorrea, disminució de la libido, sequedat vaginal, sufocacions i osteroporosis.
En el cas dels homes podem trobar disminució de la libido i impotència i en els dèficits de llarga durada caiguda del pèl corporal, disminució de la consistència testicular, manca important d'espermatozoides en el semen i ginecomàstia.
- Dèficit de GH: podem trobar deteriorament de la qualitat de vida, alteracions de la son, astènia, disminució de la massa magra i òssia, augment de la massa grassa, resistència a la insulina i dislipidèmia.
- Dèficit de prolactina: la manca de prolactina impossibilita la lactància.
- Dèficit d'hormona antidiürètica (diabetis insípida): trobarem poliúria hipotònica.
En el cas de l'hipopituïtarisme secundari a un tumor hipofisari, els pacients poden mostrar símptomes derivats de l’"efecte massa" del tumor com: cefalea (solen ser retroorbitàries), hipertensió intracranial, alteracions visuals per compressió de la via òptica (generalment hemianòpsia bitemporal), etc. Presentant a més clínica del dèficit de les cèl·lules hipofisiarias compromeses o clínica d'hipersecreció hormonal (com la hiperprolactinèmia) en el cas que el tumor sigui funcionant.
Diagnòstic
El diagnòstic de l'hipopituïtarisme es basa primerament en l’identificació del dèficit hormonal sospitat, a través d'un estudi hormonal basal o un estudi dinàmic mitjançant proves funcionals.
Posteriorment es realitzaran estudis d'imatge, sent la ressonància magnètica la tècnica d'elecció, per poder valorar l'anatomia de la hipòfisi i les estructures adjacents, amb l'objectiu de detectar alteracions. Podent precisar altres exploracions addicionals, en funció de la malaltia subjacent, com l'estudi oftalmològic en els tumors hipofisaris.
Tractament
El tractament substitutiu de l'hipopituïtarisme es basa en la reposició d'hormones dels òrgans diana.
És rellevant l'ordre de la substitució terapèutica en aquells casos en què existeixi un dèficit hormonal múltiple, sent el primer eix a substituir el corticòtrop, seguit del tiroïdal i posteriorment el gonadal i somatotropo. La reposició es realitzarà utilitzant els següents fàrmacs:
- Eix corticòtrop: en el cas de la insuficiència suprarenal central, el tractament substitutiu s'ha de fer amb glucocorticoides, sent la hidrocortisona el més utilitzat seguit de la prednisona i la dexametasona.
- Eix tiròtrop: en el cas de l'hipotiroïdisme central, el tractament substitutiu es realitza amb levotiroxina.
- Eix gonadal: en el cas de l'hipogonadisme central, el tractament substitutiu es realitzarà mitjançant l'ús de testosterona en homes i estrògens en dones.
- Eix somatòtrop: per al tractament del dèficit d'hormona de creixement s'utilitzarà GH.
En el cas dels tumors hipofisaris, en la gran majoria el tractament d'elecció és la cirurgia via transesfenoidal per a la seva resecció.
2.2. Tumors en la hipòfisi
Els tumors de la glàndula hipofisària, juntament amb altres tumors de la regió selar, representen el 15-25% de les neoplàsies intracranials. Tractant-se en la majoria dels casos d'adenomes hipofisaris (85-90%).
Els adenomes hipofisaris (AH) són tumors epitelials benignes. En funció de la seva grandària i característiques anatòmiques es classifiquen en: microadenomes ( 1 cm i 4 cm de diàmetre).
Clínicament es classifiquen en funcionants i no funcionants, depenent de si el tumor és o no secretor d'hormones hipofisàries amb capacitat de produir una síndrome endocrí específic.
Al voltant d'un terç dels AH són adenomes clínicament no funcionants. No mostren evidència clínica ni bioquímica d'excés hormonal, podent presentar però signes i símptomes relacionats amb l’"efecte massa", per afectació de les estructures veïnes, com són la cefalea o les alteracions neurooftalmològiques (com la disminució del camp visual per compressió del quiasma òptic), hiperprolactinèmia (per compressió de la tija hipofisari), a més d’hipopituarisme parcial o complet (per compressió de la pròpia hipòfisis).
Es classifiquen a més histopatológicament, en funció del contingut hormonal que presenten les cèl·lules tumorals, podent-se diferenciar:
- Adenomes secretors de prolactina (prolactinomes): és el tipus més freqüent d'AH, representant aproximadament el 80% dels adenomes funcionants i el 40-50% de tots els AH, i apareixen més freqüentment en dones.
Produeix hipogonadisme i infertilitat en ambdós sexes. Les dones poden presentar signes i símptomes com ara alteracions menstruals (oligoamenorrea) i galactorrea. I els homes, disminució de la libido, disfunció erèctil, oligoespermia, ginecomàstia i galactorrea.
- Adenomes secretors de GH (tumors eosinòfils): representen aproximadament el 20% dels AH. L'excés d'hormona de creixement produeix l'aparició de signes i símptomes de gegantisme (si es produeix a primerenca edat) o acromegàlia (si es produeix en l'edat adulta).
En el cas del gegantisme, les persones poden arribar a fer 2,4 metres d'alçada, sent gran en totes les seves proporcions, però amb debilitat.
En el cas de l'acromegàlia es produeix un creixement de les extremitats i teixits tous, podent trobar manifestacions clíniques, per afectació dels diferents òrgans, com ara: augment de la mida acral, sudoració profusa, hipertròfia ventricular, hipertensió, arítmies i insuficiència cardíaca, macroglòssia, apnees de la son i obstrucció aèria alta, diabetis mellitus i hipertrigliceridèmia, artropatia i osteoartitis, entre d'altres.
- Adenomes mixtos secretors de GH i prolactina: representen aproximadament el 8% dels AH. Els pacients que el pateixen presenten signes i símptomes d’acromegàlia i hiperprolactinemia.
- Adenomes secretors d'ACTH: representen aproximadament el 10-15% dels AH. Aquest tipus d'adenoma s'associa amb la síndrome de Cushing (descrit posteriorment en l'apartat d'alteracions en les glàndules suprarenals).
- Adenomes secretors de gonadotropines (FSH i LH): representen aproximadament el 20% dels AH. Es tracta d'adenomes clínicament no funcionants.
- Adenomes secretors de TSH: és el tipus d'AH menys freqüent, representant menys de l'1%.
- Carcinomes hipofisaris: són molt rars, representant <1% de totes les neoplàsies hipofisàries. La majoria són macroadenomes invasius hormonalment actius, que es defineixen per la presència de metàstasi a nivell cerebromedular o sistèmiques.
A més de l'ús de tractaments farmacològics i la radiació cranial, de manera individualitzada i en funció de les necessitats del pacient el tractament quirúrgic continua sent el tractament d'elecció en els casos de tumors no funcionants amb compromís visual, a més d'en els tumors funcionants, sent la via transesfenoidal l'abordatge d'elecció per la seva resecció.
Després de l'extirpació de la hipòfisis serà necessari iniciar tractament hormonal substitutiu, per suplir les funcions controlades per la glàndula i les seves hormones.
2.3. Diabetis insípida
L'hormona antidiürètica (ADH) o vasopressina se sintetitza en l'hipotàlem, emmagatzemant-se posteriorment a la hipòfisis posterior per al seu alliberament. La seva secreció és pulsativa i segueix un ritme circadià, trobant l'alliberament màxim durant la nit, produint una menor diüresi durant el període de son.
La seva regulació està condicionada per múltiples estímuls com l'estrès, les nàusees, el dolor, la hipòxia, la hipercàpnia i determinats fàrmacs, sent els principals l'osmolaritat i el volum plasmàtic.
La seva funció és mantenir l'osmolaritat i volum plasmàtic davant de qualsevol fluctuació del balanç hídric, mitjançant la seva acció en el túbul distal i col·lector de la nefrona, promovent la reabsorció d'aigua en aquest nivell. En condicions normals, un increment en l'osmolalitat sèrica indueix l'alliberament d'ADH, mentre que el descens d'aquesta inhibeix la seva secreció.
La diabetis insípida (DI) és l'alteració més freqüent de la neurohipòfisi. Es tracta d'un trastorn del metabolisme de l'aigua ocasionat per una secreció deficient o absent de l’ADH (diabetis insípida central, DIC), o per una resistència a les seves accions en els receptors hormonals existents a la nefrona (diabetis insípida). En tots dos casos, la deficiència en la seva acció a nivell renal conduirà a l'aparició de poliúria hipotònica, amb volums urinaris> 50 ml/kg /dia /> 3 l al dia i osmolalitat urinària
La majoria dels casos de DIC són adquirits, podent ser deguda també a causes hereditàries o idiopàtiques. Entre les causes trobem:
- Traumatismes cranioencefàlics (TCE) i cirurgia transesfenoidal hipotálamo- hipofisària (causes més freqüents).
- Tumoral: tumor hipofisari o metàstasi, craneofaringioma, etc.
- Radiació de la hipòfisi
- Vascular: hemorràgia cerebral, infart, aneurisma, hemorràgia intrahipotalámica, etc.
- Granulomatós: histiocitosis i sarcoïdosi.
- Infeccions del SNC: meningitis, encefalitis, tuberculosi.
- Inflamatori / autoimmune.
- Fàrmacs / toxines: fenitoïna, clorpromazina, etanol, verí de serp, entre d'altres.
- Idiopàtic: present en fins a un 25% dels casos.
- Causa congènita amb malformacions.
- Altres trastorns: hidrocefàlia, malalties degeneratives, consum alcohol, etc.
La diabetis insípida pot ser causada per certs medicaments (liti, cisplatí, amfotericina B, metoxiflurano, etc.), trastorns electrolítics (hipercalcèmia, hipopotasèmia) i altres trastorns com la pielonefritis, la poliquistosi i la nefropatia intrínseca.
Manifestacions clíniques
L'inici de la clínica sol ser brusc (hores- dies), trobant els següents signes i símptomes:
- Sensació de set diürna i nocturna, amb preferència per begudes fredes i gelades, que pot conduir a ingestes de líquids de fins a 5-20 l / dia.
- Polidípsia i poliúria extrema (d'orina molt diluïda gairebé incolora, arribant a ser de 4-16 l / dia): són les principals manifestacions d'aquesta alteració.
- Nictúria que condueix a trastorns de la son.
- Fatiga (en casos greus)
- Hipernatrèmia
Si no es realitza una reposició del líquid perdut, podem trobar els següents signes i símptomes:
- Derivats de la deshidratació com: pèrdua de pes, baixa turgència en els teixits, sequedat a les membranes mucoses, restrenyiment, debilitat muscular, marejos, taquicàrdia i hipotensió.
- Encefalopatia hipernatrèmica: irritabilitat, confusió, obnubilació, letargia, convulsions i fins i tot coma.
Diagnòstic
En l'avaluació inicial s'ha de constatar la poliúria, mitjançant una quantificació del volum urinari durant 24 hores, descartant que es tracti de poliúria osmòtica mitjançant l'anàlisi de l'osmolalitat urinària. Realitzant-se a més un estudi analític, per valorar el sodi i l'osmolaritat plasmàtica.
Se sospitarà de DI en pacients que presentin les manifestacions clíniques descrites, orina hipotònica (densitat <1005, osmolalitat 50-200 mmol / kg) i concentracions elevades de sodi (> 147 mEq / L) i de l'osmolaritat plasmàtica (> 300 mmol / kg).
És important realitzar el diagnòstic diferencial (DIC, DI nefrogènica o altres entitats que cursin amb poliúria). El perfil bioquímic, els antecedents del pacient i algunes peculiaritats clíniques poden orientar el diagnòstic. Sent d'utilitat la prova de l’ADH (injecció subcutània de vasopressina, valorant el seu efecte en la concentració de la diüresi) o la prova de deshidratació o privació d'aigua per confirmar la DIC.
Tractament
En la fase aguda, les mesures de tractament inclouen, a més de tractar el factor desencadenant, la reposició del líquid perdut realitzant-se de la següent manera:
- Si el pacient està conscient: es fomentarà la ingesta lliure d'aigua.
- Si el pacient està inconscient, hipotens o amb simptomatologia greu del SNC: s'administraran sèrums hipotònics via endovenosa, ajustant el ritme segons la diüresi a raó d'1 ml per cada ml de volum d'orina.
Es vigilarà estretament el balanç hídric, la set, el pes, els ions i l'osmolaritat plasmàtica i en orina, per evitar la hiponatrèmia.
En casos concrets, com en els que el pacient presenti adipsia i diüresi amb volums incrementats difícils de compensar amb l'aportació de líquids, s'utilitzarà la desmopresina com anàleg artificial substitutiu de l'ADH, amb una dosi inicial d’1-2 micrograms via subcutània, ajustant-se posteriorment en funció de la diüresi. Pot administrar també via endovenosa i intranasal.
Com a tractament de segona línia per a la DIC es pot utilitzar la clorpropamida, prestant atenció a la glicèmia del pacient per risc d’hipoglicèmies.
En formes parcials de DI, una dieta baixa en sodi i l'ús de diürètics tiazídics poden ser d'utilitat. A la diabetis insípida s'utilitzaran diürètics tiazídics, amb o sense associació de diürètics estalviadors de potassi (amilorida), eliminació lleu de la sal, inhibidors de prostaglandines i indometacina. Aquest tipus de DI no presenta resposta a la desmopressina.
2.4. Síndrome de secreció inadequada d'ADH
La síndrome de secreció inadequada d'hormona antidiürètica (SIADH) suposa la condició clínica contrària a la descrita anteriorment.
Al SIADH la regulació fisiològica desapareix, ocasionant un alliberament no regulada amb un excés d'ADH o una acció contínua d'aquesta sobre els seus receptors a nivell renal. En conseqüència, es produeix una major absorció d'aigua lliure a nivell renal, trobant una orina més concentrada (amb osmolalitat urinària elevada) i una osmolaritat plasmàtica i concentracions de sodi baixes per hemodilució.
Entre les causes que poden conduir a l'aparició de SIADH trobem:
- Fàrmacs: antidepressius tricíclics, carbamazepina, inhibidors de la monoaminooxidasa (IMAO), antiinflamatoris no esteroides (AINE), diürètics tiazídics, omeprazol, desmopresina, haloperidol, morfina, etc.
- Lesions en el SNC: traumatismes (TCE), hemorràgies intracranials, cirurgies cranials (inclosa la hipòfisi), ictus, tumors, abscessos cerebrals i encefalitis.
- Tumorals: sent amb més freqüència els que es localitzen a nivell del parènquima pulmonar. Podent ser degut també a tumors en pàncrees, cervell i pròstata.
- Lesions pulmonars benignes: pneumònia, pneumotòrax, atelèctasis, SDRA i asma.
- Altres causes (menys freqüents): VIH, SIADH idiopàtic de l'ancià, hiponatrèmia de l'esportista per exercici intens, etc.
Manifestacions clíniques
La hiponatrèmia del SIADH es caracteritza per presentar una volèmia normal, amb una osmolaritat plasmàtica baixa. Les manifestacions clíniques dependran de la gravetat de la hiponatrèmia i la velocitat amb la que s'instaura.
Hiponatrèmia lleu i moderada (125-134 mEq / L): les que es produeixen de manera progressiva i crònica solen ser asimptomàtiques. No obstant això, les hiponatremies agudes, amb una instauració
- Hiponatrèmia més greu i agudes
Diagnòstic
El diagnòstic s'estableix a través de la combinació de troballes clíniques i bioquímics. La hiponatrèmia (sodi 100 mOsm / kg), amb una major pèrdua de sodi urinari (> 30-40 mEq / l).
A més, s'hauran de descartar altres possibles causes d’hiponatrèmia com la disfunció renal, l'hipotiroïdisme, la fallida hepàtica, la insuficiència suprarenal, la insuficiència cardíaca o la ingesta de diürètics (tiazídics o de nansa).
Tractament
Els objectius del tractament són:
- Evitar la caiguda de les concentracions de sodi sèric
- Corregir de manera lenta i progressiva el dèficit de sodi
- Evitar una síndrome de desmielinització per una correcció excessivament ràpida de la hiponatrèmia
A més de tenir per objectiu tractar la causa subjacent, en primer lloc es valorarà la gravetat de la natremia i la presència de símptomes neurològics. En els casos d'hiponatrèmia aguda amb inici
S'ha d'administrar mitjançant l’infusió d'un bolo de 100-150 ml en 20 minuts, controlant la natremia, podent-se repetir 2-3 vegades fins millorar els símptomes o els nivells de sodi. En tot cas, s'estableix un ritme de correcció mitjana de 4-6 mEq/dia, sent el límit màxim la correcció de 8-12 mEq / l /dia.
Pot ser d'utilitat l'ús de diürètics de nansa després de l'administració de solucions hipertòniques, per reduir el risc d'insuficiència cardíaca.
En casos més crònics el maneig terapèutic anirà dirigit a restringir l'aportació de fluids a l'organisme, mitjançant una restricció hídrica 500-1000 ml / dia, mantenint l'aportació de sodi en la dieta.
3. ALTERACIONS A LA GLÀNDULA TIROIDE
La tiroide és la glàndula més gran del cos. Té forma de papallona, situada per davant de la tràquea a nivell del segon i tercer anell traqueal. Aquesta constituïda per 2 lòbuls laterals, situats lateralment a la tràquea i l'esòfag, que s'uneixen per una banda de teixit anomenada "istme". La seva grandària es correlaciona amb l'edat, la talla, el pes, la raça i la ingesta de iode de la persona, presentant una elevada capacitat de creixement.
La tiroide produeix tres hormones:
- Triiodotironina (T3)
- Tiroxina (T4)
- Calcitonina
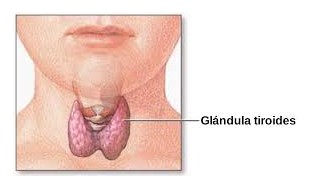
|
Il·lustració 7 Glàndula tiroides Font: wikimedia commons |
Les hormones tiroïdals triiodotironina (T3) i tetrayodotironina (T4) tenen com a funció principal regular l'activitat metabòlica cel·lular. Es sintetitzen i emmagatzemen en la glàndula tiroide a partir de diferents elements i enzims per a la seva síntesi (iode, glucoproteïna tiroglobulina, enzim peroxidasa tiroïdal, etc). A la glàndula es troben unides a la tiroglobulina, fins que són excretades en la circulació on s'uneixen generalment a proteïnes plasmàtiques (transtiretina, globulina fixadora de tiroides i albúmina), funcionant com un dipòsit extratiroideo que permet la seva disponibilitat immediata en els teixits perifèrics.
Les hormones tiroïdals afecten pràcticament en tots els sistemes del cos i funció dels teixits, incloses la taxa metabòlica basal, les concentracions de colesterol sèric, la termogènesi tissular i la resistència vascular.
La T3 és reconeguda com l'hormona tiroïdal biològicament activa, amb una vida mitjana de 24 hores, pel fet que presenta una afinitat deu vegades més alta respecte a T4 amb els receptors d'hormona tiroïdal. Per la seva banda, la T4 presenta una vida mitjana de 7 dies, és una hormona relativament feble que manté però el metabolisme corporal en un estat basal, considerant-se a més un "magatzem circulant d'hormones tiroïdals".
La calcitonina o tirocalcitonina té com a funció mantenir els valors de calci en sang. Es secreta per la tiroide en resposta a les altes concentracions de calci en plasma, causant una reducció d'aquests nivells en incrementar el seu dipòsit en l'os.
Eix hipotàlem- hipòfisis- tiroide
La funció de la tiroide està regulada per l'eix hipotàlem- hipòfisis- tiroide. La TSH és la principal hormona reguladora de la funció tiroïdal. Es tracta d'una hormona secretada per l'adenohipòfisi sota l'estímul de l'hormona alliberadora de tirotropina (TRH), secretada aquesta última per l'hipotàlem.
Les hormones tiroïdals per la seva banda, tenen un paper contrarregulatori en la secreció de TRH, conegut com a feedback negatiu. D'aquesta manera, quan es produeix un increment en la quantitat d'hormones tiroïdals en sang s'inhibeix la secreció de TRH, disminuint-se la producció de TSH en conseqüència, donant com a resultat una menor producció d'hormona tiroïdal.
3.1. Hipotiroïdisme
L'hipotiroïdisme es defineix com la situació clínica en què hi ha una disminució en la producció d'hormones tiroïdals. Pot ser primari o central, en funció de la seva etiologia.
L'hipotiroïdisme primari (HTP) és la forma més freqüent d'hipotiroïdisme (99% dels casos) i es produeix com a conseqüència d'una afectació primària de la glàndula tiroide. Entre les causes que el poden desenvolupar trobem:
- Iode: Tant el dèficit com l'excés de iode poden causar hipotiroïdisme, sent el dèficit la causa més freqüent de HTP a nivell mundial. El goll endèmic es produeix gairebé sempre en zones en què hi ha un dèficit ambiental de iode, però s'ha experimentat una disminució en la seva incidència en moltes regions amb la introducció de la sal iodada en la dieta.
El HTP per excés de iode pot donar-se per l'ús de fàrmacs com l'amiodarona, els contrastos iodats o la povidona iodada, ja que són fonts d'excés de iode i inhibeixen l’organificació del iode i la síntesi d'hormones tiroïdals, conegut com l'efecte Wolff-Chaikoff.
- Tiroïditis autoimmunitària o malaltia de Hashimoto: es tracta de la causa més freqüent de HTP en àrees on no hi ha deficiència de iode.
A mesura que evoluciona la tiroïditis de Hashimoto es produeix una pèrdua progressiva de la funció tiroïdal, causada per una infiltració i destrucció de el teixit tiroïdal intervinguda pel sistema immunitari (a partir d'anticossos i cèl·lules), podent cursar amb goll o sense.
El seu diagnòstic es confirma per la presència d'autoanticossos antitiroïdals en sang.
- Hipotiroïdisme iatrogènic secundari a tiroïdectomia (sol aparèixer a les 2-4 setmanes després d'una tiroïdectomia total), a la teràpia amb radioiode (el seu desenvolupament és més freqüent durant el primer any post tractament) o la irradiació externa del coll (per l'ús de radioteràpia).
- Fàrmacs com el liti, iode, antitiroïdals i etionamida, entre d'altres.
- Altres causes: malalties infiltratives (tiroïditis de Riedel, hemocromatosi, sarcoïdosi, leucèmia, etc.), hipotiroïdisme transitori (tiroïditis silent, postpart, tiroidectomia subtotal, agents químics) o hipotiroïdisme causat per alteracions congènites.
L'hipotiroïdisme central pot ser degut a una alteració hipofisària o hipotalàmica, que provoqui una disminució en la secreció de TSH (hipotiroïdisme secundari) o TRH (hipotiroïdisme terciari).
Representa <1% dels casos d'hipotiroïdisme, sent menys greu que el HTP, ja que hi ha una petita fracció de funció de la tiroide que es troba conservada (10-15%), per ser independent de la TSH.
Entre les causes que el produeixen trobem: tumors hipofisaris, hipotalàmics o supraselars, causes iatrogèniques (TCE, cirguía, irradiació, fàrmacs), malalties infiltratives (sarcoïdosi, hemodromatosis, histiocitosis), cadira turca buida i metàstasi, entre d'altres.
En el cas que la insuficiència tiroïdal aquest present des del naixement, s'anomena hipotiroïdisme neonatal i pot ser degut al fet que la mare hagi tingut insuficiència tiroïdal.
L'hipotiroïdisme és més comú que l’hipertiroïdisme, presentant una major prevalença en les dones, sent fins 5-8 vegades més freqüent.
Manifestacions clíniques
L'hipotiroïdisme pot ser clínicament evident o subclínic, i pot afectar a tots els sistemes orgànics.
La clínica dependrà de la magnitud del dèficit hormonal, la velocitat amb la qual es desenvolupi, l'edat del pacient i la repercussió sobre els diferents teixits. Sol instaurar-se de forma progressiva, i pot trobar els següents signes i símptomes.
Neuropsiquiàtric:
- Cefalea
- Alteració de la visió nocturna
- Nistagme
- Hipoacúsia de percepció
- Alentiment o disminució de les funcions intel·lectuals (pensament, parla, memòria i aprenentatge)
- Apatia
- Desorientació subjectiva
- Confusió
- Trastorns psiquiàtrics: depressió i paranoia amb més freqüència, a més d'ansietat i psicosi.
- Somnolència
- Hipersensibilitat a opiacis, sedants i anestèsics.
- Letargia
- Coma (evolució a coma mixedematos)
Aparell respiratori:
- Hipoventilació
- Apnea obstructiva de la son (relacionada amb la macroglòssia)
Sistema cardiovascular:
- Bradicardia
- Disminució de la despesa cardíaca i la contractibilitat cardíaca
- Reducció del flux sanguini als teixits
- Disfunció diastòlica ventricular, que produeix una disminució en la precàrrega, contribuint a l'aparició d'insuficiència cardíaca (en l'hipotiroïdisme greu)
- Hipertensió diastòlica
- Canvis en l'ECG: prolongació de l'interval PR, ona P i complex QRS amb baixa amplitud, alteracions del segment ST i ones T invertides o aplanades.
- En cas de HTP sever: vessament pericàrdic (poques vegades produeix tapament cardíac).
Funció renal:
- Disminució del flux sanguini renal, taxa de filtració glomerular i capacitat tubular reabsortiva.
Metabolisme energètic:
- Disminució del metabolisme energètic, amb baixa taxa de metabolisme basal i disminució de la gana.
- Disminució en la producció de calor, causant intolerància al fred i temperatura corporal més baixa.
- Disminució en la síntesi i degradació de proteïnes
- Acumulació de lípids (hipercolesterolèmia)
- Guany de pes
Aparell digestiu:
- Restrenyiment
- Malabsorció
- Distensió abdominal
- Hi pot haver elevació de transaminases
Sistema musculoesquelètic:
- Lentitud de moviments i retard en els reflexos osteotendinosos
- Rigidesa i dolors musculars (s'agreugen amb les temperatures fredes)
- Debilitat i fatiga
- Hipoestèsies i parestèsies en extremitats
- Mioclònies
- Dèficit en les primeres fases de la vida: disgenèsia epifisaria
Sistema hematopoètic:
- Disminució de la massa eritrocitària: anèmia normocítica normocrómica lleu
- Hi pot haver alteració en l'adhesió plaquetaria i en la coagulació
Cara, pell i annexos:
- Macroglosia
- Engruiximent de mucoses faríngies i laríngies
- Rostre, mans i peus inflats
- Edema periorbitari
- Pell pàl·lida, freda i resseca
- Major tendència a hematomes per fragilitat capil·lar i retard en la curació de ferides
- Cabell trencadís, sec, amb tendència a caure
- Ungles trencadisses, amb creixement lent
Funció reproductora:
- Dones: disminució de la libido, anovulació, menstruació excessiva i irregular, fertilitat reduïda i major risc d'avortaments espontanis.
- Homes: disminució de la libido, oligoespermia i disfunció erèctil.
Diagnòstic
Després de fer una exploració física, mitjançant la palpació i auscultació de la glàndula, es realitzaran proves per valorar la funció tiroïdal (determinacions analítiques, gammagrafia, biòpsia, etc.).
En l'hipotiroïdisme, indistintament de la seva etiologia, hi ha una disminució en la secreció d'hormones tiroïdals, apreciant-se aquesta alteració en l'analítica sanguínia.
Atès que la majoria dels casos d'hipotiroïdisme són primaris, es trobarà a més una elevació de la TSH, d'aquesta manera el millor test de cribratge de l'hipotiroïdisme. En aquests casos, es recomana completar l'analítica amb una determinació de T4L. Si es sospita d'etiologia primària autoimmune, es determinaran a més els nivells d'anticossos antitiroïdals (Ac anti TPO i Ac antitiroglobulina).
En els pacients diagnosticats d'hipotiroïdisme central, amb nivells de TSH normals o indetectables, s'avaluarà a més la funció de l'eix hipotálamo- hipofisari, realitzant estudis d'imatge de la regió selar i supraselar.
Altres troballes en l'hipotiroïdisme són: anèmia, hiponatrèmia, hipercolesterolèmia, hipertrigliceridèmia, augment de la CPK i alteracions en l'ECG.
Tractament
El tractament d'elecció de l'hipotiroïdisme és la levotiroxina (T4). Es tracta d'una prohormona, el principal avantatge és que la seva conversió a T3 es regula de manera fisiològica en funció de les necessitats dels teixits, presentant una vida mitjana de 7 dies.
Es recomana la seva ingesta en dejú, vigilant alguns aliments (cafè, fibra, soja) i fàrmacs (ferro, calci, antiàcids, inhibidors de la bomba de protons com l'omeprazol, colestiramina, anticonvulsivants, rifampicina) que disminueixen la seva absorció o alteren el seu metabolisme, per no administrar-se simultàniament.
Abans d'iniciar el tractament amb hormona tiroïdal, s'ha de descartar una alteració de l'eix adrenal per a la seva substitució prèvia, ja que si no es realitza en aquest ordre podria desencadernar-se una insuficiència suprarenal aguda.
3.2. Coma mixedematós
La crisi mixedematosa o coma mixedematós és la forma més greu de l'hipotiroïdisme, causat per un dèficit important d'hormones tiroïdals.
Pot resultar del progrés de l'hipotiroïdisme, de forma lenta i gradual, o pot desenvolupar-se abruptament per un factor precipitant com l'exposició al fred, l'ús de sedants, una infecció, traumatisme o infart agut de miocardi, la resecció tiroïdal, tractament amb fàrmacs antitiroïdals o la radioteràpia cervical.
Manifestacions clíniques
El pacient en coma mixedematós pot presentar:
- Disminució de la capacitat mental, presentant des de lleu ensopiment fins greu obnubilació
- Parla lenta i confusa
- Letargia i somnolència
- Estupor progressiu
- Convulsions
- Respiració significativament deprimida, amb sorolls respiratoris afegits
- Hipoventilació
- Ronquera
- Hipotensió i bradicàrdia
- Disminució de la despesa cardíaca
- Hipoglucèmia
- Hipotèrmia greu
- Hiponatrèmia
- Reflexos tendinosos profunds disminuïts
Aquests signes i símptomes, junt al col·lapse cardiovascular i el xoc, requereixen una intervenció immediata perquè el pacient sobrevisqui.
Diagnòstic i tractament
El diagnòstic del coma mixedematós és bàsicament clínic. Donada la gravetat de la situació, s'ha d'iniciar el tractament immediatament després del seu diagnòstic clínic i l'extracció de mostres analítiques per determinar els nivells de TSH, T4L i cortisol.
El tractament consisteix a donar suport a les funcions vitals mentre es restaura l’eutiroïdisme, a través de les següents accions:
- Administració de levotiroxina via endovenosa i hidrocortisona prèvia, en casos d'insuficiència hipofisari, suprarenal o fins que es descartin.
- Vigilància de l'estat respiratori, l'adequada ventilació i saturació d'oxigen, per si fos necessària l’assistència respiratòria amb administració d'oxigen suplementari o intubació i ventilació mecànica si el pacient progressés a estat de coma.
- Supervisió de les constants vitals i arítmies cardíaques, amb reposició de líquids endovenosos per restaurar l’hemodinàmia.
- Monitoratge de la temperatura corporal, realitzant un reescalfament passiu amb una manta per revertir la hipotèrmia. En aquells casos en què sigui necessari un reescalfament actiu, mitjançant l'ús de mantes d'escalfament, es vigilarà la presència d'hipotensió i l'increment en les demandes d'oxigen que pot causar.
- Vigilància de la glucèmia, per si precisés l'administració de glucosa intravenosa.
- Valorar possibles fonts d'infecció (sang, esput o orina) i administrar antimicrobians per a la infecció si es considera oportú.
3.3. Hipertiroïdisme
L'hipertiroïdisme es defineix com la situació clínica caracteritzada per un excés d'hormones tiroïdals, produïda com a conseqüència d'un augment en la síntesi i la secreció d'aquestes per la glàndula tiroide.
Les causes d'hipertiroïdisme poden classificar-se en dos grups, en funció de si són endògenes o exògenes.
Causes endògenes, per augment en la producció d'hormones tiroïdals:
- Malaltia de Graves Basedow (EGB): es tracta d'una afecció autoimmunitària, que sol ser hereditària, en la qual es formen autoanticossos que estimulen els receptors de TSH a la tiroide de manera no regulada.
És la causa més freqüent d'hipertiroïdisme (60- 70% dels casos), amb una major afectació en dones en edat fèrtil (relació 10: 1) i un pic d'incidència en les edats compreses entre els 20-40 anys.
Els símptomes d'hipertiroïdisme poden ser de caràcter moderat- sever, desenvolupant-se de forma ràpidament progressiva i s'associen a la presència de goll difús.
Aquesta alteració pot aparèixer després d'un xoc emocional, estrès o infecció.
- Goll multinodular i adenoma tiroïdal tòxic (BMN i ATT): es tracta de nòduls benignes situats a la glàndula tiroide que secreten hormones tiroïdals. Són la segona causa més freqüent d'hipertiroïdisme. Presenten major prevalença a mesura que s'incrementa l'edat, sent més freqüents en àrees amb deficiència de iode.
La severitat del quadre pot variar des d'un hipertiroïdisme subclínic a un franc, però en general són menys greus que en l'EGB i poden tenir predomini cardiovascular.
Causes endògenes, per augment en l'alliberament d'hormones tiroïdals:
- Tiroïditis subaguda granulomatosa de De Quervain: sol produir-se després d'un episodi víric. En la majoria dels casos es recupera l’eutiroïdisme un cop superat l'episodi inflamatori.
- Tiroïditis limfocítica (mut) i tiroïditis postpart: formen part de la patologia tiroïdal autoimmune, presentant anticossos antimicrosomals (anti TPO). La tiroïditis postpart es produeix durant l'any següent després del part.
Causes exògenes:
- Sobredosificació d'hormona tiroïdal en el seu reemplaçament
- Ingesta excessiva de iode
- Administració de contrast iodat intravenós
- Tiroïditis secundària a fàrmacs (amiodarona, liti, interferó alfa, etc.) o postradioteràpia.
Manifestacions clíniques
Les manifestacions clíniques i la severitat dels símptomes dependran dels nivells d'hormones tiroïdals, la causa de l'hipertiroïdisme i factors individuals del pacient (edat, comorbiditats).
El curs d'aquesta patologia sol ser lleu, caracteritzada per períodes de remissió i exacerbació, amb una recuperació al cap dels mesos o anys. En el cas que no s'instauri tractament pot progressar de forma irreversible.
A causa que les hormones tiroïdals intervenen en les funcions de múltiples òrgans i sistemes, podem trobar signes i símptomes en tots ells, sent les manifestacions cardiovasculars les més freqüents.
Neuropsiquiàtric:
- Por i nerviosisme
- Inquietud
- Irritabilitat
- Pèrdua de concentració
- Insomni
- Labilitat emocional
- Apatia i depressió (en ancians)
- Hipomania o mania
- Agitació
- Deliri
- Convulsions
- Estupor
- Coma
Aparell respiratori:
- Dispnea d'esforç i en repòs
- Hiperventilació
- Exacerbació de l'asma
- Signes i símptomes compressius locals, si s'associa a goll de grans dimensions, com: tos, dispnea o compressió traqueal.
Sistema cardiovascular:
- Taquicàrdia
- Palpitacions
- Hipertensió sistòlica
- Augment de la despesa cardíaca i contractibilitat cardíaca
- Angor
- Estat hiperdinàmic que pot causar, si persisteix, hipertròfia ventricular esquerra, disfunció ventricular i insuficiència cardíaca.
- Arítmies cardíaques: taquicàrdia supraventricular i fibril·lació auricular (més freqüent, especialment en ancians)
Metabolisme energètic:
- Increment en la termogènesi: intolerància a la calor, sudoració profusa i febre.
- Augment de la despesa metabòlica basal: augment de la gana i pèrdua de pes.
Aparell digestiu:
- Disfàgia (si s'associa a goll de grans dimensions, per compressió local)
- Increment en la motilitat intestinal
- Hiperdefecació o diarrea
- Malabsorció
- Elevació de les transaminases
Sistema musculoesquelètic
- Hiperreflèxia
- Fatiga i debilitat generalitzada
- Tremolor distal
- Miopatia proximal
- Incrementa la resorció òssia: osteoporosi i increment del risc de fractures (si es manté en el temps)
- Acropaquia (EGB, inflamació de teixits tous)
Cara, pell i annexos:
- Retracció parpebral
- Orbitopatía tiroïdal/exoftalmós (EGB)
- Pell humida i calenta
- Hiperhidrosi
- Fragilitat capil·lar i unguial
- Pruïja
Funció reproductora:
- Dones: alteracions menstruals (oligomenorrea / amenorrea), major risc d'avortaments espontanis i infertilitat.
- Homes: ginecomàstia i disfunció erèctil.
En el cas de les tiroïditis causades per un procés víric com la tiroïditis subaguda de De Quervain, amb un procés inflamatori secundari, el pacient pot presentar malestar general, faringitis, febre i dolor a la glàndula tiroide (moderat / intens).
Diagnòstic
El diagnòstic de l'hipertiroïdisme es realitza segons els signes, símptomes i la determinació sèrica de la TSH i hormones tiroïdals (T3 i T4), que es troben disminuïdes i incrementades respectivament.
Per determinar la seva etiologia s'obtindrà l’informació necessària mitjançant l'anamnesi, l'exploració física i les proves de laboratori i imatge (gammagrafia tiroïdal, ecografia amb Doppler de la tiroide) que es considerin oportunes en cada pacient segons la sospita etiològica.
Tractament
El tractament de l'hipertiroïdisme dependrà de la causa subjacent i consisteix amb freqüència en la combinació de teràpies. Té dos objectius principals, d'una banda aconseguir una ràpida millora dels símptomes i de l'altra disminuir els nivells d'hormones tiroïdals.
Tractament simptomàtic: es realitza mitjançant l'ús de bloquejadors betaadrenèrgics (BBA) per controlar l’hiperactivitat adrenèrgica associada a l'hipertiroïdisme. El seu ús millora els tremolors, l'ansietat, el nerviosisme, la taquicàrdia, la pressió arterial sistòlica, la debilitat muscular, la intolerància a la calor i la hiperhidrosi.
El BBA més utilitzat és el propanolol, contraindicat en pacients amb broncoespasme. En aquests casos es poden utilitzar atenolol, metoprolol o bisoprolol, per ser més cardioselectius.
Reducció dels nivells d'hormones:
- Tionamidas (metimazol, propiltiouracilo i carbimazol): són fàrmacs antitiroïdals que produeixen una inhibició en la síntesi d'hormones tiroïdals. S'han de prendre en dejú per evitar que es disminueixi la seva absorció per la seva interacció amb alguns aliments (nous, farines de soja i fibra dietètica).
Poden administrar-se de manera exclusiva o prèviament al radioiode o la cirurgia.
- Radioiode: El radioiode és captat per les cèl·lules fol·liculars de la tiroide, on emet radiació beta que produeix necrosi i destrucció de la glàndula tiroide. Després de la seva ocupació pot produir-se una secreció aguda d'hormones tiroïdals, motiu pel qual es vigilarà al pacient a la recerca de signes de tempesta tiroïdal.
El seu ús està contraindicat en la lactància i l'embaràs, es recomana evitar l'embaràs en els 6 mesos posteriors a l’ús del radioiode.
- Cirurgia: La intervenció quirúrgica es reserva per circumstàncies especials, com en dones embarassades que presenten al·lèrgia als fàrmacs antitiroïdals, pacients amb golls grans amb símptomes obstructius, en aquells que no poden prendre fàrmacs / compostos antitiroïdals o en aquells en que sigui necessari una normalització ràpida de la funció tiroïdal.
La tècnica recomanada en l'EGB i el BMN és la tiroidectomía total o gairebé total. En el cas d'ATT, la tècnica recomanada és l’hemitiroidectomia.
Previ a la cirurgia el pacient hauria d'estar eutiroidal (sent d'utilitat l'ús dels tractaments descrits anteriorment) per prevenir la crisi tiroïdal.
Els tres tractaments descrits, utilitzats per a la reducció dels nivells d'hormones tiroïdals, comparteixen les mateixes complicacions: hipotiroïdisme permanent i recaiguda o hipertiroïdisme recurrent.
3.4. Crisi tirotòxica o tempesta tiroïdal
La crisi tirotóxica o tempesta tiroïdal constitueix la màxima expressió de gravetat de l'hipertiroïdisme. Generalment té un inici sobtat / abrupte, representant una urgència mèdica.
Es tracta d'una exacerbació aguda de l'hipertiroïdisme, que pot donar-se per no rebre tractament durant molt de temps o, amb més freqüència, a conseqüència d'un esdeveniment estressant (embaràs o part, cirurgies, traumatismes, infeccions, tractament amb amiodarona o iode, cetoacidosi diabètica, estrès emocional extrem, etc).
Manifestacions clíniques
El quadre clínic és provocat per una situació hipermetabólica causada per un excés d'hormones tiroïdals en sang.
Consisteix en l'exacerbació dels símptomes tirotòxics, descrits anteriorment, podent anar acompanyats de:
- Irritabilitat extrema
- Deliri psicòtic
- Somnolència, estupor o coma
- Diplopia
- Hipertensió
- Taquicàrdia marcada (> 130 ppm) i arítmies
- Dolor toràcic
- Insuficiència cardíaca i xoc cardiogènic
- Dispnea
- Hipertèrmia: presenten temperatures corporals> 38º de fins a 41,1 ºC, amb començament insidiós aconseguint amb rapidesa nivells letals. Els ancians poden presentar normotermia.
- Vòmits i diarrea
- Dolor abdominal
Sense la instauració d'un tractament per revertir-la, la crisi tirotòxica pot conduir al col·lapse circulatori, hipotensió, coma i mort del pacient.
Diagnòstic i tractament
El diagnòstic és principalment clínic i el seu tractament ha de ser immediat per evitar la mort del pacient. Els objectius immediats del tractament són disminuir la freqüència cardíaca, prevenir el col·lapse vascular i disminuir la temperatura corporal.
Per això s'inclouen les següents mesures:
- Administrar oxigen humidificat per optimitzar l'oxigenació dels teixits i complir amb l'alta demanda metabòlica existent.
- Control dels símptomes: mitjançant l'administració de bloquejadors beta-adrenèrgics, com el propanolol via endovenosa, per bloquejar els efectes simpàtics.
- Bloqueig de la síntesi d'hormones tiroïdals: mitjançant l'administració fàrmacs antitiroïde com les tionamidas (propiltiouracil i metimazol).
- Bloqueig de la conversió perifèrica de T4 a T3: mitjançant l'administració de corticosteroides (hidrocortisona, dexametasona) o contrastos iodats (àcid iopanoico).
- Realitzar mesures de refredament per disminuir la temperatura corporal (com l'ús d'una manta hipertèrmica-hipotèrmica, bosses de gel, un ambient fresc, paracetamol). Evitant l'àcid acetilsalicílic, ja que els salicilats bloquegen l'enllaç de T3 i T4.
- Mesures de suport: administració de líquids, nutrients, vitamines i sedació si precisa.
3.5. Tumors en la tiroide: goll i malaltia nodular
Es defineix com goll tot augment de mida de la glàndula tiroïdal, ja sigui difús o nodular, prou gran per causar un edema visible al coll.
El goll simple eutiroideo o no tòxic presenta una funció tiroïdal conservada i el seu desenvolupament no està relacionat amb patologies inflamatòries, autoimmunes, ni processos infecciosos o neoplàsics. L'increment del volum glandular es deu principalment a un augment del teixit tiroïdal fol·licular, amb un patró que no permet la distinció d'aquest amb el teixit tiroïdal normal.
Per la seva banda, es defineix el nòdul tiroïdal com una lesió macroscòpica limitada dins de la glàndula tiroidea, que es distingeix a nivell radiològic per presentar un patró diferent de la resta del parènquima tiroïdal. Poden aparèixer un nòdul tiroïdal o diversos sense anar relacionat amb un augment de la mida de la glàndula (goll), denominant tiroide nodular o multinodular.
La majoria dels nòduls tiroides són benignes, petits i asimptomàtics. Però en un 2-15% dels casos es tracta de càncer de tiroide.
Tant el goll com la malaltia nodular tiroïdal (ENT) són molt freqüents en la població general, amb major afectació en dones, ancians, persones que han rebut radiacions ionitzants en la infància o en zones de deficiència de iode. En la majoria dels casos es tracta de patologies benignes.
Es poden classificar el goll i l’ENT en funció de:
- Ingesta de iode: goll esporàdic (afectació <10% de la població) o goll endèmic (afectació> 10% de la població).
La majoria dels casos de goll endèmic es deuen a una ingesta deficient de iode. No solen presentar símptomes excepte l'edema al coll, que en funció de la seva grandària pot causar símptomes compressius. Molts d'aquests golls cedeixen un cop es corregeix el desequilibri de iode.
- Morfologia: goll difús o simple, uni/multinodular i goll col·loide.
- Estat funcional: hipofunció tiroïdal (com en la tiroïditis crònica autoimmune), funció tiroïdal normal (com en el goll simple) o hiperfunció tiroidea (com en la malaltia de Graves-Basedow o al goll multinodular tòxic i l'adenoma tòxic).
- Mida: es pot classificar el goll en quatre graus (0-III) segons l'Organització Mundial de la Salut (OMS), des d'un goll tot just palpable o no palpable fins a un goll visible a la distància.
Entre les causes que el produeixen trobem el dèficit de iode (dietes pobres en peix), l'origen inflamatori (tiroïditis, post radioiode i infecciosa), les substàncies bociògenes (tionamides, salicilats, liti, iode, oli de soja o de gira-sol, etc.), les malalties tiroïdals autoimmunes (EGB i tiroïditis de Hashimoto), les alteracions congènites i les fisiològiques (pubertat i embaràs), entre d'altres.
Manifestacions clíniques
En la majoria dels casos de goll simple i malaltia nodular els pacients estan asimptomàtics, amb una funció tiroïdal dins de la normalitat.
Poden aparèixer símptomes compressius (5% dels casos) en funció de la mida i la velocitat de creixement de la glàndula o del nòdul tiroïdal com:
- Dispnea: es tracta del símptoma més comú en pacients amb goll cervical o subesternal obstructiu. Pot aparèixer a l'esforç o ser posicional en decúbit, per afectació de la tràquea.
- Tos: sol ser postural. Es troba present en el 10-30% dels pacients.
- Alteracions de la veu (disfonia, ronquera i veu bitonal) o disfàgia: són símptomes menys freqüents, produït per afectacions de grans dimensions, que reflecteixen invasió local del nervi laringi o de l'esòfag.
- Cefalea, dispnea, congestió facial, circulació col·lateral a la part superior de tòrax i ingurgitació jugular: present en el goll intratoràcic, per compressió de les estructures veïnes.
- Desviació traqueal: pot ser palpable o visible en golls asimètrics.
En el goll i els nòduls tiroidals, un creixement ràpid pot ser degut a processos neoplàsics, podent trobar masses tiroïdals costat de símptomes obstructius o infecciosos, presentant febre juntament amb dolor cervical anterior.
La importància clínica del goll i l’ENT resideix en la possibilitat de malignització, la disfunció hormonal i la compressió local d'estructures anatòmiques adjacents que puguin produir.
El càncer de tiroide representa el 90% de les neoplàsies endocrines, incrementant-se el risc de desenvolupar-lo si el pacient ha rebut radiació externa en cap, coll o tòrax en la infantesa.
A més poden complicar-se amb l'aparició d'hemorràgies, quists, fibrosi i calcificació.
- ALTERACIONS A LES GLÀNDULES PARATIROIDES
Les glàndules paratiroides estan constituïdes per quatre glàndules que estan situades a la part posterior de la tiroide, una a cada cantonada de la glàndula. Totes elles funcionen juntes i produeixen l'hormona paratiroïdal (PTH), que té com a funció principal regular el metabolisme del calci i el fòsfor, en associació amb altres hormones, actuant a nivell ossi, gastrointestinal i renal.
Actua sobre les cèl·lules òssies estimulant la resorció òssia i a nivell renal incrementant la reabsorció tubular de calci i la síntesi d’1,25 dihidroxivitamina D, que afavoreix l'absorció de calci a nivell intestinal i disminueix la reabsorció de fòsfor. Com a resultat produeix un increment en les concentracions de calci i una disminució en les de fòsfor a nivell sanguini.
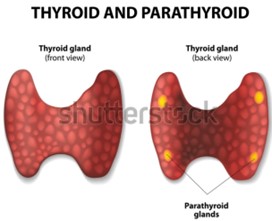
Il·lustració 8 glàndula paratiroide
font: https://www.shutterstock.com/es/image-vector/thyroid-parathyroid-gland-186033542 (Pendent posar original)
En condicions fisiològiques, les concentracions de calci en l'espai extracel·lular es troben estretament controlades. Quan es produeix un augment en la concentració de calci en aquest espai s'activen uns receptors de membrana situats a les glàndules paratiroïdals, denominats calcium sensing receptors, que suprimeixen la secreció de PTH creant un sistema de retroalimentació negativa.
4.1. Hipoparatiroïdisme
L’hipoparatiroïdisme és un trastorn endocrí que es caracteritza per presentar concentracions baixes de calci sèric (hipocalcèmia) i altes en fòsfor (hiperfosfatèmia), a conseqüència de presentar nivells indetectables o inadequadament baixos de PTH.
Les tres causes principals que poden conduir a l'hipoparatiroïdisme són:
- Defectes genètics que produeixen alteracions en el desenvolupament de les glàndules paratiroïdals, o en el seu funcionament (en la síntesi, secreció o funció de la PTH).
- Lesió autoimmunitària (hipoparatiroïdisme autoimmune)
- Ablació intencionada o lesió accidental, d'una o diverses glàndules paratiroides, durant la cirurgia cervical (tiroide, paratiroide o laríngia), tractant-se d'hipoparatiroïdisme postquirúrgic.
De totes elles, l’hipoparatiroidismo postquirúrgic és la forma més comuna de presentació d'aquest trastorn endocrí. Pot presentar-se de manera aguda i greu, precisant l'administració ràpida de calci via endovenosa per pal·liar els símptomes.
Hi ha factors de risc que afecten el desenvolupament d’hipoparatiroïdisme postquirúrgic, entre els quals trobem:
- Intervencions quirúrgiques més complexes i extenses
- Limfadenectomia
- Cirurgia per malaltia de Graves
- Recidives de goll
- Reintervencions per hemorràgia
Manifestacions clíniques
En casos lleus d’hipoparatiroïdisme és possible que no es produeixin símptomes. En els casos en què el trastorn sigui més gran podem trobar els següents signes i símptomes:
- Alteracions neuromusculars que van des de parestèsies fins tetània
- Símptomes de tetània latent com: entumiment, rampes i formigueig a les extremitats i rigidesa en mans i peus.
- Signes positius de Chvostek i Trousseau (tetània latent)
- Augment dels reflexos tendinosos profunds
- Convulsions
- Ansietat, irritabilitat, depressió i fins i tot psicosi
- Alteracions en l'ECG i arítmies cardíaques (interval QT prolongat, canvis en el segment ST)
- Hipotensió
- Broncoespasme (a la tetània manifesta)
- Disfàgia
- Dolor abdominal
- Cataractes
- Sequedat en cabell i pell
- Ungles trencadisses
- Debilitament de l'esmalt dental
Diagnòstic
El diagnòstic de l'hipoparatiroidisme es complica sovint per la presència de símptomes difusos (dolors, molèsties), sent especialment útils els estudis de laboratori per a realitzar-lo. En ells trobarem presència d'hipocalcèmia, hiperfosfatèmia i concentracions disminuïdes o indetectables de PTH.
A més es pot constatar la presència d'una major densitat òssia mitjançant radiografies òssies, a més d'alteracions cardíaques en l'ECG.
Tractament
L'objectiu del tractament és tractar la causa de l'hipoparatiroïdisme i corregir l’hipocalcèmia, mantenint unes concentracions de calci i fòsfor sèric adequades, per prevenir o eliminar els signes i símptomes derivats de l’hipocalcèmia. Per això el tractament inclou l'administració de vitamina D (dihidrotaquisterol si la funció renal aquesta conservada i calcitriol en els casos en què hi ha afectació en la funció renal), a més de suplements de calci.
La hipocalcèmia pot causar laringoespames, motiu pel qual es vigilarà l'aparició d’estridor respiratori o disfàgia que indicarien la seva aparició, per assegurar la permeabilitat de la via aèria en el cas que es comprometés.
Es vigilaran aquests signes de laringoespasme, a més de l'aparició de contraccions musculars lleus (especialment en mans), ja que podrien indicar l'aparició de tetània. Sent necessari en aquests casos l'administració de gluconat càlcic via endovenosa, per revertir la hipocalcèmia i la clínica.
A causa del risc de convulsions que hi ha es mantindrà un entorn tranquil, amb disminució d'estimulacions sensorials, per prevenir-les.
4.2. Hiperparatiroïdisme primari
L’hiperparatiroïdisme es caracteritza per un excés en l'activitat d'una o diverses de les quatre glàndules paratiroides, donant com a resultat la secreció excessiva de PTH. Aquesta promou la resorció òssia, l'absorció renal de calci i la disminució en la reabsorció de fòsfor, conduint a la descalcificació òssia, el desenvolupament de càlculs renals, la hipercalcèmia i la hipofosfatèmia.
L’hiperparatiroïdisme pot ser primari (causat per un adenoma de la paratiroide, múltiples neoplàsies endocrines o un trastorn genètic) o secundari (causat per raquitisme, deficiència de vitamina D, insuficiència renal crònica o abús de fàrmacs com la fenitoïna i els laxants).
L’hiperparatiroïdisme primari (HPP), com s'ha descrit, és un trastorn freqüent del metabolisme mineral causat per l'engrandiment d'una o més de les glàndules paratiroides. En la majoria dels casos es deu a un adenoma paratiroide únic (85%), podent ser causat també per afectació glandular múltiple per hiperplàsia difusa o adenomes múltiples (15%) o per un carcinoma paratiroidal (<1%).
En l'actualitat els pacients són diagnosticats de forma casual després de realitzar-se analítiques de rutina.
Manifestacions clíniques
Els signes i símptomes clàssics de l'HPP vindran determinats per les afectacions que es produeixin a nivell renal, ossi i en la calcèmia del pacient.
Afectació renal:
- Nefrolitiasis
- Disminució de la taxa de filtració glomerular
Afectació òssia:
- Disminució de la densitat mineral òssia
- Osteoporosi de predomini cortical
- Predisposició a fractures fàcils produïdes per la degeneració òssia
- Dolor i sensibilitat esquelètica: especialment a nivell articular i en esquena.
- Deformitats
- Osteïtis fibrosa quística
- Artritis
Alteracions en la calcèmia per hipercalcèmia:
- Alteracions neurològiques: cansament, debilitat, canvis d'humor, apatia, irritabilitat, ansietat, depressió lleu, falta de concentració, alteracions cognitives lleus, pèrdues de memòria i alteracions de la son.
- Alteracions cardiovasculars: hipertensió arterial, hipertròfia ventricular esquerra en absència d'hipertensió arterial, calcificació de la vàlvula aòrtica o mitral i arítmies cardíaques.
- Alteracions neuromusculars: debilitat muscular, astènia i atròfia, especialment a les extremitats inferiors.
- Alteracions digestives: anorèxia, nàusees, vòmits, dispèpsia, polidípsia, restrenyiment i dolor abdominal.
- Alteracions renals: poliúria.
- Confusió, coma i parada cardíaca a la tempesta paratiroïdal.
De totes elles, les manifestacions específiques de l'HPP són la nefrolitiasi (manifestació clínica més freqüent amb un 15-20% dels casos) i l’osteïtis fibrosa quística (en <2% dels casos, amb disminució de la densitat mineral òssia).
Diagnòstic
El HPP es caracteritza per hipercalcèmia, hipofosfatèmia i concentracions elevades o inadequadament normals de PTH.
Per al seu diagnòstic serà necessari realitzar dues determinacions inicials, centrades en la determinació bioquímica del calci i la PTH. La determinació d’hipercalcèmia en diverses ocasions és el millor indicador de HPP.
Les causes d'hipercalcèmia són nombroses (hipertiroïdisme, feocromocitoma, insuficiència renal, ús de fàrmacs com el liti i els tiazides, immobilització, etc.), però el HPP i el càncer suposen més del 90% dels casos, sent d'utilitat la prova d’hormona paratidoidea amb anticossos dobles per distingir de quina de les dues es tracta.
Tractament
L'únic tractament definitiu de HPP és la intervenció quirúrgica mitjançant la realització d'una paratiroidectomia.
En aquells pacients no candidats al tractament quirúrgic o en aquells que rebutgen la intervenció, es recomana una adequada hidratació (2 litres o més) amb l'objectiu d'evitar la deshidratació i prevenir l'aparició de càlculs renals, vigilant l'aparició de signes i símptomes relacionats amb l'evolució del trastorn.
4.3. Crisi hipercalcèmica
Es tracta d'una urgència endocrinològica, caracteritzada per concentracions de calci sèric> 13 mg / dl que s'associen a la disfunció multiorgànica. L’hiperparatiroïdisme primari és la causa subjacent més freqüent, sent la mortalitat d'aquesta complicació de fins a un 7%.
En la crisi hipercalcèmica es produeix una afectació de la majoria dels sistemes biològics, trobant les següents manifestacions clíniques:
- Neurològiques: d'instauració subtil podent trobar confusió, letargia i coma.
- Cardiològiques: escurçament del segment QT i arítmies cardíaques.
- Digestives: anorèxia, nàusees, vòmits i restrenyiment.
- Renals: deshidratació, oligúria i insuficiència renal aguda.
Donada la seva potencial mortalitat, la crisi hipercalcèmica ha de ser tractada immediatament a través dels següents objectius:
- Reduir la hipercalcèmia: mitjançant l'ús de calcitonina i la diàlisi en casos greus amb insuficiència renal.
- Corregir la deshidratació i incrementar l'eliminació renal de calci: es realitzarà una ràpida rehidratació mitjançant l'ús de sèrum salí isotònic via endovenosa (3-5l / dia), per mantenir un ritme diürètic de 100-150 ml / hora. I un cop corregida la hipovolèmia, es combinaran diürètics de nansa (furosemida) juntament amb l’hidratació per incrementar la calciuresis.
- Disminuir la resorció òssia: mitjançant el tractament amb bifosfonats (4 mg zoledronat en infusió endovenosa).
- ALTERACIONS DE LES GLÀNDULES SUPRARENALS
Les dues glàndules suprarenals es troben unides a tots dos ronyons a la part superior. Cada glàndula suprarenal està formada per dues capes: una capa interna (medul·la) i una capa externa (escorça), que funcionen com a glàndules endocrines independents produint les següents hormones.
Il·lustració 9 Glàndules suprarrenals Font: wikimedia commons
Medul·la suprarenal: produeix catecolamines, principalment adrenalina i noradrenalina, considerant-se una estructura neuroendocrina pel paper que exerceix en el sistema nerviós autònom. La funció de les catecolamines és regular les vies metabòliques per promoure el catabolisme del combustible emmagatzemat, satisfent d'aquesta manera les necessitats calòriques de fonts endògenes.
Escorça suprarenal: la secreció suprarenal fa possible que el cos s'adapti a tot tipus d'estrès. S'encarrega de la producció de les següents hormones esteroideas:
- Glucocorticoides: principalment cortisol, són importants per al metabolisme de la glucosa i per al de gairebé tots els òrgans del cos.
- Mineralcorticoides: com l'aldosterona, exerceixen els seus principals efectes en el metabolisme d'electròlits (com el sodi).
- Hormones sexuals: andrògens i estrògens.
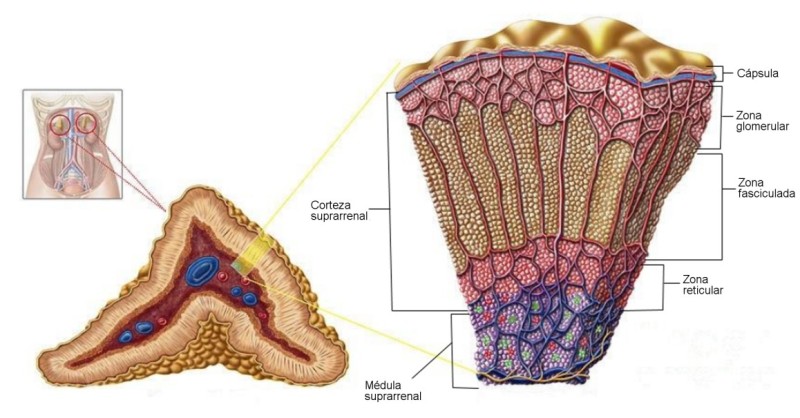
Il·lustració 10 Escorça i medul·la glàndules suprarenals
Font: wikimedia common
Alteracions en l'aldosterona
L'aldosterona es considera la principal hormona mineralocorticoide. La seva principal funció és regular l'homeòstasi del sodi, el volum plasmàtic i la pressió arterial. Mitjançant la seva acció, es produeix una disminució en l'excreció de sodi i aigua a nivell renal, produint una retenció de sodi i aigua amb una expansió de volum en conseqüència, a més d'un increment en l'excreció renal de potassi i hidrogen.
La secreció d'aldosterona es troba regulada pel sistema renina angiotensina. La renina, alliberada a nivell renal en resposta a la depleció de volum, permet el pas de l'angiotensinogen a angiotensina I inactiva. Aquesta última s'activarà a angiotensina II, a nivell pulmonar sota l'acció de l'enzim convertidor (ECA), produint vasoconstricció i promovent la síntesi i alliberament d'aldosterona per part de l'escorça adrenal.
La secreció d'aldosterona pot estar determinada a més pel potassi i la corticotropina.
5.1. Hipoaldosteronisme primari
L’hipoaldosteronisme és una síndrome que cursa amb nivells disminuïts d'aldosterona, donant lloc a l'aparició d'hiponatrèmia associada a hiperpotassèmia i disminució de la volèmia.
L’hipoaldosteronisme primari es deu a defectes primaris en la secreció de l'aldosterona, caracteritzat per una disminució en la concentració d'aldosterona i increment en els nivells de renina.
Pot ser de causa adquirida (secundari a fàrmacs, infeccions, cirurgia després de la resecció d'un aldosteronoma o com a conseqüència a estats crítics amb hipotensió / hipovolèmia com la sèpsia, pneumònia, fallada hepàtica, renal, cardíac, etc.), causa congènita (dèficit d’aldosteronasintasa) o per malaltia renal. La causa més freqüent és la insuficiència suprarenal primària, associant a més a un dèficit de glucocorticoides i andrògens suprarenals.
Manifestacions clíniques
A l’hipoaldosteronisme es produeix una disminució en la reabsorció renal de sodi i aigua, amb increment de la natriuresi i depleció de volum intravascular, a més d'una disminució de la secreció renal de l'ió hidrogen i de potassi, trobant en conseqüència les següents alteracions, signes i símptomes:
- Hiponatrèmia
- Hiperpotassèmia
- Acidosi metabòlica hiperclorèmica
- Deshidratació
- Hipotensió arterial
- Parestèsies, debilitat, astènia i fins i tot arítmies cardíaques: causades per les alteracions electrolítiques del sodi i el potassi.
Es sospitarà d’hipoaldosteronisme en aquelles situacions en què s'evidenciï hiperpotassèmia i acidosi metabòlica, principalment si s'associa a hiponatrèmia.
En primer lloc s'han de descartar altres causes d'hiperpotassèmia com els fàrmacs (digoxina, IECA, heparina, etc.) o situacions de rabdomiòlisis o hemòlisi.
En segon lloc s'ha de descartar la presència d'insuficiència adrenal primària, mitjançant la determinació de cortisol i ACTH basal.
I finalment, es determinaran els nivells basals d'aldosterona i l'activitat renina plasmàtica (basal i després estímul). En funció dels resultats obtinguts es determinarà el tipus d’hipoaldosteronisme.
Tractament
A l’hipoaldosteronisme primari es realitzarà un tractament específic en funció del factor desencadenant que l'hagi produït, com l'inici de tractament antibiòtic en la causa infecciosa.
5.2. Hiperaldosteronisme o aldosteronisme
L’hiperaldosteronisme primari (HAP) es produeix per un excés en la secreció d'aldosterona, produïda per la glàndula suprarenal, independent de sistema renina-angiotensina. Pot ser causat per diferents processos patològics com:
- Adenoma suprarenal o aldosteronoma o síndrome de Conn
- Hiperplàsia suprarenal primària (bilateral o unilateral)
- Carcinoma suprarenal (unilateral)
- Hiperaldosteronisme familiar: tractable amb l'administració de glucocorticoides.
Manifestacions clíniques
L'expressivitat clínica dependrà de les comorbiditats del pacient i del grau d’hiperaldosteronisme que presenti, sent més intens en els adenomes que en les hiperplàsies.
Les manifestacions clíniques poden ser variables, i és freqüent l'aparició de les següents alteracions, signes i símptomes:
- Hipertensió arterial (HTA): es tracta de la principal troballa clínica en l’HAP. Malgrat que alguns casos poden presentar normotensió i fins i tot hipotensió lleu, el més habitual és la presència d'hipertensió greu, de predomini diastòlic, resistent als tractaments habituals.
- Cefalea o flushing facial: derivats de l'increment de la pressió arterial.
- Debilitat, afectació visual o disminució del nivell de consciència: en casos greus per l'increment de la pressió arterial.
- Hipervolèmia sense edema
- Hipopotassèmia: tendeix a ser relativament estable, sent més freqüent en els casos més greus.
- Alteracions causades per la hipopotassèmia: neuromusculars (debilitat muscular, rampes o parestèsies), cardiològiques amb arítmies (interval QT llarg i ones U), endocrinològiques (diabetis insípida), renals (poliúria) i metabòliques (intolerància a la glucosa).
- Hipernatrèmia: sol ser lleu, amb concentracions estables al voltant de 143-147 mEq / L.
- Hipomagnesèmia: de caràcter lleu, a causa de la pèrdua urinària de magnesi.
- Predisposició a la tetània i les parestèsies: per disminució en les concentracions de calci sèric ionitzat derivades de l’alcalosi hipocalèmica.
- Alcalosi metabòlica lleu
La triada clàssica de l'HAP és la presència d'hipertensió arterial, hipopotassèmia i alcalosi metabòlica. No obstant això la hipopotassèmia és una troballa inconstant, present en una minoria dels casos, de manera que es considera la HTA normocalièmica la forma de presentació més comuna del trastorn.
L'excés d'aldosterona produeix a més toxicitat a nivell cardiovascular incrementant-se el risc de presentar esdeveniments cardiovasculars i cerebrovasculars (fibril·lació auricular, síndrome coronària aguda, accident isquèmic transitori, ictus o hemorràgia), dany en òrgans diana (hipertròfia ventricular esquerra, insuficiència cardíaca, deteriorament de la funció renal i nefroesclerosis), síndrome metabòlica i diabetis tipus 2, entre d'altres.
Diagnòstic
L'aproximació diagnòstica de l'HAP consta de tres passos:
- Cribratge: es realitzarà als pacients amb alt risc d'HAP, utilitzant-se com prova més estandarditzada el quocient aldosterona/activitat de renina plasmàtica (ARP) a través d'una extracció sanguínia. En el cas de l'HAP l'aldosterona es troba elevada i la renina suprimida.
- Confirmació: es realitzarà mitjançant proves específiques (prova de sobrecàrrega salina intravenosa o oral, prova de supressió amb fludrocortisona o la prova de captopril), a causa de l'elevat percentatge de falsos positius que pot donar l'elevació del quocient aldosterona/ARP.
- Diagnòstic etiològic: mitjançant diferents proves (TC abdominal, cateterisme de venes adrenals, estudi genètic, etc.), que permetin identificar les causes que són potencialment tractables.
Tractament
Els objectius del tractament de l'HAP són revertir els efectes adversos cardiovasculars, normalitzar els nivells de potassi sèric en pacients amb hipopotassèmia i normalitzar la pressió arterial. Per assolir-los, tenint en compte la seva etiologia, l'enfocament terapèutic inclou:
- Adrenalectomia laparoscòpica unilateral: indicada en els pacients amb hiperaldosteronisme unilateral (hiperplàsia o adenoma unilateral), el que contribuirà a la millora de l’HTA, sent curativa fins a un 60% dels casos, a més de la resolució de la hipocalèmia a la majoria dels pacients.
Previ a la cirurgia es tractarà la hipocalemia amb espironolactona. Després de la cirurgia el pacient pot necessitar l'administració de corticosteroides, líquids i altres fàrmacs per conservar la pressió arterial i prevenir complicacions agudes, pel fet que pot presentar fluctuacions en les hormones suprarrenocorticales.
- Tractament mèdic amb antagonistes el receptor de mineralcorticoides (ARM): en els casos amb HAP deguts a malaltia bilateral (hiperplàsia o aldosteronoma bilaterals), com a preparació a la cirurgia i per a aquells pacients en què la cirurgia està contraindicada o la rebutgin. L'espironolactona és l'ARM de primera elecció, utilitzant-se l’eplerenona com a alternativa en el cas que apareguessin efectes secundaris per l'ús de l'espironolactona.
- Administració de glucocorticoides: en els casos d’hiperaldosteronisme sensible a glucocorticoides, utilitzant-se la dosi més baixa possible que aconsegueixi disminuir l'ACTH per normalitzar els nivells de pressió arterial (PA) i potassi. Per a això s'utilitzarà la dexametasona com a primera línia, i la prednisona com a alternativa. En els casos en què no sigui suficient l'administració de glucocorticoides, es pot afegir un ARM.
A més, s’aconsellaran canvis en l'estil de vida per a un millor control de la PA com: control del pes corporal, evitar el consum de tabac, fer exercici regular i una dieta restringida en sodi.
5.3. Feocromocitoma
Els feocromocitomes són tumors gairebé sempre benignes secretors de catecolamines (adrenalina, noradrenalina i dopamina) que s'originen en les cèl·lules cromafines de la medul·la suprarenal o en els ganglis simpàtics o a les seves proximitats (paragangliomes). La majoria són esporàdics i hipersecretors de catecolamines i sense tractament poden associar-se amb una elevada taxa de morbimortalitat cardiovascular.
Manifestacions clíniques
Els pacients amb feocromocitones esporàdics solen presentar tumors grans associats a quadres clínics indicatius d’hipersecreció adrenèrgica, podent experimentar els següents signes i símptomes:
- Hipertensió arterial: es tracta del signe més comú, podent ser permanent (aproximadament a la meitat dels pacients) o paroxística (en la tercera part dels pacients), presentant normotensió la resta de pacients.
- Hipotensió ortostàtica (70% dels casos sense tractament)
- Cefalea pulsativa: d'intensitat i durada variables (freqüent en la major part dels pacients simptomàtics)
- Sudoració profusa (60-70% dels casos)
- Visió borrosa
- Vertigen
- Ansietat
- Dispnea
- Taquicàrdia / palpitacions (són habituals)
- Dolor toràcic
- Rubor
- Fredor en mans i peus: produïts per la vasoconstricció perifèrica.
- Tremolor
- Poliúria, polidípsia
- Dolor abdominal
- Vòmits i diarrea
- Crisi de pànic, debilitat generalitzada i dispnea: més freqüent en els tumors productors d'adrenalina.
- Altres (menys comuns): hiperglucèmia, restrenyiment, papil·ledema, hipercalcèmia o poliglobúlia.
La triada clàssica, present a la quarta part dels pacients amb feocromocitoma, consisteix en l'aparició d'episodis de cefalea paroxística, diaforesi i taquicàrdia / palpitacions en el pacient amb hipertensió. La durada dels episodis pot ser variable, tot i que no sol ser superior a 30-40 minuts. Amb el pas del temps els episodis es fan cada vegada més freqüents, intensos i duradors.
S'han descrit desencadenants que poden precipitar les crisis adrenèrgiques o paroxismes d'hipertensió, entre els quals es troben: la ingesta d'alcohol i aliments que continguin tiramina, la palpació del tumor, la inducció anestèsica o la maniobra de Valsalva.
Diagnòstic
Les indicacions per realitzar el cribratge de feocromocitoma són:
- Clínica suggestiva: triada clàssica, símptomes adrenèrgics, especialment si són paroxístics o estan precipitats pels desencadenants descrits.
- Hipertensió arterial resistent o en persones joves.
- Antecedents familiars de feocromocitoma.
- Síndromes hereditàries relacionats amb tumors productors de catecolamines
- Incidentaloma suprarenal.
En aquests casos amb sospita de feocromocitoma s'ha de fer un estudi bioquímic, confirmant el diagnòstic davant la presència d'elevació de catecolamines i metanefrinas fraccionades plasmàtiques o urinàries.
Un cop confirmat el diagnòstic bioquímic, es realitzarà un estudi de localització, mitjançant una TC (abdominopèlvica) o una ressonància magnètica (RM).
Tractament
El tractament d'elecció per als feocromocitomes és la resecció quirúrgica, mitjançant l’adrenalectomia laparoscòpica o la laparotomia oberta (indicada en tumors de grans dimensions o invasius), tractant-se de l'única opció curativa.
L'elevada morbimortalitat perioperatòria, causat per l'excés de catecolamines, amb una taxa de mortalitat del 30-45% dels casos s'ha vist reduïda fins al 0-2,9% amb les actuals tècniques quirúrgiques i la preparació mèdica que es realitza prèvia a la intervenció.
El tractament mèdic previ a l’intervenció, es realitza per prevenir les complicacions cardiovasculars (crisi hipertensiva i arrítmies) durant el període perioperatori. Aquest consisteix en:
- Bloqueig adrenèrgic (mitjançant el bloqueig de receptors alfaadrenèrgics): es realitza amb l'objectiu de controlar l’hipertensió arterial, a més de reduir el risc i la gravetat de possibles crisis hipertensives durant la intervenció, secundàries a l'alliberament massiu de catecolamines amb la manipulació del tumor.
- Per això solen utilitzar-se com a primera opció els bloquejadors dels receptors alfaadrenèrgics (fenoxibenzamina, doxazosina, prazosina i terazosina), podent-se afegir antagonistes el calci (nicardipino), quan no s'aconsegueix un control de la pressió arterial adequat, i la metirosina en associació amb bloquejadors alfa si no són efectius els fàrmacs anteriors.
Es recomana iniciar el tractament 10-14 dies abans de la intervenció quirúrgica. - Expansió de volum: els nivells elevats de catecolamines causen una vasoconstricció crònica amb disminució del volum circulant. Previ a la intervenció quirúrgica i passats 2-3 dies després de l'inici del tractament amb bloquejadors alfa, es recomana iniciar una dieta amb alt contingut en sodi (5 g / dia) i ingesta de fluids abundant (2,5 l / dia) amb l'objectiu de reposar el volum intravascular, prevenint d'aquesta manera l’hipotensió greu després de la disminució brusca dels nivells de catecolamines un cop reseccionat el tumor.
La nit prèvia a la intervenció, es recomana iniciar seroteràpia administrant 1-2 litres de solució salina isotònica, excepte en els casos en què hi hagi insuficiència cardíaca congestiva o renal concomitant.
Cal destacar que, tot i realitzar-se una adequada preparació mèdica prèvia, pot produir-se inestabilitat hemodinàmica durant la cirurgia, especialment amb l’intubació o amb la manipulació del tumor. Pot administrar nitroprussiat de sodi, fentolamina o nicardipino en aquests casos per revertir la crisi.
5.4. Malaltia d'Addison
La malaltia d'Addison és la forma més freqüent d'insuficiència suprarenal o hipofunció suprarenal. Es tracta d'un trastorn relativament infreqüent, que pot presentar-se en totes les franges d'edat i en ambdós sexes.
Els trastorns autoimmunitaris constitueixen la causa més freqüent de la malaltia d'Addison. En aquests els anticossos circulants reaccionen específicament contra el teixit suprarenal, causant la destrucció de la glàndula, produint una disminució en la secreció d'andrògens, mineralcorticoides i glucocorticoides.
La malaltia d'Addison també pot desenvolupar, per altres causes com:
- Infeccions (tuberculosi, infeccions micòtiques)
- Hemorràgia en les glàndules suprarenals
- Adrenalectomia bilateral
- Neoplàsies
- Causes d'hipofunció secundària com: hipopituarisme, supressió brusca de tractament amb corticoesteroides en tractaments de llarg termini o l'extirpació d'un tumor no endocrí secretor de corticotropina.
La crisi suprarenal aguda/crisi addisoniana aguda es produeix quan el magatzem corporal de glucocorticoides s'esgota a causa d'un traumatisme, infecció, cirurgia o un altre estresor fisiològic. Es tracta d'una urgència mèdica que necessita tractament immediat, ja que pot sobrevenir el coma i la mort.
Manifestacions clíniques
Les manifestacions clíniques típiques de la malaltia d'Addison inclouen:
- Coordinació deficient
- Depressió, labilitat emocional, confusió i apatia (20-40% dels casos)
- Alteracions cardiovasculars: hipotensió ortostàtica, disminució de la despesa cardíaca, pols feble i irregular
- Debilitat muscular o fatiga
- Hipotensió
- Hipoglucèmia en dejú
- Anorèxia i pèrdua de pes
- Desig de consumir aliments salats
- Símptomes gastrointestinals: nàusees, vòmits, restrenyiment o diarrea crònica
- Amenorrea
- Enfosquiment de cicatrius i àrees de vitiligo
- Increment en la pigmentació de la pell i mucoses
- Alteracions electrolítiques: hiperpotassèmia, hiponatrèmia i hipercalcèmia.
En la crisi addisoniana aguda trobarem:
- Alteracions neurològiques: letargia, confusió, coma.
- Cefalea
- Hipotensió arterial o xoc d'origen mixt (hipovolèmic i distributiu) resistent al tractament (aportació de volum i drogues vasoactives)
- Febre
- Profunda debilitat i fatiga
- Nàusees i vòmits intensos
- Dolor abdominal
- Signes d'irritació peritoneal
- Diarrea
- Deshidratació
- Cianosi
- Alteracions de laboratori com: hipoglucèmia, acidosi metabòlica, hiperpotassèmia, hipercalcèmia, hiponatrèmia i hipoclorèmia.
Diagnòstic
Davant la presència de les manifestacions descrites anteriorment, es sospitarà d’hipofunció suprarenal si apareixen les següents alteracions analítiques:
- Disminució dels continguts plasmàtics de cortisol i sodi sèric
- Disminució de glucosa en dejú
- Increment de les concentracions de corticotropina, potassi i nitrogen ureic (BUN) sèrics
Tractament
El reemplaçament de corticoesteroides, amb cortisona o hidrocortisona, és el tractament primari crònic en els pacients amb hipofunció suprarenal primària o secundària.
En el cas de la crisi addisoniana és necessària una intervenció immediata, incloent-hi els següents aspectes:
- Vigilància en l'aparició d'alteracions en el nivell de consciència que puguin comprometre la permeabilitat de la via aèria (progressió a l'estat de coma) i valoració de l'estat respiratori del pacient.
- Monitoratge hemodinàmic: valorant la presència de possibles arítmies secundàries a alteracions electrolítiques, signes de xoc, etc.
- Administració immediata de glucocorticoides: habitualment s'utilitzen dexametasona i hidrocortisona via endovenosa, passant-se a via oral un cop estabilitzada la fase aguda i en funció de la tolerància del pacient.
- Restabliment de l'equilibri hidroelectrolític: reposició de líquids mitjançant l'ús de cristal·loides, en funció de l’hemodinamia i la diüresi del pacient, afegint vasopressors si no hagués respost al tractament inicial. Monitoratge dels desequilibris electrolítics, realitzant un reemplaçament si calgués.
- Vigilància de les xifres de glucèmia, administrant-se glucosa endovenosa si calgués.
5.5. Síndrome de Cushing
La síndrome de Cushing és la manifestació clínica de la hiperfunció suprarenal, causat per les quantitats excessives d'hormones adrenocorticals (principalment cortisol) i en menor mesura aldostersona i andrògens.
En la síndrome de Cushing es produeix una pèrdua d'inhibició de la retroalimentació normal del cortisol, donant com a resultat quantitats excessives de cortisol circulant. Entre les causes que poden produir-ho trobem:
- Malaltia de Cushing: per hipersecreció hipofisària de corticotropina.
- Iatrogènica: per l'administració de glucocorticoides sintètics de manera mantinguda i a altes dosis.
- Tumor suprarenal (causa menys freqüent)
- Tumors secretors de corticotropina en un altre òrgan: especialment carcinoma broncogènic o pancreàtic (poc freqüent)
Manifestacions clíniques
En la síndrome de Cushing podem trobar els següents signes i símptomes, derivats de l'excés de cortisol principalment:
- Alteracions de la personalitat
- Estats confussionals, idees delirants
- Alteracions de la son
- Hipertensió i insuficiència cardíaca
- Aspecte de "cara de lluna plena"
- Rubor facial
- Debilitat muscular
- Fatiga, cansament
- Increment de pes
- Obesitat troncal, amb aprimament de les extremitats (amb pèrdua de múscul i greix)
- Intolerància a la glucosa, podent desenvolupar hiperglucèmia i diabetis
- "Giba de búfal" al coll (hipercifosi)
- Miopaties i osteoporosi
- Pell fràgil i fina, que es lesiona amb facilitat
- Estries cutànies porpra
- Hematomes
- Deteriorament en la cicatrització de ferides
- Disminució de la libido
- En dones: hirsutisme, amenorrea, atròfia de les mames, engrossiment de la veu i engrandiment del clítoris.
- Els motius principals pels quals necessiten el seu ingrés a Cures Intensives són:
- Alteracions greus del metabolisme hidrocarbonat o de l'equilibri hidroelectrolític: fonamentalment hipopotassèmia.
- Complicacions derivades de la hipertensió arterial: cardíaques o neurològiques.
Diagnòstic
El diagnòstic de la síndrome de Cushing es basa en la presència de xifres elevades de cortisol plasmàtic i en orina, confirmant-se mitjançant la realització d'una prova de supressió amb dexametasona (administració de dosis baixes de dexametasona durant la nit), en què s'evidencia la impossibilitat de suprimir la producció de cortisol.
Una prova de supressió de dexametasona amb dosis elevades i una prova de corticotropina en plasma, poden determinar a més la causa de la síndrome de Cushing.
Les proves d'imatge (TC, angiografia, RM) poden ajudar en la localització de tumors.
Tractament
El tractament de la síndrome de Cushing va dirigit a tractar la causa que el desencadena, mitjançant:
- Cirurgia: per a la resecció de tumors hipofisaris (hipofisectomia transesfenoidal) o suprarenals (adrenalectomia unilateral o bilateral).
- Radioteràpia: com a part del tractament de tumors.
- Fàrmacs: en tumors no endocrins o si el tumor és inoperable, mitjançant l'ús d'inhibidors d'enzims suprarenals (com mitotano, ketoconazol, metirapona o aminoglutetimida), vigilant de prop per si sorgeixen símptomes per un funcionament suprarenal inadequat a més d'efectes secundaris dels mateixos fàrmacs.
Reducció gradual dels corticoesteroides, si es deu a la seva administració, a les dosis mínimes requerides pel tractament de la patologia subjacent.
6. ALTERACIONS PANCREÀTIQUES
El pàncrees està situat en la corba del duodè, estenent-se horitzontalment darrere de l'estómac i expandint-se fins a la melsa. Presenta funcions tant endocrines com exocrines.
Els illots de Langerhans realitzen la funció endocrina produint, a partir de les cèl·lules que el composen, les hormones somatostatina, glucagó i insulina.
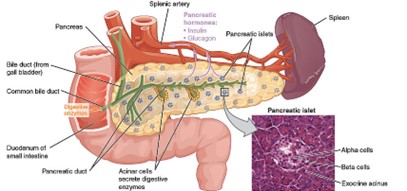
Il·lustració 11 Pàncrees i cèl·lules que el componen
Font wikimedia commons
La insulina és una hormona anabòlica o d'emmagatzematge, que té com funció principal reduir els nivells de glucèmia promovent la captació de la glucosa en el teixit adipós, incrementant l'emmagatzematge del greix dels aliments, a més de al fetge i el múscul esquelètic, on formen glucogen a partir de la glucogènesis. La insulina inhibeix a més la lipòlisi. El seu efecte metabòlic es troba contrarestat per hormones contrareguladores com el glucagó i les catecolamines.
La diabetis mellitus és una patologia clínica associada a hiperglucèmia, com a trastorn metabòlic principal, causada per una deficiència d'insulina o resistència, absoluta o relativa, a aquesta. Hi ha tres tipus de diabetis mellitus.
- Diabetis mellitus tipus 1 (5-10% dels casos de diabetis): aquest tipus de diabetis es caracteritza per presentar una destrucció de les cèl·lules beta del pàncrees, causant declinació i absència de la secreció d'insulina. Es creu que aquesta destrucció es deu a la combinació de factors genètics, immunitaris i ambientals.
- Diabetis mellitus tipus 2 (90-95% dels casos de diabetis): en aquest tipus les cèl·lules beta del pàncrees produeixen insulina, però en quantitats insuficients per contrarestar les resistències que presenten els teixits a la seva acció. Aquest tipus de diabetis apareix amb més freqüència en persones amb obesitat, antecedents familiars o antecedents de diabetis gestacional.
- Diabetis gestacional: durant l'embaràs es secreten hormones placentàries que causen resistència a la insulina i pot causar diabetis gestacional. Aquesta es defineix com qualsevol grau d'intolerància a la glucosa d'aparició durant l'embaràs. Presenten major risc per al seu desenvolupament les dones amb marcada obesitat, glucosúria, antecedents de diabetis gestacional o familiars de diabetis.
L’hipoglucèmia és la complicació aguda més freqüent i greu en pacients amb diabetis mellitus. Es considera hipoglucèmia quan la persona presenta nivells de glucèmia
A la hipoglucèmia és essencial la seva confirmació i tractament precoç mitjançant l'aportació de glucosa. Aquesta aportació es realitzarà via oral si el pacient pot ingerir, mitjançant l'aportació d'hidrats de carboni d'absorció ràpida o via endovenosa, amb l'administració de glucosa, o bé mitjançant l'administració de glucagó, endovenós o subcutani, si el pacient no pot ingerir.
En la banda oposada trobem complicacions derivades de la hiperglucèmia, com són la cetoacidosi diabètica i l'estat hiperglucèmic hiperosmolar no cetòsic.
6.1. Cetoacidosi diabètica
La cetoacidosi diabètica (CAD) és una complicació aguda de la crisi hiperglucèmica relacionada característicament amb la diabetis mellitus tipus 1, tant en pacients ja diagnosticats com en els debuts de la patologia, podent-se presentar també en persones amb diabetis mellitus tipus 2, amb menys freqüència (10-30% dels casos), en situacions d'estrès significatiu o patologia aguda.
La CAD es produeix per un dèficit absolut d'insulina disponible, com succeeix en el debut de la diabetis mellitus tipus 1 o quan s'abandona la teràpia insulínica, o un dèficit relatiu, relacionat amb un increment d'hormones contrarreguladores (glucagó, catecolamines, cortisol i hormona de creixement).
Davant la disminució de la insulina efectiva circulant es produeix una menor captació de glucosa a les cèl·lules. Com a resultat es produeix un augment en la producció de glucosa a través de la gluconeogènesi (en fetge i ronyó), la glicogenòlisi (a partir del glucogen) i la lipòlisis (a partir dels àcids grassos), amb una disminució en la seva utilització perifèrica que causa hiperglucèmia i hiperosmolaritat.
L'increment de la lipòlisi condueix a una major producció de cossos cetònics, donant lloc a l'aparició de cetonèmia i acidosi metabòlica. La cetonèmia, al costat de la hiperglucèmia existent, produeixen una diüresi osmòtica amb poliúria que genera deshidratació i una important pèrdua d'electròlits. L'acidosi metabòlica per la seva banda afecta a més en les concentracions de potassi sèric, incrementant-se a mesura que empitjora l'acidosi.
La gravetat de la CAD ve determinada principalment pel grau d'acidosi metabòlica, els nivells de bicarbonat i l'estat del nivell de consciència del pacient.
Entre les causes que poden precipitar el desenvolupament de la CAD trobem:
- Insuficiència o absència d'insulina
- Falta d'adherència a la teràpia insulínica
- Infeccions
- Patologies agudes (infart agut de miocardi, sèpsia, pancreatitis i traumatismes).
- Estresors físics o emocionals
- Cirurgies
- Fàrmacs (glucocorticoides, antipsicòtics atípics)
La causa més comuna en el desenvolupament de la CAD són les infeccions.
Manifestacions clíniques
Els pacients amb CAD solen presentar signes i símptomes poques hores després de l'inici de l'episodi, entre els quals trobem:
- Alteracions en el nivell de consciència des de letargia, obnubilació a coma.
- Cefalea
- Visió borrosa
- Hipotensió ortostàtica
- Hipotensió i taquicàrdia amb pols feble
- Xoc (en casos greus)
- Respiració de Kussmaul (hiperventilació amb respiracions ràpides i profundes).
- Poliúria, polidípsia i polifàgia
- Nictúria
- Sequedat de mucoses i signe del plec positiu
- Pèrdua de pes
- Debilitat i rampes musculars
- Símptomes gastrointestinals: anorèxia, nàusees, vòmits i dolor abdominal difús.
- Alè amb olor afruitat (produït per l'acetona)
- Hiperglucemia
- Cetonèmia i cetonúria
- Hiponatrèmia (el sodi sèric pot ser normal o elevat en situacions de pèrdua important de volum)
- Hiperpotassèmia
- Increment en les xifres de creatinina, nitrogen ureic en sang i hematòcrit, com a conseqüència de la deshidratació.
La presència d'alteracions de l'estat mental, respiració de Kussmaul o alè afruitat indiquen CAD evolucionada.
Diagnòstic
El diagnòstic de la CAD es basa en la clínica, a més d'en les troballes de laboratori que s'indiquen a continuació:
- Hiperglucèmia (250-800 mg / dl, superior en pacients en coma)
- Acidosi metabòlica (pH <7,3) o bicarbonat
- Glucosúria, cetonúria i cetonèmia
En l'ECG es pot apreciar a més alteracions relacionades amb la hiperpotassèmia.
Tractament
Es tracta d'una complicació potencialment mortal de la diabetis mellitus si no es reconeix i tracta a temps.
Un cop realitzada l'estabilització inicial de la via aèria, la respiració i la circulació com a prioritat, el tractament específic de la CAD es basa en:
- Correcció de la hipovolèmia: es realitzarà mitjançant una reanimació amb volum utilitzant solució salina isotònica inicialment, substituint-se posteriorment per altres solucions segons les necessitats del pacient (com la solució salina hipotònica o el sèrum glucosat al 5%). El pacient pot necessitar el pacient fins 6-10 L de líquids endovenosos per reposar les pèrdues causades per la hiperventilació, la poliúria, els vòmits i la diarrea.
L'expansió de volum contribueix a la correcció de l’inestabilitat hemodinàmica, l'eliminació de glucosa i cetones via renal, la millora de la sensibilitat a la insulina i la reducció dels nivells hormonals contrareguladors.
- Vigilància i reposició d'electròlits, principalment el potassi, en funció dels resultats de les proves de laboratori.
- Correcció de la hiperglucèmia gradualment: es realitzarà mitjançant la infusió endovenosa d'insulina de manera regular, per mantenir els nivells de glucosa en sang entre 150-200 mg / dl, realitzant mesuraments horaris de la glucèmia per a un adequat control d'aquesta. Després de l'estabilització de la glucèmia es reiniciarà la teràpia subcutània d'insulina, retirant l’endovenosa.
Es vigilarà la possibilitat que es produeixi hipopotassèmia, pel fet que amb l'aportació d'insulina el potassi es mobilitza cap a l'espai intracel·lular, podent causar arítmies cardíaques.
- Correcció de l'acidosi metabòlica: a mesura que es normalitza la glucèmia, mitjançant la fluidoteràpia i l'aportació d'insulina, es corregeix l'acidosi.
6.2. Estat hiperglucèmic hiperosmolar no cetòsic (HHS)
L'estat hiperglucèmic hiperosmolar no cetòsic és una descompensació metabòlica aguda greu relacionada amb la diabetis mellitus tipus 2. Es caracteritza per la presència d'hiperglucèmia marcada (600-1200 mg / dl), hiperosmolaritat plasmàtica (> 320 mOsm / L, pH> 7, 3) i greu deshidratació sense cetoacidosi.
És una complicació potencialment mortal, amb una taxa de mortalitat 10 vegades superior respecte la CAD. El resultat clínic i el pronòstic en el HHS estan determinats per factors com: l'edat, el grau de deshidratació i la presència o absència d'altres comorbiditats concomitants.
El HHS presenta una fisiopatologia similar a la CAD, amb la diferència que el HHS s'associa a uns nivells més alts d'insulina i més baixos de glucagó, sent aquests nivells d'insulina suficients per suprimir la lipòlisis i la cetogènesi (producció de cossos cetònics), presentant una cetonèmia i acidèmia molt lleus o absents. No obstant això, els nivells d'insulina són insuficients per prevenir la hiperglucèmia, presentant xifres més grans que en la CAD, la hiperosmolaritat plasmàtica i la deshidratació, sent aquestes més greus en el HHS en comparació amb la produïda en la CAD presentant més risc de col·lapse cardiovascular.
Entre les causes que poden precipitar el desenvolupament de l'HHS trobem:
- Infecció (respiratòria, gastrointestinal, genitourinària)
- Fàrmacs (diürètics tiazídics, beta bloquejants, glucocorticoides, antipsicòtics atípics)
- Patologies agudes cardiovasculars (ictus, angina de pit i infart agut de miocardi)
- Diàlisis
La causa més freqüent de l’HHS, de la mateixa manera que a la CAD, és la infecció.
Manifestacions clíniques
El desenvolupament de l'HHS és menys agut que en la CAD, amb una instauració gradual que pot trigar entre dies i setmanes. A mesura que progressa la síndrome podem trobar els següents signes i símptomes:
- Alteracions en el nivell de consciència: letargia, estupor i coma. Sent aquestes alteracions més grans que en la CAD, causades per una major hiperosmolaritat.
- Dèficit neurològic focal
- Deliris, al·lucinacions
- Major risc d'edema cerebral que en la CAD
- Alteracions en l'agudesa visual
- Freqüència respiratòria normal o taquipnea (si existeix acidosi concomitant)
- Hipotensió, taquicàrdia, pols feble
- Poliúria, polidípsia i polifàgia
- Diaforesi
- Deshidratació severa
- Sequedat en pell i mucoses
- Farciment capil·lar retardat
- Fatiga, debilitat, malestar
- Hipernatrèmia
- Glucosúria
- En el cas que sigui per un procés infecciós poden presentar a més: febre i debilitat general.
- En el cas que sigui per a una patologia cardiovascular poden presentar a més: dolor toràcic, opressió toràcica, palpitacions, cefalea i mareig.
Diagnòstic
Els criteris diagnòstics de l'HHS es defineixen pels següents paràmetres analítics, al costat de la clínica descrita:
- Hiperglucèmia (nivells 600-1200 mg / dl)
- Hiperosmolaritat plasmàtica (> 320 mOsm / L)
- pH arterial> 7,3 i bicarbonat sèric> 15 mmol / L
- Absència de cetoacidosi significativa
A més s'obtindrà informació mitjançant un electrocardiograma, Rx tòrax i / o mostres per a cultiu segons necessiti.
Tractament
Els objectius del tractament de l'HHS es basen a corregir el dèficit de volum de líquids i els desequilibris electrolítics, tractar la causa precipitant i realitzar una correcció lenta de la hiperglucèmia.
Per a això, i de la mateixa manera que ocorre en la CAD, en primer lloc es realitzarà una reanimació inicial prestant atenció a les vies respiratòries, respiració i circulació (ABC), assegurant la via aèria si el pacient presenta una puntuació en l'escala de coma de Glasgow
- Correcció de la hipovolèmia / deshidratació: es realitzarà una reanimació amb volum agressiva, amb solució salina isotònica, amb un bolo inicial de 15-20 ml / kg, seguit d'una velocitat d'infusió de 200-250 ml / h. Es vigilarà estretament el volum administrat per prevenir la sobrecàrrega de líquids i insuficiència i arítmies cardíaques.
- Vigilància i reposició d'electròlits segons necessiti.
- Correcció de la hiperglucèmia gradualment: mitjançant la infusió endovenosa d'insulina de manera regular, per mantenir els nivells de glucosa en sang al voltant de 300 mg / dl per prevenir el desenvolupament d'edema cerebral. Realitzant-se la reposició de líquids endovenosa amb sèrum glucosat al 5%, com en la CAD, quan les xifres de glucèmia disminueixen a 250-300 mg / dl.
BIBLIOGRAFIA
- Hinkle JL, Cheever KH. Enfermería medicoquirúrgica Volumen 1. 14ª Edición. Philadelphia: Wolters Kluwer; 2018
- Aragonés Manzanares R, de Rojas Román JP, Aguiar Flores E, Alcalá Peña MM, Alcalde Perez D, Aldana Díaz EM et all. Cuidados Intensivos: Atención integral al paciente crítico. España: Editorial Médica Panamericana S.A.; 2016
- Grupo de shock. Actualización en Shock: atención del paciente en shock en urgencias [internet]. 3ª edición. España: Bubok Publishing S.L; 2014 [citado 2021 Marzo 2]. Disponible en: actualizacion-de-manejo-del-paciente-en-shock-tercera-edicion.pdf (sborl.es)
- Navío Serrano AM, Abad Esteban F, Aguiló Mir S, Alonso Llasheras JE, Afonso Rivero D, Aragón Leal MA et all. Manejo del paciente en shock en urgencias [internet]. Barcelona: Edikamed S.L; 2011 [citado 2021 Marzo 2]. Disponible en: SHOCK2ED.pdf (grupodeshock.info)
- Camacho JM, Calvo C. Shock: etiología y diagnóstico. An Pediatr Contin. 2003; 1 (3): 119-24
- Avilés García M, Figueira Iglesias JC, Agrifoglio Rotaeche A, Sánches Sánchez M. Bacteriemia, sepsis y shock séptico. Medicine. 2018; 12 (52): 3066-75
- Yébenes JC, Lorencio C, Estebanc E, Espinosa L, Badia JM, Capdevilaf JA et all. Código Sepsis Interhospitalario en Catalunya: modelo organizativo territorial para la atención inciial al paciente con sepsis. Med Intensiva. 2020; 44 (1): 36-45
- Aboal J. Reposición de volumen: ¿Cristaloides o coloides?. Rev Esp Cardiol Supl. 2015; 15 (D): 15-19
- Banchón Alvarado JD, Camacho García DE, Fernández Saquicela CA, Villacís Nieto JM. Conceptos actuales de sepsis y shock séptico. Journal of America Health [Internet]. 2020 [citado 2021 Marzo 2]; 3 (2): 103-116. Disponible en: Conceptos actuales de sepsis y shock séptico | Journal of America health (jah-journal.com)
- Garnacho Montero J, Fernández Mondéjar E, Ferrer Roca R, Herrera Gutiérrez ME, Lorente JA, Ruiz Santana S et all. Cristaloides y coloides en la reanimación del paciente crítico. Med Intensiva. 2015; 39 (5): 303-315
- Levy M, Evans L, Rhodes A. The Surviving Sepsis Campaign Bundle: 2018 update. Intensive Care Med. 2018; 44: 925-928
- Vahdatpour C, Collins D, Goldberg S. Cardiogenic Shock. Journal of the American Heart Assocition [internet]. 2019 [citado 2021 Marzo 2]; 8. Disponible en: Cardiogenic Shock | Journal of the American Heart Association (ahajournals.org)
- Hotchkiss R, Moldawer L, Opal S, Reinhart K, Turnbull I, Vicent JL. Sepsis and septic shock. Nat Rev Dis Primers [internet]. 2016 [citado 2021 Marzo 2]; 2. Disponible en: Sepsis and septic shock - PubMed (nih.gov)
- Kislitsina O, Rich J, Wilcox J, Pham D, Churyla A, Vorovich E et all. Shock- Classification and Pathophysiological Priciples of Therapeutics. Current Cardiology Reviews. 2019; 15 (2): 102-113
- Hernández Palazón J, Fuentes García D, Burguillos López S, Domenech Asensi P, Sansano Sánchez TV, Acosta Villegas F. Análisis de la insuficiencia de órganos y mortalidad en la sepsis por peritonitis secundaria. Med Intensiva. 2013; 37 (7): 461-467
- Rodríguez Botoa G, Rivero Garvía M, Gutiérrez González R, Márquez Rivas J. Conceptos básicos sobre la fisiopatología cerebral y la monitorización de la presión intracraneal. Neurología. 2015; 30 (1): 16-22
- Romero Valdez JG, Pereira Q, Atilio Zini R, Canteros GE. Reacciones de hipersensibilidad. Revista de Posgrado de la Via Cátedra de Medicina [internet]. 2007 [citado 2021 Marzo 2]; 167: 11-16. Disponible en: Microsoft Word - 3_167.doc (unne.edu.ar)
- Sáez Lorenzo L, Sáez Lorenzo M, Sáez Martin V. Revisión y actualización de la fluidoterapia de reanimación en el paciente con shock hipovolémico de origen traumático. Rev enferm CyL. 2016; 8 (1): 3-23
- Carrillo Ramírez SC, Elguera Echavarría PA. Choque circulatorio. Estableciendo metas enla reanimación con líquidos. Acta Medica Grupo Ángeles. 2017; 15 (1): 78-82
- Alemparte Pardavila E, Aller Fernández V, Bouza Vieiro MT, Cortés Cañones JR, Galeiras Vázquez R, García Monge MJ et all. SHOCK: identificación y manejo [Internet]. A Coruña: Seteseis Comunicación Creatividade SL y Complexo Hospitalario Universitario A Coruña (CHUAC); 2011 [citado 2021 Marzo 2]. Disponible en: (PDF) SHOCK: Identificación y Manejo (researchgate.net)
- González Villavelázquez ML, García Gonzalez A. Traumatismo craneoencefálico. Revista Mexicana de Anestesiología. 2013; 36 (1): 186-193
- González Posada MA, Biarnés Suñe A, Naya Sieiro JM, Salvadores de Arzuaga CI, Colomina Soler MJ. Damage Control Resuscitation en el paciente traumático. Rev Esp Anestesiol Reanim. 2019; 66 (7): 394-404
- Narváez I, Canabal A, Martín C, Sánchez M, Moron A, Alcalá J et all. Incidencia y evolución de la miocardiopatía séptica en una cohorte de pacientes con sepsis y shock séptico. Med Intensiva. 2018; 42 (5): 283- 291
- Zariquiey Esteva G, Santa Candela P. A propósito de un caso: intervenciones enfermeras a una paciente con shock anafiláctico en la UCI. Enferm Intensiva. 2017; 28 (2): 80-91
- Sánchez D, Lara B, Clausdorff H, Guzmán A. Generalidades y manejo inicial del shock. ARS MEDICA Revista de Ciencias Medicas. 2018; 43 (3): 66-76
- López Cruz F, Reyes Barragán G, Tapia Ibáñez EX, Paz Cordero DC, Ochoa Morales X, Cano Esquivel AA et all. Choque hipovolémico. An Med (Mex). 2018; 63 (1): 48-54
- Galeiras Vázquez R, Ferreiro Velasco ME, Mourelo Fariña M, Montoto Marqués A, Salvador de la Barrera S. Actualización en lesión medular aguda postraumática. Parte 1. Med Intensiva. 2017; 41 (4): 237- 247
- Dave S, Cho JJ. Neurogenic Shock [internet].StatPearls Publishing; 2021 [citado 2021 Marzo 2]. Disponible en: Neurogenic Shock - StatPearls - NCBI Bookshelf (nih.gov)
- Rhodes A, Evans L, Alhazzani W, Levy M, Antonelli M, Ferrer R et all. Campaña para sobrevivir a la sepsis: recomendaciones internacionales para el tratamiento de la sepsis y el choque septicémico: 2016. Critical Care Medicine. 2017; 45 (3): 486-568
- Haseer Koya H, Paul M. Shock [internet] StatPearls Publishing; 2021 [citado 2021 Marzo 2]. Disponible en: Shock - StatPearls - NCBI Bookshelf (nih.gov)
- Velasco Zúñiga R. Shock. Unidad de Urgencias Pediátricas. Hospital Universitario Río Hortega Valladolid. 2020
- Sabatier C, Monge I, Maynar J, Ochagavia A. Valoración de la precarga y la respuesta cardiovascular al aporte de volumen. Med Intensiva. 2012; 36 (1): 45-55
- Diaztagle Fernández JJ, Rodríguez Murciaa JC, Sprockel Diaz JJ. La diferencia venoarterial de dióxido de carbono en la reanimación de pacientes con sepsis grave y shock séptico: una revisión sistemática. Med Intensiva. 2017; 41 (7): 401- 410
- Palencia Herrejón E, Bueno García B. Nuevas guías de práctica clínica de la «Campana˜ sobrevivir a la sepsis»: lectura crítica. Med Intensiva. 2013; 37 (9): 600-604
- Grupo de trabajo de sepsis. Documento de Consenso (SEMES-SEMICYUC). Recomendaciones del manejo diagnóstico-terapéutico inicial y multidisciplinario de la sepsis grave en los Servicios de Urgencias hospitalarios. Med Intensiva. 2007; 31 (7): 375-87
- Grupo de trabajo de enfermedades infecciosas y sepsis. Estudio nacional de vigilancia de infección nosocomial en servicios de medicina intensiva ENVIN HELICS Informe 2019 [Internet]. España: Sociedad Española de Medicina Intensiva Crítica y Unidades Coronarias (SEMICYUC); 2019 [citado 2021 Marzo 2]. Disponible en: ENVIN-UCI '14 (vhebron.net)
- Ochagavía E, Baigorri F, Mesquida J, Ayuela JM, Ferrándiz A, García X, et al. Monitorización hemodinámica en el paciente crítico. Recomendaciones del Grupo de Trabajo de Cuidados Intensivos Cardiológicos y RCP de la Sociedad Espanola ˜ de Medicina Intensiva, Crítica y Unidades Coronarias. Med Intensiva. 2014; 38 (3): 154-169
- Mateu Campos ML, Ferrándiz Sellés A, Gruartmoner de Vera G, Mesquida Febrer J, Sabatier Cloarec C, Poveda Hernández Y, et al. Técnicas disponibles de monitorización hemodinámica. Ventajas y limitaciones. Med Intensiva. 2012; 36 (6): 434-444
- Grupo código sepsis. Plan de asistencia a la sepsis de Galicia. CÓDIGO SEPSIS [Internet]. Galicia: Xunta de Galicia; 2018 [citado 2021 Marzo 2]. Disponible en: CODIGO_SEPSE_CASTELLANO_WEB.pdf (sergas.es)
- Bravo Jover R, Morcillo Huertas J, Candela AB, Marín Real S, Martínez Baltanás A, Pascual Pérez R. Sepsis en adultos. España: Fisterra; 2020 [citado 2021 Marzo 2]. Disponible en: Guía clínica de Sepsis en adultos (fisterra.com)
- Empendium. Manual panamericano de medicina interna. Shock [Internet]. Polonia: Empendium [citado 2021 Marzo 2]. Disponible en: Shock - Enfermedades cardiovasculares - Enfermedades - Medicina Interna Basada en la Evidencia (empendium.com)
- Gersch C, Heimgartner NM, Rebar CR, Willis LM. Enfermería medicoquirúrgica. 4ªed. Philadelphia: Wolters Kluwer; 2017
- Woodruff DW. Enfermería fácil: Enfermería del paciente en estado crítico. 4ªed. Philadelphia: Wolters Kluwer; 2016
- Picó A, Aranda López I, Sesmilo G, Toldos González O, Japón MA, Luque RM et al. Recomendaciones sobre el diagnóstico e informe anatomopatológico de los tumores neuroendocrinos hipofisarios. Consenso de expertos de la Sociedad Española de Endocrinología y Nutrición y de la Sociedad Española de Anatomía Patológica. Endocrilogía, Diabetes y Nutrición. 2020; 1-12
- Blanco Carrera C, Cabañas Durán M, Tasende Fernández C, Rubio García JA. Tirotoxiocosis e hipertiroidismo. Medicine. 2020; 13 (13): 718-26
- Espinosa de Ycaza AE. Mujer, corazón y tiroides. Rev Colomb Cardiol. 2018; 25 (S1): 42-48
- Caneo C, Aedo I, Riquelme MJ, Fardella C. Disfunción tiroidea y trastornos del ánimo: revisión del estado del arte. Rev Med Clin Condes. 2020; 31 (2): 122-129
- Tortosa F, Webb S. Aspectos novedosos en histopatología de la hipófisis. Endocrinol Diabetes Nutr. 2017; 64 (3): 152-161
- Ortiz Flores AE, Araujo Castro M, Pascual Corrales E, Escobar Morreale HF. Síndrome de secreción inadecuada de hormona antidiurética. Medicine. 2020; 13 (18): 1000-6
- García Martínez MA, Martínez de Lagrán Zurbano I, García de Lorenzo y Mateos A. Recomendaciones para el tratamiento nutrometabólico especializado del paciente crítico: respuesta metabólica al estrés. Grupo de Trabajo de Metabolismo y Nutrición de la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias (SEMICYUC). Med Intensiva. 2020; 44 (S1):15-18
- Rojas D. Manejo de los tumores de hipófisis. Rev Med Clin Condes. 2017; 28 (3): 409-419
- Trifu DS, Gil- Fournier Esquerra NG, Peláez Torres N, Álvarez Hernández J. Hipotiroidismo. Medicine. 2020; 13 (13): 727-34
- Pascual Corrales E, Araujo Castro M, Ortiz Florez AE, Escobar Morreale HF. Hipopituitarismo. Medicine. 2020; 13 (15): 856-64
- Díez JJ. Hipoparatiroidismo postquirúrgico: un trastorno de interés creciente entre los endocrinólogos. Endocrinol Diabetes Nutr. 2019; 66 (7): 399-401
- Muñoz Torrez M, García Martín A. Hiperparatiroidismo primario. Med Clin (Barc). 2018; 150 (6): 226-232
- Rodríguez Gómez IA, Bernabeu I, Guillín C, Casanueva FF. Hiperaldosteronismo e hipoaldosteronismo. Medicine. 2016; 12 (14): 787-94
- Iturregui Guevara M, Larrán Escandón L, López Tinoco C. Enfermedades de la secreción de aldosterona. Medicine. 2020; 13 (19): 1072-82
- Araujo Castro M, Pascual Corrales E, Ortiz Flores AE, Escobar Morreale HF. Eje hipotálamo hipofisario. Fisiología y patología. Medicine. 2020; 13 (15): 846-855
- Galofre Martínez MC, Daguer Menco A, Rodríguez Cantillo J, Ramos Villegas Y, Barciela E, Moscote Salazar LR. Disfunción tiroidea en el paciente crítico: fisiopatología, evaluación y manejo. Acta Colomb Cuid Intensivo. 2019: 1-6
- Pascual Corrales E, Araujo Castro M, Ortiz Flores AE, Escobar Morreale HF. Diabetes insípida. Medicine. 2020; 13 (18): 993-9
- Tasende Fernández C, Rodríguez Troyano MJ, Lallena Pérez S, Álvarez Hernández J. Bocio y enfermedad nodular. Medicine. 2020; 13 (13): 709-17
- Mateo Gavira I, Baena Nieto G, García García Doncel L, Torres Barea IM. Actualización sobre el manejo diagnóstico y terapéutico del feocromocitoma y el paraganglioma. Medicine. 2020; 13 (19): 1083-93
- Hinkle JL, Cheever KH. Enfermería medicoquirúrgica Volumen 2. 14ª Edición. Philadelphia: Wolters Kluwer; 2018
- Belda Hofheinz S, Del Villar Guerra P, Palacios Cuesta A. Cetoacidosis diabética. An Pediatr Contin. 2014; 12 (2): 55-61
- Serrano Carmona JL, Luna Aljama J, Parra Moreno MD. Abordaje de la Cetoacidosis diabética: a propósito de un caso. Rev Paraninfo Digital [Internet], 2015; 22 [citado 2021 Abril 2]. Disponible en: http://www.index-f.com/para/n22/178.php
- Adeyinka A, Kondamudi NP. Hyperosmolar Hyperglycemic Nonketotic Coma [Internet] StatPearls Publishing; 2021 [citado 2021 Abril 2]. Disponible en: Hyperosmolar Hyperglycemic Nonketotic Coma - StatPearls - NCBI Bookshelf (nih.gov)
- Ghimire P, Dhamoon AS. Ketoacidosis [Internet] StatPearls Publishing; 2021 [citado 2021 Abril 2]. Disponible en: Ketoacidosis - StatPearls - NCBI Bookshelf (nih.gov)
- García Martínez MA, Martínez de Lagrán Zurbano I, García de Lorenzo y Mateos A. Recomendaciones para el tratamiento nutrometabólico especializado del paciente crítico: respuesta metabólica al estrés. Grupo de Trabajo de Metabolismo y Nutrición de la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias (SEMICYUC). Med Intensiva. 2020; 44 (S1): 15-18
- Vaquerizo Alonso C, Bordejé Laguna L, Fernández Ortega JF. Recomendaciones para el tratamiento nutrometabólico especializado del paciente crítico: introducción, metodología y listado de recomendaciones. Grupo de Trabajo de Metabolismo y Nutrición de la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias (SEMICYUC). Med Intensiva. 2020; 44 (S1): 1-14
- Juan Díaz M, Mateu Campos ML, Sánchez Miralles A, Martínez Quintana ME, Mesejo Arizmendi A. Recomendaciones para el tratamiento nutrometabólico especializado del paciente crítico: monitorización y seguridad.Grupo de Trabajo de Metabolismo y Nutrición de la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias (SEMICYUC). Med Intensiva. 2020; 44 (S1): 44-51
- Savino P, Patiño JF. Metabolismo y nutrición del paciente en estado crítico. Rev Colomb Cir. 2016; 31: 108-27
- Valls Matarín J, del Cotillo Fuente M, Grané Mascarell N, Quintana S. Variación de la masa muscular y el peso en el paciente crítico. Enferm Intensiva. 2015; 26 (3): 86-91
- Vaquerizo Alonso C. Nutrición parenteral en el paciente crítico: indicaciones y controversias. Nutr Clin Med. 2017; 11 (1): 26-41
- Martín López JI, Rodríguez Delgado ME, López Torres G, Albendín García L. Estrategia nutricional y metabólica en el paciente séptico en Cuidados Intensivos. Revisión bibliográfica. Parainfo Digital. 2015; 22
- Zamora Elson M, Martínez Carmona JF. Ruiz Santana S. Recomendaciones para el tratamiento nutrometabólico especializado del paciente crítico: consecuencias de la desnutrición en el paciente crítico y valoración del estado nutricional.Grupo de Trabajo de Metabolismo y Nutrición de la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias (SEMICYUC). Med Intensiva. 2020; 44 (S1): 19-23
- Gutierrez G, Reines HD, Wulf-Gutierrez ME. Clinical review: Hemorrhagic shock. Critical Care. 2004; 8 (5): 373-381
