La mort encefàlica, com a definició clínica, va aparèixer en la dècada dels anys cinquanta, quan Mollaret i Goulon (1959) van examinar per primera vegada a pacients amb un quadre clínic que sobrepassava a l'estat de coma, diferent dels estats comatosos coneguts fins aleshores. A aquest quadre clínic li van cridar "coma Depasse": pèrdua total de la consciència, de la motilitat, dels reflexos, de la sensibilitat i de les funcions vegetatives.
El 1968, el Comitè de la Universitat de Harvard va presentar els primers criteris per al diagnòstic de mort cerebral, que incloïen: coma profund, apnea, absència total de reflexos cefàlics i espinals, electroencefalograma sense activitat cerebral i midriasi en absència d'intoxicació per drogues o en absència d'hipotèrmia, quadre que s'ha de mantenir durant 24 hores com a mínim.
Fins llavors, el significat de la mort d'una persona es referia de manera específica a criteris cardiològics; no obstant això, a partir d'aquest any, el concepte s'amplia a la mort sota criteris neurològics, o el que actualment es coneix com a mort encefàlica.
Els "Criteris de Harvard", al costat del concepte de "coma Depasse" van canviar el paradigma de la mort, entesa com la fi de la persona quan es diagnostica la mort encefàlica, el que ha afavorit que cada vegada sigui més acceptat el principi de la donació com a part integral de les cures a la fi de la vida.
A Espanya, la donació d'òrgans es planteja habitualment a tot pacient en situació de mort encefàlica, si no presenta contraindicacions mèdiques. A més, comptem amb un marc regulador i el suport institucional necessaris per a la pràctica de donació en asistòlia controlada (Tema 4), o en aquells pacients que es preveu que moriran després de la retirada o limitació del suport vital (Limitació del Tractament de Suport vital LTSV) com veurem també en el Tema 4.
Avui dia és una realitat l'ingrés en una Unitat de Cures Intensives per iniciar o continuar amb el tractament de suport vital (ventilació mecànica electiva), amb l'objectiu de possibilitar la donació d'òrgans en pacients amb dany cerebral catastròfic en què s'ha desestimat el tractament per considerar-se fútil (Cures Intensives Orientats a la Donació).
1. DIAGNÒSTIC DE MORT ENCEFÀLICA
La mort encefàlica es defineix com el fracàs complet i irreversible de les funcions de l'encèfal (hemisferis cerebrals, cerebel i tronc de l'encèfal), amb incapacitat per al manteniment autònom de l'homeòstasi corporal, acompanyat de la cessació de la funció cardiocirculatòria i de la ventilació espontània, portant a l'inici del procés de mort i putrefacció.
Qualsevol patologia intracranial greu provoca un augment de la pressió intracranial (PIC), que provoca una disminució de la perfusió cerebral (PPC). La disminució progressiva del flux sanguini cerebral impossibilita mantenir l'oxigenació i el metabolisme cerebral adequat. Quan la PIC s'eleva per sobre de la tensió arterial sistòlica del pacient, cessa definitivament el flux sanguini cerebral i es produeix la mort encefàlica.
No obstant això, certes funcions endocrines i certa activitat metabòlica (consum de glucosa i oxigen), poden persistir durant un curt període de temps. El suport vital avançat permet mantenir aquestes funcions durant 24-48 hores, fent possible l'opció de la donació.
Les patologies que poden evolucionar a mort encefàlica, i en què el pacient pot ser considerat donant són:
- Accident cerebrovascular, isquèmic o hemorràgic.
- Traumatisme cranioencefàlic greu.
- Encefalopatia postanòxica (per parada cardiorespiratòria).
- Alguns tipus de tumor cerebral primari.
Segons el Reial Decret 1723/2012, per certificar la mort encefàlica d'un pacient (coma arreactiu d'etiologia estructural coneguda) sempre cal fer una exploració neurològica sistemàtica, completa i rigorosa, juntament d'un període d'observació o espera apropiat. Aquesta mateixa disposició assenyala que el certificat de mort encefàlica l'han de signar tres metges, dels quals un ha de ser neuròleg o neurocirurgià i un altre d'ells el metge intensivista responsable del pacient, i entre els quals no ha de trobar-se el coordinador de trasplantament ni cap membre de l'equip extractor-trasplantador. L'hora de la mort que es registra en la història clínica és l'hora en la qual es completa i finalitza el diagnòstic de mort, després de la realització de l'exploració neurològica,
Certificar la ME és un diagnòstic que comporta una gran responsabilitat mèdica, ètica i legal, ja que precedeix a la retirada de les mesures de suport, incloent la desconnexió de la ventilació mecànica, i a realitzar l'extracció d'òrgans per a trasplantament.
L'obtenció d'òrgans de morts només pot realitzar-se després del diagnòstic i certificació de mort encefàlica (Annex I de l'RD 1723/2012), i segons les exigències ètiques, els avenços científics en la matèria i la pràctica mèdica acceptades.
Però abans de realitzar l'exploració del potencial donant, cal comprovar que el pacient es troba en unes condicions clíniques adequades que no alterin les troballes de l'exploració neurològica: que hi hagi estabilitat hemodinàmica, que l'oxigenació i ventilació siguin les adequades, que la temperatura corporal sigui> 35º C, que no hi hagi alteracions metabòliques o endocrines que puguin ser la causa del coma, i que el pacient no es trobi sota els efectes de fàrmacs depressors del sistema nerviós central o bloquejants neuromusculars.
Les troballes en l'exploració neurològica que determinen la mort encefàlica es basen en tres pilars: coma arreactiu, absència de reflexos i presència d'apnea.
1.1. Mort troncoencefàlica "aïllada".
És una situació poc freqüent que apareix quan la causa del coma és una afecció purament infratentorial (cerebel i tronc encefàlic), com hemorràgies o Accident Vascular Cerebral (AVC) isquèmic. En aquests casos, la circulació cerebral està present a través de les artèries caròtides internes, i pot aparèixer certa activitat elèctrica en l’electroencefalograma (EEG) durant diversos dies, i encara més si el pacient és portador d'un drenatge ventricular de líquid cefaloraquidi (LCR ); pot haver-hi també presència de potencials evocats, encara que l’exploració neurològica sigui compatible amb mort encefàlica.
En aquests casos, a Espanya el Reial Decret 2070/1999 obliga que, a més de l'exploració clínica, s'ha de realitzar un EEG o una altra prova diagnòstica que demostri l'absència de la funció dels hemisferis cerebrals.
1.2. Exploració neurològica.
Coma arreactiu. El pacient ha de trobar-se en coma arreactiu profund (Glasgow 3), sense resposta motora o vegetativa a l'estímul dolorós, produït en el territori dels nervis cranials. No hi ha d'haver postures de descerebració ni de decorticació. La presència d'activitat motora d'origen espinal (coll, tòrax, abdomen i extremitats), espontània o induïda, no invalida el diagnòstic de mort encefàlica.
Històricament la mort significava immobilitat; però, ja alguns físics i filòsofs com Descartes, van esmentar la persistència de certs moviments en el cos humà després de la mateixa, com per exemple després de la decapitació.
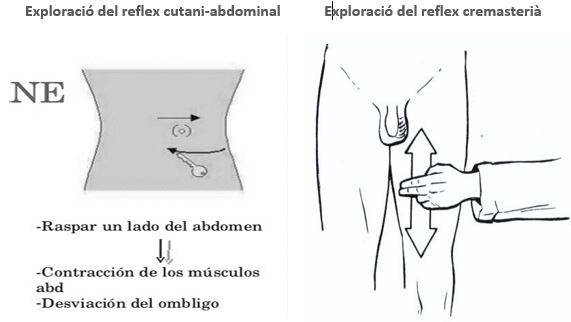
Pot aparèixer activitat motora espinal, tant reflecteix com espontània, (33% al 75% dels casos) en estar la medul·la espinal indemne. Entre els més freqüents es troben el reflex cutani-abdominal (contracció dels músculs abdominals de la mateixa banda on es realitza una estimulació cutània), el reflex cremasterià (elevació del testicle en homes, o contracció del llavi major en la dona, en estimular la cara interna de la cuixa o la massa dels adductors).
Poden apareix també el reflex plantar flexor o Babinski, reflex de retirada, el "signe de Llàtzer" (elevació i aproximació de tots dos braços, i que en la seva presentació més espectacular, s'acompanya de sedestació), moviment en ventall dels dits dels peus "peu ondulant", priapisme, mioclònies espinals, etc.
Exploració del reflex cutani-abdominal Exploració del reflex cremasterià
Reflex de Babinski
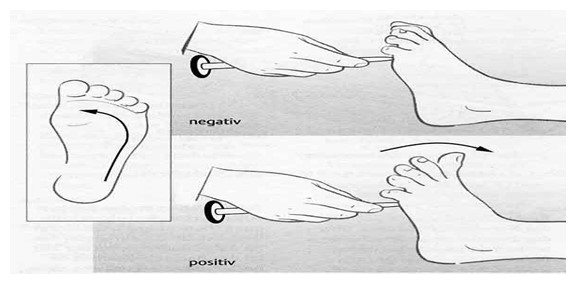
Font: https://cienciaexplicada.com/reflejos-superficiales-cutaneos-y-mucosos.html
Signe de Llàtzer
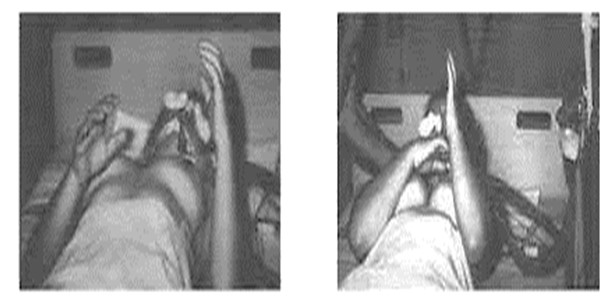
Font: criminòlegs, criminalistes i experts en ciències forenses. Vist a Facebook.
Absència de reflexos troncoencefàlics: fotomotor, corneal, nauseós, tusígeno, oculocefálico i oculovestibular. L'exploració s'ha de fer de manera seqüencial i ordenada en sentit cabal. En situació de mort encefàlica no hauria d'aparèixer cap moviment facial, ni espontani ni per estimulació àlgica (Maniobra de Foix).
Reflex fotomotor: reacció de les pupil·les davant d'una llum potent. Patològic: absència de reacció. S'ha d'explorar tant el reflex directe com el consensual (obrir els dos ulls mentre s'estimula amb la llum cadascun per separat). Pot aparèixer anisocoria sense que això modifiqui el resultat de l'exploració. Les pupil·les estaran midriàtiques, i no hi ha parpelleig espontani.
El reflex fotomotor cal explorar abans de realitzar el test d'atropina, ja que pot alterar-se per l'ús d'aquest fàrmac.
Reflex corneal: contracció palpebral a l'estímul tàctil de la còrnia. Patològic: no hi ha resposta de parpelleig, ni retirada, ni llagrimeig ni enrogiment. S'ha de prestar especial cura en valorar aquest reflex per no danyar la còrnia i produir lesions que impossibiliten la seva donació.
Reflex nauseós: resposta nàusea a l'estímul tàctil de l'orofaringe. Patològic: a l'estimular la base de la llengua, la paret posterior de la faringe, el vel de paladar i l’úvula no apareix cap resposta nàuseosa.
Reflex tussígen: és l'últim reflex que desapareix, i la seva valoració es realitza amb el pacient connectat a ventilació mecànica, assegurant l'aportació d'oxigen, i introduint una sonda d'aspiració pel tub endotraqueal fins a les vies respiratòries baixes. Patològic: no hi ha resposta tussígena en l'estimulació de la via aèria.
Reflex oculovestibular: amb el capçal del llit elevat a 30º, s'injecten 50 cc d'aigua a 4ºC en cada conducte auditiu, mantenint les parpelles berts; els ulls es dirigeixen cap al costat en què s'ha irrigat l'aigua. Patològic: absència de moviments oculars.
Reflex oculocefàlic: mantenint les parpelles obertes, es lateralitza cap a un costat i un altre el cap, amb moviments enèrgics, i els moviments oculars van en contra del moviment cefàlic, "ulls de nina". Patològic: els moviments oculars són sinèrgics als moviments cefàlics.
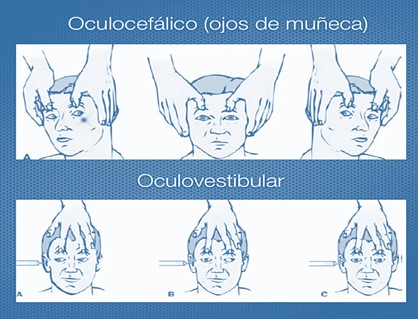
Font: Parells cranials 8: Nervi vestibulococlear. Vist a YouTube
Absència de resposta al "test d'atropina". Resposta cardíaca per l'estimulació del nervi vague amb un agent inhibidor de l'acetilcolina (Atropina). S'ha de fer sempre després de l'exploració clínica, i per un accés venós pel qual no s’infonguin fàrmacs cronotròpics (Dopamina, dobutamina, etc.)
Test d'atropina: després de l'administració endovenosa de 0,04 mg / kg de Sulfat d’Atropina no ha d'existir un increment superior al 10% de la freqüència cardíaca inicial abans d'aplicar el fàrmac.
Apnea demostrada amb el "test d'apnea" o de retirada de la ventilació mecànica, comprovar que no existeixen moviments respiratoris en situació d'hipercàpnia i acidosi (PCO2 en sang arterial> 60 mmHg).
Test d'apnea: es pren una mostra de gasos arterials per verificar que el pH, el pO2 i el PCO2 estan en rang adequat. Es pre-oxigena al pacient amb FiO2a el 100% durant 15-20 minuts. Passat aquest temps, es desconnecta de la ventilació mecànica, col·locant una cànula a prop de la carina amb oxigen al 100%, ja 6-8 litres / minut. Els moviments respiratoris han d'estar abolits. Es cursen gasos arterials seriats post desconnexió de la ventilació mecànica fins a arribar PCO2 > 60 mmHg o pO2
En absència de moviments respiratoris la prova és positiva (patològica).
Juntament amb l'exploració neurològica, la realització de proves instrumentals complementa el diagnòstic de mort encefàlica, sobretot en aquelles situacions que dificulten el diagnòstic clínic. El tipus de prova i el nombre de test a realitzar s'ha de valorar de forma individual, analitzant les aportacions diagnòstiques que proporcionaran les tècniques emprades.
I encara que des d'un punt de vista científic no són obligatòries, en els casos que tenen caràcter d'obligatorietat són:
- Situacions que dificulten el diagnòstic clínic de mort encefàlica.
- Absència de lesió destructiva cerebral demostrable per evidència clínica o per neuroimatge.
- Quan la lesió causal sigui en un principi infratentorial (encèfal i tronc de l'encèfal).
Les proves diagnòstiques s'enquadren en dos grups:
- Proves que avaluen la funció neuronal: electroencefalografia (mostrarà absència d'activitat elèctrica cerebral, o línia isoelèctrica, durant almenys mitja hora) i potencials evocats multimodals (en condicions de mort encefàlica desapareixen les respostes evocades d'origen encefàlic); Índex biespectral BIS® (el valor BIS tendeix a 0 quan esdevé la mort encefàlica, sent 100 el valor d'un pacient despert).
- Proves que avaluen el flux sanguini cerebral: arteriografia, angiografia, angiogammagrafia, i sonografia Doppler transcranial.
- Altres proves instrumentals diagnòstiques que es poden realitzar en mort encefàlica són: anàlisi de l'ona de Pressió Intracraneal (PIC) i pressió de perfusió cerebral (PPC). En pacients en què la mort encefàlica s'ha produït per una hipertensió intracranial refractària, el valor de la PIC apareixerà elevat i la PPC serà de zero o negativa.
En el cas de nounats, lactants i nens, el diagnòstic clínic de mort encefàlica es basa en els mateixos criteris que en els adults, encara que amb algunes peculiaritats:
- En el cas de lactants, l'exploració neurològica ha d'incloure la valoració del reflex de succió i recerca.
- En els nens de fins a 24 mesos és obligatori que la temperatura corporal es trobi per sobre de 35º C abans de realitzar l'exploració neurològica.
- Les proves instrumentals han d'ajustar a l'edat de l'infant.
1.3 Període d'observació.
Per realitzar el diagnòstic de mort encefàlica és necessari conèixer la causa de la lesió cerebral. A més, aquesta lesió ha de ser irreversible.
Es recomana repetir l'exploració neurològica segons períodes ja establerts, i establir més uns períodes mínims d'observació, que s'han de valorar de forma individual, tenint en compte el tipus i la gravetat de la lesió causant (en encefalopaties isquèmic-anòxiques el període d'observació serà més gran que per lesions traumàtiques o vasculars), així com de les proves instrumentals realitzades, que poden determinar escurçar o fins i tot ometre aquest període, segons criteri mèdic.
Si el diagnòstic de mort encefàlica es realitza per la clínica, el període d'observació s'allargarà i es repetirà:
- Davant la sospita de l'ús de fàrmacs depressors del SNC, el període d'observació ha de perllongar segons la vida mitjana dels fàrmacs administrats.
- La normativa espanyola recomana que l'exploració neurològica es repeteixi al cap de sis hores en cas de lesió destructiva coneguda, i a les 24 hores en cas d'encefalopatia anòxica.
- En el cas de nounats i fins a 24 mesos d'edat, es recomana un període d'observació que oscil·la de 24 a 48 hores, tot i que es pot ometre si, amb una prova instrumental diagnòstica, es demostra absència del flux sanguini cerebral.
La llei estableix que el període d'observació és obligatori en els següents casos:
- Pacients sota els efectes de drogues depressores del sistema nerviós central.
- Pacients amb greus deterioraments craniofacials, o qualsevol altra situació que impedeixi una exploració neurològica completa.
- Intolerància al test d'apnea.
- Hipotèrmia, amb temperatura central <32º C.
- Quan no es pot objectivar una lesió destructiva cerebral, ni per l'evidència clínica ni per neuroimatge.
- Quan l'existència d'una lesió irreversible dels hemisferis cerebrals s'ha de demostrar amb una prova instrumental.
2. MANTENIMENT DEL DONANT.
Després de la mort encefàlica d'un pacient, només hi ha dues possibles actuacions:
- Retirar totes les mesures de suport i esperar que el pacient entri en asistòlia.
- Iniciar el procés de donació en mort encefàlica, per a això cal mantenir al potencial donant en condicions fisiològiques òptimes per assegurar la viabilitat dels òrgans.
Els canvis fisiopatològics que esdevenen en una persona després de la mort encefàlica converteixen el potencial donant en un "pacient crític inestable", i obliguen a un monitoratge estricte i específica, i a establir una terapèutica adequada per evitar el deteriorament dels òrgans; d'aquí es deriva que el seu maneig es faci fonamentalment en les Unitats de Crítics, sota metges intensivistes i amb personal d'infermeria especialitzat. Generalment, les morts encefàliques que tenen lloc a les UCIs solen estar més controlades i amb millor maneig terapèutic, ja que la majoria són pacients amb dany neurològic greu que no responen al tractament, i ja des d'aquest moment es comença a plantejar la possibilitat de la donació, tant dins de l'equip assistencial, com a la família.
La mort encefàlica no és una situació estàtica, sinó un procés dinàmic que, a través de múltiples mecanismes, pot afectar significativament la qualitat dels òrgans extraïbles. Per això és fonamental identificar el moment en què els objectius del tractament canvien de ser terapèutics a dirigir-se a l'optimització de la funció dels òrgans per ser trasplantats, és a dir, en el moment que se certifica el diagnòstic de mort encefàlica comença el manteniment del potencial donant.
S'anomena "manteniment del donant" al conjunt de procediments, diagnòstics i teràpies que es fan servir en el possible donant des de l'establiment de la mort encefàlica fins a l'inici de les tècniques de preservació dels òrgans, que es realitza al quiròfan.
Aquest període pot durar des d'unes poques hores fins a diversos dies, la major part transcorre a la Unitat de Crítics, i està relacionat amb les necessitats de la família, requeriments logístics relacionats amb el trasllat dels equips d'extracció, de la disponibilitat i preparació dels quiròfans, i de la necessitat de realitzar proves d'avaluació en el donant.
2.1. Canvis fisiopatològics derivats de la mort encefàlica.
El procés de mort encefàlica provoca en l'organisme una sèrie de canvis fisiopatològics secundaris a la destrucció dels centres encefàlics, que poden derivar en lesions dels òrgans del potencial donant. Aquestes alteracions segueixen una seqüència rostre-cabal, i s'agrupen en tres grans blocs: trastorns hemodinàmics, trastorns hormonals i trastorns secundaris a un procés inflamatori.
Apareixen abans i durant l’enclavament, en l'anomenada fase adrenèrgica-tempesta catecolamínica, i després del procés d'enclavament, un cop instaurada la mort encefàlica, per la pèrdua de tots els mecanismes autoreguladors, i que produiria la mort per asistòlia.
És vital conèixer aquestes alteracions fisiopatològiques per anticipar-nos i poder controlar o minimitzar les complicacions que poden anar apareixent.
La lesió primària supratentorial o hemisfèrica produeix augment de la pressió intracranial, que deriva en una herniació del pacient, sent aquest el patró més freqüent de l'establiment de mort encefàlica. Secundari a la disminució de la pressió de perfusió, es produeix una isquèmia del tronc cerebral, i al seu torn, la isquèmia del mesencèfal activa el sistema parasimpàtic, i fa que inicialment aparegui bradicàrdia i hipotensió; posteriorment, l'afectació del pont activa el sistema simpàtic amb l'aparició de la Tríade de Cushing: Augment de la pressió arterial, respiració irregular i bradicàrdia.
La següent fase apareix amb la isquèmia del nucli vasomotor del bulb, que desencadena la "tempesta catecolaminèrgica", és a dir, alliberament massiu de catecolamines amb estimulació del sistema simpàtic, produint-se una crisi hipertensiva amb taquicàrdies i taquiarrítmies.
Apareix vasoconstricció generalitzada que compromet el flux sanguini dels òrgans, i contribueix a una disfunció del ventricle esquerre, que al costat de la disfunció del ventricle dret per l'augment de la resistència dels vasos pulmonars per la vasoconstricció, afavoreix que es desenvolupi l'edema pulmonar neurogènic.
La posterior destrucció de centre vasomotor bulbar produeix el cessament de la descàrrega catecolaminèrgica, que provoca la pèrdua progressiva de l'autoregulació i del to simpàtic vascular i miocàrdic, portant a una fase d'hipotensió per vasodilatació, amb hipovolèmia relativa i disfunció miocàrdica, de manera que la despesa cardíaca es veu compromès. L'evolució natural d'aquest procés és la hipotensió progressiva i la parada cardíaca.
El centre respiratori també es veu afectat, provocant al principi un patró respiratori irregular, que deriva en l'abolició de l'estímul ventilatori en l'etapa final.
L'afectació de la hipòfisi posterior produeix un dèficit de vasopressina que desencadena una diabetis insípida.
L'afectació del centre regulador de l'hipotàlem pot produir hipertèrmia central en un principi, per acabar amb hipotèrmia a causa de la pèrdua de la termoregulació.
La isquèmia-reperfusió produïda per la tempesta de catecolamines, la baixa despesa cardíaca i el restabliment circulatori a partir del tractament d'elecció, provoquen una intensa reacció inflamatòria que afecta els diferents òrgans.
Aquest patró clínic pot variar en intensitat, depenent de la localització de la lesió inicial o de la velocitat d'aparició de la hipertensió intracranial; així, encara que la inestabilitat hemodinàmica és comú, la durada de la tempesta catecolamínica, la diabetis insípida o la hipo-hipertemia són variables.
La mort encefàlica desencadena a curt termini el cessament de l'activitat cardiocirculatòria, el que portaria a la pèrdua irreversible d'òrgans per a donació. És per això que el correcte manteniment de potencial donant d'òrgans, en condicions òptimes de perfusió i oxigenació, assegura la correcta viabilitat dels òrgans per ser trasplantats.
2.2. Monitoratge al donant potencial.
El monitoratge del potencial donant d'òrgans ha de ser igual de rigorosa que abans de la diagnosi de mort encefàlica.
El monitoratge hemodinàmic serveix de guia per a l'administració de fluïdoteràpia i drogues vasoactives i inotròpiques, necessàries amb el progrés del quadre clínic que hem vist, secundari a la mort encefàlica.
Les recomanacions van dirigides al monitoratge contínua de les constants vitals: electrocardiografia, pressió arterial (catèter arterial), pressió venosa central (catèter venós central), pulsioximetria, temperatura i diüresi, així com el monitoratge hemodinàmica avançada amb catèter Swan-Ganz o sistema Picco (Premi Contour cardíac Output), per conèixer la despesa cardíac continu, sobretot en els casos en què es requereix l’admnistración de catecolamines a dosis altes.
L'ecocardiograma permet valorar la funció cardíaca i avaluar la resposta als fluids, als fàrmacs inotròpics i vasopressores. Podria ser necessari un ecocardiograma transesofàgic si hi ha anormalitats a la paret toràcica o per determinar amb més precisió la funció cardíaca o valvular.
El monitoratge inclou anàlisis de sang general seriats, i proves complementàries específiques (cultius microbiològics, radiografies, ecografies, etc.). El monitoratge de la saturació venosa mixta, i l'excés de bases i el lactat sèric es consideren paràmetres d'utilitat per valorar la perfusió perifèrica dels òrgans en general, i dels quals seran recuperats per a trasplantament en particular.
Segons el "Protocol del manteniment del potencial donant", elaborat per la SEMICYUC (Societat Espanyola de Medicina Intensiva, Crítica i Unitats Coronàries) i l'ONT (Organització Nacional de Trasplantaments), els objectius a assolir i mantenir en el potencial donant són:
- Temperatura corporal:> 35º C
- Pressió arterial mitjana: 60-110 mmHg
- Pressió arterial sistòlica:> 100 mmHg
- Freqüència cardíaca:> 100 ppm
- Pressió capil·lar pulmonar: 8-14 mmHg
- Pressió venosa central: 10-12 mmHg (
- Índex cardíac: 3.0 - 5.0 l / min / m2
- Diüresi:> 1 ml / Kg / h
- Saturació d'oxigen:> 95%
- Glucèmia capil·lar:
- Hematòcrit: 20 - 30%
- Hemoglobina:> 7 g / dl
2.3. Problemes específics i tractament.
El tractament del potencial donant va encaminat a contrarestar les alteracions fisiopatològiques que es produeixen en el procés de mort encefàlica, ja que ha perdut la seva capacitat de resposta fisiològica, i depèn completament del nostre maneig i tractament.
Pèrdua de la respiració espontània. El centre respiratori es veu afectat, provocant al principi un patró respiratori irregular, fins que es produeix l'abolició de l'estímul ventilatori en l'etapa final, sent necessària la ventilació mecànica invasiva per assegurar una bona oxigenació tissular, mantenir l'equilibri àcid-base, i completar el diagnòstic de mort encefàlica del donant (test d'apnea).
L'ús d'estratègies ventilatòries protectores del pulmó: volum corrent 6-8 ml / kg, juntament amb nivells de PEEP elevats, entre 8-10 mmHg, s'ha associat amb l'augment de pulmons viables i recuperats respecte a estratègies ventilatòries més convencionals.
Cal contemplar les complicacions habituals que poden sorgir en un pacient crític connectat a ventilació mecànica: pneumònia associada a ventilació mecànica, administració d'antibiòtics profilàctics en cas de sospita de broncoaspiració o en intubació no electives, etc., i adoptar les mesures habituals de cures per evitar-les, com són el correcte segellat de la via aèria amb la pilota del pneumotaponament, mantenir la capçalera del llit a 30º, aspiració de secrecions, etc.
Hipotensió. La fluïdoteràpia és el tractament d'elecció per mantenir la tensió arterial (TAM> 60 mmHg), diüresi (> 0,5 ml / kg / h), PVC de 3-10 mmHg, i despesa cardíaca adequada, que garanteixen l'adequada perfusió dels òrgans, sempre que el donant estigui monitorat de forma correcta, i així evitar la sobrecàrrega hídrica i l'edema pulmonar neurogènic.
La hipotensió pot alterar la funció d'alguns òrgans, però no suposa una contraindicació per a la donació, sempre que no s'hagi lesionat l'òrgan per trasplantar.
En el cas d'hipotensió refractària, està indicat l'ús de vasopressores si amb la fluïdoteràpia no s'arriba al perfil hemodinàmic marcat, ja que la hipotensió genera hipoperfusió i danyaria els òrgans poden ser donats.
Hipertensió i arrítmies. Apareixen en les fases inicials i s'han de tractar precoçment, ja que provoquen microinfarts cardíacs i poden danyar tots els òrgans poden ser donats. El tractament de primera opció són β-bloquejants (esmolol) en combinació amb vasodilatadors com urapidil, Nitroprussiat o Nicarpidino, segons els valors de la tensió arterial i la freqüència cardíaca.
La tempesta de catecolamines desencadena arrítmies, tant auriculars com ventriculars. La bradicàrdia refractària no respon a l’Atropina, s'administra Dopamina, al costat de simpaticomimètics (Isoprenol o Adrenalina). Si cal, es col·loca un marcapassos extern temporal.
L'hormona tiroïdal, al costat de Vasopresina i Metilprednisolona poden utilitzar per restaurar el to vascular en els casos de gran inestabilitat hemodinàmica que no respon al tractament amb fluids i vasopresores.
La hipotèrmia, les alteracions electrolítiques o la hipoxèmia poden desencadenar arítmies, tant supraventriculars com ventriculars, i un cop corregida la causa, es tracten amb Amiodarona (taquicàrdia supraventricular) o Lidocaïna (taquicàrdia ventricular).
Diabetis insípida neuronal. Després de la mort encefàlica, el dany en l'eix hipotàlem-neurohipòfisi produeix una disminució o inhibició de l'hormona antidiürètica (ADH). Apareix en el 90% dels donants.
La disminució de la ADH produeix la diabetis insípida i cursa amb diüresi> 4 ml / kg / hi disminució de l'osmolaritat urinària. És d'inici brusc i produeix una important disminució de la volèmia, alteracions electrolítiques (pèrdues de potassi, magnesi, calci i fosoforo) i hiperosmolaritat plasmàtica, que poden ocasionar greus trastorns de l'ritme cardíac i inestabilitat hemodinàmica.
Es tracta amb ADH exògena (Desmopresina o Vasopresina), al costat d'una reposició adequada de la volèmia i d'electròlits.
Per normalitzar la volèmia s'administrarà fluïdoteràpia. El sèrum d'elecció dependrà de la situació hidroelectrolítica en què es trobi el donant, sent d'elecció cristal·loides isotònics (Ringer Lactat).
Alteració de les hormones tiroïdals. Síndrome Eutiroideo. La necrosi de la hipòfisi provoca disminució, i posterior desaparició, de les hormones T3 i T4, portant a una acidosi làctica i deteriorament hemodinàmic i cardíac del potencial donant. Alguns autors recomanen administrar hormona tiroïdal costat de corticoides (Hidrocortisona) en cas d'inestabilitat persistent i refractària a amines vasoactives.
Durant el procés de mort encefàlica es pot produir una depleció dels nivells de cortisol i corticotropina (ACTH), i el tractament amb corticoides ajuda a gestionar el control endocrí-metabòlic, i per tant, millorar el control hemodinàmic.
Hiperglucèmia. Apareix secundària a la tempesta de catecolamines, a l'estat inflamatori, a la reducció del metabolisme en mort encefàlica, a la hipotèrmia i a l'ús de corticoides. Es pot produir també una resistència a la insulina que deriva en acidosi metabòlica i cetosi, amb una diüresi osmòtica amb poliúria, que contribueix a la deshidratació del donant. El tractament consisteix en perfusió endovenosa contínua d'insulina ràpida, amb monitoratge horària fins a regularitzar la glucèmia, i la disminució de l'aportació de glucosa exògena. Un cop reguladal glucèmia, es pot continuar amb pauta mòbil d'insulina subcutània.
Control de l'equilibri hidro-electrolític. Mantenir un balanç hidro-electrolític adequat evita l'edema dels òrgans per a trasplantament (pulmó, pàncrees, fetge i ronyons), i assegura una adequada perfusió tissular. Per exemple, una diüresi correcta (1-2 ml / kg / h) indica adequada perfusió renal, i per tant, de tots els altres òrgans.
Alteracions amb el potassi, tant hipo com hiper, són potencialment perilloses per al ritme cardíac, o la hipernatremia en el cas de la funció hepàtica, per la qual cosa han de manejar-se de forma agressiva, amb l'administració i reposició d'electròlits endovenosos.
En el cas d’hipernatrèmia s'administra solució de Dextrosa al 5%. L'excés de solucions salines pot afavorir la hipernatrèmia i la hiperclorèmia.
L'excés de solucions glucosades pot causar hiponatrèmia i hiperglucèmia per deshidratació cel·lular i poliúria.
Alteracions de l'hemostàsia.La destrucció del tronc de l'encèfal, i l'alliberament de material tromboplàstic des del cervell necròtic, així com l’hemodilució, la politransfusió, la hipotèrmia, la coagulopatia de consum, entre d'altres, provoquen alteracions de sistema de la coagulació, que es manifesten amb el desenvolupament de la CID (Coagulació Intravascular Disseminada) i l'aparició de fibrinòlisi, i consum de plaquetes. L'objectiu és mantenir en rang les plaquetes, fibrinogen i protombina.
En general són situacions transitòries i no contraindiquen la donació de cap òrgan. La transfusió d'hemoderivats aconsegueix mantenir un transport adequat d'oxigen, amb un hematòcrit en rang del 20%.
Hipotèrmia. És una manifestació molt freqüent en els donants potencials, secundària a la destrucció de centre termoregulador hipotalàmic. En situacions de mort encefàlica, la pèrdua de control de la temperatura corporal comporta l'aparició d'un estat de poiquilotermia: vasoconstricció perifèrica, disminució del metabolisme cel·lular, pèrdua de la capacitat de tremolar i hipotonia muscular. L'administració de fluids a temperatura inferior a la del donant, i la temperatura del box contribueixen també a l'aparició d'una hipotèrmia espontània i progressiva, d'aparició ràpida, i que un cop instaurada, és difícil revertir, de manera que el millor tractament és la prevenció.
L'objectiu és mantenir la temperatura corporal> 35 º C (en la legislació espanyola s'accepta com a vàlida una temperatura superior a 32º C), utilitzant mantes tèrmiques, administrant líquids calents (37º C) i gasos inspirats calents, augmentant la temperatura ambiental, etc.
És important destacar que una temperatura corporal entre 20º C i 28º C fa que el pacient pugui estar comatós i amb abolició dels reflexos troncoencefàlics, provocant una situació similar a la mort encefàlica.
Les alteracions fisiopatològiques secundàries a la hipotèrmia són greus, i van en proporció a major grau d'hipotèrmia: disminució de la despesa cardíaca, hipotensió arterial, arrítmies (risc de fibril·lació ventricular). Una hipotèrmia
Nutrició. Si bé l'aportació nutricional és fonamental per mantenir les reserves de glucogen hepàtic, un cop instaurada la mort encefàlica es perd el to vagal, i disminueix la motilitat i la capacitat d'absorció intestinal, de manera que la nutrició enteral sol ser mal tolerada. Pot mantenir-se a dosis mínimes com a agent protector.
Si el donant prèviament era portador de nutrició parenteral total (NPT), pot ser útil mantenir-la.
Es recomana el manteniment dels protectors gàstrics i la profilaxi de la trombosi venosa profunda un cop diagnosticada la mort encefàlica.
- CURES INTENSIVES ORIENTADES A LA DONACIÓ D'ÒRGANS (CIOD).
Les Cures Intensives Orientats a la Donació (CIOD) es defineixen com l'inici o la continuació de cures intensives (ingrés a UCI, ventilació electiva no terapèutica (VENT), suport vasoactiu, etc.) en pacients amb dany cerebral catastròfic, en els quals s'ha desestimat el tractament mèdic o quirúrgic amb finalitat curativa per criteris de futilitat, que són considerats com a possibles donants per la seva probable evolució a mort encefàlica, i no tenen contraindicacions mèdiques per a la donació; entenent com a pacient amb dany cerebral catastròfic al pacient amb patologia neurològica greu que comporta un risc de mort imminent.
L'objectiu dels CIOD és incorporar l'opció de la donació d'òrgans com a part de les cures a la fi de la vida (Resolució de Madrid 2010), i comprenen un conjunt de mesures que garanteixen el confort i la dignitat del pacient amb dany cerebral catastròfic en el procés de morir, permeten l'evolució natural a mort encefàlica i asseguren la preservació dels òrgans per a donació.
S'entén com a tractament fútil aquell tractament que es preveu no pot complir els objectius pel que fa a curació de la malaltia o millora dels símptomes, segons el parer dels professionals, basats en l'evidència i en la bioètica, de manera que els efectes nocius de mantenir-lo no compensen amb les expectatives de curació.
Com en tot procés de donació, és imprescindible conèixer la voluntat prèvia del pacient pel que fa a la donació, per la qual cosa l’intensivista al costat del coordinador de trasplantaments, han de verificar que no ha deixat constància expressa de la seva negativa a la donació, per la qual cosa segons el Reial Decret 1723/2012 de 28 de desembre, tots som donants d'òrgans si no hem deixat constància, verbal o escrita, en cas contrari.
Tot i això, s'ha de mantenir una entrevista prèvia amb els seus familiars, en aquells pacients amb dany cerebral catastròfic considerats possibles donants, amb un procés d'informació específic cap a la família, previ a l'evolució a ME, i dirigit a la sol·licitud per instaurar o continuar amb les cures intensives. Aquesta entrevista forma part d'un procés continu de comunicació, adequat a cada família, en el qual s'informa en un principi sobre la situació crítica, el pronòstic fatal i la futilitat del tractament del pacient. Aquesta informació ha de ser progressiva, i ajudant a la família en la comprensió de la informació i en la presa de decisions.
En la següent fase, el coordinador de trasplantaments de sol·licitar la continuació de les mesures de suport amb l'objectiu de permetre la donació un cop instaurada la ME. I un cop diagnosticada, es comunicarà la mort a la família, i es continua amb la sol·licitud del consentiment familiar per a l'obtenció d'òrgans i teixits.
La SEMICYUC (Societat Espanyola de Medicina Intensiva, Crítica i Unitats Coronàries) disposa d'un Codi Ètic com a guia d'aplicació als serveis de medicina intensiva, en el qual es destaca el dret a la informació veritable, comprensible i adequada a les necessitats de cada pacient, i la presa de decisions per representació. Pel que fa al principi d'autonomia del pacient, destaca la importància del consentiment informat, el Document d'Instruccions Prèvies o Voluntats Anticipades i el dret a morir amb dignitat.
A la pràctica, els CIOD han de defensar, i no vulnerar, els quatre principis de la bioètica:
- Principi d'autonomia: fent possible plantejar l'opció de la donació d'òrgans, i possibilitar aquesta opció si el pacient desitjava ser donant.
- Principi de beneficència: la donació pot suposar un consol per a la família davant la pèrdua d'un ésser estimat, a través de valors com la solidaritat i el compromís social. A més, fer extensiu els CIOD com a part del procés de donació, alleuja les llistes d'espera per a pacients que necessiten un òrgan per millorar la seva supervivència o qualitat de vida.
- Principi de no maleficència: els CIOD han de respectar la dignitat del pacient, procurant sempre l'absència de patiment, i assegurant el confort del pacient.
- Principi de justícia: una adequada selecció del possible donant, i arribar a un acord amb la família pel que fa al temps d'espera a l’UCI fins a la instauració de la mort encefàlica, possibilita una gestió eficient i proporcionada dels recursos sanitaris.
En el projecte ACCORD-Espanya-ONT consta que, el temps mitjà d'ingrés a l’UCI d'un pacient amb dany cerebral catastròfic fins que va morir amb l'objectiu de la donació, és d'un dia de mitjana, de manera que la utilització de recursos d'UCI es justifica amb l'ajuda que es proporciona a la sostenibilitat de sistema de donació.
Projecte ACCORD (Achieving Comprehen Sive Coordination in Organ Donation): formen part d'aquest Projecte 15 països europeus, amb 67 UCIs en total, per tal de descriure les pràctiques de cures a la fi de la vida en pacients morts a conseqüència d'un dany cerebral catastròfic.
3.1 Identificació del pacient com a candidat a CIOD.
Quan l'equip mèdic responsable d'un pacient amb dany cerebral catastròfic decideix no s'inicia o retirar les mesures de tractament curatiu, és quan es pot considerar l'opció dels CIOD. Això comporta l'opció de la donació d'òrgans, de manera que el cas s'ha de comunicar al coordinador de trasplantaments, qui avaluarà al pacient, basant-se en dos aspectes: la possibilitat que evolucioni a mort encefàlica en un espai de temps curt, ja que no hi hagi contraindicacions mèdiques per a la donació.
Si es considera que l'evolució a mort encefàlica no es produirà en un curt període de temps, no es plantejarà la possibilitat de CIOD.
La valoració del pronòstic s'ha de fer per un equip multidisciplinari, amb professionals de diferents especialitats (neurologia, medicina intensiva, medicina interna i anestèsia, entre altres), i en la qual el coordinador de trasplantament no ha de participar. Per a la presa de decisions clíniques, "s'ha de buscar un equilibri entre l'evidència científica disponible en els actuals models pronòstics / escales de gravetat, l'experiència clínica i les preferències del pacient expressades verbalment o per representació".
Posteriorment, la selecció del pacient com a possible donant ha d'estar avalada per la valoració del metge intensivista, amb experiència en patologia neurocrítica i en factors pronòstics, i determinada per dades clíniques, monitoratge, i proves complementàries, especialment per un TAC cranial, que ens dóna informació sobre la gravetat de la lesió estructural, la localització, i signes d'hipertensió cranial i herniació cerebral.
Les cures intensives orientades a la donació CIOD s'han de fer respectant l'autonomia i dignitat del pacient, i sempre garantint que no s'incorre maleficència: en tot moment ha d'assegurar el confort i l'absència de patiment al pacient.
Un cop presa la decisió de reorientar l'objectiu terapèutic davant el risc de mort imminent, es notificarà el coordinador de trasplantaments, amb la major antelació possible, perquè es posi en marxa tot el procés de donació. La decisió sobre el pronòstic del pacient i els criteris que modifiquen el pla d'actuació, així com la notificació del cas al coordinador de trasplantaments, ha de constar per escrit en la història clínica del pacient.
Si es determina el dany cerebral catastròfic i es continua amb el procés de CIOD, el coordinador de trasplantaments pren el lideratge per al maneig del possible donant, i comença la valoració indicada en tot donant, que inclou una revisió minuciosa de la seva història clínica, i la realització de les proves complementàries necessàries per descartar la presència d'infeccions cròniques o altres alteracions, i avaluar l'estat dels òrgans per a trasplantament (Tema 2).
No es plantejarà l'opció de CIOD si s'identifiquen contraindicacions absolutes per a la donació d'òrgans.
Algorisme de les cures intensives orientades a la donació
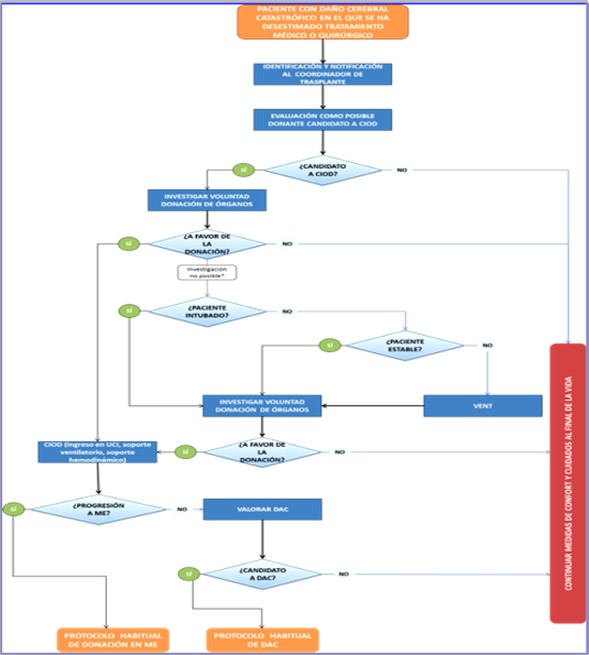
Font: Cures Intensives Orientades a la Donació d'Òrgans. Recomanacions.
3.2 Entrevista amb la família.
En tot procés de donació, la informació a la família i l'obtenció del permís de donació són un dels moments més delicats.
En el cas dels CIOD és encara més dolorós i compromès per la situació que es planteja als familiars, que poden entendre-ho com una prolongació innecessària del patiment el pacient, o donar-los falses esperances pel que fa al pronòstic.
El pacient amb dany cerebral catastròfic pot trobar-se en diferents escenaris, que condicionen com es plantejarà l'entrevista prèvia amb la família, i el posterior maneig clínic del pacient segons la informació proporcionada i la seva decisió.
Pacient fora d'UCI en què no s'ha iniciat ventilació mecànica. Si no hi ha risc de parada cardiorespiratòria imminent, l'entrevista es dirigeix al fet que la família accepti l'opció de la donació, i així el pacient ingressa a UCI per iniciar el procés de CIOD. En el cas que es trobi clínicament inestable, pot considerar l'opció de l'ingrés a UCI i l'inici de la ventilació mecànica per tal de preservar els òrgans per donació, i posteriorment es podrà realitzar l'entrevista amb la família, en unes condicions que permeten dedicar més temps a l'atenció i la informació. Si la família no accepta la possibilitat de la donació, es retiren les mesures de suport vital que s'han iniciat, i es garanteix el confort del pacient mentre evoluciona de forma natural la malaltia.
Si el pacient ha estat intubat i connectat a ventilació mecànica pels Serveis d'Emergències extrahospitalaris, o al mateix Servei d'Urgències, L'entrevista amb la família va dirigida cap a l'opció d'instaurar els CIOD a l'UCI i la posterior donació. Si la família es nega, es retiraran les mesures de suport vital aplicades, reorientant el tractament cap a mesures de confort. També hi ha l’opció de l'ingrés del pacient en UCI i, un cop a la unitat, realitzar l'entrevista amb la família plantejant-los les diferents opcions d'actuació. En les primeres hores d'atenció extrahospitalària o d'ingrés a urgències, la família es troba en un estat de bloqueig psicològic i bloqueig emocional que, de vegades, no els permet assimilar tota la informació.
Pacient ingressat a l'UCI en el qual es planteja la limitació del tractament de suport vital. L'entrevista amb la família es dirigeix al manteniment del pacient com a donant potencial fins a la instauració de la mort encefàlica, o si la família decideix continuar amb la retirada del suport vital, es pot plantejar l'opció de la donació en asistòlia controlada.
En qualsevol cas, s'ha de deixar constància en la història clínica del pacient les opcions que s'han plantejat a la família, i la decisió que aquesta ha pres.
El concepte d'entrevista en CIOD difereix del concepte d'entrevista per a la donació d'òrgans. L'entrevista prèvia es realitza per informar la família de la situació del pacient amb dany cerebral catastròfic, abans que s'instauri la mort encefàlica, i va dirigida a la sol·licitud del consentiment per establir CIOD.
Ha d'estar liderada pel coordinador de trasplantaments, ja que és el professional més format i capacitat per a aquest fi.
La informació ha de ser clara, proporcionant de manera comprensible i adaptada a les necessitats de cada família. Ha de ser progressiva, de manera que al principi s'informarà del pronòstic d'extrema gravetat.
Una vegada que la família ha acceptat el pronòstic fatal, és quan es planteja l'opció dels CIOD, explicant detalladament les mesures terapèutiques necessàries que s'han d'adoptar per a fer possible la donació (intubació orotraqueal, connexió a ventilació mecànica, suport vital, i sobretot que el pacient ingressarà a la Unitat de Cures Intensives), i se'ls informarà que, abans de res, es garantirà el confort i l'absència de patiment el pacient fins a l'evolució definitiva de mort encefàlica.
Ha de comunicar-se que aquesta evolució passa en 24-72 hores generalment, però que a vegades pot perllongar-se, o que finalment passi que no es produeixi la mort encefàlica, de manera que la família ha de saber que sempre té l'opció de canviar la seva decisió, ja que si no es produís en el període de temps consensuat amb la família, o la família no desitja perllongar l'espera, s'hauran de retirar els dispositius aplicats, i les cures estaran orientats cap al manteniment de mesures de confort, i així permetre l'evolució natural de la malaltia.
S'ha de documentar en la història clínica del pacient tota la informació recollida en l'entrevista amb la família, així com deixar constància de la decisió presa; però el consentiment per a l'aplicació dels CIOD no substitueix el consentiment informat per a la donació d'òrgans.
La següent fase de l'entrevista és la que va destinada a sol·licitar el consentiment per a l'inici de mesures de suport, un cop instaurada la mort encefàlica, per a la preservació d'òrgans per a la donació. És un altre document que s'emplena en el moment que es produeix la defunció.
3.3. Cures a la fi de la vida del possible donant.
Tots els professionals de la Unitat de Crítics, metges, infermeres, personal auxiliar, etc., adquireixen la responsabilitat d'assegurar la cura del pacient en el procés de morir, vetllant per la seva dignitat i confort. En aquells pacients que es consideren possibles donants, a més, cal instaurar les mesures de suport necessàries per a assegurar la preservació dels òrgans per a trasplantament, però donant prioritat al confort dins de les cures a la fi de la vida del pacient en situació d'agonia.
Per tant, la teràpia farmacològica que utilitzem en les cures a la fi de la vida tindrà com a objectius pal·liar el dolor, minimitzar la dispnea i controlar el deliri.
- Han de retirar les mesures de neuroprotecció i de control de la hipertensió intracranial (barbitúrics, sedants, drenatge ventricular, solucions hiperosmolars, etc.).
- Els fàrmacs bloquejants neuromusculars (BNM) no s'han d'iniciar mai en situació de limitació del suport vital. Si el pacient els està rebent, han de retirar-se, per poder avaluar els símptomes. Es pot administrar analgèsia i sedació si precisa, d'acord amb els objectius marcats.
- Encara que es considera que els pacients amb dany cerebral catastròfic no senten dolor, dispnea o patiment, hi ha certa incertesa respecte a la possibilitat que quedi algun rastre de percepció residual, ja que a vegades es manifesta amb les respostes fisiològiques típiques del dolor com són la taquicàrdia, hipertonia, sudoració, i taquipnea. La família percep aquestes manifestacions amb veritable angoixa i ansietat; per això, es recomana l'administració de fàrmacs de vida mitjana molt curta (Propofol o Remifentanilo), que suprimeixin aquestes manifestacions i per tant alleugen el patiment de la família, però no interfereixen en el diagnòstic mentre es produeix la mort encefàlica.
- Quan passat el temps d'espera pactat amb la família per al desenvolupament de la mort encefàlica, aquesta no s'ha produït i la família no desitja perllongar l'espera, han de retirar totes les mesures de suport vital i considerar la possibilitat de la donació en asistòlia controlada.
Pel que fa al manteniment del possible donant, fins a la instauració de la mort encefàlica, el maneig serà el mateix que qualsevol pacient crític, però desestimant el tractament per a la hipertensió cranial. La diferència en el manteniment i cures del pacient en el qual es decideixen CIOD, radica que permet anticipar-nos als canvis fisiopatològics que es produeixen en el procés de mort encefàlica. En qualsevol cas, l'objectiu és optimitzar la perfusió i preservar la funcionalitat dels òrgans objecte del trasplantament.
Durant l'ingrés a UCI, el coordinador de trasplantaments completa l'avaluació del possible donant i la viabilitat dels òrgans, de la mateixa manera que en qualsevol altre procés de donació.
- LIMITACIÓ DEL TRACTAMENT DE SUPORT VITAL (LTSV) ORIENTAT A LA DONACIÓ D'ÒRGANS.
Les Unitats de Cures Intensives van sorgir a mitjans de la dècada dels 60 a conseqüència dels importants i ràpids avenços científics i tècnics de la medicina, el que va fer possible instaurar tractaments per resoldre malalties, i millorar la supervivència i la qualitat de vida dels pacients en molts casos que, d'altra manera, haguessin mort irremeiablement. Com a conseqüència, l'atenció mèdica es va tornar més tecnificada, creant la falsa sensació de comptar amb recursos il·limitats per preservar la vida.
Però en cap cas, les tècniques de suport vital permeten curar la malaltia de base, i el manteniment artificial de les funcions vitals no s'ha de confondre amb una millora de la malaltia. Només en aquells casos en què es va resoldre el problema agut, s'aconsegueix que el pacient pugui desconnectar dels equips de suport i recuperar la seva funcionalitat.
Es consideren tractaments de suport vital a l’UCI: ventilació mecànica, teràpies de depuració extrarrenal, fàrmacs vasoactius, la nutrició artificial (enteral i parenteral), els hemoderivats, etc.
A mitjans dels anys 90, coincidint amb un corrent humanista basat en la "Humanització de les UCIs", sorgeix el repte d'administrar adequadament la tecnologia, d'orientar de forma racional l'ús d'aquestes tecnologies cap a protegir la vida en aquells malalts amb patologies recuperables, i limitar-la en aquells casos en què la medicina no ho pot resoldre per no allargar la vida de forma artificial.
Paral·lelament, ha anat canviant la forma de relació metge-pacient, passant de ser una relació paternalista, a convertir-se en una relació d'ajuda en què es dóna prioritat als desitjos del pacient, respectant la seva autonomia, i amb una creixent responsabilitat dels professionals, metges i infermeres, en les decisions de la limitació del tractament de suport vital.

Neix llavors el terme Limitació de l'Esforç Terapèutic (LET) per referir-se a un tractament a la fi de la vida. Però, encara que el terme sigui encertat en referir-se a la retirada de mesures de suport vital, pel que fa a les cures a la fi de la vida se segueixen aplicant mesures terapèutiques per pal·liar el dolor, l'ansietat i millorar el confort del pacient en procés de morir, per tant, l'esforç terapèutic continu.
A la fi dels 80 neix el concepte de Limitació del Tractament de Suport Vital (LTSV), que engloba tant la decisió de retirar o no iniciar les mesures de suport, quan la malaltia és irreversible, o el tractament pot ser inadequat, fútil o inútil, permetent així l'evolució natural i inevitable de la malaltia cap al procés de mort, com l'aplicació de mesures de confort per evitar el sofriment, i adequar les mesures diagnòstiques i de monitoratge a l'objectiu pal·liatiu.
"Si els resultats no són els esperats, no hi ha benefici per al pacient i per tant, es considera que no està indicat seguir amb el mateix, es retirarà. Legal i èticament és el mateix ometre de retirar una teràpia de suport vital".
Tot i així, la situació clínica del pacient canvia en tot aquest procés, de manera que l'adequació de mesures i procediments ha de formar part del pla de cures individualitzades de cada pacient, i seria més encertat utilitzar el terme "adequació de l'esforç terapèutic".
La decisió de LTSV s'ha de prendre per consens dels professionals implicats en la cura del pacient, la SEMICYUC recomana que la decisió de LTSV s'ha de discutir col·lectivament, metges i infermeres, i de prendre per consens. La decisió de LTSV ha d'estar basada en l'evidència mèdica actual, i abans de res prevaldrà el desig del pacient, ja sigui perquè es trobi amb capacitat al moment, o perquè deixi constància a través de la seva voluntat anticipada. L'equip mèdic que atén el pacient ho comunica i explica la situació als seus familiars, i en aquells casos en què no s'està d'acord amb la decisió, la participació del Comitè d'Ètica Assitencial pot resoldre el conflicte i facilita el consens.
"Conèixer les voluntats del pacient davant la presa de decisions, i establir mecanismes per al respecte a la seva voluntat, es concep com una expressió del respecte a la dignitat personal, d'especial rellevància en el final de la vida".
Presa de decisions clíniques
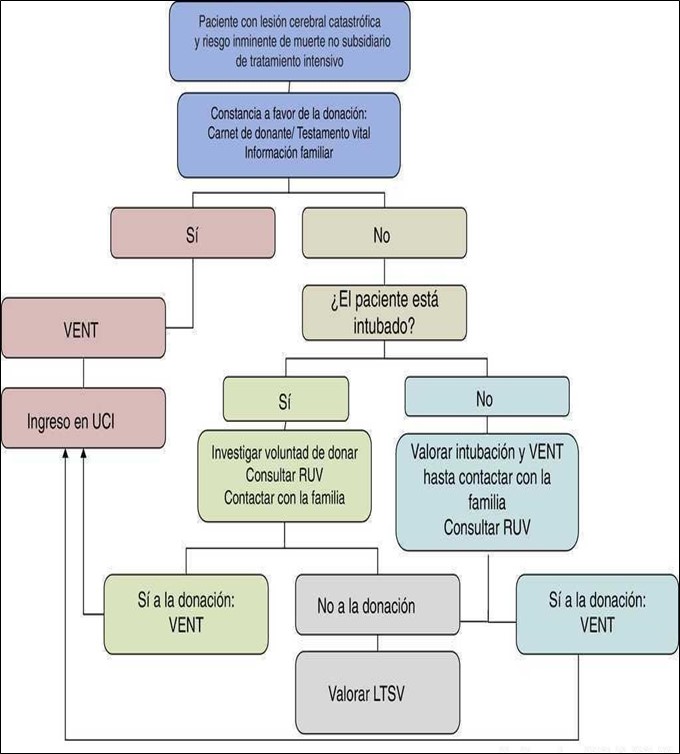
Font: Medicina intensiva i donació d'òrgans. ¿Explorant les últimes fronteres?
NOTA: RUV: Registre d'últimes voluntats.
Perquè el pacient, o els seus familiars, puguin formar part de la presa de decisions se'ls ha d'informar de manera clara, assegurant-se en tot moment que han comprès la informació proporcionada. Mai s'ha de responsabilitzar ni a familiars ni al propi pacient de la decisió, sigui quina sigui, ni el professional ha d'influir ni coaccionar a aquesta decisió.
En aquest punt, cal assenyalar que les mesures de LTSV no tenen implicació penal ni constitueixen fet de delicte, sempre que estiguin avalades amb una adequada indicació i aplicació. La LTSV no produeix la mort del pacient, sinó que permet que arribi com a resultat natural de la seva malaltia; mentre que l'eutanàsia és l'acció directa i intencionada, encaminada a provocar la mort d'una persona prèvia a la seva petició expressa.
Recentment al nostre país s'ha aprovat la Llei Orgànica 3/2021 de 24 de març, que regula l'eutanàsia i el suïcidi mèdicament assistit: el professional sanitari proporciona els mitjans necessaris perquè la persona pugui suïcidar-se de manera efectiva, prèvia petició expressa del pacient.
Continuant amb la definició de termes relacionats amb les cures a la fi de la vida, la "Doctrina del doble Efecte" fa referència a l'administració de fàrmacs per tal de fer possible el màxim confort del pacient, encara que de forma col·lateral suposin escurçar breument la vida del pacient. La DDE no té a veure amb l'administració de fàrmacs per posar fi a la vida del pacient de forma accelerada.
La Societat Espanyola de Cures Pal·liatives defineix com sedació pal·liativa l'administració de fàrmacs a un pacient terminal, previ consentiment exprés i per escrit del pacient o familiar, en les dosis i combinacions de fàrmacs necessàries per reduir el seu nivell de consciència i alleujar els símptomes que li causen patiment.
4.1 Aplicació de la Limitació del Tractament de Suport Vital.
En general, les formes de LTSV en Medicina Intensiva són:
- Limitació per a l'ingrés a l'UCI.
- Ingrés a l'UCI de pacient en els quals ja s'ha decidit retirar o no iniciar algun tipus de mesura terapèutica, inclosa la reanimació cardiopulmonar.
El tipus de LTSV depèn de les característiques de cada malaltia, i fins i tot de cada pacient, considerant com a part del pla de cures a la fi de la vida. Per exemple, es recomana evitar la LTSV en els primers dies d'evolució del pacient amb patologia neurocrítica greu, realitzant en un principi un tractament agressiu amb fins curatius, i observant l'evolució abans de prendre qualsevol decisió.
A la pràctica diària, els escenaris en què ens trobem l'aplicació del LTSV es poden classificar en 5 grups.
Omissió o retirada del suport vital a l'UCI. L'omissió, o no iniciar un tractament, és un acte passiu, basant-se que el tractament no produirà cap benefici per al pacient. A vegades, la futilitat d'un tractament només es pot comprovar observant el resultat "Trial of Therapy", de manera que en un principi s'instaura el tractament, i si no s'obté el benefici esperat, serà retirat.
La retirada del tractament és un acte actiu que suposa una major responsabilitat per al metge responsable del pacient.
"El període de temps des de l'inici de la limitació fins a la defunció del pacient és menor després de la retirada del suport vital que després del no inici, el que suposa escurçar l'agonia per al pacient, i menor estrès per a la família i professionals".
Ordre de no RCP. És la limitació més freqüent, i es planteja tant en el Servei d'Urgències com a l'UCI, com en qualsevol altre servei del propi hospital. El que sí que és comú en qualsevol situació, és que l’ordre de no RCP ha de constar per escrit en la història clínica del pacient, un cop valorada pel metge responsable, i consensuada amb la família, amb el propi pacient si és possible, i amb la resta de l'equip mèdic i d'infermeria.
Ingrés a UCI amb tractament limitat. Es realitza en pacients d'edat avançada i amb gran nombre de comorbiditats, davant l'agudització d'un procés determinat,
per oferir la possibilitat de sobreviure a aquest procés; però es consensua amb la família, i amb el propi pacient, no aplicar tractaments més agressius.
També es considera en aquests pacients l'aplicació de tractaments intensius sense limitacions, condicionats en un temps limitat, generalment 48-72 hores, de tal manera que, si en aquest període de temps el tractament resulta fútil, es retiren les mesures adoptades i el tractament s'orienta cap al confort del pacient.
No ingrés a l'UCI. Aquest tipus de limitació es dóna sempre fora de l'UCI, sigui a Urgències o en qualsevol servei de l'hospital, generalment amb pacient d'edat avançada, amb múltiples comorbiditats i patologies cròniques avançades.
A la Unitat de Crítics, el procés de donació d'òrgans sempre va unit a les cures a la fi de la vida. És fonamental explicar a la família, un cop han acceptat la limitació del suport vital, la possibilitat de la donació.
En aquest cas se'ns plantegen dues opcions, retirar la ventilació mecànica i que la mort es produeixi per criteris cardiorespiratoris, o continuar amb el suport i que la mort aparegui per criteris neurològics o mort encefàlica.
- L'EXTRACCIÓ DELS ÒRGANS EN QUIRÒFAN.
Una vegada que s'ha acabat amb el procés de valoració del possible donant, es considera que és vàlid per a la donació, la família accepta i comprèn el procés que s'ha de fer, i s'han complert els tràmits legals, el donant mort és trasllat a quiròfan per realitzar l'extracció / obtenció dels òrgans susceptibles de donació.
La documentació necessària per a realitzar l'extracció, que prèviament ha d'estar emplenada, és: autorització per a l'extracció d'òrgans, certificat de mort, autorització judicial en cas necessari, acta d'extracció en què s'especifiquen els òrgans que s’extrauran, i un dossier amb tota la informació necessària sobre el donant per a cada equip (extractor i trasplantador), que ha d'incloure un informe detallat sobre les característiques del donant i de l'òrgan del trasplantant, amb els estudis i resultats que s'han realitzat, quin ha estat el procés d'extracció de l'òrgan i les solucions de preservació utilitzades.
El coordinador de trasplantaments de l'hospital d'extracció és l'encarregat de supervisar tot el procés de l'obtenció d'òrgans: el trasllat del donant a quiròfan, coordinar els equips extractors i als equips trasplantadors, que, a més, poden pertànyer al mateix hospital o poden traslladar-se des d'un altre centre, i que també són responsables de tot el procés. El coordinador també serà l'encarregat que els òrgans es mantinguin en condicions òptimes de perfusió i oxigenació un cop extrets, i del seu envasat i etiquetatge, perquè arribin al seu destí junt amb la documentació necessària.
L’ONT s'encarrega de la gestió i coordinació dels aspectes logístics relacionats amb l'extracció, com són programar l'hora en què s'ha de realitzar segons el temps que durarà el transport i disponibilitat de personal extractor-implantador, validesa dels òrgans, i, al costat del coordinador de l'hospital extractor, s'encarreguen de la disponibilitat dels quiròfans i de personal, sobretot del material específic per a la intervenció, com són la preparació i manteniment de la cadena de fred per als líquids de preservació, i del material necessari per a l'empaquetament i etiquetatge dels òrgans.
L'ONT assigna els òrgans seguint els criteris de distribució establerts, tant territorials com clínics:

El trasllat del donant mort des de l’UCI a quiròfan és un moment delicat i crític, en el qual s'ha d'assegurar la preservació dels òrgans, sobretot dels pulmons, ja que són susceptibles de deteriorar i invalidar per les desconnexions dels respiradors (respirador d'UCI - respirador de trasllats - respirador de quiròfan), sent necessari utilitzar estratègies de ventilació de protecció pulmonar i maniobres de reclutament.
Cal tenir previst el material quirúrgic necessari per a l'extracció, inclòs un desfibril·lador. Al quiròfan, es mantindrà la mateixa monitorització en el donant mort que a l'UCI (monitoratge hemodinàmica bàsica i avançada) per detectar i actuar en cas d'inestabilitat hemodinàmica, hipotèrmia, trastorns del ritme, etc. Una vegada que els equips extractors arriben a quiròfan, es comunica a l'ONT que s'inicia l'extracció dels òrgans. És fonamental la coordinació entre tots els equips extractors perquè cada un tingui definit el seu moment d'actuar i evitar així improvisacions que podrien provocar la pèrdua d'òrgans.
L'extracció dels òrgans és un procés complex, que comporta l'actuació i coordinació de diverses disciplines quirúrgiques (toràcica, abdominal, cardíaca, etc.), i comprèn dues fases ben diferenciades:
- Cirurgia "in situ" o extracció: es practica en el donant d'òrgans amb l'objectiu d'extreure un òrgan sa i viable.
- Cirurgia "ex situ" o cirurgia de banc: consisteix en la preparació final de l'òrgan ja extret i perfós, i s'efectua fora del cos del donant.
En el moment de l'extracció d'òrgans, el donant pot trobar-se hemodinàmicament estable o inestable. En el cas del donant inestable, amb risc d'aturada cardíaca, cal realitzar tècniques d'extracció superràpides, gairebé sense dissecció dels òrgans a extreure, sent prioritari salvar el màxim nombre d'òrgans. Si el donant es troba hemodinàmicament estable, permet la dissecció, canulació, perfusió i extracció reglada dels òrgans.
La tècnica quirúrgica i la incisió, dependrà dels òrgans que s'ha decidit extreure, ja sigui abdominal (laparotomia), toràcica (esternotomia) o de totes dues. Un cop realitzada la incisió, es fa palpació i una primera inspecció visual per detectar anomalies en els òrgans, i fins i tot es poden prendre mostres per realitzar biòpsies si fos necessari (el resultat s'ha de tenir abans de finalitzar l'extracció o prèvia a l'implant dels òrgans). Aquesta primera inspecció es comunica a l'ONT, i un cop acceptats els diferents òrgans se li comunica al coordinador, que al seu torn ho notifica als centres implantadors, i es continua amb la intervenció dels diferents equips extractors.
Després es realitza la dissecció dels òrgans, sempre en aquest ordre:
1º òrgans toràcics: cor i pulmó.
2n òrgans abdominals: fetge, pàncrees, intestí i ronyons.
Un cop disseccionats els òrgans, l'anestesista els hepariniza (heparina sòdica), i es procedeix a la canulació, camplaje[1] i exanguinació. Tant la dissecció com la canulació ho fan els equips extractors, de forma simultània i coordinada. Ha de registrar-se l'hora en què es realitza el camplaje i comunicar-ho a l'ONT.
S'inicia llavors la primera fase de la preservació dels òrgans amb la infusió de les solucions de preservació: agents o procediments químics, físics o d'un altre tipus amb la finalitat d'aturar o retardar el deteriorament que pateixen els òrgans, des de la defunció fins al trasplantament en el cas de donació en asistòlia, o des de la seva extracció fins al seu trasplantament en el cas de mort encefàlica o donació de viu.
Un cop refredats i perfundits, es realitza l'extracció dels òrgans, seguint el mateix ordre en què s'ha realitzat la dissecció: òrgans toràcics, òrgans abdominals, empelts vasculars i extracció de teixits.
Un cop extrets, els equips extractors decideixen si els òrgans són vàlids per a trasplantament o no. Si s'ha pres una biòpsia, s'espera al resultat d’aquesta.
Qualsevol incident durant l'extracció ha de quedar documentat.
La següent fase és la cirurgia de banc parcial o completa, per tal de deixar preparats els òrgans per al trasplantament. La cirurgia de banc es realitza en condicions d'hipotèrmia, s'eliminen tots els teixits sobrants i es prepraran els pedicles vasculars, incloent les reconstruccions arterials o venoses. Aquesta cirurgia pot fer-se en el centre d'obtenció, o quan l'òrgan arriba al centre trasplantador.
Es procedeix llavors a la preservació dels òrgans extrets. L'extracció, l'emmagatzematge i el trasplantament d'un òrgan alteren ja de per si, l'homeòstasi de l'òrgan mateix i pot ser determinant perquè sigui funcional després del trasplantament. La lesió de l'òrgan passa com a resultat del temps d'isquèmia, tant de la isquèmia calenta (període que comprèn des de la interrupció de la circulació de l'òrgan fins a la perfusió amb la solució hipotèrmica de preservació), com de la isquèmia freda (període que comprèn des de la perfusió hipotèrmica de l'òrgan fins al seu trasplantament en el receptor).
En l'actualitat, el mètode més utilitzat de preservació d'òrgans és la preservació hipotèrmica mitjançant conservació en fred. Per a això s’infonen líquids a baixa temperatura (4ºC per norma general) que refreden l'òrgan i realitzen un rentat intravascular per arrossegament.
Altres tècniques de preservació són:
Preservació en màquina de perfusió hipotèrmica (MPH). Després del rentat inicial al quiròfan, l'òrgan s'introdueix en un dispositiu que manté un flux controlat de forma contínua o pursátil, amb solució de preservació freda (0-4º C) que permet a més netejar de microtrombes del torrent circulatori i eliminar els productes metabòlics finals.
Preservació normotèrmica, amb líquids de preservació a temperatura 25-37ºC que han demostrat potencials beneficis, sobretot en òrgans procedents de donació en asistòlia, al disminuir les resistències vasculars i afavorir l'augment de l'alliberament d'oxigen.
Els temps de preservació depenen de l'òrgan mateix; per exemple, cor i pulmó requereixen temps de preservació freds molt curts, mentre que el ronyó pot emmagatzemar-se durant 40 hores.
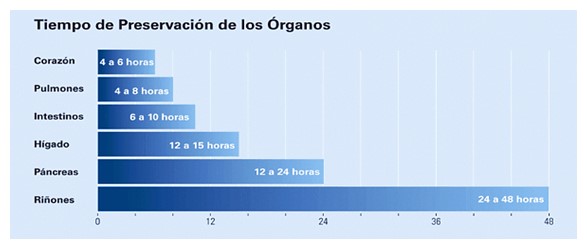
L'empaquetatge dels òrgans, un cop realitzada la preservació correcta, es realitza de forma individualitzada per a cada òrgan. Com a norma comuna, cada òrgan s'introdueix en doble bossa, en un contenidor rígid estèril i en gel, per assegurar la temperatura adequada durant el transport. Cada òrgan anirà acompanyat de mostres de teixit: gangli, melsa i sang, segons el que indiqui l'equip de trasplantament.
Quan l'òrgan ha de traslladar-se a un centre diferent de centre d'obtenció, s'acompanyarà de la següent documentació (Article 12 de Reial Decret 1723/2012):
- Etiquetatge exterior, comuna entre comunitats i països europeus, en el qual consta una indicació que es trasllada un òrgan humà, especificant el tipus d'òrgan i la seva ubicació anatòmica:
"Òrgan humà per a trasplantament. Manipular amb cura"
Font: Transport i logística internacional-WordPress.com organisme oficial
- Procedència i destinació de l'òrgan (centres d'obtenció i centre de trasplantament), amb el nom dels responsables de l'enviament i la recepció, amb les seves respectives adreces i números de telèfon.
- Dia i hora de sortida de centre d'obtenció.
- Recomanacions de transport (temperatura i posició adequades).
- Informe sobre les característiques del donant i de l'òrgan, la seva extracció i les solucions de preservació utilitzades.
- Els estudis realitzats i els seus resultats.
La reconstrucció del cadàver ha de ser molt acurada i amb el màxim respecte, i és fonamental mantenir la dignitat del cadàver i l'aspecte extern, que generalment no canvia de forma apreciable, i només queda una cicatriu suturada a la pell del tòrax i abdomen.
En el cas d'extracció de teixits, com còrnies o ossos, es col·loquen pròtesis per recuperar el volum i fermesa després de l'extracció. El coordinador ha d’assegurar-se que s'ha realitzat correctament abans de ser lliurat a la família.

