La muerte encefálica, como definición clínica, apareció en la década de los años cincuenta, cuando Mollaret y Goulon (1959) examinaron por primera vez a pacientes con un cuadro clínico que sobrepasaba al estado de coma, diferente a los estados comatosos conocidos hasta entonces. A este cuadro clínico le llamaron “coma depassé”: pérdida total de la conciencia, de la motilidad, de los reflejos, de la sensibilidad y de las funciones vegetativas.
En 1968, el Comité de la Universidad de Harvard presentó los primerios criterios para el diagnóstico de muerte cerebral, que incluían: coma profundo, apnea, ausencia total de reflejos cefálicos y espinales, electroencefalograma sin actividad cerebral y midriasis en ausencia de intoxicación por drogas o en ausencia de hipotermia, cuadro que debe mantenerse durante 24 horas como mínimo.
Hasta entonces, el significado del fallecimiento de una persona se refería de manera específica a criterios cardiológicos; no obstante, a partir de ese año, el concepto se amplía al fallecimiento bajo criterios neurológicos, o lo que actualmente se conoce como muerte encefálica.
Los “Criterios de Harvard”, junto al concepto de “coma depassé” cambiaron el paradigma de la muerte, entendida como el fin de la persona cuando se diagnostica la muerte encefálica, lo que ha favorecido que cada vez sea más aceptado el principio de la donación como parte integral de los cuidados al final de la vida.
En España, la donación de órganos se plantea habitualmente a todo paciente en situación de muerte encefálica, si no presenta contraindicaciones médicas. Además, contamos con un marco regulatorio y el apoyo institucional necesarios para la práctica de donación en asistolia controlada (Tema 4), o en aquellos pacientes que se prevé que van a fallecer tras la retirada o limitación del soporte vital (Limitación del Tratamiento de Soporte Vital LTSV) como veremos también en el Tema 4.
Hoy día es una realidad el ingreso en una Unidad de Cuidados Intensivos para iniciar o continuar con el tratamiento de soporte vital (ventilación mecánica electiva), con el objetivo de posibilitar la donación de órganos en pacientes con daño cerebral catastrófico en los que se ha desestimado el tratamiento por considerse fútil (Cuidados Intensivos Orientados a la Donación).
1. DIAGNÓSTICO DE MUERTE ENCEFÁLICA
La muerte encefálica se define como el fracaso completo e irreversible de las funciones del encéfalo (hemisferios cerebrales, cerebelo y tronco del encéfalo), con incapacidad para el mantenimiento autónomo de la homeostasis corporal, acompañado del cese de la función cardiocirculatoria y de la ventilación espontánea, llevando al inicio del proceso de muerte y putrefacción.
Cualquier patología intracraneal grave provoca un aumento de la presión intracraneal (PIC), que provoca una disminución de la perfusión cerebral (PPC). La disminución progresiva del flujo sanguíneo cerebral imposibilita mantener la oxigenación y el metabolismo cerebral adecuado. Cuando la PIC se eleva por encima de la tensión arterial sistólica del paciente, cesa definitivamente el flujo sanguíneo cerebral y se produce la muerte encefálica.
Sin embargo, ciertas funciones endocrinas y cierta actividad metabólica (consumo de glucosa y oxígeno), pueden persistir durante un corto periodo de tiempo. El soporte vital avanzado permite mantener estas funciones durante 24–48 horas, haciendo posible la opción de la donación.
Las patologías que pueden evolucionar a muerte encefálica, y en las que el paciente puede ser considerado donante son:
- Accidente cerebrovascular, isquémico o hemorrágico.
- Traumatismo craneoencefálico grave.
- Encefalopatía post-anóxica (por parada cardiorrespiratoria).
- Algunos tipos de tumor cerebral primario.
Según el Real Decreto 1723/2012, para certificar la muerte encefálica de un paciente (coma arreactivo de etiología estructural conocida) siempre es necesario realizar una exploración neurológica sistemática, completa y rigurosa, junto a un periodo de observación o espera apropiados. Esta misma disposición señala que el certificado de muerte encefálica lo deben firmar tres médicos, de los cuales uno debe ser neurólogo o neurocirujano y otro de ellos el médico intensivista responsable del paciente, y entre los que no debe encontrarse el coordinador de trasplante ni ningún miembro del equipo extractor-trasplantador. La hora del fallecimiento que se registra en la historia clínica es la hora en la que se completa y finaliza el diagnóstico de muerte, tras la realización de la exploración neurológica, el periodo de observación y las pruebas instrumentales necesarias.
Certificar la ME es un diagnóstico que conlleva una gran responsabilidad médica, ética y legal, ya que precede a la retirada de las medidas de soporte, incluyendo la desconexión de la ventilación mecánica, y a realizar la extracción de órganos para trasplante.
La obtención de órganos de fallecidos solo puede realizarse tras el diagnóstico y certificación de muerte encefálica (Anexo I del RD 1723/2012), y según las exigencias éticas, los avances científicos en la materia y la práctica médica aceptadas.
Pero antes de realizar la exploración del potencial donante, hay que comprobar que el paciente se encuentra en unas condiciones clínicas adecuadas que no alteren los hallazgos de la exploración neurológica: que haya estabilidad hemodinámica, que la oxigenación y ventilación sean las adecuadas, que la temperaura corporal sea > 35º C, que no haya alteraciones metabólicas o endocrinas que puedan ser la causa del coma, y que el paciente no se encuentre bajo los efectos de fármacos depresores del Sistema Nervioso Central y/o bloqueantes neuromusculares.
Los hallazgos en la exploración neurológica que determinan la muerte encefálica se basan en tres pilares: coma arreactivo, ausencia de reflejos y presencia de apnea.
1.1. Muerte troncoencefálica “aislada”
Es una situación poco frecuente que aparece cuando la causa del coma es una afección puramente infratentorial (cerebelo y tronco encefálico), como hemorragias o Accidente Vascular Cerebral (AVC) isquémico. En estos casos, la circulación cerebral está presente a través de las arterias carótidas internas, y puede aparecer cierta actividad eléctrica en el electroencefalograma (EEG) durante varios días, y aún más si el paciente es portador de un drenaje ventricular de líquido cefalorraquídeo (LCR); puede haber también presencia de potenciales evocados, aunque la exploración neurológica sea compatible con muerte encefálica.
En estos casos, en España el Real Decreto 2070/1999 obliga a que, además de la exploración clínica, se debe realizar un EEG u otra prueba diagnóstica que demuestre la ausencia de la función de los hemisferios cerebrales.
1.2. Exploración neurológica
Coma arreactivo. El paciente tiene que encontrarse en coma arreactivo profundo (Glasgow 3), sin respuesta motora o vegetativa al estímulo doloroso, producido en el territorio de los nervios craneales. No deben existir posturas de descerebración ni de decorticación. La presencia de actividad motora de origen espinal (cuello, tórax, abdomen y extremidades), espontánea o inducida, no invalida el diagnóstico de muerte encefálica.
Históricamente la muerte significaba inmovilidad; sin embargo, ya algunos físicos y filósofos como Descartes, mencionaron la persistencia de ciertos movimientos en el cuerpo humano tras la misma, como por ejemplo tras la decapitación.
Puede aparecer actividad motora espinal, tanto refleja como espontánea, (33% al 75% de los casos) al estar la médula espinal indemne. Entre los más frecuentes se encuentran el reflejo cutáneo-abdominal (contracción de los músculos abdominales del mismo lado donde se realiza una estimulación cutánea), el reflejo cremastérico (elevación del testículo en hombres, o contracción del labio mayor en la mujer, al estimular la cara interna del muslo o la masa de los adductores).
Pueden aparece también el reflejo plantar flexor o Babinski, reflejo de retirada, el “signo de Lázaro” (elevación y aproximación de ambos brazos, y que en su presentación más espectacular, se acompaña de sedestación), movimiento en abanico de los dedos de los pies “pie ondulante”, priapismo, mioclonías espinales, etc.
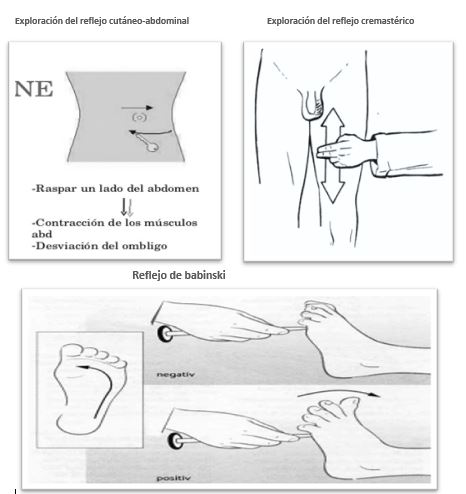
Fuente: https://cienciaexplicada.com/reflejos-superficiales-cutaneos-y-mucosos.html
Signo de Lázaro
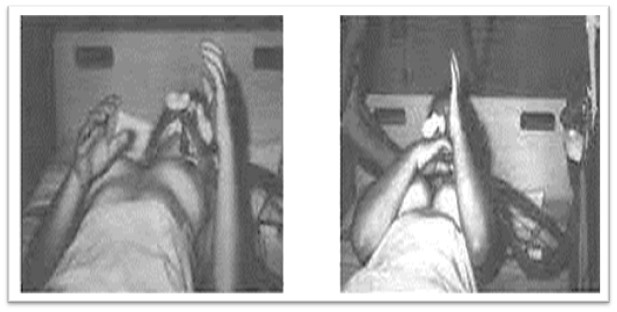
Fuente: criminólogos, criminalistas y expertos en ciencias forenses. Visto en Facebook.
Ausencia de reflejos troncoencefálicos: fotomotor, corneal, nauseoso, tusígeno, oculocefálico y oculovestibular. La exploración debe hacerse de forma secuencial y ordenada en sentido caudal. En situación de muerte encefálica no debería aparecer ningún movimiento facial, ni espontáneo ni por estimulación álgica (Maniobra de Foix).
Reflejo fotomotor: reacción de las pupilas ante una luz potente. Patológico: ausencia de reacción. Debe explorarse tanto el reflejo directo como el consensual (abrir los dos ojos mientras se estimula con la luz cada uno por separado). Puede aparecer anisocoria sin que ello modifique el resultado de la exploración. Las pupilas estarán midriáticas, y no hay parpadeo espontáneo.
El reflejo fotomotor debe explorarse antes de realizar el test de atropina, ya que puede alterarse por el uso de este fármaco.
Reflejo corneal: contracción palpebral al estímulo táctil de la córnea. Patológico: no hay respuesta de parpadeo, ni retirada, ni
lagrimeo ni enrojecimiento. Se debe prestar especial cuidado al valorar este reflejo para no dañar la córnea y producir lesiones que imposibiliten su donación.
Reflejo nauseoso: respuesta nauseosa al estímulo táctil de la orofaringe. Patológico: al estimular la base de la lengua, la pared posterior de la faringe, el velo del paladar y la úvula no aparece ninguna respuesta nauseosa.
Reflejo tusígeno: es el último reflejo que desaparece, y su valoración se realiza con el paciente conectado a ventilación mecánica, asegurando el aporte de oxígeno, e introduciendo una sonda de aspiración por el tubo endotraqueal hasta las vías respiratorias bajas. Patológico: no hay respuesta tusígena en la estimulación de la vía aérea.
Reflejo oculovestibular: con el cabezal de la cama elevado a 30º, se inyectan 50 cc de agua a 4º C en cada conducto auditivo, manteniendo los párpados biertos; los ojos se dirigen hacia el lado en el que se ha irrigado el agua. Patológico: ausencia de movimientos oculares.
Reflejo oculocefálico: manteniendo los párpados abiertos, se lateraliza hacia un lado y otro la cabeza, con movimientos enérgicos, y los movimientos oculares van en contra del movimiento cefálico, “ojos de muñeca”. Patológico: los movimientos oculares son sinérgicos a los movimientos cefálicos.
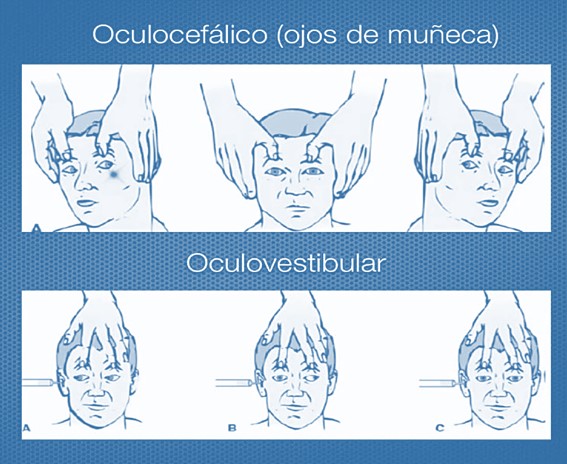
Fuente: Pares craneales 8: Nervio vestibulococlear. Visto en youtube
Ausencia de respuesta al “test de atropina”. Respuesta cardiaca por la estimulación del nervio vago con un agente inhibidor de la acetilcolina (Atropina). Debe realizarse siempre después de la exploración clínica, y por un acceso venoso por el que no se infundan fármacos cronotropos (Dopamina, Dobutamina, etc)
Test de atropina: tras la administración endovenosa de 0,04 mg/Kg de Sulfato de Atropina no debe existir un incremento superior al 10% de la frecuencia cardiaca inicial antes de aplicar el fármaco.
Apnea demostrada con el “test de apnea” o de retirada de la ventilación mecánica, comprobando que no existen movimientos respiratorios en situación de hipercapnia y acidosis (pCO2 en sangre arterial > 60 mmHg).
Test de apnea: se toma una muestra de gases arteriales para verificar que el pH, el pO2 y el pCO2 están en rango adecuado. Se pre-oxigena al paciente con FiO2 al 100% durante 15-20 minutos. Pasado este tiempo, se desconecta de la ventilación mecánica, colocando una cánula cerca de la carina con oxígeno al 100%, y a 6-8 litros/minuto. Los movimientos respiratorios deben estar abolidos. Se cursan gases arteriales seriados post desconexión de la ventilación mecánica hasta alcanzar pCO2 > 60 mmHg o pO2 < 50 mmHg.
En ausencia de movimientos respiratorios la prueba es positiva (patológica).
Junto con la exploración neurológica, la realización de pruebas instrumentales complementa el diagnóstico de muerte encefálica, sobre todo en aquellas situaciones que dificultan el diagnóstico clínico. El tipo de prueba y el número de test a realizar debe valorarse de forma individual, analizando las aportaciones diagnósticas que proporcionarán las técnicas empleadas.
Y aunque desde un punto de vista científico no son obligatorias, en los casos que tienen carácter de obligatoriedad son:
- Situaciones que dificultan el diagnóstico clínico de muerte encefálica.
- Ausencia de lesión destructiva cerebral demostrable por evidencia clínica o por neuroimagen.
- Cuando la lesión causal sea en un principio infratentorial (encéfalo y tronco del encéfalo).
Las pruebas diagnósticas se encuadran en dos grupos:
- Pruebas que evalúan la función neuronal: electroencefalografía (mostrará ausencia de actividad eléctrica cerebral, o línea isoeléctrica, durante al menos media hora) y potenciales evocados multimodales (en condiciones de muerte encefálica desaparecen las respuestas evocadas de origen encefálico); Índice Biespectral BIS® (el valor BIS tiende a 0 cuando acontece la muerte encefálica, siendo 100 el valor de un paciente despierto).
- Pruebas que evalúan el flujo sanguíneo cerebral: arteriografía, angiografía, angiogammagrafía, y sonografía Doppler transcraneal.
- Otras pruebas instrumentales diagnósticas que se pueden realizar en muerte encefálica son: análisis de la onda de Presión Intracraneal (PIC) y presión de perfusión cerebral (PPC). En pacientes en los que la muerte encefálica se ha producido por una hipertensión intracraneal refractaria, el valor de la PIC aparecerá elevado y la PPC será de cero o negativa.
En el caso de recién nacidos, lactantes y niños, el diagnóstico clínico de muerte encefálica se basa en los mismos criterios que en los adultos, aunque con algunas peculiaridades:
- En el caso de lactantes, la exploración neurológica debe incluir la valoración del reflejo de succión y búsqueda.
- En los niños de hasta 24 meses es obligatorio que la temperatura corporal se encuentre por encima de 35º C antes de realizar la exploración neurológica.
- Las pruebas instrumentales han de ajustarse a la edad del niño.
1.3 Periodo de observación
Para realizar el diagnóstico de muerte encefálica es necesario conocer la causa de la lesión cerebral. Además, esta lesión deber ser irreversible.
Se recomienda repetir la exploración neurológica según periodos ya establecidos, y establecer además unos periodos mínimos de observación, que deben valorarse de forma individual, teniendo en cuenta el tipo y la gravedad de la lesión causante (en encefalopatías isquémico-anóxicas el periodo de observación será mayor que para lesiones traumáticas o vasculares), así como de las pruebas instrumentales realizadas, que pueden determinar acortar o incluso omitir este periodo, según criterio médico.
Si el diagnóstico de muerte encefálica se realiza por la clínica, el periodo de observación se alargará y se repetirá:
- Ante la sospecha del uso de fármacos depresores del SNC, el periodo de observación debe prolongarse según la vida media de los fármacos administrados.
- La normativa española recomienda que la exploración neurológica se repita a las seis horas en caso de lesión destructiva conocida, y a las 24 horas en caso de encefalopatía anóxica.
- En el caso de neonatos y hasta 24 meses de edad, se recomienda un periodo de observación que oscila de 24 a 48 horas, aunque podrá omitirse si, con una prueba instrumental diagnóstica, se demuestra ausencia del flujo sanguíneo cerebral.
La ley establece que el periodo de observación es obligatorio en los siguientes casos:
- Pacientes bajo los efectos de drogas depresoras del Sistema Nervioso Central.
- Pacientes con graves deterioros craneofaciales, o cualquier otra situación que impida una exploración neurológica completa.
- Intolerancia al test de apnea.
- Hipotermia, con temperatura central < 32º C.
- Cuando no se puede objetivar una lesión destructiva cerebral, ni por la evidencia clínica ni por neuroimagen.
- Cuando la existencia de una lesión irreversible de los hemisferios cerebrales se tiene que demostrar con una prueba instrumental.
2. MANTENIMIENTO DEL DONANTE
Después de la muerte encefálica de un paciente, solo existen dos posibles actuaciones:
- Retirar todas las medidas de soporte y esperar que el paciente entre en asitolia.
- Iniciar el proceso de donación en muerte encefálica, para lo cual es necesario mantener al potencial donante en condiciones fisiológicas óptimas para asegurar la viabilidad de los órganos.
Los cambios fisiopatológicos que acontecen en una persona después de la muerte encefálica convierten al potencial donante en un “paciente crítico inestable”, y obligan a una monitorización estricta y específica, y a establecer una terapéutica adecuada para evitar el deterioro de los órganos; de aquí se deriva que su manejo se haga fundamentalmente en las Unidades de Críticos, bajo médicos intensivistas y con personal de enfermería especializado. Generalmente, las muertes encefálicas que ocurren en las UCIs suelen estar más controladas y con mejor manejo terapéutico, ya que la mayoría son pacientes con daño neurológico grave que no responden al tratamiento, y ya desde este momento se empieza a plantear la posibilidad de la donación, tanto dentro del equipo asistencial, como a la familia.
La muerte encefálica no es una situación estática, sino un proceso dinámico que, a través de múltiples mecanismos, puede afectar significativamente la calidad de los órganos extraíbles. Por eso es fundamental identificar el momento en el que los objetivos del tratamiento cambian de ser terapéuticos a dirigirse a la optimización de la función de los órganos para ser trasplantados, es decir, en el momento que se certifica el diagnóstico de muerte encefálica comienza el mantenimiento del potencial donante.
Se denomina “mantenimiento del donante” al conjunto de procedimientos, diagnósticos y terapias que se emplean en el posible donante desde el establecimiento de la muerte encefálica hasta el inicio de las técnicas de preservación de los órganos, que se realiza en el quirófano.
Este periodo puede durar desde unas pocas horas hasta varios días, la mayor parte transcurre en la Unidad de Críticos, y está relacionado con las necesidades de la familia, requerimientos logísiticos relacionados con el traslado de los equipos de extracción, de la disponibilidad y preparación de los quirófanos, y de la necesidad de realizar pruebas de evaluación en el donante.
2.1. Cambios fisiopatológicos derivados de la muerte encefálica
El proceso de muerte encefálica provoca en el organismo una serie de cambios fisiopatológicos secundarios a la destrucción de los centros encefálicos, que pueden derivar en lesiones de los órganos del potencial donante. Estas alteraciones siguen una secuencia rostro-caudal, y se agrupan en tres grandes bloques: trastornos hemodinámicos, trastornos hormonales y trastornos secundarios a un proceso inflamatorio.
Aparecen antes y durante el enclavamiento, en la llamada fase adrenérgica-tormenta catecolamínica, y después del proceso de enclavamiento, una vez instaurada la muerte encefálica, por la pérdida de todos los mecanismos autorreguladores, y que produciría la muerte por asistolia.
Es vital conocer estas alteraciones fisiopatológicas para anticiparnos y poder controlar o minimizar las complicaciones que pueden ir apareciendo.
La lesión primaria supratentorial o hemisférica produce aumento de la presión intracraneal, que deriva en una herniación del paciente, siendo éste el patrón más frecuente del establecimiento de muerte encefálica. Secundario a la disminución de la presión de perfusión, se produce una isquemia del tronco cerebral, y a su vez, la isquemia del mesencéfalo activa el sistema parasimpático, y hace que inicialmente aparezca bradicardia e hipotensión; posteriormente, la afectación del puente activa el sistema simpático con la aparición de la Tríada de Cushing: aumento de la presión arterial, respiración irregular y bradicardia.
La siguiente fase aparece con la isquemia del núcleo vasomotor del bulbo, que desencadena la “tormenta catecolaminérgica”, es decir, liberación masiva de catecolaminas con estimulación del sistema simpático, produciéndose una crisis hipertensiva con taquicardias y taquiarritmias.
Aparece vasoconstricción generalizada que compromete el flujo sanguíneo de los órganos, y contribuye a una disfunción del ventrículo izquierdo, que junto a la disfunción del ventrículo derecho por el aumento de la resistencia de los vasos pulmonares por la vasoconstricción, favorece que se desarrolle el edema pulmonar neurogénico.
La posterior destrucción del centro vasomotor bulbar produce el cese de la descarga catecolaminérgica, que provoca la pérdida progresiva de la autorregulación y del tono simpático vascular y miocárdico, llevando a una fase de hipotensión por vasodilatación, con hipovolemia relativa y disfunción miocárdica, por lo que el gasto cardiaco se ve comprometido. La evolución natural de este proceso es la hipotensión progresiva y la parada cardiaca.
El centro respiratorio también se ve afectado, provocando en un principio un patrón respiratorio irregular, que deriva en la abolición del estímulo ventilatorio en la etapa final.
La afectación de la hipófisis posterior produce un déficit de vasopresina que desencadena una diabetes insípida.
La afectación del centro regulador del hipotálamo puede producir hipertermia central en un principio, para terminar con hipotermia debido a la pérdida de la termorregulación.
La isquemia-reperfusión producida por la tormenta de catecolaminas, el bajo gasto cardiaco y el restablecimiento circulatorio a partir del tratamiento de elección, provocan una intensa reacción inflamatoria que afecta a los diferentes órganos.
Este patrón clínico puede variar en intensidad, dependiendo de la localización de la lesión inicial o de la velocidad de aparición de la hipertensión intracraneal; así, aunque la inestabilidad hemodinámica es común, la duración de la tormenta catecolamínica, la diabetes insípida o la hipo-hipertemia son variables.
La muerte encefálica desencadena a corto plazo el cese de la actividad cardiocirculatoria, lo que llevaría a la pérdida irreversible de órganos para donación. Es por esto que el correcto mantenimiento de potencial donante de órganos, en condiciones óptimas de perfusión y oxigenación, asegura la correcta viabilidad de los órganos para ser trasplantados.
2.2. Monitorización en el donante potencial
La monitorización del potencial donante de órganos debe ser igual de rigurosa que antes del diagnóstico de muerte encefálica.
La monitorización hemodinámica sirve de guía para la administración de fluidoterapia y drogas vasoactivas e inotrópicas, necesarias con el progreso del cuadro clínico que hemos visto, secundario a la muerte encefálica.
Las recomendaciones van dirigidas a la monitorización continua de las constantes vitales: electrocardiografía, presión arterial (catéter arterial), presión venosa central (catéter venoso central), pulsioximetría, temperatura y diuresis, así como la monitorización hemodinámica avanzada con catéter Swan-Ganz o sistema PICCO (Pulse Contour Cardiac Output), para conocer el gasto cardiaco continuo, sobre todo en los casos en los que se requiere la admnistración de catecolaminas a dosis altas.
El ecocardiograma permite valorar la función cardiaca y evaluar la respuesta a los fluidos, a los fármacos inotrópicos y vasopresores. Podría ser necesario un ecocardiograma transesofágico si existen anormalidades en la pared torácica o para determinar con mayor precisión la función cardiaca o valvular.
La monitorización incluye análisis de sangre general seriados, y pruebas complementarias específicas (cultivos microbiológicos, radiografías, ecografías, etc.). La monitorización de la saturación venosa mixta, y el exceso de bases y el lactato sérico se consideran parámetros de utilidad para valorar la perfusión periférica de los órganos en general, y de los que serán recuperados para trasplante en particular.
Según el “Protocolo del mantenimiento del potencial donante”, elaborado por la SEMICYUC (Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias) y la ONT (Organización Nacional de Trasplantes), los objetivos a alcanzar y mantener en el potencial donante son:
- Temperatura corporal: > 35º C
- Presión arterial media: 60–110 mmHg
- Presión arterial sistólica: > 100 mmHg
- Frecuencia cardiaca: > 100 ppm
- Presión capilar pulmonar: 8–14 mmHg
- Presión venosa central: 10–12 mmHg (< 8 mmHg en el donante de pulmón)
- Índice cardiaco: 3.0 – 5.0 l/min/m2
- Diuresis: > 1 ml/Kg/h
- Saturación de oxígeno: > 95%
- Glucemia capilar: < 150 mg/dl
- Hematocrito: 20 – 30 %
- Hemoglobina: > 7 g/dl
2.3. Problemas específicos y tratamiento
El tratamiento del potencial donante va encaminado a contrarrestar las alteraciones fisiopatológicas que se producen en el proceso de muerte encefálica, ya que ha perdido su capacidad de respuesta fisiológica, y depende completamente de nuestro manejo y tratamiento.
Pérdida de la respiración espontánea. El centro respiratorio se ve afectado, provocando en un principio un patrón respiratorio irregular, hasta que se produce la abolición del estímulo ventilatorio en la etapa final, siendo necesaria la ventilación mecánica invasiva para asegurar una buena oxigenación tisular, mantener el equilibrio ácido-base, y completar el diagnóstico de muerte encefalica del donante (test de apnea).
El empleo de estrategias ventilatorias protectoras del pulmón: volumen corriente 6-8 ml/Kg, junto con niveles de PEEP elevados, entre 8-10 mmHg, se ha asociado con el aumento de pulmones viables y recuperados respecto a estrategias ventilatorias más convencionales.
Es necesario contemplar las complicaciones habituales que pueden surgir en un paciente crítico conectado a ventilación mecánica: neumonía asociada a ventilación mecánica, administración de antibióticos profilácticos en caso de sospecha de broncoaspiración o en intubación no electivas, etc., y adoptar las medidas habituales de cuidados para evitarlas, como son el correcto sellado de la via aérea con el balón del neumotaponamiento, mantener la cabecera de la cama a 30º, aspiración de secreciones, etc.
Hipotensión. La fluidoterapia es el tratamiento de elección para mantener la tensión arterial (TAM > 60 mmHg), diuresis (> 0,5 ml/Kg/h), PVC de 3-10 mmHg, y gasto cardiaco adecuados, que garantizan la adecuada perfusión de los órganos, siempre que el donante esté monitorizado de forma correcta, y así evitar la sobrecarga hídrica y el edema pulmonar neurogénico.
La hipotensión puede alterar la función de algunos órganos, pero no supone una contraindicación para la donación, siempre que no se haya lesionado el órgano para trasplantar.
En el caso de hipotensión refractaria, está indicado el uso de vasopresores si con la fluidoterapia no se alcanza el perfil hemodinámico marcado, ya que la hipotensión genera hipoperfusión y dañaría los órganos donables.
Hipertensión y arritmias. Aparecen en las fases iniciales y deben tratarse precozmente, ya que provocan microinfartos cardiacos y pueden dañar todos los órganos donables. El tratamiento de primera opción son β-bloqueantes (Esmolol) en combinación con vasodilatadores como Urapidilo, Nitroprusiato o Nicarpidino, según los valores de la tensión arterial y la frecuencia cardiaca.
La tormenta de catecolaminas desencadena arritmias, tanto auriculares como ventriculares. La bradicardia refractaria no responde a la Atropina, se administra Dopamina, junto a simpaticomiméticos (Isoprenol o Adrenalina). Si es necesario, se coloca un marcapasos externo temporal.
La hormona tiroidea, junto a Vasopresina y Metilprednisolona pueden utilizarse para restaurar el tono vascular en los casos de gran inestabilidad hemodinámica que no responde al tratamiento con fluidos y vasopresores.
La hipotermia, las alteraciones electrolíticas o la hipoxemia pueden desencadenar arritmias, tanto supraventriculares como ventriculares, y una vez corregida la causa, se tratan con Amiodarona (taquicardia supraventricular) o Lidocaína (taquicardia ventricular).
Diabetes insípida neuronal. Tras la muerte encefálica, el daño en el eje hipotálamo-neurohipófisis produce una disminución o inhibición de la hormona antidiurética (ADH). Aparece en el 90% de los donantes.
La disminución de la ADH produce la diabetes insípida y cursa con diuresis > 4 ml/Kg/h y disminución de la osmolaridad urinaria. Es de inicio brusco y produce una importante disminución de la volemia, alteraciones electrolíticas (pérdidas de potasio, magnesio, calcio y fosoforo) e hiperosmolaridad plasmática, que pueden ocasionar graves trastornos del ritmo cardiaco e inestabilidad hemodinámica.
Se trata con ADH exógena (Desmopresina o Vasopresina), junto a una reposición adecuada de la volemia y de electrolitos.
Para normalizar la volemia se administrará fluidoterapia. El suero de elección dependerá de la situación hidroelectrolítica en la que se encuentre el donante, siendo de elección cristaloides isotónicos (Ringer Lactato).
Alteración de las hormonas tiroideas. Síndrome Eutiroideo. La necrosis de la hipófisis provoca disminución, y posterior desaparición, de las hormonas T3 y T4, llevando a una acidosis láctica y deterioro hemodinámico y cardiaco del potencial donante. Algunos autores recomiendan administrar hormona tiroidea junto a corticoides (Hidrocortisona) en caso de inestabilidad persistente y refractaria a aminas vaosacitvas.
Durante el proceso de muerte encefálica se puede producir una deplección de los niveles de cortisol y hormona adrenocorticotropa (ACTH), y el tratamiento con corticoides ayuda a manejar el control endocrino-metabólico, y por tanto, mejorar el control hemodinámico.
Hiperglucemia. Aparece secundaria a la tormenta de catecolaminas, al estado inflamatorio, a la reducción del metabolismo en muerte encefálica, a la hipotermia y al uso de corticoides. Se puede producir también una resistencia a la insulina que deriva en acidosis metabólica y cetosis, con una diuresis osmótica con poliuria, que contribuye a la deshidratación del donante. El tratamiento consiste en perfusión endovenosa continua de insulina rápida, con monitorización horaria hasta regularizar la glucemia, y la disminución del aporte de glucosa exógena. Una vez regulada la glucemia, se puede continuar con pauta móvil de insulina subcutánea.
Control del equilibrio hidro-electrolítico. Mantener un balance hidro-electrolítico adecuado evita el edema de los órganos para trasplante (pulmón, páncreas, hígado y riñones), y asegura una adecuada perfusión tisular. Por ejemplo, una diuresis correcta (1-2 ml/Kg/h) indica adecuada perfusión renal, y por tanto, de todos los demás órganos.
Alteraciones con el potasio, tanto hipo como hiper, son potencialmente peligrosas para el ritmo cardiaco, o la hipernatremia en el caso de la función hepática, por lo que deben manejarse de forma agresiva, con la administración y resposición de electrolitos endovenosos.
En el caso de hipernatremia se administra solución de Dextrosa al 5%. El exceso de soluciones salinas puede favorecer la hipernatremia y la hipercloremia.
El exceso de soluciones glucosadas puede causar hiponatremia e hiperglucemia por deshidratación celular y poliuria.
Alteraciones de la hemostasia.La destrucción del tronco del encéfalo, y la liberación de material tromboplastínico desde el cerebro necrótico, así como la hemodilución, la politransfusión, la hipotermia, la coagulopatía de consumo, entre otras, provocan alteraciones del sistema de la coagulación, que se manifiestan con el desarrollo de la CID (Coagulación Intravascular Diseminada) y la aparición de fibrinolisis, y consumo de plaquetas. El objetivo es mantener en rango las plaquetas, fibrinógeno y protombina.
En general son situaciones transitorias y no contraindican la donación de ningún órgano. La transfusión de hemoderivados consigue mantener un transporte adecuado de oxígeno, con un hematocrito en rango del 20%.
Hipotermia. Es una manifestación muy frecuente en los donantes potenciales, secundaria a la destrucción del centro termorregulador hipotalámico. En situaciones de muerte encefálica, la pérdida del control de la temperatura corporal comporta la aparición de un estado de poiquilotermia: vasoconstricción periférica, disminución del metabolismo celular, pérdida de la capacidad de tiritar e hipotonía muscular. La administración de fluidos a temperatura inferior a la del donante, y la temperatura del box contribuyen también a la aparición de una hipotermia espontánea y progresiva, de aparición rápida, y que una vez instaurada, es difícil revertir, por lo que el mejor tratamiento es la prevención.
El objetivo es mantener la temperatura corporal > 35º C (en la legislación española se acepta como válida una temperatura superior a 32º C), utilizando mantas térmicas, administrando líquidos calientes (37º C) y gases inspirados calientes, aumentando la temperatura ambiental, etc.
Es importante destacar que una temperatura corporal entre 20º C y 28º C hace que el paciente pueda estar comatoso y con abolición de los relfejos troncoencefálicos, provocando una situación similar a la muerte encefálica.
Las alteraciones fisiopatológicas secundarias a la hipotermia son graves, y van en proporción a mayor grado de hipotermia: disminución del gasto cardiaco, hipotensión arterial, arritmias (riesgo de fibrilación ventricular). Una hipotermia <28º C puede provocar asistolia, hiperglicemia y cetosis, trastornos de la coagulación y atelectasias (por la disminución de la actividad mucociliar), con lo que el riesgo de perder órganos funcionales es elevado.
Nutrición. Si bien el aporte nutricional es fundamental para mantener las reservas de glucógeno hepático, una vez instaurada la muerte encefálica se pierde el tono vagal, y disminuye la motilidad y la capacidad de absorción intestinal, por lo que la nutrición enteral suele ser mal tolerada. Puede mantenerse a dosis mínimas como agente protector.
Si el donante previamente era portador de nutrición parenteral total (NPT), puede ser útil mantenerla.
Se recomienda el mantenimiento de los protectores gástricos y la profilaxis de la trombosis venosa profunda una vez diagnosticada la muerte encefálica.
3. CUIDADOS INTENSIVOS ORIENTADOS A LA DONACIÓN DE ÓRGANOS (CIOD)
Los Cuidados Intensivos Orientados a la Donación (CIOD) se definen como el inicio o la continuación de cuidados intensivos (ingreso en UCI, ventilación electiva no terapéutica (VENT), soporte vasoactivo, etc.) en pacientes con daño cerebral catastrófico, en los que se ha desestimado el tratamiento médico o quirúrgico con finalidad curativa por criterios de futilidad, que son considerados como posibles donantes por su probable evolución a muerte encefálica, y no tienen contraindicaciones médicas para la donación; entendiendo como paciente con daño cerebral catastrófico al paciente con patología neurológica grave que conlleva un riesgo de fallecimiento inminente.
El objetivo de los CIOD es incorporar la opción de la donación de órganos como parte de los cuidados al final de la vida (Resolución de Madrid 2010), y comprenden un conjunto de medidas que garantizan el confort y la dignidad del paciente con daño cerebral catastrófico en el proceso de fallecer, permiten la evolución natural a muerte encefálica y aseguran la preservación de los órganos para donación.
Seentiende como tratamiento fútil aquel tratamiento que se prevé no puede cumplir los objetivos en cuanto a curación de la enfermedad o mejoría de los síntomas, a juicio de los profesionales, basados en la evidencia y en la bioética, por lo que los efectos nocivos de mantenerlo no compensan con las expectativas de curación.
Como en todo proceso de donación, es imprescindible conocer la voluntad previa del paciente con respecto a la donación, para lo que el intensivista junto al coordinador de trasplantes, deben verificar que no ha dejado constancia expresa de su negativa a la donación, por lo que según el Real Decreto 1723/2012 de 28 de diciembre, todos somos donantes de órganos si no hemos dejado constancia, verbal o escrita, de lo contrario.
Aún así, debe mantenerse una entrevista previa con sus familiares, en aquellos pacientes con daño cerebral catastrófico considerados posibles donantes, con un proceso de información específico hacia la familia, previo a la evolución a ME, y dirigido a la solicitud para instaurar o continuar con los cuidados intensivos. Esta estrevista forma parte de un proceso continuo de comunicación, adecuado a cada familia, en el que se informa en un principio sobre la situación critica, el pronóstico fatal y la futilidad del tratamiento del paciente. Esta información debe ser progresiva, y ayudando a la familia en la comprensión de la información y en la toma de decisiones.
En la siguiente fase, el coordinador de trasplantes solicitará la continuación de las medidas de soporte con el objetivo de permitir la donación una vez instaurada la ME. Y una vez diagnosticada, se comunicará el fallecimiento a la familia, y se continua con la solicitud del consentimiento familiar para la obtención de órganos y tejidos.
La SEMICYUC (Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias) dispone de un Código Ético como guía de aplicación a los servicios de medicina intensiva, en el que se destaca el derecho a la información verdadera, comprensible y adecuada a las necesidades de cada paciente, y a la toma de decisiones por representación. En cuanto al principio de autonomía del paciente, destaca la importancia del Consentimiento Informado, el Documento de Instrucciones Previas o Voluntades Anticipadas y el derecho a morir con dignidad.
En la práctica, los CIOD deben defender, y no vulnerar, los cuatro principios de la bioética:
- Principio de autonomía: haciendo posible plantear la opción de la donación de órganos, y posibilitar dicha opción si el paciente deseaba ser donante.
- Principio de beneficencia: la donación puede suponer un consuelo para la familia ante la pérdida de un ser querido, a través de valores como la solidaridad y el compromiso social. Además, hacer extensivo los CIOD como parte del proceso de donación, alivia las listas de espera para pacientes que necesitan un órgano para mejorar su supervivencia o calidad de vida.
- Principio de no maleficencia: los CIOD deben respetar la dignidad del paciente, procurando siempre la ausencia de sufrimiento, y asegurando el confort del paciente.
- Principio de justicia: una adecuada selección del posible donante, y llegar a un acuerdo con la familia respecto al tiempo de espera en la UCI hasta la instauración de la muerte encefálica, posibilita una gestión eficiente y proporcionada de los recursos sanitarios.
En el proyecto ACCORD–España–ONT consta que, el tiempo medio de ingreso en la UCI de un paciente con daño cerebral catastrófico hasta su fallecimiento con el objetivo de la donación, es de un día de media, por lo que la utilización de recursos de UCI se justifica con la ayuda que se proporciona a la sostenibilidad del sistema de donación.
Proyecto ACCORD (Achieving Comprehen Sive Coordination in Organ Donation): forman parte de este Proyecto 15 países europeos, con 67 UCIs en total, con el fin de describir las prácticas de cuidados al final de la vida en pacientes fallecidos como consecuencia de un daño cerebral catastrófico.
3.1 Identificación del paciente como candidato a CIOD.
Cuando el equipo médico responsable de un paciente con daño cerebral catastrófico decide no inicia o retirar las medidas de tratamiento curativo, es cuando se puede considerar la opción de los CIOD. Esto conlleva la opción de la donación de órganos, por lo que el caso debe comunicarse al coordinador de trasplantes, quien realiza una evaluación del paciente, basada en dos aspectos: la posibilidad de que evolucione a muerte encefálica en un espacio de tiempo corto, y a que no existan contraindicaciones médicas para la donación.
Si se considera que la evolución a muerte encefálica no se producirá en un corto periodo de tiempo, no se planteará la posibilidad de CIOD.
La valoración del pronóstico debe hacerse por un equipo multidisciplinar, con profesionales de diferentes especialidades (neurología, medicina intensiva, medicina interna y anestesia, entre otras), y en la que el coordinador de trasplante no debe participar. Para la toma de decisiones clínicas, “se debe buscar un equilibrio entre la evidencia científica disponible en los actuales modelos pronósticos/escalas de gravedad, la experiencia clínica y las preferencias del paciente expresadas verbamente o por representación”.
Posteriormente, la selección del paciente como posible donante debe estar avalada por la valoración del médico intensivista, con experiencia en patología neurocrítica y en factores pronósticos, y determinada por datos clínicos, monitorización, y pruebas complementarias, especialmente por un TAC craneal, que nos da información sobre la gravedad de la lesión estructural, la localización, y signos de hipertensión craneal y herniación cerebral.
Los cuidados intensivos orientados a la donación CIOD deben realizarse respetando la autonomía y dignidad del paciente, y siempre garantizando que no se incurre maleficiencia: en todo momento debe asegurarse el confort y la ausencia de sufrimiento del paciente.
Una vez tomada la decisión de reorientar el objetivo terapéutico ante el riesgo de fallecimiento inminente, se notificará al coordinador de trasplantes, con la mayor antelación posible, para que se ponga en marcha todo el proceso de donación. La decisión sobre el pronóstico del paciente y los criterios que modifican el plan de actuación, así como la notificación del caso al coordinador de trasplantes, debe constar por escrito en la historia clínica del paciente.
Si se determina el daño cerebral catastrófico y se continua con el proceso de CIOD, el coordinador de trasplantes toma el liderazgo para el manejo del posible donante, y comienza la valoración indicada en todo donante, que incluye una revisión minuciosa de su historia clínica, y la realización de las pruebas complementarias necesarias para descartar la presencia de infecciones crónicas u otras alteraciones, y evaluar el estado de los órganos para trasplante (Tema 2).
No se planteará la opción de CIOD si se identifican contraindicaciones absolutas para la donación de órganos.
Algoritmo de los cuidados intensivos orientados a la donación
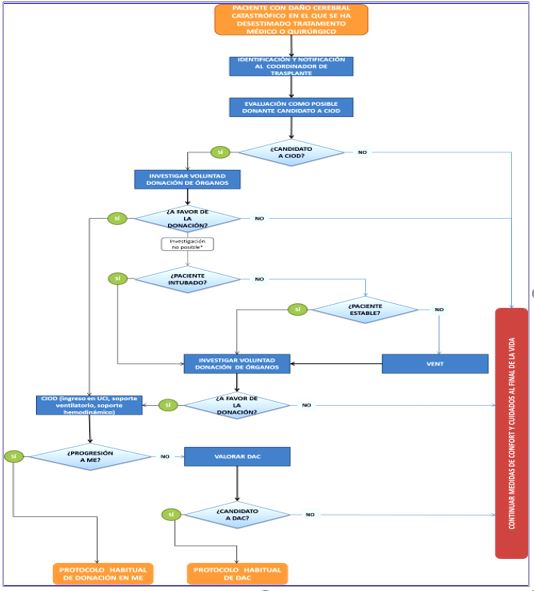
Fuente: Cuidados Intensivos Orientados a la Donación de Órganos. Recomendaciones.
3.2 Entrevista con la familia.
En todo proceso de donación, la información a la familia y la obtención del permiso de donación son uno de los momentos más delicados.
En el caso de los CIOD es aún más doloroso y comprometido por la situación que se plantea a los familiares, que pueden entenderlo como una prolongación innecesaria del sufrimiento del paciente, o darles falsas esperanzas en cuanto al pronóstico.
El paciente con daño cerebral catastrófico puede encontrarse en diferentes escenarios, que condicionan cómo se planteará la entrevista previa con la familia, y el posterior manejo clínico del paciente según la información proporcionada y su decisión.
Paciente fuera de UCI en el que no se ha iniciado ventilación mecánica. Si no existe riesgo de parada cardiorrespiratoria inminente, la entrevista se dirige a que la familia acepte la opción de la donación, y así el paciente ingresa en UCI para iniciar el proceso de CIOD. En el caso de que se encuentre clínicamente inestable, puede considerarse la opción del ingreso en UCI y el inicio de la ventilación mecánica con el fin de preservar los órganos para donación, y posteriormente se podrá realizar la entrevista con la familia, en unas condiciones que permiten dedicar más tiempo a la atención y la información. Si la familia no acepta la posibilidad de la donación, se retiran las medidas de soporte vital que se han iniciado, y se garantiza el confort del paciente mientras evoluciona de forma natural la enfermedad.
Si el paciente ha sido intubado y conectado a ventilación mecánica por los Servicios de Emergencias extrahospitalarios, o en el propio Servicio de Urgencias, la entrevista con la familia va dirigida hacia la opción de instaurar los CIOD en la UCI y la posterior donación. Si la familia se niega, se retirarán las medidas de soporte vital aplicadas, reorientando el tratamiento hacia medidas de confort. También cabe la opción del ingreso del paciente en UCI y, una vez en la unidad, realizar la entrevista con la familia planteándoles las diferentes opciones de actuación. En las primeras horas de atención extrahospitalaria o de ingreso en urgencias, la familia se encuentra en un estado de bloqueo psicológico y bloqueo emocional que, a veces, no les permite asimilar toda la información.
Paciente ingresado en la UCI en el que se plantea la limitación del tratamiento de soporte vital. La entrevista con la familia se dirige al mantenimiento del paciente como donante potencial hasta la instauración de la muerte encefálica, o si la familia decide continuar con la retirada del soporte vital, se puede plantear la opción de la donación en asistolia controlada.
En cualquier caso, se ha de dejar constancia en la historia clínica del paciente las opciones que se han planteado a la familia, y la decisión que ésta ha tomado.
El concepto de entrevista en CIOD difiere del concepto de entrevista para la donación de órganos. La entrevista previa se realiza para informar a la familia de la situación del paciente con daño cerebral catastrófico, antes de que se instaure la muerte encefálica, y va dirigida a la solicitud del consentimiento para establecer CIOD.
Debe estar liderada por el coordinador de trasplantes, ya que es el profesional más formado y capacitado para este fin.
La información debe ser clara, proporcionándose de manera comprensible y adaptada a las necesidades de cada familia. Debe ser progresiva, de manera que en un principio se informará del pronóstico de extrema gravedad.
Una vez que la familia ha aceptado el pronóstico fatal, es cuando se plantea la opción de los CIOD, explicando detalladamente las medidas terapéuticas necesarias que se adoptarán para hacer posible la donación (intubación orotraqueal, conexión a ventilación mecánica, soporte vital, y sobre todo que el paciente ingresará en la Unidad de Cuidados Intensivos), y se les informará que, ante todo, se garantizará el confort y la ausencia de sufrimiento del paciente hasta la evolución definitiva de muerte encefálica.
Debe comunicarse que esta evolución ocurre en 24-72 horas generalmente, pero que en ocasiones puede prolongarse, o que finalmente ocurra que no se produzca la muerte encefálica, por lo que la familia debe saber que siempre tiene la opción de cambiar su decisión, ya que si no se produjera en el periodo de tiempo consensuado con la familia, o la familia no desea prolongar la espera, se deberán retirar los dispositivos aplicados, y los cuidados estarán orientados hacia el mantenimiento de medidas de confort, y así permitir la evolución natural de la enfermedad.
Se debe documentar en la historia clínica del paciente toda la información recogida en la entrevista con la familia, así como dejar constancia de la decisión tomada; pero el consentimiento para la aplicación de los CIOD no sustituye al Consentimiento Informado para la donación de órganos.
La siguiente fase de la entrevista es la que va destinada a solicitar el consentimiento para el inicio de medidas de soporte, una vez instaurada la muerte encefálica, para la preservación de órganos para la donación. Es otro documento que se cumplimenta en el momento que se produce el fallecimiento.
3.3. Cuidados al final de la vida del posible donante.
Todos los profesionales de la Unidad de Críticos, médicos, enfermeras, personal auxiliar, etc., adquieren la responsabilidad de asegurar el cuidado del paciente en el proceso de morir, velando por su dignidad y confort. En aquellos pacientes que se consideran posibles donantes, además, es necesario instaurar las medidas de soporte necesarias para asegurar la preservación de los órganos para trasplante, pero dando prioridad al confort dentro de los cuidados al final de la vida del paciente en situación de agonía.
Por tanto, la terapia farmacológica que utilicemos en los cuidados al final de la vida tendrá como objetivos paliar el dolor, minimizar la disnea y controlar el delirio.
- Deben retirarse las medidas de neuroprotección y de control de la hipertensión intracraneal (barbitúricos, sedantes, drenaje ventricular, soluciones hiperosmolares, etc.).
- Los fármacos bloqueantes neuromusculares (BNM) no deben iniciarse nunca en situación de limitación del soporte vital. Si el paciente los está recibiendo, deben retirarse, para poder evaluar los síntomas. Se puede administrar analgesia y sedación si precisa, de acuerdo con los objetivos marcados.
- Aunque se considera que los pacientes con daño cerebral catastrófico no sienten dolor, disnea o sufrimiento, hay cierta incertidumbre respecto a la posibilidad de que quede algún rastro de percepción residual, ya que en ocasiones se manifiesta con las respuestas fisiológicas típicas del dolor como son la taquicardia, hipertonía, sudoración, y taquipnea. La familia percibe estas manifestaciones con verdadera angustia y ansiedad; por ello, se recomienda la administración de fármacos de vida media muy corta (Propofol o Remifentanilo), que supriman estas manifestaciones y por tanto alivian el sufrimiento de la familia, pero no interfieren en el diagnóstico mientras se produce la muerte encefálica.
- Cuando pasado el tiempo de espera pactado con la familia para el desarrollo de la muerte encefálica, ésta no se ha producido y la familia no desea prolongar la espera, deben retirarse todas las medidas de soporte vital y considerar la posibilidad de la donación en asistolia controlada.
En cuanto al mantenimiento del posible donante, hasta la instauración de la muerte encefálica, el manejo será el mismo que cualquier paciente crítico, pero desestimando el tratamiento para la hipertensión craneal. La diferencia en el mantenimiento y cuidados del paciente en el que se deciden CIOD, radica en que permite anticiparnos a los cambios fisiopatológicos que se producen en el proceso de muerte encefálica. En cualquier caso, el objetivo es optimizar la perfusión y preservar la funcionalidad de los órganos objeto del trasplante.
Durante el ingreso en UCI, el coordinador de trasplantes completa la evaluación del posible donante y la viabilidad de los órganos, de la misma forma que en cualquier otro proceso de donación.
4. LIMITACIÓN DEL TRATAMIENTO DE SOPORTE VITAL (LTSV) ORIENTADO A LA DONACIÓN DE ÓRGANOS
Las Unidades de Cuidados Intensivos surgieron a mediados de la década de los 60 como consecuencia de los importantes y rápidos avances científicos y técnicos de la medicina, lo que hizo posible instaurar tratamientos para resolver enfermedades, y mejorar la supervivencia y la calidad de vida de los pacientes en muchos casos que, de otra manera, hubieran muerto irremediablemente. Como consecuencia, la atención médica se volvió más tecnificada, creando la falsa sensación de contar con recursos ilimitados para preservar la vida.
Pero en ningún caso, las técnicas de soporte vital permiten curar la enfermedad de base, y el mantenimiento artificial de las funciones vitales no debe confundirse con una mejoría de la enfermedad. Solo en aquellos casos en los que se resolvió el problema agudo, se logra que el paciente pueda desconectarse de los equipos de soporte y recuperar su funcionalidad.
Se consideran tratamientos de soporte vital en la UCI: ventilación mecánica, terapias de depuración extrarrenal, fármacos vasoactivos, la nutrición artifical (enteral y parenteral), los hemoderivados, etc.
A mediados de los años 90, coincidiendo con una corriente humanista basada en la “Humanización de las UCIs”, surge el reto de administrar adecuadamente la tecnología, de orientar de forma racional el uso de estas tecnologías hacia proteger la vida en aquellos enfermos con patologías recuperables, y limitarla en aquellos casos en los que la medicina no lo puede resolver para no alargar la vida de forma artificial.

Paralelamente, ha ido cambiando la forma de relación médico-paciente, pasando de ser una relación paternalista, a convertirse en una relación de ayuda en la que se da prioridad a los deseos del paciente, respetando su autonomía, y con una creciente responsabilidad de los profesionales, médicos y enfermeras, en las decisiones de la limitación del tratamiento de soporte vital.
Nace entonces el término Limitación del Esfuerzo Terapéutico (LET) para referirse a un tratamiento al final de la vida. Pero, aunque el término sea acertado al referirse a la retirada de medidas de soporte vital, en cuanto a los cuidados al final de la vida se siguen aplicando medidas terapéuticas para paliar el dolor, la ansiedad y mejorar el confort del paciente en proceso de fallecer, por tanto, el esfuerzo terapéutico continua.
A finales de los 80 nace el concepto de Limitación del Tratamiento de Soporte Vital (LTSV), que engloba tanto la decisión de retirar o no iniciar las medidas de soporte, cuando la enfermedad es irreversible, o el tratamiento puede ser inapropiado, fútil o inútil, permitiendo así la evolución natural e inevitable de la enfermedad hacia el proceso de muerte, como la aplicación de medidas de confort para evitar el sufrimiento, y adecuar las medidas diagnósticas y de monitorización al objetivo paliativo.
“Si los resultados no son los esperados, no hay beneficio para el paciente y por lo tanto, se considera que no está indicado seguir con el mismo, se retirará. Legal y éticamente es lo mismo omitir que retirar una terapia de soporte vital”.
Aun así, la situación clínica del paciente cambia en todo este proceso, por lo que la adecuación de medidas y procedimientos debe formar parte del plan de cuidados individualizados de cada paciente, y sería más acertado utilizar el término “adecuación del esfuerzo terapéutico”.
La decisión de LTSV debe tomarse por consenso de los profesionales implicados en el cuidado del paciente, la SEMICYUC recomienda que la decisión de LTSV debe discutirse colectivamente, médicos y enfermeras, y tomarse por consenso. La decisión de LTSV debe estar basada en la evidencia médica actual, y ante todo prevalecerá el deseo del paciente, ya sea porque se encuente capacitado en el momento, o porque ha dejado constancia a través de sus Voluntades Anticipadas. El equipo médico que atiende al paciente lo comunica y explica la situación a sus familiares, y en aquellos casos en los que no se está de acuerdo con la decisión, la participación del Comité de Ética Assitencial puede resolver el conflicto y facilita el consenso.
“Conocer las voluntades del paciente ante la toma de decisiones, y establecer mecanismos para el respeto a su voluntad, se concibe como una expresión del respeto a la dignidad personal, de especial relevancia en el final de la vida”.
Toma de decisiones clínicas
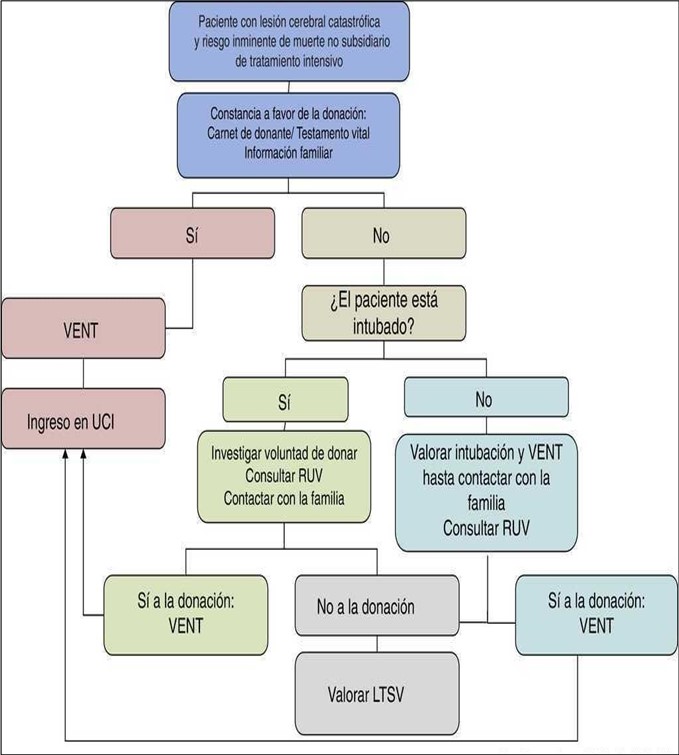
Fuente: Medicina intensiva y donación de órganos. ¿Explorando las últimas fronteras?
NOTA: RUV: Registro de últimas voluntades.
Para que el paciente, o sus familiares, puedan formar parte de la toma de decisiones se les debe informar de forma clara, asegurándose en todo momento que han comprendido la información proporcionada. Nunca se debe responsabilizar ni a familiares ni al propio paciente de la decisión, sea cual sea, ni el profesional debe influir ni coaccionar en esta decisión.
En este punto, es necesario señalar que las medidas de LTSV no tienen implicación penal ni constituyen hecho de delito, siempre que estén avaladas con una adecuada indicación y aplicación. La LTSV no produce la muerte del paciente, sino que permite que llegue como resultado natural de su enfermedad; mientras que la eutanasia es la acción directa e intencionada, encaminada a provocar la muerte de una persona previa a su petición expresa.
Recientemente en nuestro país se ha aprobado la Ley Orgánica 3/2021 de 24 de marzo, que regula la eutanasia y el suicidio médicamente asistido: el profesional sanitario proporciona los medios necesarios para que la persona pueda suicidarse de forma efectiva, previa petición expresa del paciente.
Continuando con la definición de términos relacionados con los cuidados al final de la vida, la “Doctrina del doble Efecto” hace referencia a la administración de fármacos con el fin de hacer posible el máximo confort del paciente, aunque de forma colateral supongan acortar brevemente la vida del paciente. La DDE no tiene que ver con la administración de fármacos para acabar con la vida del paciente de forma acelerada.
La Sociedad Española de Cuidados Paliativos define como sedación paliativa la administración de fármacos a un paciente terminal, previo consentimiento expreso y por escrito del paciente o familiar, en las dosis y combinaciones de fármacos necesarias para reducir su nivel de conciencia y aliviar los síntomas que le causan sufrimiento.
4.1 Aplicación de la Limitación del Tratamiento de Soporte Vital.
En general, las formas de LTSV en Medicina Intensiva son:
- Limitación para el ingreso en la UCI.
- Ingreso en la UCI de paciente en los que ya se ha decidido retirar o no iniciar algún tipo de medida terapéutica, incluída la reanimación cardiopulmonar.
El tipo de LTSV depende de las características de cada enfermedad, e incluso de cada paciente, considerándolo como parte del plan de cuidados al final de la vida. Por ejemplo, se recomienda evitar la LTSV en los primeros días de evolución del paciente con patología neurocrítica grave, realizando en un principio un tratamiento agresivo con fines curativos, y observando la evolución antes de tomar cualquier decisión.
En la práctica diaria, los escenarios en los que nos encontramos la aplicación del LTSV se pueden clasificar en 5 grupos.
Omisión o retirada del soporte vital en la UCI. La omisión, o no iniciar un tratamiento, es un acto pasivo, en base a que el tratamiento no va a producir ningún beneficio para el paciente. En ocasiones, la futilidad de un tratamiento solo puede comprobarse observando el resultado “Trial of Therapy”, por lo que en un principio se instaura el tratamiento, y si no se obtiene el beneficio esperado, será retirado.
La retirada del tratamiento es un acto activo que supone una mayor responsabilidad para el médico responsable del paciente.
“El periodo de tiempo desde el inicio de la limitación hasta el fallecimiento del paciente es menor después de la retirada del soporte vital que tras el no inicio, lo que supone acortar la agonía para el paciente, y menor estrés para la familia y profesionales”.
Órden de no RCP. Es la limitación más frecuente, y se plantea tanto en el Servicio de Urgencias como en la UCI, como en cualquier otro servicio del propio hospital. Lo que sí es común en cualquier situación, es que la órden de no RCP debe constar por escrito en la historia clínica del paciente, una vez valorada por el médico responsable, y consensuada con la familia, con el propio paciente si es posible, y con el resto del equipo médico y de enfermería.
Ingreso en UCI con tratamiento limitado. Se realiza en pacientes de edad avanzada y con gran número de comorbilidades, ante la agudización de un proceso determinado,
para ofrecer la posibilidad de sobrevivir a dicho proceso; pero se consensua con la familia, y con el propio paciente, no aplicar tratamientos más agresivos.
También se considera en estos pacientes la aplicación de tratamientos intensivos sin limitaciones, condicionados en un tiempo limitado, generalmente 48-72 horas, de tal forma que, si en ese periodo de tiempo el tratamiento resulta fútil, se retiran las medidas adoptadas y el tratamiento se orienta hacia el confort del paciente.
No ingreso en la UCI. Este tipo de limitación se da siempre fuera de la UCI, ya sea en Urgencias o en cualquier servicio del hospital, generalmente con paciente de edad avanzada, con múltiples comorbilidades y patologías crónicas avanzadas.
En la Unidad de Críticos, el proceso de donación de órganos siempre va unido a los cuidados al final de la vida. Es fundamental explicar a la familia, una vez han aceptado la limitación del soporte vital, la posibilidad de la donación.
En este caso se nos plantean dos opciones, retirar la ventilación mecánica y que la muerte se produzca por criterios cardiorrespiratorios, o continuar con el soporte y que la muerte aparezca por criterios neurológicos o muerte encefálica.
5. LA EXTRACCIÓN DE LOS ÓRGANOS EN EL QUIRÓFANO.
Una vez que se ha terminado con el proceso de valoración del posible donante, se considera que es válido para la donación, la familia acepta y comprende el proceso que se realizará, y se han cumplido los trámites legales, el donante fallecido es traslado al quirófano para realizar la extracción/obtención de los órganos susceptibles de donación.
La documentación necesaria para realizar la extracción, que previamente debe estar cumplimentada, es: autorización para la extracción de órganos, certificado de muerte, autorización judicial en caso necesario, acta de extracción en la que se especifican los órganos que se van a extraer, y un dosier con toda la información necesaria sobre el donante para cada equipo (extractor y trasplantador), que debe incluir un informe detallado sobre las características del donante y del órgano del trasplante, con los estudios y resultados que se han realizado, cual ha sido el proceso de extracción del órgano y las soluciones de preservación utilizadas.
El coordinador de trasplantes del hospital de extracción es el encargado de supervisar todo el proceso de la obtención de órganos: el traslado del donante al quirófano, coordinar a los equipos extractores y a los equipos trasplantadores, que, además, pueden pertenecer al mismo hospital o pueden trasladarse desde otro centro, y que también son responsables de todo el proceso. El coordinador también será el encargado de que los órganos se mantengan en condiciones óptimas de perfusión y oxigenación una vez extraídos, y de su envasado y etiquetado, para que lleguen a su destino junto a la documentación necesaria.
La ONT se encarga de la gestión y coordinación de los aspectos logísticos relacionados con la extracción, como son programar la hora en la que debe realizarse según el tiempo que durará el transporte y disponibilidad de personal extractor-implantador, validez de los órganos, y, junto al coordinador del hospital extractor, se encargan de la disponibilidad de los quirófanos y del personal, sobre todo del material específico para la intervención, como son la preparación y mantenimiento de la cadena de frío para los líquidos de preservación, y del material necesario para el empaquetado y etiquetado de los órganos.
La ONT asigna los órganos siguiendo los criterios de distribución establecidos, tanto territoriales como clínicos:
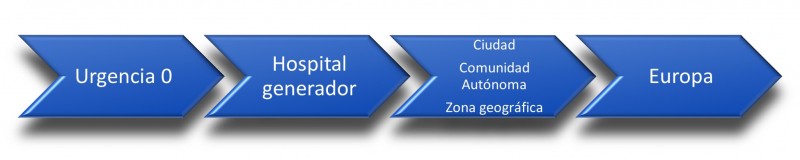
El traslado del donante fallecido desde la UCI al quirófano es un momento delicado y crítico, en el que se debe asegurar la preservación de los órganos, sobre todo de los pulmones, ya que son susceptibles de deteriorarse e invalidarse por las desconexiones de los respiradores (respirador de UCI - respirador de traslados - respirador de quirófano), siendo necesario utilizar estrategias de ventilación de protección pulmonar y maniobras de reclutamiento.
Es necesario tener previsto el material quirúrgico necesario para la extracción, incluído un desfibrilador. En el quirófano, se mantendrá la misma monitorización en el donante fallecido que en la UCI (monitorización hemodinámica básica y avanzada) para detectar y actuar en caso de inestabilidad hemodinámica, hipotermia, trastornos del ritmo, etc. Una vez que los equipos extractores llegan al quirófano, se comunica a la ONT que se inicia la extracción de los órganos. Es fundamental la coordinación entre todos los equipos extractores para que cada uno tenga definido su momento de actuar y evitar así improvisaciones que podrían provocar la pérdida de órganos.
La extracción de los órganos es un proceso complejo, que conlleva la actuación y coordinación de varias disciplinas quirúgicas (torácica, abdominal, cardiaca, etc.), y comprende dos fases bien diferenciadas:
- Cirugía “in situ” o extracción: se practica en el donante de órganos con el objetivo de extraer un órgano sano y viable.
- Cirugía “ex situ” o cirugía de banco: consiste en la preparación final del órgano ya extraído y perfundido, y se efectúa fuera del cuerpo del donante.
En el momento de la extracción de órganos, el donante puede encontrarse hemodinámicamente estable o inestable. En el caso del donante inestable, con riesgo de parada cardiaca, es necesario realizar técnicas de extracción súper-rápidas, sin apenas disección de los órganos a extraer, siendo prioritario salvar el máximo número de órganos. Si el donante se encuentra hemodinámicamente estable, permite la disección, canulación, perfusión y extracción reglada de los órganos.
La técnica quirúrgica y la incisión, dependerá de los órganos que se ha decidido extraer, ya sea abdominal (laparotomía), torácica (esternotomía) o de ambas. Una vez realizada la incisión, se hace palpación y una primera inspección visual para detectar anomalías en los órganos, e incluso pueden tomarse muestras para realizar biopsias si fuese necesario (el resultado debe tenerse antes de finalizar la extracción o previa al implante de los órganos). Esta primera inspección se comunica a la ONT, y una vez aceptados los diferentes órganos se le comunica al coordinador, que a su vez lo notifica a los centros implantadores, y se continúa con la intervención los diferentes equipos extractores.
Después se realiza la disección de los órganos, siempre en este orden:
1º órganos torácicos: corazón y pulmón.
2º órganos abdominales: hígado, páncreas, intestino y riñones.
Una vez diseccionados los órganos, el anestesista los hepariniza (heparina sódica), y se procede a la canulación, camplaje y exanguinación. Tanto la disección como la canulación lo hacen los equipos extractores, de forma simultánea y coordinada. Debe registrarse la hora en la que se realiza el camplaje y comunicarlo a la ONT.
Se inicia entonces la primera fase de la preservación de los órganos con la infusión de las soluciones de preservación: agentes o procedimientos químicos, físicos o de otro tipo con la finalidad de detener o retrasar el deterioro que sufren los órganos, desde el fallecimiento hasta el trasplante en el caso de donación en asistolia, o desde su extracción hasta su trasplante en el caso de muerte encefálica o donación de vivo.
Una vez enfriados y perfundidos, se realiza la extracción de los órganos, siguiendo el mismo orden en el que se ha realizado la disección: órganos torácicos, órganos abdominales, injertos vasculares y extracción de tejidos.
Una vez extraídos, los equipos extractores deciden si los órganos son válidos para trasplante o no. Si se ha tomado una biopsia, se espera al resultado de la misma.
Cualquier incidente durante la extracción debe quedar documentado.
La siguiente fase es la cirguía de banco parcial o completa, con el fin de dejar preparados los órganos para el trasplante. La cirguía de banco se realiza en condiciones de hipotermia, se eliminan todos los tejidos sobrantes y se prepraran los pedículos vasculares, incluyendo las reconstrucciones arteriales y/o venosas. Esta cirugía puede hacerse en el centro de obtención, o cuando el órgano llega al centro trasplantador.
Se procede entonces a la preservación de los órganos extraídos. La extracción, el almacenaje y el trasplante de un órgano alteran ya de por sí, la homeostasis del propio órgano y puede ser determinante para que sea funcional tras el trasplante. La lesión del órgano ocurre como resultado del tiempo de isquemia, tanto de la isquemia caliente (periodo que comprende desde la interrupción de la circulación del órgano hasta la perfusión con la solución hipotérmica de preservación), como de la isquemia fría, (periodo que comprende desde la perfusión hipotérmica del órgano hasta su trasplante en el receptor).
En la actualidad, el método más utilizado de preservación de órganos es la preservación hipotérmica mediante conservación en frío. Para ello se infunden líquidos a baja temperatura (4º C por norma general) que enfrían el órgano y realizan un lavado intravascular por arrastre.
Otras técnicas de preservación son:
Preservación en máquina de perfusión hipotérmica (MPH). Tras el lavado inicial en el quirófano, el órgano se introduce en un dispositivo que mantiene un flujo controlado de forma continua o pursátil, con solución de preservación fría (0-4º C) que permite además limpiar de microtrombos del torrente circulatorio y eliminar los productos metabólicos finales.
Preservación normotérmica, con líquidos de preservación a temperatura 25-37ºC que han demostrado potenciales beneficios, sobre todo en órganos procedentes de donación en asistolia, al disminuir las resistencias vasculares y favorecer el aumento de la liberación de oxígeno.
Los tiempos de preservación dependen del propio órgano; por ejemplo, corazón y pulmón requieren tiempos de preservación fríos muy cortos, mientras que el riñón puede almacenarse durante 40 horas.
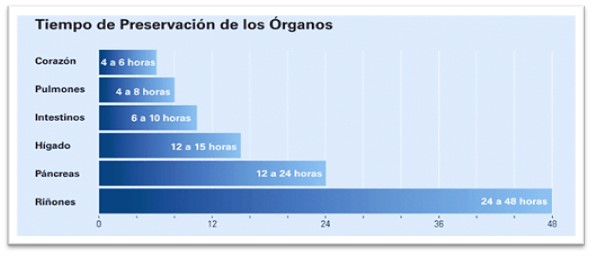
|
Fuente: organ-viability-chart-in-spanish- citar bien840x390.gif_1798549306 Donante de órganos |
El empaquetado de los órganos, una vez realizada la preservación correcta, se realiza de forma individualizada para cada órgano. Como norma común, cada órgano se introduce en doble bolsa, en un contenedor rígido estéril y en hielo, para asegurar la temperatura adecuada durante el transporte. Cada órgano irá acompañado de muestras de tejido: ganglio, bazo y sangre, según lo que indique el equipo de trasplante.
Cuando el órgano debe trasladarse a un centro diferente del centro de obtención, se acompañará de la siguiente documentación (Artículo 12 del Real Decreto 1723/2012):
- Etiquetado exterior, común entre comunidades y países europeos, en el que consta una indicación de que se traslada un órgano humano, especificando el tipo de órgano y su ubicación anatómica:
“Órgano humano para trasplante. Manipular con cuidado”

Fuente: Transporte y logística internacional-WordPress.com organismo oficial
- Procedencia y destino del órgano (centros de obtención y centro de trasplante), con el nombre de los responsables del envío y la recepción, con sus respectivas direcciones y números de teléfono.
- Día y hora de salida del centro de obtención.
- Recomendaciones de transporte (temperatura y posición adecuadas).
- Informe sobre las características del donante y del órgano, su extracción y las soluciones de preservación utilizadas.
- Los estudios realizados y sus resultados.
La reconstrucción del cadáver debe ser muy cuidadosa y con el máximo respeto, y es fundamental mantener la dignidad del cadáver y el aspecto externo, que generalmente no cambia de forma apreciable, y solo queda una cicatriz suturada en la piel del tórax y abdomen.
En el caso de extracción de tejidos, como córneas o huesos, se colocan prótesis para recuperar el volumen y firmeza tras la extracción. El coordinador debe asegurarse de que se ha realizado correctamente antes de ser entregado a la familia.

BIBLIOGRAFÍA
- Abradelo de Usera M, Muela A, Aldabó Pallás T, et al. Donación en asistolia en España: Situación actual y recomendaciones. Documento de consenso nacional 2012 [Internet] 2012. Disponible en: http//www.ont.es.
- Actividad de donación y trasplante. España 2019. Memorias ONT [Internet]. Disponible en: http://www.ont.es/infesp/Memorias
- Alonso M, Álvarez Miranda M, Álvarez Vázquez M, et al. El modelo español de coordinación y trasplantes. ONT [Internet]. Madrid: Grupo Aula Médica SL; 2008. Disponible en: http//www.ont.es
- Álvarez Rrodríguez J. Coordinación del equipo de trasplantes. Revistas científicas. [Internet] 1999. Disponible en: http://revistas.ucm.es
- Aristizabal AM, Caicedo LA, Martínez JM, et al. Xenotrasplantes, una realidad cercana a la práctica clínica: revisión de la literatura. Cirugía española [Internet] 2017; 95 (2): 62-72. Disponible en: http://www.elsevier.es.
- Benítez Hernández P. Cuidados de enfermería al paciente donante de órganos y tejidos en muerte encefálica. Revisión bibliográfica [Internet]. Universidad de la Laguna, 2020. Disponible en:https://riull.ull.es/xmlui/bitstream/handle
- Cano Ochando E, Nistal Villan E. Avances y retos en investigación en el trasplante de órganos. Fundación Ramón Areces. Revista-fra [Internet]; (22): 104-117. Disponible en: https://www.fundacionareces.es/recursos/doc/portal/2019/12/27
- Carnevale Romina P. La impresora de órganos. Ficciones y realidades de la producción de tejidos artificiales. Química Viva [Internet]. 2010; 9(2): 76-85 Disponible en: https://www.redalyc.org/articulo.oa
- César Juárez ÁA, Olivos Meza A, Landa Solís C, et al . Uso y aplicación de la tecnología de impresión y bioimpresión 3D en medicina. Rev. Fac. Med. [Internet] 2018; 61 (6): 43-51. Disponible en: http://www.scielo.org.mx/scielo.
- Ciria R, Garrote D, Briceño J, et al. Donación en asistolia. Medicina clínica monográfico [Internet] 2012; 13 (1): 7–11. Disponible en:http//www.elsevier.es
- Consideraciones éticas en el trasplante de donante vivo. Comité de Bioética de Catalunya [Internet] 2012.Disponible en: http://canalsalut.gencat.cat
- Cuidados Intensivos orientados a la donación de órganos. Recomendaciones. Grupo de trabajo SEMICYUC-ONT [Internet] 2017. Disponible en: http//www.ont.es
- De Frutos MA, Daga D, Ruiz P, Requena MV. Donantes de órganos. Visto en: www.sld.cu/galerias/pdf/sitios/pdguanabo/transp.pdf
- d´Empaire G, de d´Empaire ME, Encinoso J. Limitación de medidas terapéuticas en los pacientes críticos. Gac Méd [Internet] 2002; 110 (1): 92-109. Disponible en: http://ve.scielo.org/scielo.php
- Díaz A. Número total de trasplantes de córnea realizados en España 2011-2017. Visto en: es.statista.com
- Documento de Consenso del Grupo deEstudio de la Infección en el Trasplante(GESITRA)pertenecientealaSociedadEspañola de Enfermedades Infecciosas y MicrobiologíaClínica(SEIMC)ylaOrganizaciónNacionaldeTrasplantes(ONT)sobrelosCriteriosdeSelección del DonantedeÓrganosSólidosen relaciónalasEnfermedadesInfecciosas 2019. Disponible en Google.
- Donación cruzada. Programa nacional de donación renal cruzada en España. ONT. Versión 6.0. 2015. Visto en google
- Dueñas Jurado JM. Protocolos clínicos de actuación ante el proceso de donación y extracción de órganos y tejidos para transplante en donación en muerte encefálica. Cuadernos de Medicina Forense [Internet] 2015; 21 (1-2): 34-42. Disponible en: http//scielo.isciii.es
- Elizalde J, Lorente M. Coordinación y donación. Anales Sis San [Internet] 2006; 29 (2): 35-43. Disponible en: http://scielo.isciii.es/scielo.php
- Escudero D. Diagnóstico de muerte encefálica. Med. Intensiva [Internet] 2009; 33 (4): 185-195. Disponible en: http://scielo.isciii.es/scielo.php
- Escudero D, Otero J. Medicina intensiva y donación de órganos. ¿Explorando las últimas fronteras? Med. Intensiva [Internet] 2015; 39 (6): 366-374. Disponible en: http//www.medintensiva.org.
- Eslava Abaurrea ON, Ciganda Cenoz M, Ameztoy Echenique X. Donación en asistolia Maastricht III, concepto, manejo y cuidados de Enfermería en las Unidades de Cuidados Intensivos. Ocronos-editorial científico-técnica. [Internet] 2019. Disponible en: https://revistamedica.com/donacion-en-asistolia-maastricht-iii-cuidados-enfermeria-uci/
- Fleta Asín B., Gonzalvo Liarte MC, Cía Gómez P. Quimerismo: origen e implicaciones médicas. Revista Clínica española [Internet] 2006, 206 (7): 340-342. Disponible en: http://www.revclinesp.es
- González J. Últimos avances en el trasplante de órganos. Avances en salud [Internet] 2020. Health Tech spain.es. Disponible en: https://healthtechspein.es
- Gutiérrez E, Amado A. Selección del donante y criterios de viabilidad de los órganos: expansión de los criterios de donación. Rev Soc Esp Enferm Nefrol [Internet] 2007; 10 (2): 15-25. Disponible en: http://scielo.isciii.es/scielo.php?
- Historia del trasplante. CUCAIBA. Centro único coordinador de ablación e implante de la provincia de Buenos Aires. Ministerio de salud. Disponible en: http://www.cucaiba.gba.gov.ar/?page_id=166
- https://www.lavanguardia.com/historiayvida/mas-historias/20171130/47311455485/8-avances-que-marcaron-la-historia-de-los-trasplantes.html
- López Hernández E, Jaramillo Magaña JJ, Solís H. Alteraciones fisiopatológicas en la muerte encefálica: su importancia para decisiones de manejo y donación de órganos. Gac. Méd. Méx [Internet] 2004; 140 (2): 199-209. Disponible en: http://www.scielo.org.mx/scielo.php?
- Martí Manyalich V. Evolución del procuramiento de órganos en el mundo. Revista médica clínica las Condes [Internet] 2010; 21 (2): 145-151. Disponible en: https://www.elsevier.es
- Miñambres García E, et al. Protocolo Nacional de mantenimiento del potencial donante en muerte encefálica. SEMICYUC-ONT. [Internet] 2020. Disponible en: http://www.ont.es
- Pérez Villares JM. Donación en asistolia. Cuad. med. forense [Internet] 2015; 21(1-2): 43-49. Disponible en: http://scielo.isciii.es/scielo.php
- Plan estratégico en donación y trasplante de órganos. 2018-2022. Sistema español de donación y trasplante. Ministerio de Sanidad, Consumo y Binestar Social y ONT. Visto en Google
- Plan de acción para la mejora de la donación y el trasplante de órganos. “Plan donación cuarenta”. ONT. 2008. Visto en Google.
- Quesada Ballesteros A. Cuidados de enfermería en un potencial donante de órganos. Mantenimiento en UCI. Disponible en: https://www.concursos.formacionalcala.es/ganadores
- Real Padilla MJ, García Fernández JM, Nuño Calderón MC, et al. Donantes con criterios expandidos por edad. Enfermería docente [Internet]2011; 93:4-6. Visto en: http://www.index-f.com/edocente/93pdf/93-004.pdf
- Royo Vergara R. Análisis de la actuación de enfermería en la donación en asistolia controlada tipo III de Maastrich en la Unidad de Cuidados Intensivos. Elaboración de un algoritmo de actuación enfermero. Trabajo de fin de grado de enfermería. 2015-2016. Disponible en:https://academica-e.unavarra.es/xmlui/bitstream/handle
- Sanz J. Cirugía plástica en la antigüedad. Historias de la historia. [Internet] 2019. Disponible en: http://historiasdelahistoria.com
- Solar P, Ovalle R, Simian E, Escobar J, Beca JP. Tres factores que influyen en la actitud de las personas ante la donación de órganos. Rev Chil Cir [Internet]. 2008; 60 (3): 262-267. Disponible en: https://scielo.conicyt.cl/scielo.php
- Ucio P. Introducción a la figura del coordinador de trasplante intrahospitalario dentro del sistema de Salud Pública. Visto en: http://masteralianza.ont.es/download/tesinas_master_2019/Jazmin%20Ovelar.pdf
