1. PILOTA CONPNMTRAPULSACIÓ AÒRTICA.
La pilota de contrapulsació intraaòrtica (BCPIA) és el dispositiu que permet l'assistència coronària de curta durada que és més utilitzat en l'actualitat a causa del seu fàcil maneig i funcionament, així com als seus excel·lents resultats.
Com a funció principal es defineix per augmentar la circulació de la sang durant la fase diastòlica. La forma d'aconseguir-ho és omplint la pilota que es col·loca en l'aorta, de forma sincronitzada amb el cor, durant la fase de relaxació o diàstole.
A l'fer això, augmentem la pressió arterial diastòlica i vam aconseguir que augmenti la circulació coronària i, com a conseqüència, ajudem a millorar la funció de cor, quan cal.
El mecanisme bàsic per a crear assistència coronària pel qual realitza el seu efecte consisteix en un desplaçament de volums produint així un descens de la postcàrrega del ventricle esquerre (VI), i dóna com a resultat una disminució de la feina cardíac, del consum d'oxigen del miocardi i , per tant, es deriva a un augment de la pressió diastòlica que permetrà millorar la perfusió coronària a nivell proximal i la perfusió perifèrica a nivell distal.
Des del punt de vista del tipus d'assistència, s'ha de considerar com una assistència en sèrie que requereix obligatòriament l'activitat del ventricle i que provoca un augment limitat del volum d'ejecció.
Descripció i funcionament.
És una pilota inflable, que va inserit sobre un catèter, i que es col·loca en l'aorta toràcica descendent a uns 2 cm. distal a la subclàvia esquerra.
El seu inflat i desinflat es realitza amb gas comprimit que té la consola base i, està sincronitzat amb l'ECG del pacient o la seva pressió arterial.
Quan la pilota es sincronitza amb l'electrocardiograma, ho fa amb les ones R i T. L'ona R coincideix amb la sístole ventricular per al desinflat i l'ona T és l'índex elèctric de la diàstole per l'inflat.
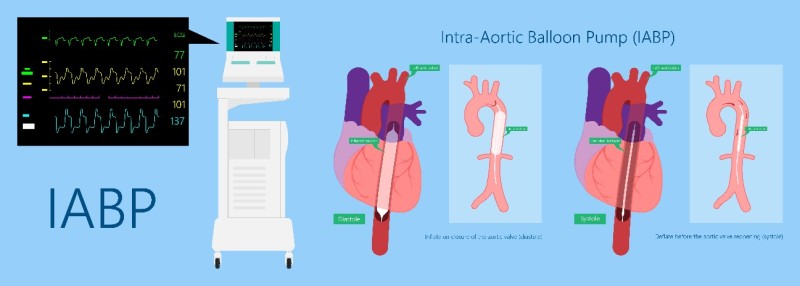
Imatge 45: BCPIA
En obrir-se la vàlvula aòrtica que es realitza durant la sístole, la pilota col·locada s'acaba de desinflar, i provoca una reducció sobtada i significativa de la PA facilitant la injecció ventricular. En reduir la postcàrrega, es redueix l'estrès de la paret ventricular i el consum miocàrdic d'oxigen.
En tancar-se la vàlvula aòrtica, és a dir, durant la diàstole s'infla la pilota, augmentant així la pressió arterial i desplaça la sang augmentant el flux coronari, augmentant lleument el dèbit cardíac.
Abans de la inserció de la pilota en l?aAorta, és molt important assegurar-se triar la mida adequada per al pacient, hi ha diferents models que dependran de les recomanacions comercials segons la talla del pacient i està disponible en diversos volums, principalment de 30, 40 i 50cc .
Així mateix, també cal recordar que, un cop inflat, la mida de la pilota no ha d'excedir del 80-90% del diàmetre de l'aorta descendent.
En l'actualitat dit procediment es realitza a les sales d'hHemodinàmica, sota fluoroscòpia, el catèter s'insereix per via percutània en l'artèria femoral, encara que també pot inserir de manera percutània a través de l'artèria braquial.
Un cop introduït, s'ha de col·locar a l'aorta descendent, amb la punta que és radiopaca a uns 2-3cm per sota de l'artèria subclàvia esquerra.
Depenent de l'hemodinàmica del pacient en el moment, els cicles de l'BCPIA es poden programar cada cicle cardíac del pacient o espaiar (1: 2, 1: 4, 1: 8) segons la freqüència cardíaca del pacient.
Així mateix, el deslletament de l'aparell s'ha de fer mitjançant la disminució en el ritme de ciclat.
La pilota ha de mantenir-se contrapulsant fins a la seva retirada, no pot estar aturat més de 15 min. És important mantenir-lo amb heparina per no coagular el catèter.
Indicacions.
El BCPIA està indicat per a pacients amb fallada ventricular esquerra o en diagnòstic de xoc cardiogènic que no responen al tractament farmacològic i en què hi ha una lesió potencialment reversible. La finalitat del dispositiu és proporcionar suport circulatori fins que es resolgui la fase aguda d'isquèmia cardíaca o de fallida cardíaca.
Contraindicacions.
El BCPIA està contraindicat davant la presència d'insuficiència aòrtica, ja que empitjora la regurgitació.
D'altra banda, no ha de ser col·locat en pacients amb sospita o certesa de dissecció aòrtica, ja que la seva col·locació a la falsa llum pot desembocar en l'augment de la dissecció o fins i tot en ruptura aòrtica.
L'existència d'aneurismes abdominals de grans dimensions pot facilitar el trencament de l'aorta a aquest nivell.
La inserció percutània del BCPIA s'ha d'evitar en pacients amb malaltia vascular perifèrica greu, ja que pot precipitar la trombosi intravascular o l'embòlia amb isquèmia de l'extremitat.
I també, encara que no és contraindicació absoluta, la col·locació d'un BCPIA ha de ser acuradament valorada en pacients amb septicèmia o alteracions greus de la coagulació. Es valorarà en aquests casos el factor risc / benefici per al pacient.
Cures d'infermeria durant i després del procediment.
Les cures d'infermeria durant tot el procés de col·locació i les seves cures pre i post col·locació així com la seva retirada, aniran encaminats cap al benestar del pacient i proporcionar les mesures necessàries per disminuir la seva ansietat davant del procediment desconegut per a aquest.
Explicarem el procediment i les possibles sensacions que pot experimentar, des de la punció fins al seu funcionament.
Escoltar les preocupacions del pacient i resoldre els seus dubtes.
Vigilar i realitzar el control d'infeccions.
Monitoratge respiratori i signes vitals.
Les cures Post-procediment:
Repòs absolut en llit amb canvis posturals segons protocol hospitalari.
Monitoratge de constants vitals.
Avaluar posicionament del catèter comprovant la posició de la consola amb determinació analítica constant d’hemograma i coagulació (risc de trombosi de catèter)
Control de l'existència de sagnat o hematoma.
Avaluar punt d'inserció femoral, polsos distals, coloració i temperatura de l'extremitat afectada.
2. MARCAPAÀSSOS TEMPORAL.
El marcapassos temporal o transitori es pot definir com un dispositiu electrònic que permet iniciar les contraccions miocàrdiques quan l'estimulació pròpia del cor és insuficient, ja sigui per falta de conducció dels impulsos elèctrics o perquè la freqüència sigui massa baixa per mantenir una despesa cardíac adequat.
Imatge 46: dispositiu marcapassos intern
Indicacions:
- En infart agut de miocardi. Les indicacions per al marcapassos en aquest context inclouen el desenvolupament d'un nou bloqueig de branca de novo.
- En cas de Bradicardia. El marcapassos temporal està indicat en pacient amb bradicàrdia hemodinàmicament significativa.
- S'indica per sobreestimular i acabar un flúter auricular, taquicàrdia supraventricular i taquicàrdia ventricular monomòrfica sostinguda.
- Com a tractament pont fins implantació de marcapassos permanent en pacient amb bloqueig AV complet, bloqueig de segon grau i disfunció sinusal severa.
- En casos de taquicàrdia ventricular.
- Miocarditis de manera profilàctica, en procediments d’intervencionismes amb risc.
Contraindicacions.
Pacient amb problemes d'accés vascularCoagulació amb INR
Descripció i funcionament.
El marcapàs transitori està format per un generador amb el qual es poden establir els següents paràmetres:
2.1 Intensitat de sortida (Output).
Un cop col·locat el catèter de marcapassos, la persona circulant comença elevar la intensitat fins que apareix en el monitor de registre cardíac l'espícula originada per ell, seguida per un QRS ample, que serà indicatiu propi d'una estimulació ventricular. La intensitat necessària perquè es desencadeni aquest complex es denomina llindar d'excitació. Generalment, quan un marcapassos intern està situat, el llindar d'excitació és inferior a 1 mA.
Seguidament elevarem la intensitat fins al doble del llindar per garantir que en cap cas serà insuficient. No és convenient pujar més del doble perquè correm el risc de danyar la paret cardíaca.
2.2. Freqüència cardíaca.
Es defineix com el valor que representa el nombre de vegades que el marcapassos funciona per minut. Si aquest manté un ritme acceptable en el pacient, establirem una freqüència sobre 50 sístoles per minut, perquè no interfereixi en l'activitat cardíaca. Si el pacient no és capaç de mantenir una freqüència suficient s'ha de pujar la freqüència per aconseguir una despesa cardíac adequat.
És important saber que el fet d'estimular només el ventricle, el volum d'ejecció es veu reduït en un 20% a conseqüència de la falta d'aportació auricular. L'increment més significatiu de la despesa es produeix amb freqüències de 80- 90 impulsos / min. Però això eleva el consum d'oxigen a nivell de miocardi, de manera que, generalment, no s'ha de sobrepassar freqüències de 70- 80 impulsos / min.
2.3. Sensibilitat.
S'encarrega de regular l'eficiència del marcapassos per detectar l'activitat elèctrica intrínseca. La seva mida és en milivolts i s'ajusta per permetre que el marcapassos controli per demanda, és a dir quan no percebi activitat elèctrica.
El generador del marcapassos genera un corrent que es transmet per l'electro-catèter i arriba fins l'elèctrode, en entrar en contacte directe amb el cor del pacient. Aquest estímul produeix la despolarització miocàrdica i posteriorment, l'estímul torna al generador i completa així el circuit elèctric. L’electrocatèter pot ser intravenosos o epicàrdic.
L'estimulació temporal transvenosa és la forma més habitual que s'utilitza i es realitza mitjançant punció en vena jugular interna dreta, de la vena subclàvia dreta o de la vena femoral, i es dirigeix l'elèctrode al ventricle dret.
2.4. Cures d'infermeria.
Valorar l'estat actual del pacient per evitar o detectar precoçment les possibles complicacions intra o postoperatòries.
Valorar coneixement del pacient sobre el procediment i el seu estat emocional.
Comprovar via venosa permeable per al procediment.
Monitoratge de les constants vitals.
Un cop implantat s'ha d'examinar la zona de punció del catèter com a mínim un cop al dia, prevenir signes d'infecció i tapat amb apòsit estèril, igual que el procediment que ha de ser el més estèril possible.
Es realitzarà ECG de 12 derivacions diàriament
Comprovar la funció del marcapassos diàriament, i determinar els llindars de sensibilitat i estimulació, així com el ritme basal del pacient, disminuint la freqüència d'estimulació gradualment fins al cessament.
Complicacions.
La col·locació d'un marcapassos transitori pot estimular músculs, de vegades això pot generar dolor, caldrà desplaçar l'elèctrode per allunyar-lo del múscul pectoral sense alterar el control del ritme cardíac per minimitzar-lo.
Desplaçament de l'electrocatèter provocant trastorns del ritme.
Infeccions tant durant com post procediment.
Pneumotòrax.
Batecs ectòpics.
Perforació de la paret del miocardi i taponament cardíac que poden arribar a comprometre la vida del pacient.
3. HIPOTÈRMIA CONTROLADA.
La hipotèrmia controlada terapèutica es defineix com l'aplicació de fred, amb l'objectiu de disminuir de manera controlada la temperatura corporal, entre 32 i 34ºC durant un període de 12 a 24 hores, disminuint d'aquesta manera, les alteracions neurològiques secundàries a l'aturada cardíaca, el consum d'oxigen a nivell cerebral i els requeriments metabòlics, entre un 6 i un 7% aproximadament per cada grau que disminueix la temperatura corporal.
El control de la temperatura corporal en un estat d'hipotèrmia té com a avantatges afavorir la neuroprotecció causa de diversos factors:
• Disminueix els processos que produeixen una mort cel·lular de manera que es redueix l'alliberament d'aminoàcids excitadors i radicals lliures.
• Reducció del metabolisme cerebral per millorar la relació d'aportació i consum d'oxigen afavorint les àrees isquèmiques.
• Antagonistal calci disminuint la lesió cel·lular.
• Modulació de la resposta inflamatòria i de l'apoptosi neuronal.
• Bloqueig de mecanismes excitotòxics com és l'alliberament de radicals lliures.
• Preservació de la síntesi proteica.
• Disminució de l'edema neurogènic.
Per aconseguir aquesta temperatura, s'utilitzen dos mètodes els anomenats intravasculars i els superficials. Sent el primer més ràpid i eficaç a l'hora d'obtenir la temperatura, però no hi ha una evidència clara sobre quin mètode és millor per això tots dos mètodes són emprats per obtenir una reducció de la hipotèrmia.
A més, durant tot el procés és important tenir un control de la temperatura i dels efectes adversos que es poden produir sent els més comuns els tremolors, infeccions, arrítmies ...
La hipotèrmia terapèutica es porta a terme en quatre fases:
- Inducció.
- Manteniment.
- Reescalfament o Rewarming.
- Estabilització tèrmica.
L'objectiu de la fase d'inducció és fer que el pacient arribi a una temperatura entre 32 i 34ºC, descendint entre 1 i 1'3ºC per hora, ja que es considera un equilibri entre els beneficis clínics i els efectes secundaris, que es veuen agreujats a temperatures més baixes.
La Societat Espanyola de Medicina Intensiva, Crítica i Unitats Coronàries (SEMICYUC) recomana dur-la a terme en els primers 20 minuts, fins i tot en el medi extrahospitalari, ja que millora de forma significativa la supervivència i pronòstic neurològic dels pacients, encara que de vegades no és possible tenir accés a aquest tipus de teràpia extrahospitalària.
La velocitat de descens de temperatura sempre depèn del mètode utilitzat.
Actualment hi ha diversos mètodes disponibles per realitzar el refredament, però l'administració de fluids intravenosos, com sèrum fisiològic o Ringer Lactat, refredats a 4ºC, és la tècnica més emprada per la seva senzillesa i rapidesa, juntament amb l'administració de bosses de gel col·locades en anglès , aixelles, coll i cap.
Aquestes tècniques són segures i eficaces, però tenen la dificultat de mantenir la hipotèrmia, per la qual cosa s'han d'associar a una altra tècnica que mantingui al pacient amb la temperatura desitjada, com, per exemple, les mantes i matalassos tèrmics.
En la fase de manteniment, l'objectiu és mantenir una temperatura corporal entre 32 i 34ºC durant 12 a 24 hores amb les mínimes diferències tèrmiques. Posteriorment, a la fase de reescalfament o rewarming, s'augmenta la temperatura del pacient entre 0'2 i 0'4ºC a l'hora, fins a aconseguir una temperatura corporal de 37ºC.
Finalment, s'ha d'aconseguir una estabilització tèrmica que consisteix a mantenir una normotèrmia controlada, en les 12 hores posteriors a aconseguir una temperatura corporal de 37ºC.
S'ha d'evitar la hipertèrmia, ja que és un factor de risc associat amb una taxa molt alta de probabilitat de mort.
El pronòstic del pacient que rep tractament d'hipotèrmia després de PCR, dependrà també de factors influents com el ritme inicial desfibril·lable, l'edat del pacient, a menor edat millor pronòstic, si la PCR ha estat o no presenciada i temps sense flux coronari.
La hipotèrmia controlada no augmenta el risc ni el nombre de complicacions en comparació amb pacients similars que no han estat tractats amb hipotèrmia terapèutica; és important recalcar que aquesta, no té efectes secundaris greus ni complicacions associades a mortalitat, de manera que risc / benefici aquesta ben diferenciat.
Tot i que la hipotèrmia terapèutica s'ha demostrat que millora la supervivència, qualitat de vida i minimitza les seqüeles dels pacients recuperats després d'una aturada cardíaca, només es porta a terme la realitzada de manera intravascular en molt poques unitats de cures intensives espanyoles, encara que la seva evolució en l'expansió i posada en marxa és molt favorable, això és degut a la manca de formació en aquestes tècniques i la sobrecàrrega de cures que la hipotèrmia terapèutica comporta, això genera prescindir-ne.
Les nombroses cures i coneixements que requereixen aquest tipus de pacients, com ara la canalització de catèters venosos perifèrics i centrals, el manteniment dels mateixos, les cures de les vies aèries, el maneig de la ventilació mecànica invasiva, el control de sedació i el monitoratge de la mateixa, el monitoratge de constants vitals, la col·locació i cures de la sonda vesical i de sistemes de monitoratge hemodinàmic, i a més la realització de les tècniques per a la inducció i manteniment de la hipotèrmia, generen de vegades dubtes o temors al personal d'infermeria no habituat a aquest procediment,per la qual cosa minimitzaria aquests temors la realització d'un pla de cures d'infermeria protocol·litzat per facilitar l'estandardització de les cures que requereix el pacient sotmès a hipotèrmia terapèutica intravascular.
Però sempre podrem aplicar les tècniques no invasives conegudes en tots els centres hospitalaris i en atenció pre-hospitalària per iniciar i realitzar la hipotèrmia terapèutica:
- Mantes i Matalassos amb sistema d'aire.
- Sistemes d'aigua circulants.
- Coixinet d'hidrogel.
- Ús de tovalloles fredes .... etc.
La seva aplicació serà distribuïda a fFront, coll, aAixelles, aAbdomen, zZona inguinal principalment.
BIBLIOGRAFIA.
- Lahera Juliá, V; Garrido Astray, C. Sistema cardiovascular. En: Tresguerres, Jesús A.F; Villanúa Bernués, M.A.; López Calderón Barreda, A, editores. Anatomía y Fisiología del Cuerpo Humano. Madrid: McGraw-Hill/Interamericana de España; 2009. p. 111-41.
- Gray, 2º tomo, Anatomía de Gray, 38ª edición, Editorial Harcout Brace, Madrid,1998, pp. 700-744.Testut, L; Latarjet, A; Tomo segundo, Tratado de anatomía humana, novena ed.Editorial Salvat Editores SA, Barcelona, 1971, pp. 4-154.
- Bouchet, A Cuilleret, J, Tórax, Anatomía descriptiva y funcional, Editorial Médica Panamericana SA, 1979, pp. 150-229.
- Monzón Martín D, Rubio Alcañiz V. Paciente portador de marcapasos. En: Guía de intervención rápida de enfermería en cuidados intensivos. 1ªed. Madrid: Difusión avances Enfermería; 2007.p.200-201
- Manual of Cardiovascular Medicine. SP. Marso, BP. Griffin, E.J Topol. Capítulo51. Marcapasos temporal endovenoso.
- Manual de procedimientos de enfermería en Hemodinámica y cardiología intervencionista. AEEC. Tema 47. Marcapaso Transitorio. V. Rubio, J. Suárez, M. Martel.
- Garatti A, Russo C, Lanfranconi M, et al. Mechanical circulatory support for cardiogenic shock complicating acute myocardial infarction: an experimental and clinical review. ASAIO J. 2007;
- Noel BM, Gleeton O, Barbeau GR. Transbrachial insertion of an intra-aortic balloon pump for complex coronary angioplasty. Catheter Cardiovasc Interv. 2003; 60:36-9.
- Müllner M, Urbanek B, Havel C, et al. Vasopressors for shock. Cochrane Database Syst Rev 2004.
- Martín-Hernández H, López-Messa J, Pérez-Vela J, Molina-Latorre R, Cárdenas-Cruz A, Lesmes-Serrano A, et al. Manejo del síndrome posparada cardíaca. Med Intensiva. 2010; 34(2):107-126.
- Carcela Salvador T, Gutiérrez Macías Á, Macías Vaz AM. Enfriar a tiempo puede salvar la vida. Doc Enferm. 2014 Sep;(55):8-11.
- Bernard SA, Gray TW, Buist MD, Jones BM, Silvester W, Gutteridge G, Treatment of comatose survivors of out-of-hospital cardiac arrest with induced hypothermia. 346(2002), pp 557-563.
- Barreña Oceja I, Gil Martín FJ, García de Vicuña Meléndez A, Rodríguez Delgadillo MÁ, Gutiérrez Herrador G, Vázquez Naveira MP. Resultados de la puesta en marcha de un protocolo de hipotermia terapéutica en la parada cardiaca consensuado entre un sistema de emergencias médicas y un servicio de urgencias hospitalario. Emergencias. 2012; 24(1):39-43.
- A. Ristic, M.izmazio, A. Yehuda, A. Anastasakis, L.P.Badano, A.Brucato, et al. Triage strategy for urgent management of cardiac tamponade. Eu Hear J., 35(2014)pp 2279-2284
- Lawin Peter. Cuidados intensivos. Barcelona: Salvat 2006
- European Resuscitation Council 2015. Consejo de Resucitación Cardiopulmonar.
- Miguel R de et al. Manual del cuso de Sindrome coronario Agudo. Diagnostico y tratamiento y cuidados de enfermeria. Madrid MC Graw Hill 2003
- Yaraví FD. El gasto cardíaco; Disponible fcm.uncu.edu.ar/medicina
- Serrano Poyato, C; Alonso Moreno,A. Garcia Rueda,S. Procedimientos intervencionistas percutáneos especiales. Pericardiocentesis. Capitulo VII. Tema 26.1 195-200 Asociación española de Cardiologia.
- Hochman JS, Sleeper LA, Webb JG, et al. Early revascularization in acute myocardial infarction complicated by cardiogenic shock. N Engl J Med. 1999; 341: 625-34.
- Gandhi SK, Powers JC, Nomeir AM, et al. The pathogenesis of acute pulmonary edema associated with hypertension. N Engl J Med. 2001; 344: 17-22.
- Vega JA, Avilés F, Preparación del paciente y cuidados generales. Aribay V, Gómez M, Jimenez R, Santos S, Serrano C; Manual de enfermeria en cardiología y hemodinamica. Protocolos Unificados 2007,416 pp.
- D’Ortencio AO,Lauga A,Perel C. Balón de contrapulsación intraaortico. Insuficiencia Cardíaca.2008; 3(4):184-195
- Cuenca JJ, Fojón S.Manual de contrapulsación intraaortica.Barcelona.Edikamed; 2012.
- Fuente Ramos M. Enfermería médico-quirúrgica. Col. Enfermeria S21. 3ed. Madrid: Difusión Avances de Enfermeria (DAE);2015
- Mancia G, Fagard R, Narkiewicz K, Redon J, Zanchetti A, Böhm M, et al. Guía de práctica clínica de la ESH/ESC 2013 para el manejo de la hipertensión arterial. Rev.Esp. Cardiologia 2013; 66(11): 880.e1-e64.
- Royo-Bordonada MA, Lobos Bejarano JM, Villar Álvarez F, Sans S, Pérez A, Pedro-Botet J, et al. Comentarios del Comité Español Interdisciplinario de Prevención Cardiovascular (CEIPC) a las guías europeas de prevención cardiovascular 2012. Rev. Esp. Salud Pública 2013; 87:103-20.
- Álvarez, J. M., J. M. Maroto, y L. F. Arós. Guia del enfermo coronario.Madrid: Sociedad Espanola de Cardiologia, 2006.
- María Cruz Martín Delgado, José Luis García Garmendia, María Paz Fuset Cabanes, Enrique Fernández-Mondéjar. Competencias profesionales y trabajo en equipo en pacientes con enfermedades cardiacas agudas y críticas.Rev Esp Cardiol. 2016;69:63210.1016/j.recesp.2016.01.026
- G.D. Perkins, et al., European Resuscitation Council Guidelines 2021: Executive summary, Resuscitation (2021) Traducción oficial al castellano del Consejo Español de RCP (CERCP)
- Part 1: introduction to the International Guidelines 2000 for CPR and ECC . A consensus on science. European Resuscitation Council.Resuscitation 2000; 46:315, doi:http://dx.doi.org/10.1016/s0300-9572(00)00269-0.
