Espanya ha desenvolupat una activitat de donació i trasplantament extraordinària, fonamentada bàsicament en la donació d'òrgans en mort encefàlica (ME), i compta amb mesures d'índole organitzatives, legislatiu i polític, i el suport sanitari necessari, totes elles encaminades d'optimitzar la identificació de donants potencials i convertir-los en donants reals.
No obstant això, la reducció de la mortalitat en situacions compatibles amb la donació en ME, com són la reducció de mortalitat per accidents de trànsit o malalties cerebrovasculars, i l'augment de supervivència de pacients crítics i neurocrítics, contribueixen a que el potencial de donació a mort encefàlica sigui cada vegada més insuficient per cobrir la demanda d'òrgans del nostre país. Si li afegim el canvi que es produeix en el perfil del donant en ME, sent aquests donants més anyencs i amb més comorbiditats (DCE), fa que progressivament sigui un procés de menor rendibilitat i amb menor expectatives d'èxit.
La donació en asistòlia, al nostre país, arrenca en la dècada dels 80 amb experiències aïllades a Madrid, Barcelona i la Corunya, gràcies a una estreta col·laboració entre els serveis d'emergències i els coordinadors de trasplantaments.
Però és a partir de 2012, amb el Document de Consens Nacional de Donació en asistòlia, ia través d'un programa en què es requereix la col·laboració de metges de diferents especialitats, tant intra com extrahospitalaris, dels coordinadors de trasplantaments, i de jutges i forenses, quan aquest tipus de donació es converteix en una pràctica habitual en els nostres hospitals, fins al punt que, en l'actualitat, un de cada quatre donants ho és en DA.
La donació en asistòlia forma part del Pla Estratègic de l'ONT per augmentar l'índex de trasplantaments. I tot i l'experiència adquirida en aquest camp, l'índex total d'òrgans trasplantats segueix sent inferior als de la ME, i l'índex de donants a DA descartats és superior als descartats en ME.

La Primera Conferència Internacional sobre Donació en asistòlia es va celebrar a Maastrich el 1995, i identificava quatre categories de donants en asistòlia depenent del context en què es produïa l'aturada cardiorespiratòria. I tot i que aquesta classificació és la que s'utilitza en l'àmbit internacional, no capta la realitat del nostre país pel que fa al tipus de DA que es porta a terme. L'experiència ha demostrat la necessitat de diferenciar entre la parada cardiorespiratòria (PCR) que es produeix en el medi extrahospitalari, de la qual es produeix en el medi hospitalari.
Sorgeix llavors la classificació de Maastrich modificada (Madrid 2011), que recull dos grans grups:
- Donació en asistòlia no controlada (DA no controlada).
Tipus I. Morts fora de l'hospital que no són ressuscitats per diverses raons.
Tipus II. Ressuscitació infructuosa: pacients que pateixen una PCR i en els quals les maniobres de reanimació no tenen el resultat esperat. A més, aquí podem diferenciar dos subgrups:
II a. Extrahospitalària: la PCR passa en l'àmbit extrahospitalari, atesa pels serveis d'emergències, i el pacient és traslladat a l'hospital amb compressions toràciques mecàniques i suport ventilatori.
II b. Intrahospitalària: la PCR és intrahospitalària, presenciada per personal sanitari, i les maniobres de reanimació s'inicien immediatament.
- Donació en asistòlia controlada.
Tipus III. A l'espera de l'aturada cardíaca en aquells pacients en els quals s'ha decidit instaurar limitació del tractament de suport vital (LTSV).
Tipus IV. Aturada cardíaca en mort encefàlica. La PCR passa mentre s'estableix el diagnòstic de mort encefàlica, o després de la diagnosi de ME, però abans de ser portat a la sala d'operacions per a l'extracció dels òrgans. Si no es restableix la funció cardiada, s'orienta cap a la donació en asistòlia.
Com hem vist, la nostra Legislació regula, en el Reial Decret 1723/2012 de 28 de desembre, les activitats per a l'obtenció i utilització d'òrgans humans, i la coordinació territorial en matèria de donació i trasplantament d'òrgans i teixits. Així mateix recull que la mort d'una persona pot diagnosticar-se amb la confirmació del cessament irreversible de les funcions cardíaques i respiratòries (mort per PCR), o de les funcions encefàliques (ME).
En el mateix Reial Decret, l'article 9 estableix que l'obtenció d'òrgans de morts només podrà fer-se previ diagnòstic i certificació de la mort (segons el que estableix el mateix RD), les exigències ètiques, els avenços científics en la matèria, i la pràctica mèdica acceptada.
El cessament cardíac i respiratori es reconeixerà mitjançant un examen clínic, a més d'un període d'observació determinat. L'hora de la mort serà l'hora en què es va diagnosticar el cessament de l'activitat cardiorespiratòria, i s'ha de fer per tres metges que no poden formar part de l'equip extractor o implantador dels òrgans.
El grup de pacients que s'inclouen en el grup de DA controlada són aquells que pateixen una lesió cerebral irreversible, però que no compleixen els criteris de mort encefàlica, i tots aquells pacients amb malalties pulmonars i musculoesquelètiques en fase terminal, lesions espinals greus, o aquells pacients en què la reanimació cardiopulmonar ha estat infructuosa i es determina un dany neurològic desastrós.
1. LIMITACIÓ DEL TRACTAMENT DE SUPORT VITAL (LTSV) ORIENTAT A LA DONACIÓ EN ASISTÒLIA CONTROLADA.
La donació en asistòlia és una tècnica relativament nova al nostre país, i malgrat els avenços en els coneixements sobre la matèria, i en l'adquisició d'experiència, l'índex d'òrgans obtinguts en donació en asistòlia segueix sent inferior al dels obtinguts en ME, ja que la donació en asistòlia està molt limitada pel temps d'isquèmia calenta, que pot danyar els òrgans i fer-los inviables, sobretot en aquells casos en què la PCR es produeix de forma imprevista i no es coneix el temps exacte d'isquèmia calent.
Tot i que la limitació del suport vital l'hem vist àmpliament en el Tema 3, és important fer alguns apunts, i mostrar la diferència que hi ha entre orientar la LTSV cap a la donació en mort encefàlica o cap a la donació en asistòlia.
La decisió de LTSV és independent de la possibilitat de la donació d'òrgans, i es realitza en les Unitats de Crítics en aquells hospitals que disposin d'un protocol d'LTSV, consensuat entre els professionals i els Comitès d'Ètica. L'actuació a la LTSV s'ha de basar en les Recomanacions de Tractament a la fi de la vida del pacient crític, desenvolupades pel Grup de Bioètica de la SEMICYUC.
Abans de sol·licitar la donació d'òrgans, després de la LTSV, el coordinador de trasplantaments i el metge responsable del pacient, realitzaran les proves necessàries per assegurar que no hi ha contraindicacions absolutes per a la donació.
Quan es planteja a la família la decisió de LTSV, és important fer-los entendre la situació real del pacient. És una situació difícil d'acceptar, i la família necessita temps per assimilar la informació i exposar els seus dubtes. Un cop han acceptat i han comprès la situació, i deixant passar el temps necessari perquè superin el primer moment de dolor, serà el coordinador de trasplantaments qui plantejarà la possibilitat de la donació en asistòlia d'òrgans i teixits.
Durant l'entrevista és important deixar clar a la família que la seva negativa per a la donació és igualment acceptable, i que no influirà en les cures i l'atenció que s'aplicaran tant al pacient com a la família, fins que esdevingui la mort.
Si la família accepta la donació, és fonamental explicar el procediment complet:
Lloc on es retirarà el suport vital. La retirada de les tècniques de suport vital (ventilació mecànica, extubació, drogues vasoactives, etc.) es realitza després que la família hagi signat el consentiment per a la donació. El lloc més adequat per a la desconnexió de la ventilació mecànica és la Unitat de Cures Intensives en la qual es trobi el pacient, tot i que dependrà de cada centre, de les possibilitats per atendre el pacient i als seus familiars, i del mètode de preservació i extracció empleats. Si es realitza al quiròfan, l'extubació dependrà exclusivament de l'equip assistencial de l'UCI on estava ingressat el pacient. El quiròfan ha de comptar amb tota la infraestructura preparada per a l'extracció d'òrgans i teixits, i així minimitzar els temps d'isquèmia.
Tant si es realitza en el quiròfan com en la Unitat de Crítics, s'ha d'oferir a la família la possibilitat d'acompanyar el pacient fins a l'últim moment. La seva decisió, en un sentit o en un altre, sempre ha de ser respectada.
Un cop extubat el pacient i fins a l'aparició de l'asistòlia, tant al quiròfan com a l’UCI, s'han de registrar els períodes d'hipotensió, hipòxia o anúria, monitorant:
- Pressió arterial invasiva: sistòlica, diastòlica i mitja.
- Freqüència i ritme cardíac.
- Pulsioximetria.
- Diüresi inicial (extubació) i final (PCR)
Intervencions pre-mortem. A la DAC cal fer algunes intervencions prèvies a la mort del pacient dirigides a optimitzar el procés de la donació, facilitant la perfusió i preservació dels òrgans i teixits. Generalment són: administració de 500-1000 UI / Kg d'heparina sòdica EV abans de la retirada del suport vital, o entre l'extubació terminal i l'asistòlia, i administració d'hemoderivats i altres fàrmacs. Cal que la família entengui que l'administració de fàrmacs està destinada a millorar la funció de l'òrgan després del trasplantament, i no a accelerar la mort del potencial donant.
A vegades és necessària la canulació (artèria i venes femorals), i la perfusió in situ de líquid de preservació, prèvies a l'extubació. En aquest cas, a més del consentiment per la donació és necessari sol·licitar el document de consentiment informat a la família per a la realització d'aquestes tècniques. S'ha d'informar també a la família de la possibilitat que després de la retirada del SV no es produeixi l'asistòlia, de manera que el pacient continuarà a l'UCI amb les cures a la fi de la vida adequades. Sempre es mantindrà la sedació i analgèsia a les dosis necessàries per garantir el confort, i evitar el patiment del pacient.
Un cop retirat el suport vital, ha de ser un intensivista, aliè al procés de la donació, que confirmi la mort després d'observar durant 5 minuts: absència de corba en el monitoratge invasiva arterial, apnea i absència de resposta a estímuls.
Si transcorregudes dues hores no es produeix l’asistòlia, el pacient torna o roman a l’UCI, on es continuen les cures a la fi de la vida.
2. DIAGNÒSTIC DE MORT PER CRITERIS CIRCULATORIS I RESPIRATORIS.
El diagnòstic de mort per criteris circulatoris i respiratoris, és a dir en asistòlia, es basa en el cessament irreversible de la circulació sanguínia i absència de respiració espontània.
El concepte d’irreversibilitat varia segons parlem de DAC o DA no controlada. En aquesta última, es considera irreversible quan després de realitzar les maniobres de RCP segons els protocols establerts per les societats científiques competents, ha estat impossible restaurar la respiració i la circulació, després d'un període d'observació no inferior a 5 minuts. I en referir-nos a la DAC, la determinació d’irreversible se certifica després del període d'observació (5 minuts) durant el qual hi ha un cessament de la funció cardiorespiratòria, sense maniobres de RCP.
Per certificar la mort per criteris cardiorespiratoris s'ha de verificar que:
- S'han realitzat maniobres de reanimació avançada (SVA), que han estat infructuoses i que s'han realitzat per un temps adequat, que dependrà de l'edat del pacient i de les circumstàncies que van provocar l'aturada cardiorespiratòria, seguint els protocols establerts per les societats científiques pertinents. En casos d'hipotèrmia inferior a 32º C, s'ha d'escalfar al pacient abans de certificar el cessament irreversible de les funcions cardíaca i respiratòria.
- O bé que no està indicada la ressuscitació cardiopulmonar segons criteris mèdics, i segons les recomanacions de les societats científiques competents.
L'absència de circulació sanguínia ha de quedar demostrada per a l'almenys un dels següents troballes, o per qualsevol altra prova instrumental que acrediti garantia diagnòstica per a això:
- Asistòlia en un electrocardiograma continu.
- Absència de flux sanguini en el monitoratge invasiva de la pressió arterial (catèter arterial).
- Absència de flux aòrtic en un ecocardiograma.
Les alteracions que es produeixen durant el temps d'isquèmia calenta indueixen al ràpid deteriorament cel·lular, estructural i funcional, així com a una situació d'inflamació cel·lular que deriva en la mort de la cèl·lula per trencament de la seva membrana i necrosi. Per regla general, les guies de pràctica clínica i el consens d'experts, s'accepta que el temps transcorregut des de la retirada del suport vital fins a l’asistòlia sigui de 30 a 90 minuts, en funció de l'òrgan a trasplantar.
Si no es produeix l'asistòlia en aquest període de temps, es posarà fi al procés de donació i es continuaran amb les cures de confort a la fi de la vida.
Per no crear falses esperances a familiars i cercles pròxims, i com a eina predictora per al coordinador de trasplantaments, existeixen scores de probabilitat d’asistòlia: "Criteris UNOS", "Escala de la Universitat de Wisconsin", "Escala de United Network for Organ Sharing" , "DCD-N score", (per citar alguns exemples), que fan predicció del temps en què apareixerà l’asistòlia, assignant una puntuació a diversos ítems, com la presència o no de drogues vasoactives, dades antropomètriques del pacient, l'edat, la presència o no d'intubació orotraqueal, presència o no de respiració espontània després de 10 minuts de la retirada de la ventilació mecànica, i / o saturació d'oxigen, etc., encara que cap d'elles té molt valor predictiu en la pràctica clínica, ja que depenen de les característiques de cada pacient, i sovint precisen la realització del test d'apnea, el que produeix encara més complicacions en el pacient.
3. DETECCIÓ I AVALUACIÓ DEL POTENCIAL DONANT EN ASISTÒLIA. CRITERIS D'EXCLUSIÓ.
Quan es parla del procés de DA, és important diferenciar la DA controlada (DAC) i la DA no controlada, ja que tots dos processos es diferencien en diversos aspectes, com són la forma en què es detecta al potencial donant, els temps d'isquèmia, la possibilitat d'administrar premortem substàncies preservadores que milloren la viabilitat de l'empelt, les tècniques de canulació i extracció, el procés per obtenir l'autorització per iniciar el procés de donació, i en el cas de la DA no controlada, és necessària la participació i coordinació dels professionals de l'atenció extrahospitalària.
Es considera possible donant en asistòlia controlada al pacient amb dany cerebral greu que no deriva en ME, o amb fallada circulatori i respiratori, i sense contraindicacions mèdiques per a la donació d'òrgans.
La detecció del donant en DAC comença quan l'equip assistencial decideix adequar o retirar el suport vital per considerar-lo fútil, com hem vist anteriorment, o en aquells casos en què el pacient amb dany cerebral catastròfic no acaba en mort encefàlica, i la família està disposada a fer la donació, però decideix no perllongar l'espera. En aquest moment l'objectiu terapèutic canvia de ser curatiu a l'aplicació de mesures de confort, tant del pacient com dels seus familiars.
En el cas de la DA no controlada, la detecció i avaluació de potencial donant es realitza in situ, i el seu manteniment i trasllat a l'hospital són, possiblement, les principals limitacions en aquest tipus de donació, ja que requereixen un servei d'emergències bé dotat i entrenat en maniobres de preservació d'òrgans, i comptar amb el suport de serveis aliens a l'hospital, com les Forces i Cossos de Seguretat, imprescindibles per al trasllat de la víctima a l'hospital i localitzar els seus familiars.
L'avaluació del possible donant en DAC no difereix de l'avaluació del donant en ME, i es realitza seguint les pautes que hem vist en el Tema 2, com són la revisió minuciosa de la seva història clínica, la realització de proves complementàries (anàlisi de sang, determinació del grup sanguini, cribratge serològic, estudi d'histocompatibilitat, estudi microbiològic i marcadors tumorals), proves d'imatge, etc.
Per tant, és un potencial donant en asistòlia controlada aquell pacient sense evidències de contraindicacions absolutes: tumors, infecció no controlada o disfunció multiorgànica, en els quals s'ha decidit aplicar mesures de LTSV, i en els quals s'espera que es produeixi una aturada cardiorespiratòria a les hores següents a la retirada de les mesures de suport.
Les patologies i situacions que poden derivar en una donació en asistòlia controlada són:
- Pacients amb patologia neurològica greu, amb pronòstic funcional catastròfic en què no és previsible l'evolució a mort encefàlica. S'inclouen pacients en coma o en estat vegetatiu per lesions cerebrals de causa isquèmica, hemorràgica o traumàtica, lesions medul·lars altes o malalties neuromusculars altes.
- Pacients amb patologies respiratòries o cardiològiques, amb evolució o pronòstic desfavorable, en què les mesures terapèutiques han estat ineficaços.
Les contraindicacions per a la donació, tant absolutes com relatives, són comuns a qualsevol tipus de donació, ja sigui en mort encefàlica o en donació en asistòlia. Encara que la majoria dels programes són més restrictius pel que fa a la donació en asistòlia, sobretot per la DA no controlada.
Així, l'ONT recomana per a la donació en asistòlia no controlada:
- Edat del donant entre 1 i 55 anys, (65 anys per a la DAC), revisable segons estudis de viabilitat per a la donació d'òrgans i teixits.
- És acceptable qualsevol tipus de parada cardiorespiratòria, sense excloure les produïdes per agressió.
- Es descarten aquells donants que presenten lesions toràciques o abdominals que comportin sagnat massiu (tot i que les lesions abdominals poden no contraindicar l'extracció pulmonar), i els que tinguin marques o indicis d'addicció a drogues parenterals.
- Absència d'infeccions sistèmiques o malalties neoplàsiques que suposen una contraindicació per a la donació.
- A més, es descartarà el possible donant si el temps transcorregut des de la parada cardiorespiratòria fins a l'inici del suport vital avançat (temps de parada) supera els 15 minuts, o si el temps transcorregut des de la parada cardiorespiratòria fins a l'arribada a l'hospital supera les dues hores.
És de summa importància en el cas de la DAC el temps en què es produirà la mort, un cop retirades les mesures de suport vital o temps d'isquèmia calenta, que és el factor més important per determinar la viabilitat de l'òrgan a trasplantar, encara aquest període depèn de les condicions hemodinàmiques o respiratòries del pacient, és a dir, del temps que roman en hipoperfusió.
Temps en el procés de donació en asistòlia controlada.
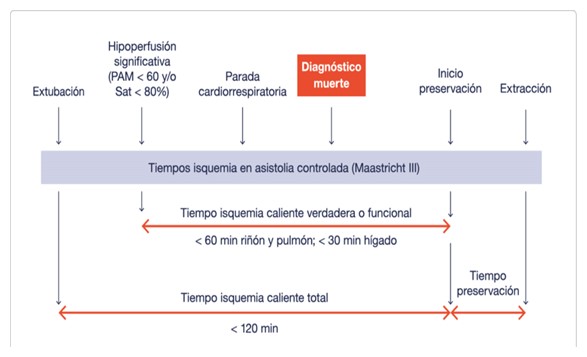
Font: Donació-asistòlia-Maastricht-III-Ocronos-Editorial cientificotècnica.
4. ACTIVACIÓ DEL CODI DE DONANT EN ASISTÒLIA NO CONTROLADA.
Un cop identificat un potencial donant en asistòlia no controlada, i amb una valoració positiva per a la donació, a Espanya s'utilitza una seqüència comuna per a l'activació i posada en marxa de tota la logística, tant intrahospitalària com extrahospitalària, necessària per a optimitzar i preservar els òrgans per a la donació.
Operatiu extrahospitalari:
- Alertar el centre hospitalari de referència i a coordinador de trasplantaments que s'està realitzant un intent de reanimació.
- Constatació dels criteris d'inclusió in situ del potencial donant en asistòlia i primera comprovació del temps en asistòlia i de RCP.
- Intubació orotraqueal in situ, amb tub endotraqueal de gran calibre, i ventilació mecànica amb FiO2 d'1 i freqüència ventilatòria de 15 rpm.
- El trasllat es realitza amb cardiocompresió automàtica contínua.
- Col·locació d'accés venós per fluidoteràpia, evitant la sobrehidratació i l'administració de fàrmacs.
- L'ambulància ha d'anar a velocitat constant, evitant acceleracions i desacceleracions.
- Informació per al personal de l'hospital:
- Filiació personal de la víctima: nom i cognoms, edat, sexe, antecedents personals (si es coneixen), dades de familiars i el contacte, i causa de la PCR.
- Hora exacta de la PCR, hora d'inici de les maniobres de RCP i hora de transferència a l'hospital.
- Possibles lesions hemorràgiques, accessos venosos canulats, estat del tub endotraqueal (presència de sang, moc, altres restes). Gasometria arterial. Test de drogues, i si es disposa d'elles, tira reactiva de VIH i ECOFAST (ecografia centrada en 4 punts per determinar hemoperitoneu, hemopericardi o hemo / pneumotòrax).
Recursos humans, materials i logística:
- Ambulàncies amb SVA o helicòpters medicalitzats.
- Coordinació amb altres serveis: bombers, cossos de seguretat, etc.
- Connexió telefònica directa amb el coordinador de trasplantaments, que ha d'acceptar el trasllat del potencial donant i activar el Codi de Donació en asistòlia.
- Avís als serveis d'urgències i medicina intensiva de l'hospital receptor de la imminent arribada del potencial donant.
- L'arribada a l'hospital ha de ser abans de 120 minuts des de la PCR.
- El servei d'emergències ha de comptar amb un protocol de DA, i l'hospital amb un programa de trasplantaments.
- A l'arribada a l'hospital de destí, es canulen catèters de doble pilota per iniciar, de forma ràpida, la perfusió amb màquines de circulació extracorpòria.
Una vegada que el coordinador de trasplantaments rep l'avís d'un possible DA no controlada s'ha de personar al centre, activar als equips d'extracció, i a tot el personal necessari i implicat en el procés (cirurgians, infermeres, patòlegs, microbiòlegs, etc.). El coordinador torna a avaluar al donant per seguir o no, amb el procés de donació, segons els criteris generals de selecció de donants, i els específics per al donant a asistòlia (temps d'isquèmia), abans de realitzar l'entrevista amb la família i demanar la sol·licitud de donació. L’intensivista o el metge d'urgències, aliens al procés de donació, han de certificar la mort per criteris cardiorespiratoris.
Els casos de mort violenta o sospitosa d'acte criminal, o en aquells casos en què el metge que certifica la mort té dubtes pel que fa a la causa de la mort, entrarien en un procés judicial. En aquest cas, s'envia una sol·licitud al jutjat de guàrdia per iniciar les maniobres de preservació del cadàver, encara que en el Reial Decret 2070/1999 assenyala que, si transcorreguts 15 minuts des de la sol·licitud al Jutjat no existeix resposta, podran iniciar les maniobres de preservació per considerar-autoritzades. Després del consentiment de la família per a la donació, s'estableix una segona comunicació amb el Jutjat per lliurar: consentiment de la família per a la donació, dades de la història clínica que haguessin pogut afectar les circumstàncies de la mort, còpia de l'informe d'urgències, sol·licitud dels òrgans i teixits a extreure,
S’obtenen llavors mostres de sang, grup sanguini, serologies i teixit limfàtic (gangli) tan aviat com es pugui, per fer el tipatge HLA, i s'administra al potencial donant un bolo d'heparina de 500 UI / kg de pes.
S'han d'extreure també una mostra de 20 cc de sang, 20 cc d'orina i 20 cc de sucs gàstrics, que quedaran a disposició de Jutjat d'Instrucció (seguint el protocol de cadena de custòdia establert), així com qualsevol altra mostra o dada que requereixin.
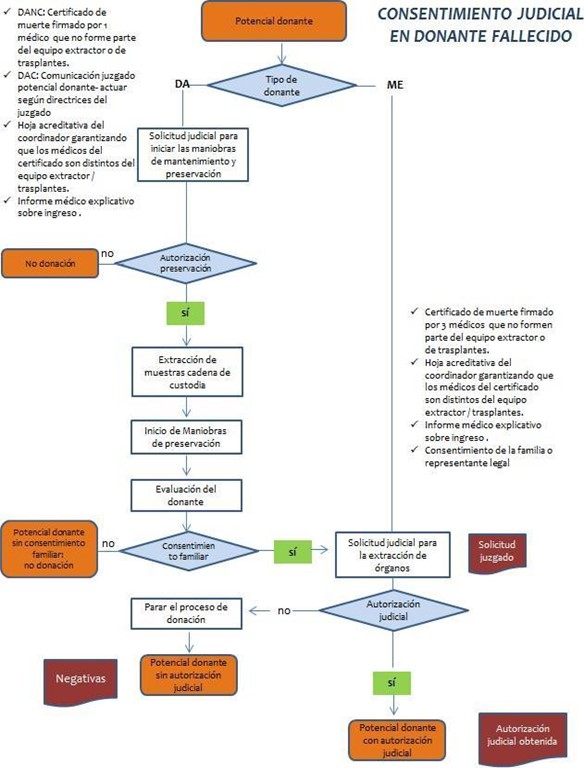
Font: Procés de consentiment a la donació de mort. ONT
La comunicació i localització de la família es fa a través de la policia, o per dades internes de l'hospital. El temps límit per localitzar-los i obtenir la seva autorització per a la donació és de 4 hores.
Posteriorment, es trasllada al pacient a la UCI o a la sala d'operacions per iniciar les maniobres de preservació, que han d'estar instaurades en menys de 120 minuts des que es va produir la PCR.
Un cop obtinguda l’autoriación s'extreuen els òrgans, ronyons, fetge i pulmons, així com els teixits, i es procedeix a la seva preservació i registre d'òrgans segons els protocols establerts (Tema 3). El procés acaba amb la comunicació al Jutjat del final de l'extracció.
Temps en el procés de donació en asistòlia no controlada.
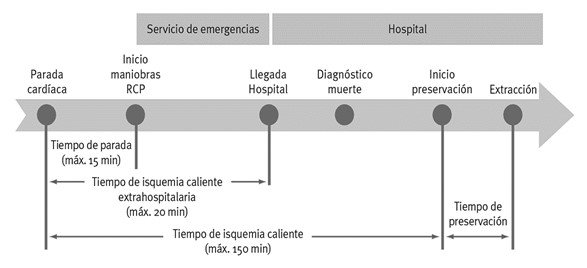
Font: Revista de formació per a Tècnics en Emergències sanitàries- ZONA TES.
4.1. Entrevista amb la família en el donant en asistòlia no controlada.
Hem vist en temes anteriors que l'entrevista amb la família en el procés de donació és un dels moments més delicats de tot el procés, per les condicions que envolten la mort d'un ésser estimat. En el cas de la donació en asistòlia no controlada, el coordinador de trasplantaments ha de cuidar encara més la forma en què es realitza l'entrevista amb la família, donades les especials característiques que es reuneixen en aquest tipus de donants. D'una banda, es tracta de morts sobtades o inesperades, amb tota la càrrega emocional que això suposa per a la família; i d'altra banda, el temps de què es disposa per comunicar la defunció i sol·licitar la donació és molt escàs.
Per a això, se segueix el següent protocol:
- Un cop localitzats als familiars per la policia, són acompanyats fins a l'hospital.
- A la seva arribada són rebuts per personal de l'hospital que els acompanya a una sala privada, si és possible amb telèfon per a comunicacions amb familiars, romanent amb ells per intentar atenuar la sensació de solitud i desemparament.
- És l’intensivista qui comunica a la família la mort del pacient. I una vegada que han acceptat la situació, i transcorregut un temps prudencial per gestionar el seu dolor, és quan el coordinador de trasplantaments els planteja la possibilitat de la donació.
- L'abordatge de l'entrevista és diferent per dos factors determinants: primer per l'inesperat de la mort, i segon per la impossibilitat que tota la família estigui present en la informació i la presa de decisions.
Si bé l'entrevista familiar està definida dins d'un esquema general de sol·licitud d'òrgans, en aquest cas s'introdueixen algunes variacions. Per exemple, cal donar més temps que en el cas de ME o DA controlada des de la comunicació de la mort fins a la sol·licitud de la donació. La comunicació de la mort provoca major explosió de sentiments, secundaris sempre a l'inesperat de la mort. En el cas de ME, hi ha hagut oportunitat d'anar preparant a la família per al fatal desenllaç mentre el pacient està ingressat a l'UCI.
I no obstant això, la mort per criteris cardiorespiratoris és un concepte més assequible per a la major part de les persones que el concepte de mort encefàlica, quan romanen al costat del potencial donant, i aquest segueix monitorat i connectat a ventilació mecànica. És important dir que la donació en asistòlia planteja menys negatives familiars que la donació en mort encefàlica.
5. PRESERVACIÓ I EXTRACCIÓ D'ÒRGANS.
Un cop retirat el suport vital, és imprescindible controlar en temps del període agònic, el temps d'isquèmia calenta total, i l'inici precoç de les maniobres de preservació d'òrgans.
- Temps d'isquèmia calenta total: temps que transcorre des de la retirada del suport vital fins a l'inici de les maniobres de preservació dels òrgans.
- Temps d'isquèmia calenta veritable o funcional: temps que transcorre des d'una hipoperfusió significativa i mantinguda (saturació d'oxigen en pulsioximetria <80% o TA sistòlica
- Don’t touch Període o període d'observació: temps que transcorre des de la parada cardiorespiratòria fins a la certificació de la mort. És el temps mínim per descartar fenòmens d'auto-ressuscitació, i encara que varia segons la legislació de cada país (entre 2 i 20 minuts), a Espanya s'ha establert un temps mínim de 5 minuts.
- Temps de preservació: temps que transcorre des de l'inici de les maniobres de preservació (perfusió in situ o circulació extracorpòria) fins a l'inici de l'extracció d'òrgans.
- Temps d'isquèmia freda: temps que transcorre des de l'inici de la perfusió de solució freda fins a la cirurgia del trasplantament.
Un cop obtinguda l'autorització, i certificada la mort del pacient, després de 5 minuts d'observació en què no hi ha d'haver corba en el monitoratge arterial, ni respiració espontània, ni resposta a estímuls dolorosos, i l’asistòlia està demostrada pel cessament de les contraccions cardíaques en una ecocardiografia, i l'absència d'activitat elèctrica queda reflectida en el monitor, comença el procediment de preservació dels òrgans, de forma precoç, per reduir al màxim el temps d'isquèmia calenta.
Les maniobres de preservació dels òrgans es realitzaran o bé a la pròpia Unitat de Crítics o al quiròfan, segons les característiques i necessitats de cada hospital, i les porten a terme l'equip quirúrgic de trasplantaments, amb el suport i supervisió del coordinador de trasplantaments.
En el cas de la donació en asistòlia, les tècniques de preservació es diferencien segons siguin els òrgans d'elecció, és a dir, si van destinades a la preservació d'òrgans abdominals, o la preservació pulmonar.
Preservació d'òrgans abdominals. Es divideixen en dos grans grups, atenent a l'objectiu terapèutic que es vol obtenir:
- Tècniques de refredament ràpid, encaminades a reduir el metabolisme cel·lular i preservar els òrgans de l'efecte perjudicial de la isquèmia calenta: perfusió in situ i recirculació hipotèrmica.
- Tècniques de restabliment de la perfusió dels òrgans amb sang normotèrmica oxigenada, destinades a recuperar el metabolisme cel·lular i la seva càrrega energètica, recuperant així la lesió isquèmica: recirculació nomotèrmica o NECMO.
Perfusió in situ (exclusivament per a extracció renal): Seran necessàries la canulació d'artèria i vena femorals, premortem o post mortem. Es realitza el drenatge del contingut hemàtic, i es perfunde el líquid de preservació. Pot ser necessari administrar vasodilatadors, anticoagulants o fibrinolítics. El donant es manté amb compressió toràcica constant i ventilació mecànica fins al seu trasllat a quiròfan, on es realitza l'extracció superràpida dels òrgans, i la perfusió freda amb les solucions de preservació.
Perfusió in situ
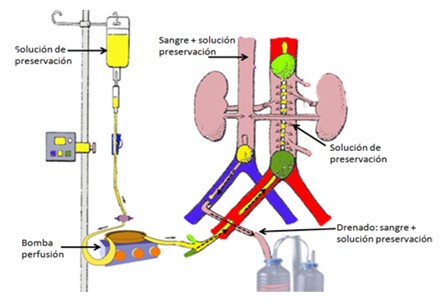
Font: Donació i trasplantaments d'òrgans i teixits.
Recirculació hipotèrmica (exclusivament per a extracció renal): s'utilitza la circulació extracorpòria ECMO, amb canulació premortem dels vasos femorals, i oclusió amb pilota de l'aorta toràcica per assegurar la recirculació selectiva dels òrgans abdominals. La sang s'oxigena i es refreda a 15 º C, cosa que permet un refredament més suau i progressiu dels òrgans, proporcionant una millor perfusió distal i una oxigenació contínua dels òrgans en la fase d'hipotèrmia.
Recirculació normotèrmica regional (PRN) o membrana d'oxigenació (NECMO). Aconsegueix millor funcionalitat de l'òrgan i menor nombre de complicacions posttrasplantament. És la tècnica d'elecció per a la preservació d'òrgans abdominals a DA, sobretot en DA no controlada. La tècnica és similar a la recirculació hipotèrmica, però la sang es manté a 37º C fins a la perfusió freda amb la solució de preservació en el quiròfan. S'ha de reheparinitzar cada 90 minuts amb 250 UI / kg d'heparina sòdica, i es perllonga fins a la visualització dels òrgans en el quiròfan i la posterior perfusió freda amb la solució de preservació. El temps mínim de NECMO és de 30-60 minuts i el màxim és de 4 hores fins a l'extracció dels òrgans.
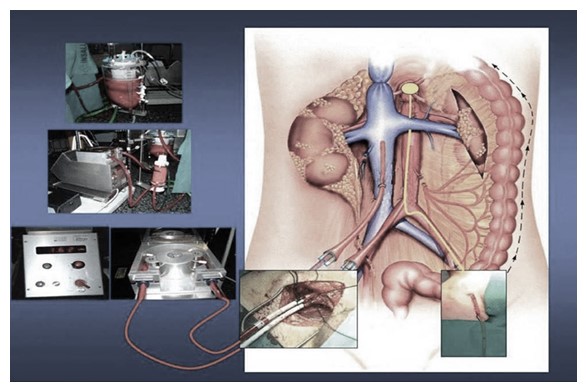
font: Donació després de la mort cardíaca. Parada cardíaca en el manteniment del donant en mort encefàlica. Rev. Medicina Intensiva
Preservació d'òrgans toràcics: pulmó. Es realitzen paral·lelament a les tècniques de preservació abdominal. El pulmóés l'únic òrgan que no requereix circulació per mantenir el seu metabolisme aerobi, a causa del mecanisme de difusió passiva a través de la membrana alveolar. S'ha demostrat que hi ha intercanvi gasós després de 2 hores d'isquèmia calenta en absència de circulació pulmonar.
Després de la retirada de la ventilació mecànica, i després de l'inici de la preservació dels òrgans abdominals, s'insereixen drenatges toràcics bilaterals pels quals s’infon la solució de preservació a 4ºC, fins a aconseguir el col·lapse dels pulmons.
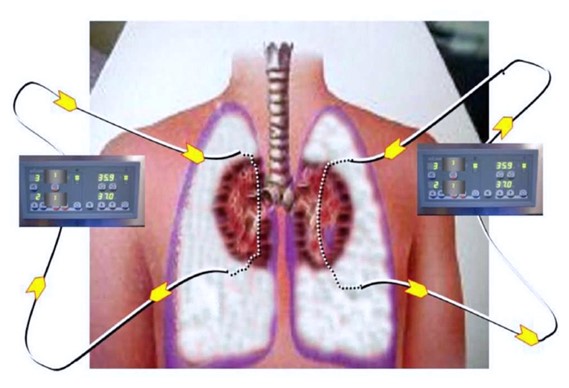
Font: Donació després de la mort cardíaca. Rev. Medicina Intensiva
Perfusió pulmonar ex vivo
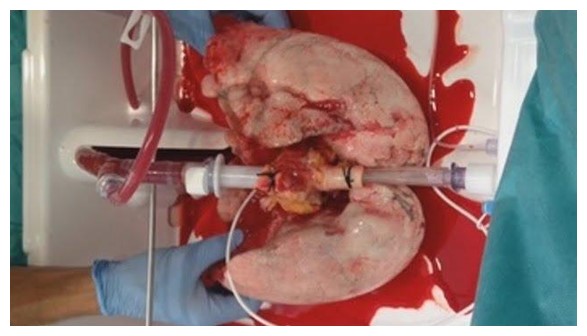
Font: "Ex viu". La màquina que dóna un respir al trasplantament pulmonar. Vist a YouTube
Les maniobres de preservació es suspendran en les següents situacions:
- Quan un cop obtinguts tots els permisos es realitzi l'extracció d'òrgans.
- Quan no s’obtinguin el necessari consentiment familiar i permís judicial.
- Passades 4 hores de bypass sense haver completat els requisits necessaris per iniciar l'extracció.
En el moment de l'extracció d'òrgans, el donant a cor aturat sol trobar hemodinàmicament inestable, per la qual cosa és necessari realitzar tècniques d'extracció ràpides, gairebé sense dissecció dels òrgans a extreure, sent prioritari salvar el màxim nombre d'òrgans. Si el donant es troba hemodinàmicament estable, seria possible la dissecció, canulació, perfusió i extracció reglada dels òrgans.
Els òrgans s'extrauran després del consentiment familiar i autorització judicial si escau. Durant el període de preservació es contacta amb les oficines d'intercanvi d'òrgans (ONT-OCATT) per informar de l'existència d'un potencial donant i així poder realitzar l'adjudicació dels òrgans segons els criteris de distribució establerts. El temps de resposta dels equips extractors s'ha de reduir a mínim.
Tècnica d'extracció superràpida. És la tècnica d'extracció més utilitzada en alguns centres, i ha de ser realitzada per cirurgians experimentats.En aquesta tècnica, l'única intervenció prèvia a la certificació de la mort que es fa sobre el donant és l'administració d'heparina, prèvia a l'extubació, per preservar la perfusió dels òrgans. Es realitza a continuació una canulació post-mortem que permet l'extracció d'òrgans abdominals i toràcics (pulmó) de manera simultània, amb excel·lents resultats en la funció i supervivència dels empelts.
- Extracció abdominal: Un cop declarat la mort, es realitza immediatament una laparotomia mitjana amb canulació aòrtica infrarenal, per introduir la solució freda de preservació i heparinitzar. Després es clampa l'aorta supracelíaca, i es realitza el drenatge per la vena cava inferior, per poder delimitar el territori de perfusió. Paral·lelament, es refreden de forma externa dels òrgans abdominals amb sèrum gelat o gel, i es realitza la perfusió a través de la porta, també amb sèrum gelat i heparina. Els òrgans es poden extreure en bloc o per separat. Amb aquesta tècnica, la perfusió freda pot iniciar-se en menys de 3 minuts des de la certificació de la mort.
- Extracció toràcica: després de la declaració de la defunció, es realitza una esternotomia mitjana i es reintuba al pacient iniciant mesures de reclutament manual. S'obre el pericardi fins a l'arc aòrtic i l'artèria pulmonar, es canula el tronc comú i es subjecta una cànula manualment. Es calampa l'aorta descendent i s'inicia la perfusió del líquid de preservació. Després es drena l'aurícula esquerra i es secciona la cava inferior a nivell de la desembocadura de l'aurícula dreta. La resta del procediment és similar al d'una extracció en mort encefàlica, amb extracció en bloc de tots dos pulmons i cor.
Un cop s'han extret els òrgans, el següent pasés realitzar la cirurgia de banc parcial o completa i la seva conservació, amb la tècnica clàssica de la preservació estàtica freda, com els òrgans procedents de l'extracció en mort encefàlica, per tal de deixar-los preparats per al trasplantament.
L'empaquetat dels òrgans es realitza amb la mateixa tècnica de la doble bossa i contenidor rígid, i cada òrgan anirà acompanyat de mostres de teixit: gangli, melsa i sang, segons el que indiqui l'equip de trasplantament, acompanyat de la documentació necessària: procedència i destinació de l'òrgan, dia i hora de sortida de centre d'obtenció, recomanacions de transport, informe sobre les característiques del donant i de l'òrgan, la seva extracció i les solucions de preservació utilitzades, i els estudis realitzats i els seus resultats.
Font: Urbantecno.com
Finalment, la reconstrucció del cadàver ha de ser molt acurada i es farà amb el màxim respecte, i és fonamental mantenir la dignitat del cadàver i l'aspecte extern abans de ser lliurat a la família.
