1. INTRODUCCIÓ
Una complicació que és relativament freqüent en els pacients crítics és la insuficiència renal aguda (IRA) o fracàs renal agut (FRA) que es caracteritza per un deteriorament de la funció renal. La mortalitat en aquests pacients és molt alta, no per causa de l'IRA si no per què són pacients en estat crític amb sèpsia, fallada multiorgànica, xoc ... El tractament de l'IRA és una de les coses que ha evolucionat més en els últims anys en les unitats de crítics. El tractament que s'utilitzaria tradicionalment en un pacient amb IRA és l'hemodiàlisi intermitent convencional, tècnica que produïa complicacions i desequilibris relacionats amb la pèrdua excessiva i ràpida d’electròlits i líquid, el que, al seu torn, provocava variacions del pH, hipotensions, alteracions en la concentració de CO2 i O2, etc. Una altra tècnica de depuració que es podia utilitzar era la diàlisi peritoneal, que estava contraindicada en els pacients que s'havien sotmès a intervencions quirúrgiques abdominals o amb problemes d'infeccions. Les dues tècniques eren mal tolerades pels pacients crítics, amb inestabilitat hemodinàmica, a més resultaven ineficaços, ja que era molt difícil extreure en 4 hores els líquids que s'havien acumulat en 24 h. Aquest desajust dels líquids limitava seriosament una aportació nutricional adequat, de manera que molts pacients estaven mal nodrits, el que afavoria les infeccions i altres complicacions. Les dues tècniques eren mal tolerades pels pacients crítics, amb inestabilitat hemodinàmica, a més resultaven ineficaços, ja que era molt difícil extreure en 4 hores els líquids que s'havien acumulat en 24 h. Aquest desajust dels líquids limitava seriosament una aportació nutricional adequat, de manera que molts pacients estaven mal nodrits, el que afavoria les infeccions i altres complicacions. Les dues tècniques eren mal tolerades pels pacients crítics, amb inestabilitat hemodinàmica, a més resultaven ineficaços, ja que era molt difícil extreure en 4 hores els líquids que s'havien acumulat en 24 h. Aquest desajust dels líquids limitava seriosament una aportació nutricional adequat, de manera que molts pacients estaven mal nodrits, el que afavoria les infeccions i altres complicacions.
Amb l'avenç en les tècniques de depuració hi ha una millora en el tractament de l'IRA del pacient crític, ja que les noves teràpies permeten eliminar aigua, electròlits i altres substàncies de rebuig de manera lenta i contínua. Així es poden administrar sèrums i aportar les dosis adequades de nutrició sense risc de sobrecàrrega de volum, sense canvis bruscos d’electròlits i amb una bona tolerància hemodinàmica.
Des de llavors les tècniques de reemplaçament renal han anat evolucionant gràcies als avenços tècnics, de manera que s'han pogut ampliar les seves indicacions, ha millorat la rendibilitat depurativa i tot això garantint una gran seguretat per al pacient. Per això, a causa d'aquesta ampliació ia les diferents variants tècniques, és més apropiat anomenar-tècniques contínues de depuració extracorpòria (TCDEC).
2. AVANTATGES D'UTILITZAR LES TCDEC
- El principal avantatge és que aporta més estabilitat hemodinàmica i així pot utilitzar-se en pacients crítics, ja que, al tractar-se d'un tractament lent i continuat, evita canvis bruscos en la volèmia del pacient i permet una gran flexibilitat en el maneig hidroelectrolític i el control metabòlic, amb un bon control dels líquids. Per això es considera la tècnica d'elecció per al tractament del FRA en pacients crítics.
- Facilita l'administració de nutrició a dosis plenes i medicació endovenosa. Gràcies al control de la volèmia.
- Fa possible l'extracció de líquids. El balanç hídric negatiu beneficia el tractament de l'edema agut pulmonar i disminueix la pressió hidrostàtica en la circulació pulmonar, millorant l'intercanvi gasós.
- Permet l'aclariment de substàncies circulants com els mediadors d'inflamació que intervenen en l'evolució de la síndrome de distrès respiratori de l'adult (SDRA) i la síndrome de disfunció multiorgànica (SDMO).
3. INCONVENIENTS DE LES TCDEC
- Hi ha un major temps de contacte de la sang amb material estrany, i per això existeix també major risc de reacció inflamatòria.
- A l'ésser una teràpia llarga hi ha més necessitat d'anticoagulació.
- Risc d ’infradosificació d'antibiòtics.
- Repòs relatiu del pacient.
4. INDICACIONS
La major incidència de FRA es troba en els pacients ingressats a les UCI. En el 80% dels casos aquesta insuficiència renal es tracta amb TCDEC. Les indicacions poden ser renals o no renals.
Indicacions renals
- Insuficiència renal aguda que es manifesta amb disminució de la funció excretora (diüresi menor de 0.5 ml / kg / h.) O pèrdua de capacitat dels
ronyons per excretar nitrogen i altres substàncies de rebuig (augment de la creatinina sèrica d’almenys 0.5 mg / dl o xifres majors del 50% sobre el valor basal).
- Insuficiència renal crònica aguditzada.
Cal tenir en compte que les TCDEC no curen l’IRA, sinó que substitueixen la funció renal mentre els ronyons es recuperen.
Indicacions no renals
- Hipervolèmia, amb IRA o sense. Ajuda a eliminar líquid de l'espai intersticial.
- Xoc sèptic. Com ja hem dit, el balanç negatiu, disminueix la pressió hidrostàtica, de manera que afavoreix l'intercanvi gasós, així milloren la funció pulmonar i hemodinàmica del pacient crític.
- Síndrome de disfunció multiorgànica. A causa de l'aclariment d'algunes substàncies com els mediadors d'inflamació (citoquines), afavoreix una millora hemodinàmica i respiratòria, i sembla que també una millora en la seva evolució.
- Insuficiència cardíaca congestiva i cirurgia cardíaca. Les TDEC aconsegueixen disminuir el volum intravascular i intersticial en insuficiència cardíaca congestiva resistent al tractament convencional. A més d'aconseguir una millora hemodinàmica durant el postoperatori.
- Fallada hepàtica. Pot ser d'utilitat per al control de líquids durant i en el postoperatori del trasplantament hepàtic mantenint l'estabilitat hemodinàmica del pacient.
- Intoxicacions. L'eliminació lenta, però contínua d'algunes drogues, evita el possible efecte rebot que de vegades passa amb l'hemodiàlisi convencional en el tractament d'intoxicacions.
- Acidosi làctica. Permet l'administració de grans quantitats de bicarbonat sense el risc d’hipernatrèmia ni d’hipervolemia.
- Alteracions electrolítiques. Les TDEC normalitzen les concentracions electrolítiques amb la utilització de líquids de diàlisi i de reposició adequats a les necessitats del pacient.
- Hiper / hipotèrmia. El circuit extracorpori permet regular la temperatura de la sang del pacient, per així corregir una hipotèrmia o una hipertèrmia que no respon als tractaments convencionals.
- Rabdomiòlisis i Síndrome d'aixafament. L'alliberament de mioglobina que es produeix en la rabdomiòlisi i la síndrome d'aixafament, pot produir una fallada renal que es pot corregir amb les TCDEC, ja que la mioglobina es pot
- Eliminar a través de les membranes dels circuits.
- Grans cremats. Es poden utilitzar les TCDEC per a un major control dels líquids i de l'estat catabòlic del pacient.
5. PRINCIPIS BÀSICS DE LES TCDEC
Les TCDEC consisteixen en el contacte indirecte entre la sang i el líquid de diàlisi a través d'una membrana semipermeable que permet el pas de substàncies d'un compartiment a l'altre (sanguini i dialitzador). En totes les TCDEC els soluts s'extreuen de la sang perquè passin al compartiment de l'ultrafiltrat del dialitzador.
Perquè la teràpia funcioni, infermeria té un paper fonamental, ja que és la responsable de l'inici, manteniment i fi de la teràpia. I a més és la responsable del control hemodinàmic i hídric del pacient.
La funció de la membrana depèn de la mida dels seus porus i, del pes molecular dels soluts. El pes molecular del solut depèn de 2 factors:
- Velocitat: la velocitat d'una molècula és inversament proporcional al seu pes molecular. És a dir, com més baix sigui el pes de la molècula, més es mou i per tant més vegades xoca contra la membrana. En canvi, les molècules més grans, es mouen menys i xoquen amb menys freqüència contra la membrana semipermeable i es fa més complicat que traspassin la membrana.
- Mida: Els soluts més grans, tenen més pes molecular. Quan la mida del solut s'aproxima o excedeix la mida del porus de la membrana, el seu pas a través seu serà més difícil.
Mitjançant aquestes tècniques es substitueixen les funcions de filtració glomerular i parcialment la funció tubular, tot i que no substitueixen les funcions endocrines.
Els principis físics en què es basen les TCDE són difusió, ultrafiltració, convecció i adsorció.
DIFUSIÓ
És el mecanisme a través del qual els soluts passen a través de la membrana semipermeable que separa dues solucions de diferent concentració i el desplaçament es produeix a favor de gradients de concentració.
El líquid de diàlisi no conté determinades substàncies denominades detritus, que sí es troben a la sang, de manera que aquestes substàncies travessaran la membrana fins a igualar-la concentració en els dos compartiments. Els soluts passen a través de la membrana de forma passiva i sense pas de solvent (aigua), es produeix per la diferència de concentració existent a banda i banda de la membrana. Com a resultat s'aconsegueix l'equilibri de gradient de concentració entre les dues solucions separades per la membrana semipermeable. Per aconseguir-ho, enfrontem la sang del pacient amb el líquid de diàlisi contra corrent al llarg del filtre.
Per tant, es produirà un moviment de molècules des de la zona de més alta concentració (sang) fins a la de menor concentració (líquid de diàlisi). L'eficàcia de la diàlisi dependrà de:
- Gradient de concentració a banda i banda de la membrana.
- Característiques de la membrana: mida del porus, superfície i gruix.
- La mida de la molècula: Com més gran sigui el pes de la molècula més difícil serà el seu pas a través dels porus de la membrana.
Aquest mecanisme aclareix millor les substàncies de pes molecular baix (
ULTRAFILTRACIÓ
Aquest procés consisteix en què una pressió osmòtica o hidroestàtica empeny l'aigua a través de la membrana i s'extreu només líquid sense pretendre la depuració de soluts.
La taxa d'ultrafiltració depèn de:
- El gradient de pressió que s'exerceix. El volum d'ultrafiltrat depèn en gran part de la pressió.
- De la superfície de la membrana.
- Del coeficient d’ultrafiltració (KUF), és a dir el grau de permeabilitat a l'aigua de la membrana. Aquesta permeabilitat depèn del gruix de la membrana i de la mida dels seus porus. La permeabilitat a l'aigua d'una membrana s'indica pel KUF, que es defineix com els mil·lilitres de líquid per hora (ml / h) que traspassen la membrana, per cada mil·límetre de mercuri (mmHg) de pressió transmembrana. Cada membrana té el seu propi KUF. Un KUF de 5 indica que perquè es filtrin 1.000 ml / h es requereix un gradient de pressió de 200 mmHg. De manera que com més alt sigui el KUF menys pressió necessita per filtrar.
CONVECCIÓ
El transport convectiu consisteix en el pas de soluts a través de la membrana semipermeable arrossegats per l'aigua. De manera que s'eliminen simultàniament aigua i soluts, en resposta a la diferència de pressió que hi ha a banda i banda de la membrana. Passa líquid del costat de major pressió cap al costat de menor pressió, arrossegant soluts.
Aquest pas d'aigua a través de la membrana permet també el pas d'una gran quantitat de soluts que estan dissolts en aquesta aigua. Així s'eliminen molts soluts corporals, però no es produeix una disminució en la seva concentració. Per això, la composició electrolítica del plasma és molt semblant a la concentració electrolítica de l'ultrafiltrat. L'ultrafiltrat és el líquid extret de la sang a través de la membrana de diàlisi a través d'aquestes tècniques. De manera, que la depuració no depèn del gradient de concentració (com en el cas de la difusió), sinó sobretot del volum d'ultrafiltrat.
La quantitat d'aigua que passa d'un costat a un altre de la membrana depèn de la pressió que s'exerceix, per tant, és un transport actiu. El pas de solut, en canvi, és passiu, ja que va dissolt en l'aigua que traspassa la membrana. La quantitat de solut que es filtra depèn de diversos factors:
- El pes molecular. Els soluts amb un gran pes molecular no poden travessar la membrana. Els de menys pes molecular, passen dissolts en l'aigua, en la mateixa concentració.
- La quantitat d'ultrafiltrat que s'extreu.
- Les característiques de la membrana.
- Del KUF. La permeabilitat d'una membrana a l'aigua es mesura pel seu coeficient d'ultrafiltració, que rep el nom de KUF. Com ja hem dit anteriorment el KUF es defineix com el nombre de mil·lilitres de líquid per hora que traspassa la membrana per cada mil·límetre de mercuri (mmHg) de gradient de pressió transmembrana.
La convecció aclareix substàncies de pes molecular petit (Urea, creatinina, àcid úric, glucosa, sodi, potassi, clor, fòsfor, etc.), però també és efectiva amb les de pes molecular mitjà.
ADSORCIÓ
Les membranes amb què estan fabricades els hemofiltres, tenen certa capacitat d'adsorció, és a dir, que algunes molècules queden "atrapades" a la superfície de la membrana del filtre. Generalment absorbeixen toxines endògenes o exògenes i també alguns mediadors inflamatoris. Es podrien utilitzar en el tractament de les intoxicacions i pacients sèptics, encara que la seva eficàcia està discutida.
6. TIPUS DE TCDEC
ULTRAFILTRACIÓ CONTINUA LENTA (SCUF)
L'objectiu d'aquest tractament és extreure l'excés de líquid en pacients crítics, de manera lenta i continuada mitjançant la ultrafiltració. No es pretén l'eliminació de solut. Per tant, no es reposa amb cap líquid de substitució. És a dir, no s'utilitza ni líquid de diàlisi ni de reposició. El flux de sang que se sol utilitzar oscil·la entre 50-100 ml / min. Per a l’ultrafiltrat se sol programar entre 2-5 ml / min. d'extracció.
Permet el control de fluids en situacions de sobrecàrrega hídrica (ICC resistent al tractament convencional).
HEMOFILTRACIÓ VENO-VENOSA CONTINUA (CVVHF)
És la tècnica contínua de reemplaçament renal més utilitzada en les unitats de crítics a Espanya. Consisteix en la filtració de solut arrossegat per l'aigua a través de la membrana per transport convectiu i l'extracció de líquid a través de la ultrafiltració. En aquest cas, sí que serà necessari reposar líquids, per aconseguir un balanç hídric adequat per al pacient, ja que s'extreu més volum de què realment volem eliminar. Aquesta reposició pot ser pre-filtre o post-filtre. La reposició pre-filtre és menys eficient, ja que la sang es dilueix amb el líquid de reposició abans d'entrar en el filtre.
Amb aquesta teràpia aconseguim depurar tant petites molècules (urea, creatinina, fosfats i ions) com a molècules de major pes molecular. Pot ser molt útil en IRA, hiperkaliemia, sèpsia, intoxicacions i grans cremats.
HEMODIÀLISI VENO-VENOSA CONTÍNUA (CVVHD)
S'utilitza la difusió com a mecanisme de depuració de solut, i la ultrafiltració per eliminar volum. Amb aquest tractament es necessita líquid de diàlisi que entra al filtre de forma contínua, a contra corrent del flux sanguini. D'aquesta manera, vam aconseguir enfrontar el líquid de diàlisi amb la sang a través d'una membrana i el pas de solut es produeix per diferència de gradients de concentració. Amb aquesta teràpia es depuren sobretot molècules petites (urea i creatinina), no és tan eficaç per a molècules mitjanes.
La pèrdua d'aigua a través de la membrana és petita pel que no serà necessària la reposició de volum. És a dir, en aquest cas, només s'utilitza líquid de diàlisi.
HEMODIAFILTRACIÓ VENO-VENOSA CONTÍNUA (CVVHDF)
Amb aquest tractament intervenen els dos mecanismes que coneixem, el transport per difusió i per convecció, a més de la ultrafiltració per eliminar volum.
Gràcies a la difusió podem eliminar molècules de baix pes molecular (menors a 500 Daltons), ia aquest procés se li afegeix el mecanisme convectiu que elimina eficaçment molècules més grans (per sobre de 1000 daltons).
L'alta taxa d'ultrafiltració (extracció de líquid) fa necessària la reposició de líquids. Per tant, amb aquesta teràpia utilitzarem líquid de diàlisi i de reposició.
7. CATÈTERS I ACCESSOS VASCULARS
7.1 Introducció
El catèter es pot definir com un "tub de material biocompatible que ens permet arribar a una vena de gran calibre amb un bon flux de sang i utilitzar-lo per a finalitats terapèutiques".
Als anys 50 Seldinger va desenvolupar la tècnica de cateterització percutània dels vasos sanguinis. Consisteix en la introducció d'una guia metàl·lica flexible, per la llum de l'agulla amb la qual s'ha realitzat la punció del vas sanguini. Es retira l'agulla, deixant només la guia. Després s'introdueix el catèter que volem utilitzar a través de la guia, que finalment es retira. Així el catèter queda a l'interior del vas sanguini.
Als anys seixanta, Quinton i Scribner van idear un sistema que consistia en 2 cànules, una inserida en una artèria i l'altra en una vena propera.
El 1961, Shaldon va desenvolupar la canulació d'artèria i vena femorals per diàlisi i, posteriorment, la utilització de catèters de doble llum.
Amb el temps va anar augmentant la demanda de catèters per a la realització de TCDEC, i amb els avenços tecnològics es van anar utilitzant diferents materials per a la fabricació d'aquests catèters i nous dissenys per minimitzar els riscos i millorar l'eficàcia dels tractaments.
Es pot afirmar que el catèter és un component clau per a la correcta realització de les TCDEC. Sense un bon catèter i sense un bon accés vascular que garanteixi un bon flux de sang, no serà possible dur a terme cap d'aquests tractaments, i insistir-hi, només significarà una pèrdua de temps i material i suposarà una sobrecàrrega de treball per al personal d'infermeria.
7.2 Tipus de catèter
PEL SEU ÚS
- Permanents o tunelitzats: Aquest tipus de catèter s'escull per utilitzar-lo durant un llarg període de temps, poden durar fins a 5 anys. Donen menys problemes d'infecció. S'usen en pacients amb insuficiència renal crònica amb els quals no es pot usar, per algun motiu, la fístula arteriovenosa (FAV).
- Temporals o no tunelitzats: Són els més utilitzats en les Unitats de Cures Intensives. La seva durada mitjana és de 3 setmanes.
SEGONS EL NOMBRE DE LLUMS
- D'1 llum: Antigament s'usaven 2 catèters d'1 llum, per canalitzar una vena i una artèria per realitzar les tècniques arteriovenoses, però avui en dia estan en desús.
- De 2 llums: Són els més utilitzats en les unitats de crítics per a realitzar les TCDEC. Són catèters d'entre 11 i 14Fr.
- De 3 llums: Són catèters especials, la tercera llum es pot utilitzar per administrar medicació, seroteràpia, nutrició ...
PER LA SEVA CONFIGURACIÓ INTERNA
- coaxial: La part distal del catèter és per al retorn de la sang o llum venosa. La part proximal, que conté diversos orificis és per a l'entrada de sang o línia arterial.
- Doble D: La part distal del catèter, amb 1 orifici més 3 laterals, és per al retorn o línia venosa. La part proximal, amb 5 orificis, per a l'entrada de la sang o línia arterial.
- Canó d'escopeta: La part distal és per al retorn de la sang, és a dir, és la llum venosa. La part proximal consta d'un sol orifici i és per a l'entrada de la sang (llum arterial). Aquest tipus de catèters són els més utilitzats actualment en les unitats de crítics, ja que disminueixen la formació de fibrina en els orificis d'entrada i sortida i permeten un bon flux de sang, amb baixa resistència a la tornada, disminuint així les pressions d'entrada i sortida.
PER LA SEVA FORMA
- Corbs: Estan indicats per a les jugulars o subclàvies, a més resulten més còmodes per a la mobilitat del pacient si aquest no està sedat.
- Rectes: Es poden utilitzar per a qualsevol via, jugular, subclàvia o femoral.
PER LA SEVA COMPOSICIÓ (MATERIAL)
- PVC (Clorur de polivinil): Cada vegada s'usen menys perquè són poc biocompatibles i massa rígids, el que afavoreix els traumatismes vasculars i les infeccions.
- Poliuretà: Són els més utilitzats en les unitats de crítics, ja que són biocompatibles i faciliten la seva col·locació i permanència, ja que són durs per
la seva inserció, però s'estoven una vegada inserits, adaptant-se a l'anatomia de l'pacient. Tenen menys tendència a complicacions trombòtiques.
- Silicona: Són els més biocompatibles i per això s'utilitzen en catèters permanents. Són molt flexibles i duradors, amb menor incidència d'infeccions.
PER LA SEVA LONGITUD
- De 6 a 12cm: Pediàtrics
- De 15 a 20 cm: Aquests catèters estan indicats per a vies superiors (subclàvia i jugular). Cal tenir en compte que les vies superiors esquerres han de ser més llargues, per acabar a l'atri dret. Jugular / subclàvia dreta: 20 cm. Jugular / subclàvia esquerra: 3-5 cm més.
- De 20 a 24 cm: Aquests catèters estan indicats per a vies inferiors (femoral).
PEL SEU CALIBRE
- De 6 a 8 Fr: Una llum. Indicats en pacients pediàtrics.
- D’11 a 12 Fr: Dos llums. Indicats per a tècniques convencionals de diàlisi.
- De 13 a 14 Fr: Dos llums. Són els més utilitzats actualment en tècniques de depuració contínua, acabats en canó d'escopeta. Permet mantenir uns fluxos correctes amb baixes pressions.
A més, cal tenir en compte la llei de Poiseuille que relaciona calibre i longitud dels catèters. La llei de fluids de Poiseuille indica que el flux de sang que s'aconsegueix amb un catèter és directament proporcional al radi del catèter i inversament proporcional a la seva longitud. "Un augment del 20% en el diàmetre del catèter proporciona el doble de flux de sang, amb unes pressions menors (fujos> 350 ml / min)". Per això, els catèters de 13 Fr són els que més s'utilitzen actualment a les TDEC.

Imatge 8 Set d’accés vascular per purificació de sang extracorpòria

Imatge 9: Catèter de 2 llums

Imatge 10 Canó d'escopeta
7.3 Elecció de la via d'inserció
Un cop s'ha triat el catèter que es va a utilitzar segons les característiques del pacient, si és adult o pediàtric, la seva mida corporal i si es va a punxar el costat dret o esquerre, cal decidir la via que es va a canalitzar, per això s'han de tenir en compte diversos factors, la situació de cada pacient, l'experiència del facultatiu que realitza la punció i l'anatomia del pacient. Per a realitzar les TCDEC és necessari un flux sanguini elevat, entre 200-400ml / min. Per això, és important aconseguir un accés vascular que asseguri obtenir aquest flux sanguini. La punta dels catèters de vies superiors (jugular i subclàvia) s'ha de col·locar en la unió de la vena cava superior i l'atri dret, per evitar així recirculacions. La punta dels catèters femorals s'ha de situar en la vena cava inferior.
Segons les recomanacions de l’ADQI
- En adults no és recomanable utilitzar la via subclàvia, ni en nens la femoral, pel risc de trombosi i estenosi.
- Es recomana utilitzar l’ecògraf per canalitzar la via.
- Utilitzar els catèters de poliuretà per a les TCDEC.
El catèter es pot girar 180º i també permet utilitzar la llum arterial del catèter com venosa i la llum venosa del catèter com arterial. Això no obstant, està desaconsellat intercanviar el paper de les llums, a causa de la recirculació que es produeix quan per l'extrem arterial del catèter entra la sang ja dialitzada, ja que pot tornar a entrar al circuit per l'altra llum, sent de nou depurada i ocasionant una disminució en l'aclariment de les substàncies.
El catèter es mantindrà heparinitzat quan no s'utilitzi, amb heparina a l’1% en la quantitat que ens indiqui el propi catèter. La llum venosa és més llarga que l’arterial, en cadascuna de les llums s'indica la quantitat d'heparina que hem d'administrar. Si hem de reiniciar la teràpia, primer retirarem l'heparina del catèter. La manipulació en tot moment del catèter i les seves connexions es faran amb la màxima asèpsia possible.
Cal avaluar diàriament la necessitat del catèter venós i retirar quan no sigui necessari.
7.4 Procediment d'inserció
- Comprovar que sigui el pacient correcte.
- Informar el pacient de la tècnica que es va a realitzar.
- Rentat de mans.
- Totes les persones presents han de portar gorra i mascareta.
- Preparar el material necessari.
- Per a l’asèpsia cutània prèvia a la col·locació del catèter, es farà servir preferentment una solució de clorhexidina, si no fos possible, s'utilitzarà alcohol de 70 graus o povidona iodada. L’antisèptic ha d'assecar completament abans de la inserció, en el cas de la povidona iodada, s'ha de deixar actuar almenys 2 minuts. Si es torna a palpar la zona de punció després de l'asèpsia cutània, haurà de fer també de forma asèptica.
- La col·locació de catèters venosos centrals i arterials ha de ser una tècnica estèril, amb totes les mesures de barrera, és a dir, gorra, ulleres protectores, mascareta, bata, guants estèrils i talles estèrils. Els professionals que estiguin ajudant a la persona que realitza la tècnica, o estiguin dins del box han de portar també, com a mínim, barret i màscara. Les talles estèrils han de cobrir al pacient del cap als peus.
- La punció es realitza seguint el mètode Seldinger.
7.5 Complicacions relacionades amb la inserció
- Punció arterial.
- Arrítmies a l'introduir la guia.
- Embòlia aèria.
- Pneumotòrax.
- Hemotòrax.
- Fístula arteriovenosa.
- Hemorràgia retroperitoneal.
7.6 Complicacions relacionades amb la permanència i cura
- Trombosi del catèter.
- Mal funcionament: recolzament, torsió, contacte amb la paret del vas sanguini, trombosi parcial.
- Recirculació.
- Estenosi venosa.
- Endocarditis.
- Infecció del punt d'inserció.
- Sèpsia o xoc sèptic.
7.7 Inici del tractament
Cal seguir els protocols de cada centre, però hi ha unes recomanacions generals que cal tenir en compte.
- El primer que hem de fer abans d'iniciar el tractament, és retirar el segell d'heparina de les 2 llums. Retirem 3 ml de cadascuna de les llums i es rebutja.
- Netejarem les 2 llums amb sèrum fisiològic estèril.
- Comprovar la permeabilitat de les 2 llums. Amb una xeringa de 20ml, aspirarem sang de la llum arterial o d'entrada, si s'omple en 6s sense dificultat, és perquè la llum és permeable i ens pot proporcionar un bon flux de sang. S'introdueixen els 20ml de sang per la llum de retorn, hauria de poder introduir-se en 6s sense resistències. A aquest procediment se li denomina test de flux. L'intercanvi de les llums, si ens trobem amb dificultats
per omplir la xeringa de sang, només és una solució temporal fins que es canviï el catèter, ja que provocarà una recirculació i per tant, el tractament perd eficàcia.
- Quan estiguin les línies connectades, es protegiran les connexions amb unes gases amb antisèptic.
7.8 Durant el tractament
- Evitar les manipulacions en la mesura del possible.
- Control del punt de punció.
- Control de les connexions.
7.9 Fi del tractament
- Preparar dues xeringues amb 20 ml de solució salina 0'9% per rentar els llums.
- Segellar cada lumen del catèter amb la quantitat d'heparina que indica el catèter. Per a això, s'ha d'administrar l'heparina i immediatament pinçar la llum, per assegurar-nos un segellat correcte. Els llums han de tancar són taps i romandran pinçades fins que tornin a utilitzar-se.
- Protegir els llums amb gases o caixes de NTP.
8. MEMBRANES
Les TCDEC han tingut una evolució força ràpida en els últims anys, i ha estat molt lligada a les millores tècniques que s'han produït en aquest camp ia l'evolució dels materials utilitzats. En els anys 90 van aparèixer les membranes sintètiques d'alt flux i alta permeabilitat, que tenen una gran biocompatibilitat i han suposat un pas molt important en el desenvolupament d'aquestes tècniques. Actualment són les més usades en les TCDEC.
S'ha passat també de sistema arteriovenós, al sistema venovenós, primerament, amb 2 bombes fins a l'actualitat, amb màquines de 5 bombes.
El filtre ha d'estar compost per membranes biocompatibles, d'alta permeabilitat i, preferiblement, amb capacitat d'adsorció de substàncies que es vulguin depurar.
La biocompatibilitat es pot definir (Maduell Canals, 2005) com «la capacitat d'actuar dels materials, instruments, procediments o sistemes d'una aplicació específica sense produir una resposta clínica adversa per part de l'organisme». A les TCDEC es refereix a la resposta de l'organisme en posar en contacte la sang amb els materials necessaris per realitzar aquest tractament. El component més determinant és la membrana dialítica, tot i que també cal tenir en compte la resta de components com les línies, els líquids de diàlisi, les agulles ... El contacte de la sang del pacient amb la membrana origina una resposta per part del pacient com l'activació de la coagulació, l'agregació leucocitària, estimulació de la producció de mediadors inflamatoris o activació plaquetària.
La permeabilitat. Les membranes emprades en les TCDE són membranes semipermeables, permetent el pas d'aigua i de soluts d'una forma molt similar a com ho fa un ronyó sa, és a dir, sense pas de cèl·lules ni molècules superiors als 30.000 Da. La permeabilitat d'una membrana es mesura pel KUF o coeficient d' ultrafiltrat (Es defineix com el nombre de ml / h que es filtra a través de la membrana per cada mm de Hg de pressió transmembrana). Les membranes sintètiques que s'usen actualment tenen una alta permeabilitat, és a dir tenen un KUF alt. Poden aconseguir els 15-20-25ml / h / mmHg d' ultrafiltrat amb una pressió transmembrana (PTM) estàndard. Es consideren membranes de baixa permeabilitat quan el KUF està per sota de 12 i d'alta permeabilitat quan està per sobre de 20ml / h / mmHg.
Pel que fa a la filtració dels soluts, com ja s'ha explicat anteriorment, en la difusió, les molècules petites es filtren depenent del gradient de concentració. Les molècules més grans només es filtraran si són més petites que els porus de la membrana, principalment per transport convectiu.
La capacitat depurativa de la convecció depèn de la quantitat de volum ultrafiltrat i del coeficient de cribratge (sieving coefficient o relació entre la concentració del solut en el líquid d’ultrafiltrat i la concentració del solut en el plasma).
El sieving coefficient serveix, a més, per classificar la membrana pel que fa a la permeabilitat als soluts. En les membranes que s'usen normalment, es considera un punt de tall aproximat de 55.000 Daltons (Da) per així evitar la eliminació de proteïnes plasmàtiques amb aquests tractaments, especialment l'albúmina.
Un altre factor que intervé en la permeabilitat de la membrana és la seva superfície.
Adsorció. S'entén per adsorció, la capacitat de la membrana de retenir algunes substàncies. Amb l'evolució de les TCDEC es va comprovar que algunes substàncies havien disminuït en sang i no es trobaven en l’ ultrafiltrat, i que per tant s'havien quedat a filtre. La capacitat absortiva no és igual en totes les membranes i va disminuint amb l'ús per la saturació de la membrana. Actualment, s'han comercialitzat alguns filtres que contenen resines amb capacitat absortiva específica. Això ha permès el tractament de patologies com la sèpsia o la insuficiència hepàtica greu.
9. CIRCUITS
Els circuits per realitzar aquestes teràpies estan compostos per diferents línies, sensors de pressió, bombes ... que fan possible la sortida de sang del pacient perquè passi pel circuit i sigui filtrada, i de nou es retorni al pacient amb les màximes garanties de seguretat. Encara que existeixen diferents monitors en el mercat i cada model té les seves particularitats, hi ha uns elements essencials que són comuns en tots els monitors. A més, cal tenir en compte, que totes les línies disposen de clamps, per facilitar la manipulació i augmentar la seguretat, i que cada línia es representa amb un color que ajuda a identificar-la de manera visual.
LÍNIES hemàtiques (d’entrada i retorn)
- Línia d'entrada, aferent o arterial que es representa amb el color vermell.
- Línia de retorn, eferent o venosa que es representa amb el color blau.
LÍNIA DE L’EFLUENT que es representa amb el color groc.
LÍNIA DEL LÍQUID DE REPOSICIÓ que es representa amb el color violeta.
LÍNIA DEL LÍQUID DE DIÀLISI que es representa amb el color verd.
10. PRESA DE PRESSIÓ
- Pressió d'entrada.
- Pressió prefiltre.
- Pressió de retorn.
- Pressió de l'efluent.
- Pressió transmembrana.
Pressió d'entrada: És una pressió negativa que depèn:
- De l'estat de la llum arterial del catèter.
- De l'estat de la línia d'entrada.
- De la velocitat de la bomba de sang.
Pressió prefiltre: És una pressió positiva, de fet, és la més positiva de tot el circuit, que depèn:
- Del flux de sang.
- De l'estat del filtre.
Pressió de retorn: És una pressió positiva, que depèn:
- Del flux de sang.
- De l'estat de la línia de retorn.
- De l'estat de la llum venosa del catèter.
Al atrapabombolles de la línia de retorn es troba un filtre que impedeix que els coàguls que es generen al llarg del circuit puguin arribar a pacient, la seva funció és retenir-los, el que provoca un augment de la pressió de retorn o venosa, que ens avisa que pot obstruir totalment (coagulació del filtre).
Pressió de l'efluent: Pot ser positiva o negativa. Depèn:
- Del KUF (Coeficient d' ultrafiltrat)
- De la velocitat de la bomba de sang.
- Nombre de capil·lars que funcionen en el filtre.
Si la pressió de l'efluent és positiva és perquè el filtre funciona correctament.
Si la pressió de l'efluent és negativa és per què s'han perdut capil·lars eficaços dins el filtre.
Pressió transmembrana (PTM): És una pressió positiva. depèn:
- Del flux de l'efluent.
La velocitat o flux de la bomba d'efluent afecta directament la pressió transmembrana. Un augment d'aquesta pressió expressa que s'ha coagulat part de la superfície, i que alguns capil·lars no són funcionants.
El control de les diferents pressions no evitarà la coagulació dels filtres, però si ens permetran avançar-nos als possibles problemes i evitar les pèrdues hemàtiques del pacient per coagulació dels circuits i filtres.
Pressions normals de sistema:
Pressió d'entrada: -50 a -150.
- Si és alta: per desconnexió de la línia, excés de volum circulant.
- Si és baixa: capficament de la línia arterial, obstrucció del catèter, velocitat de bomba excessiva.
Pressió de retorn: +50 a +150
- Depèn del flux, de l'estat de la línia de retorn (possibles capficaments) i de l'estat del catèter (obstrucció o possible adhesió del catèter a la paret del vas)
Pressió del filtre: +100 a +250
- És la pressió més positiva de tot el circuit. Si és alta pot ser per coàguls en el filtre o catèter.
Pressió de l'efluent: Pot ser positiva o negativa de +50 a -150
- A l'iniciar el tractament serà positiva i pot anar disminuint progressivament fins a fer-negativa (vol dir que el filtre s'està coagulant)
11. BOMBES
El monitor disposa de cinc bombes per:
- Sang.
- Efluent (ultrafiltrat).
- Líquid de Reposició.
- Líquid de Diàlisi.
- Anticoagulant.
12. ALARMES
Sistemes de seguretat:
Detector d'aire a la línia venosa posterior a l'atrapa-bombolles amb el seu clamp de seguretat.
Detector de fuites hemàtiques en la línia d'efluent. Si s'activa és pel trencament de capil·lars del filtre i el pas d'hematies a l'efluent.
Sistemes d'alarma:
La màquina haurà d'activar un sistema d'alarma sonora i visual, així com les possibles causes que provoquen el problema i les solucions.
Dins d'alarmes del circuit hemàtic distingim:
- Alarma de pressió arterial.
- Alarma de pressió prefiltre.
- Alarma de pressió venosa.
- Alarma de pressió transmembrana (PTM).
- Alarma de detecció d'aire, en la línia venosa.
- Alarma de detecció de fuites hemàtiques, per trencament de capil·lars.
Altres alarmes són:
- Alarmes de detecció de portes de bombes obertes.
- Alarmes dels circuits de substitució i de diàlisi.
- Alarmes relacionades amb el circuit d'anticoagulació.
- Alarmes relacionades amb el subministrament de xarxa o de l'estat de la bateria.
13. LÍQUIDS
Les TCDEC es fan servir cada vegada més en les unitats de crítics. Com ja hem comentat anteriorment, el seu principal avantatge respecte a les tècniques intermitents és que no es produeixen canvis hidroelectrolítics bruscos i d'aquesta manera, evitem la inestabilitat hemodinàmica, el pacient tolera millor el tractament i és més efectiu. Perquè la depuració sigui correcta, és necessària una reposició d'una elevada quantitat horària d’ ultrafiltrat, que s'obté del pacient, amb un líquid amb una composició fisiològica i una concentració de substàncies determinada. Aquest líquid ha de servir per reposar tots els components normals del plasma menys les substàncies que desitgem eliminar.
L'objectiu dels líquids és aproximar el plasma del pacient al qual hauria de ser, la composició normal.
En l'actualitat, s'aconsegueix un millor control del pacient amb l'ús de grans volums de fluids per a reposició o diàlisi. Això atorga una gran importància a la composició dels líquids.
Les solucions de reposició / diàlisi han d'estar compostes d'aigua i ions. La concentració d' ions ha de reflectir la composició normal del plasma.
Sodi (Na +) 135-145 mEq / l
Potassi (K +) 3,5-5 mEq / l
Clor (Cl-) 100-110 mEq / l
Calci (Ca2 +) 3-4 mEq / l
Magnesi (Mg +) 2 mEq / l
Bicarbonat (HCO3) 25-30 mEq / l
Glucosa (1 g / l)
Aquestes solucions són estèrils i han de trobar-se lliures de pirògens i endotoxines, en la seva composició. Les bosses són portadores d'un port d'injecció per afegir altres medicacions si fos necessari. Després de la reconstitució, s'ha demostrat que la solució reconstituïda té una estabilitat de 24 h.
Els pacients portadors de TCDEC, hauran de tenir un control analític periòdic per vigilar la composició del plasma.
Cal recordar que el potassi ...
Entra i surt molt fàcilment a sang per difusió.
Per convecció, amb xoc contra la membrana del capil·lar, entra i surt també al plasma del pacient.
La composició ideal màxima del plasma és de 5 mEq / l, per tant, els líquids no poden contenir més de 25 mEq per cada 5 litres de solució.
Es recomana que les bosses dels líquids continguin tota la mateixa concentració de potassi per evitar errors i desajustos.
Cal recordar que el bicarbonat ...
Ve separat de la bossa gran i cal barrejar-abans de la seva administració.
Precipita amb facilitat amb el calci.
Si no es barreja, provocarà un mal funcionament de la bàscula.
Líquid de diàlisi
Quan ens interessa depurar gran quantitat de substàncies de baix pes molecular, s'utilitza el mecanisme de la difusió, la teràpia escollida serà l'hemodiàlisi. Per a això es necessita un líquid de diàlisi que, per diferència de gradients de concentració, feu possible el pas de solut a través de la membrana. En aquest cas no hi ha una pèrdua significativa d'aigua plasmàtica del pacient. Es necessita un líquid de diàlisi que reposi les substàncies que volem mantenir, però que no contingui les substàncies que es pretenen eliminar.
En el cas de l’ hemodiafltració, en què s'uneixen els dos mecanismes d'eliminació (difusió i convecció), la composició adequada per a cada un dels líquids és la mateixa que quan es fan servir per separat.
Líquid de reposició
Un dels mecanismes de depuració d'aquestes teràpies és la convecció. Mitjançant la convecció i per una diferència de pressió que s'exerceix en un dels compartiments del filtre, es produeix l'eliminació de gran quantitat d'aigua
plasmàtica del pacient, que arrossega soluts. A més aigua plasmàtica filtrada, més soluts eliminats.
Normalment, s'intenta seguir la relació de depuració de 35 ml / kg / h, el que suposa reposar una gran quantitat de líquid (en un pacient de 70Kg, una reposició horària de 2.450ml / h). Aquest líquid ha d'aproximar-se al que seria la composició ideal del plasma.
Hem d'evitar qualsevol manipulació, ja que s'administren directament al torrent sanguini, per mantenir així la seva esterilitat.
Reposició postfiltre
És l'opció ideal per administrar el líquid de reposició. L'inconvenient és que pot produir-se una hemoconcentració en el filtre per la quantitat d'aigua plasmàtica que s'elimina de la sang, el que pot afavorir la coagulació del filtre.
Reposició prefiltre
En aquest cas la reposició es realitza abans d'arribar al filtre, disminueix l’hemoconcentració, però pot produir una disminució en l'eficàcia de la depuració de soluts.
Reposició prefiltre i postfiltre
Amb les màquines actuals la reposició es pot realitzar de manera simultània pre i post filtre, quan es treballa amb hemofiltració, aprofitant així els avantatges que ofereixen les dues opcions.
14. ESCALFADORS
Els pacients amb teràpies de depuració extracorpòria pateixen una baixada de temperatura, a causa del circuit extracorpori i a la gran quantitat de líquids que s'administren. Per això, els monitors, en l'actualitat, disposen d'un escalfador per escalfar els líquids o escalfar la sang. En el cas que la màquina no disposi d'això, s'han d'utilitzar mantes tèrmiques per evitar la hipotèrmia.
15. ANTICOAGULACIÓ AMB HEPARINA
La coagulació dels circuits és la complicació més comuna quan es realitzen TCDEC. És un problema seriós, ja que produeix una pèrdua de recursos, una càrrega de treball addicional per al personal, una pèrdua de sang del pacient i una disminució en l'eficàcia del tractament, a causa de les interrupcions. S'estima que un set pot utilitzar-se fins 72 h, però moltes vegades no arriben aquest temps perquè es coagulen. Per això, es fa necessari l'ús d' anticoagulació en el circuit durant la teràpia. L'elecció de l'anticoagulant i la seva dosi dependran de les característiques del pacient. En la majoria dels casos, es tria l'heparina Na com anticoagulant. Normalment s'acarnissa el circuit amb una solució amb heparina Na (5000 U / l). I a més es deixa una perfusió contínua a dosis baixes (de 5 a 10 U / kg / h). Normalment els monitors de TCDE porten incorporada una bomba específica per a això. L’ anticoagulació de la sang amb citrat sòdic o àcid cítric dextrosa (ACD) és una de les últimes novetats, molt útil quan, per les característiques del pacient està contraindicat utilitzar heparina Na. Consisteix en la utilització de citrat que s'administra quan la sang surt del pacient, per quelar el calci en el circuit i així mantenir la sang descoagulada en el mateix. Aquest efecte es reverteix administrant calci abans de retornar la sang al pacient.
16. ANTICOAGULACIÓ AMB citrats
16.1 Introducció
Com ja hem comentat, en les tècniques de reemplaçament renal cal anticoagular el circuit, per allargar la vida del filtre i evitar la seva coagulació el que significaria pèrdues de sang per al pacient, més treball i augment dels costos.
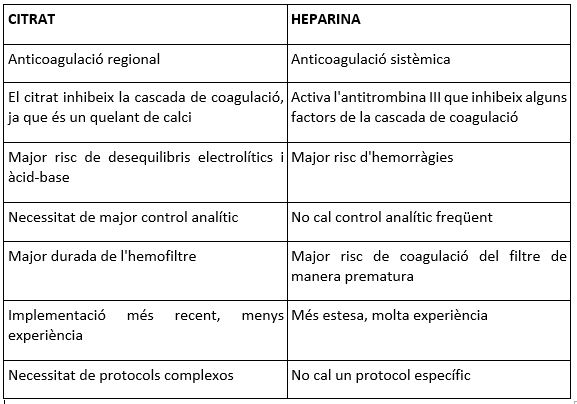
L'heparina Na és l'anticoagulant més utilitzat fins ara, tot i que s'associa amb un risc de sagnat i està contraindicat en alguns pacients. Davant aquest problema s'han desenvolupat altres alternatives, la més utilitzada és l’anticoagulació regional amb citrats (ARC).
16.2 Com funciona el citrat?
El calci iònic juga un paper fonamental en la cascada de coagulació de la sang. El citrat és un quelant de calci, de manera que, si el citrat és capaç de "segrestar" el calci iònic, lliure que hi ha a la sang, es desactivarà la cascada de coagulació.
L' anticoagulació amb citrats consisteix en l'administració contínua de citrat en el circuit extracorpori, just a la sortida de sang del pacient, abans de la bomba de sang. Quan el citrat es barreja amb la sang, es produeix la unió amb el calci iònic, formant un complex Ci-Ca, d'aquesta manera disminueix el nivell de calci iònic en la sang del circuit. A la fi del circuit, per no provocar una hipocalcèmia al pacient es reposa en administració contínua el calci per restaurar l'estat de coagulació fisiològic. Cal fer controls analítics regulars durant la teràpia, per comprovar els nivells tant del pacient com de la màquina, i ajustar-los si cal.
16.3 Indicacions i contraindicacions
indicacions:
- Alt risc de sagnat.
- Trombocitopènia induïda per heparina.
Contraindicacions:
- Fallada hepàtica severa.
- Intolerància al citrat.
16.4 Solucions
- Citrats
La concentració de citrat que se sol utilitzar és de 3mmol / litre.
- Calci.
Hi ha diferents solucions comercialitzades. Les més utilitzades són:
Gluconat càlcic al 10% en vials de 10 ml contingut efectiu de calci: 2.23 mmol / 10mL (223 mmol / L).
Clorur c Clorur càlcic al 10% en vials de10 ml contingut efectiu de calci: 9,13mEq / 10mL = 4.57 / 10mL (457 mmol / L)
- Líquid de diàlisi
Solució sense calci:
- Líquid de reposició
Solució sense calci. A la reposició postfiltre podria utilitzar un líquid amb calci, però augmentaria el risc de coagulació de la línia de retorn.
16.5 Muntatge del filtre
El muntatge dependrà de la màquina de la qual disposem. Necessita d'un fungible específic per a anticoagulació amb Ci-Ca i d'unes solucions específiques com ja hem comentat. Cal seguir els passos que ens indica el monitor.
L’encebat del circuit es realitzarà sense heparina.
16.6 Control analític
Abans d'iniciar la teràpia amb citrats, cal extreure una analítica del pacient per saber quin és el seu calci iònic basal i corregir si fos necessari fins a nivells normals. La mostra s'ha d'extreure del catèter arterial en el cas que disposi. Si no és portador de catèter arterial l'extracció es realitzarà d'un accés venós pel qual no s'estigui administrant clorur càlcic.
Després de la connexió al pacient s'han de fer controls analítics seriats, es recomanen cada 6h. Del pacient i del filtre. La mostra del filtre s’haurà d’extreure de la línia blava. Així es podran ajustar les dosis de citrat i de calci periòdicament.
El citrat és un anticoagulant que quan entra a l'organisme es metabolitza en bicarbonat.
Un excés de citrat pot derivar en una alcalosi (excés de bicarbonat en sang). Per revertir aquesta situació es podria disminuir el flux de sang (disminueix la dosi de citrat) o podríem augmentar la dosi del líquid de diàlisi (augmenta l'eliminació del bicarbonat) en un 20%.
Un dèficit de citrat pot produir acidosi (dèficit de bicarbonat en sang). Per revertir aquesta situació podríem augmentar el flux de sang (Augmenta la dosi de citrats) o disminuir la dosi de diàlisi (disminueix l'eliminació de bicarbonat) en un 20%.
17. CURES D'INFERMERIA
Per al bon funcionament i efectivitat de les TCDEC, hi ha uns passos fonamentals que són, el correcte encebat del circuit, la correcta col·locació del set, els controls continus i les cures d'infermeria. Cal dur a terme un monitoratge horària tant del pacient com de la teràpia, mitjançant una gràfica dissenyada especialment per a quan el pacient és portador de TCDEC
Infermeria és el personal sanitari que passa 24h a la banda del malalt. La seva capacitat per prevenir o resoldre qualsevol incident és molt important per poder oferir unes cures de qualitat. Infermeria ha de saber interpretar les dades que dóna el monitor.
Les cures d'infermeria comprenen:
- Control de les constants vitals.
- Manteniment de l'asèpsia.
- Control de la perfusió tissular.
- Manteniment i maneig del catèter per a la TDEC.
- Control electrolític.
- Mobilitzacions.
- Evitar la hipotèrmia.
- Manteniment del circuit.
CONTROL DE CONSTANTS VITALS
S'han d'utilitzar gràfiques de monitoratge hemodinàmic i gràfiques de diàlisi, per detectar els possibles problemes, registrar-los i fer canvis en el tractament si fos necessari.
MANTENIMENT DE L’ASÈPSIA
Cal extremar les mesures d'asèpsia en les següents situacions:
- La canalització de l'accés vascular. La inserció del catèter ha de ser una tècnica estèril.
- La cura del punt d'inserció del catèter. Seguirem el protocol de la unitat sobre la cura de vies centrals.
- Les manipulacions de les connexions de les línies amb el catèter.
- Les manipulacions del catèter. Farem servir guants estèrils, gases i talles estèrils i mascareta.
- Evitarem les manipulacions innecessàries del catèter i les connexions, per evitar en la mesura possible, l'entrada de microorganismes.
- Rentat de mans abans i després de cada procediment.
CONTROL DE LA PERFUSIÓ TISSULAR
Cal vigilar la zona propera al punt d'inserció, per comprovar que hi hagi una bona perfusió. Cal controlar:
- Temperatura.
- Color.
- Polsos distals.
- Inflamació, mal ..
MANTENIMENT I MANEIG DEL CATÈTER
Un bon manteniment i maneig del catèter és molt important, ja que significarà allargar la vida i eficàcia del filtre.
- Elecció d'un catèter adequat a la vena d'elecció (calibre i longitud). Es recomana utilitzar un catèter de doble llum de 13 Fr de longitud adequada a la vena d'elecció i acabat en canó d'escopeta.
- Realitzar el test de flux abans de suturar el catèter.
- En el cas de no començar la teràpia immediatament, netejar i heparinitzar dues llums (amb els ml. D'heparina que la pròpia llum indica) per garantir la seva permeabilitat i correcte funcionament.
- Cada vegada que interrompem la teràpia, rentar dues llums amb 20ml de SF i després heparinitzar.
- En reiniciar la teràpia, aspirar l'heparina que s'ha introduït anteriorment i realitzar el test de flux.
- Si el test de flux no és correcte, podem mobilitzar el pacient, l'extremitat, es pot mobilitzar el catèter, rotar ... Si res d'això funciona, caldrà canviar el catèter.
CONTROL ELECTROLÍTIC
L'objectiu és aproximar el plasma del pacient a la composició normal. Les TCDEC serveixen per eliminar soluts no desitjats de la sang del pacient. Però a més de rebutjar els soluts no desitjats, també s'eliminen altres substàncies de baix pes molecular que travessen la membrana del filtre. Per corregir aquest desequilibri electrolític de la sang, els líquids que es fan servir en aquestes teràpies porten incorporats certs ions (Ca2 +, Mg2 +, Na +, Cl, lactat i HCO3) per reposar aquestes pèrdues. Per això és tan important el control analític, per detectar aquests desequilibris i corregir-los. Es recomana realitzar una analítica a l'inici de la teràpia i mentre duri el tractament caldrà tenir un control analític en funció de les necessitats del pacient. Per realitzar l'extracció de sang per a aquests controls es pot obtenir directament del pacient o mitjançant la línia d'entrada (línia vermella) punxant en la presa de mostres més pròxima al pacient, desinfectant primer. Es pot conèixer l'estat de l'anticoagulació del filtre amb una mostra de sang de la via de retorn (línia blava) per a realitzar controls.
MOBILITZACIONS DEL PACIENT
Estar connectat a una màquina d' hemofiltració no hauria de significar limitar les mobilitzacions del pacient, si aquestes són beneficioses per a ell. Per realitzar aquestes mobilitzacions:
- El catèter ha d'estar ben fixat.
- Evitar estrebades i capficament de les llums o línies.
- Comprovar que les connexions estan ben tancades.
EVITAR LA HIPOTÈRMIA
Els pacients amb hemofiltració solen patir una baixada de temperatura, a causa del circuit extracorpori i a l'intercanvi de líquids. Per evitar-ho, moltes màquines disposen d'un escalfador en la línia de retorn i si no és així utilitzarem mantes tèrmiques.
18. PREPARACIÓ DEL MONITOR
Hi ha diferents monitors en el mercat, cada un amb les seves característiques concretes. S’ha de sempre les recomanacions de fabricant i dels manuals. Per al seu correcte muntatge cal seguir cadascun dels passos que ens mostra la pantalla.

Imatge 11: hemofiltre Fresenius

Imatge 12: hemofiltre Prismaflex

Hemofiltre prismaflex vs fresenius
19. MANTENIMENT DEL CIRCUIT
Per al bon funcionament del circuit s'han de tenir alguns aspectes en l'inici, transcurs i final del tractament.
19.1. Inici del tractament
- Escollir el tractament indicat per al nostre pacient.
- Muntatge del filtre seguint els passos que indica la màquina.
- Revisar que estiguin ben tancades les connexions de rosca.
- Omplir la càmera venosa fins al nivell marcat i el controlarem durant el tractament.
- Carregar la xeringa d'heparina.
- Comprovació del catèter (test de flux).
- Connectar al pacient.
- En el moment de la connexió, iniciarem el tractament amb una velocitat de sang baixa, entre 80-100ml/h i la resta dels fluxos es deixaran a 0. Després s'anirà pujant la velocitat de la bomba de sang fins al nivell pautat pel metge (controlar que les pressions d'entrada i retorn estan dins dels límits normals). Després s'introduiran la resta dels fluxos.
- Registrar totes les dades a la gràfica de TCDEC.
- És important conservar la línia en I que inclou el set.
19.2. Durant el tractament
- Registrar totes les dades del tractament en la gràfica, sobretot les pressions. Especial atenció a les pressions del filtre> 300, a les de la PTM> 250 ja l'alarma "el filtre s'està coagulant".
- Canvi de bosses quan sigui necessari. Ens podem avançar si fos necessari.
- Vigilar el nivell d'ompliment de la càmera venosa.
- Realitzar balanços mínims cada 24/h i registrar-lo.
- Registrar sempre que s'aturi el tractament per algun motiu com TAC, cirurgia, canvi de catèter, coagulació del filtre ...
- Recirculació: En el cas d'haver de parar el tractament per un breu període de temps podem utilitzar la recirculació. Ha 2 alternatives, recircular amb salí o amb sang.
Recirculació
Recirculació amb salí:
- S'ha de parar el tractament i escollir l'opció de recirculació amb salí.
- Desconnectar del pacient la línia d'entrada i connectar-la a un sèrum fisiològic a través de la I, que prèviament s'haurà purgat (línia en I que inclou el set i hem de guardar).
- Retornar la sang al pacient.
- Un cop s'hagi tornat la sang al pacient desconnectar la línia de retorn i connectar-la a la llum lliure de la línia en I.
- Amb les 2 línies (entrada i retorn) connectades a la solució salina a través de la I es pot iniciar la recirculació.
- Rentar i segellar el catèter segons el protocol de la unitat.
- Pot passar que el circuit no quedi completament net i la màquina ens avisi de detecció de sang en el set. Confirmarem "sense sang".
- La recirculació amb solució salina té un temps màxim, que pot variar segons la màquina, normalment no supera els 120min.
- Quan puguem reconnectar al pacient, es pararà la recirculació i seguirem els passos que ens indiqui el monitor. En aquesta opció la màquina requereix un nou encebat.
Recirculació amb sang:
- S'ha de parar el tractament i escollir l'opció de recirculació sanguínia.
- Es desconnecten les 2 línies del pacient i es connecten entre elles i es pot iniciar la recirculació.
- Rentar i segellar el catèter segons el protocol de la unitat.
- Pot aparèixer l'advertència "detecció sang en set". Premerem el botó de continuar per seguir amb la recirculació.
- La recirculació amb sang sol tenir un temps màxim de 60 min.
- Quan puguem reiniciar el tractament, es pararà la recirculació i podem tornar a reconnectar les línies. El tractament es reprèn sense necessitat d'encebament.
CAL RECORDAR:
- Mentre sona una alarma no s'està realitzant el tractament.
- Quan la bomba de sang està parada hi ha risc de coagulació immediata del filtre.
- Si volem moure la màquina, podem desendollar sense necessitat d'apagar i tornar-la a endollar.
19.3 Fi del tractament
- Aturar el tractament.
- Pinçar la línia d'entrada o arterial i la llum arterial del catèter i desconnectar-.
- Rentar la llum arterial del catèter amb 20 ml. de sèrum fisiològic.
- Connectar la línia arterial del circuit a una solució salina amb una clau de tres passos i obrir el sèrum i la línia d'entrada.
- Escollirem l'opció de retorn manual per tornar la major part de sang al pacient (el circuit quedarà de color rosat).
- A l'acabar, pinçar la línia d'entrada i de retorn. Pinçar també les 2 llums del catèter i desconnectar-les.
- Netejar amb sèrum fisiològic i segellar amb heparina segons protocol de la unitat. Col·locar els 2 taps.
- Protegir el catèter segons el protocol de la unitat.
- Rebutjar el circuit (és recomanable pinçar primer tots els clamps) i les bosses.
- Registrar el balanç real abans d'aturar la màquina.
20. OPTIMITZAR EL FILTRE
20. 1 Quin és el temps òptim de durada del filtre?
Els fabricants no es posen d'acord sobre quina hauria de ser la durada del filtre, s'estableix entre 48 i 72 h. A la pràctica hospitalària es solen fer servir fins a les 72 h, encara que en molt poques ocasions aguanten més de 48h. El problema es troba en els casos en què no duren ni 24 hores, llavors es considera que hi ha una obstruccció precoç del filtre. Per això, és important tenir en compte tots els factors que intervenen en l'augment de la durada i l'eficàcia del filtre.
20.2 Accés vascular i catèter
Cal seleccionar l'accés venós i el catèter més adequat en cada cas.
- La tècnica d'inserció del catèter hauria de realitzar un professional amb experiència.
- Evitar la canalització de la via subclàvia en pacients amb risc d'estenosi o trombosi.
- Seleccionar el catèter adequat pel que fa a longitud, calibre i terminació, es considera que el calibre és més determinant que la longitud.
20.3 Filtres
Per anar bé adequar la membrana al pacient i al tractament que administrarem. Tot i que no sempre es disposa de diferents tipus de membrana al centre.
Les teràpies d'alt flux requereixen filtres de major grandària.
L'elecció de la membrana dependrà del criteri mèdic.
20.4 Encebat correcte
- Respectar el volum d'encebament.
- Heparinitzar el sèrum amb què es realitza el grumeig. (5000ui / l). Excepte si farem servir un altre tipus d'anticoagulació.
- Si hi ha dubtes sobre si l'encebat s'ha realitzat correctament (observem aire al circuit), repetirem el grumeig.
20.5 Gestió d'alarmes
És important que els professionals d'infermeria tinguin un bon domini d'aquestes tècniques i sàpiguen actuar amb eficàcia i rapidesa quan es disparen les alarmes, sobretot quan s'atura la bomba de sang, perquè quan això passa augmenta molt el risc de coagulació del filtre. Si minimitzem les parades augmentés la durada del filtre.
20.6 Control de pressions
El personal d'infermeria ha de conèixer quins són els rangs de pressions adequats, per conèixer així l'estat del filtre i del circuit i poder anticipar-se als problemes. Aquestes pressions s'han de registrar a cada hora, el més important és observar com és la tendència. Així podrem anticipar-nos a una coagulació del filtre i retornar a temps la sang al pacient i evitar-li pèrdues de sang.
20.7 Anticoagulant
- Elecció de l'anticoagulant més apropiat per a cada pacient
- Heparina sòdica.
- Heparina de baix pes molecular.
- Citrats.
20.8 Ajust del tractament adequat
La fracció de filtració (FF) és la quantitat de sèrum que s'extreu de la sang que passa pel filtre, en un període de temps determinat. Cal recordar que de la quantitat de sang que passa pel filtre no tot és líquid, hi ha elements formes.
Per ajustar bé el tractament, és important saber amb què FF treballarem, ja que d'ella depèn la durada i eficàcia de l'filtre. L'ideal és treballar amb una FF que no superi el 25%. Si la FF s'acostés al 100% deixaria soles en el filtre a les cèl·lules formes de la sang, el que suposaria una coagulació immediata.
FF = flux UF / flux plasmàtic
Flux UF = extracció líquid pacient + reposició prefiltre + reposició postfiltre.
Flux plasmàtic = flux de sang × (1 - hematòcrit / 100) + reposició prefiltre.
20. 9 Reposició
La reposició prefiltre pot servir per prevenir l'obstrucció del filtre, ja que disminueix l’hemoconcentració.
La reposició postfiltre evita coàguls a la cambra d'aire.
BIBLIOGRAFIA
- Cutillas B. Generalidades (Sistema urinario)- Definición del sistema urinario. [Internet]. Enfermera virtual. Barcelona: Col·legi Oficial d'Infermeres i Infermers de Barcelona; 2009. [consultado 10 enero 2021]. Disponible en: www.infermeravirtual.com
- Cutillas B. Vías urinarias (Sistema urinario)- Las vías urinarias extrarrenales. [Internet]. Enfermera virtual. Barcelona: Col·legi Oficial d'Infermeres i Infermers de Barcelona; 2009. [consultado 10 enero 2021]. Disponible en: www.infermeravirtual.com
- Cutillas B. Riñones (Sistema urinario). [Internet]. Enfermera virtual. Barcelona: Col·legi Oficial d'Infermeres i Infermers de Barcelona; 2009. [consultado 10 enero 2021]. Disponible en: www.infermeravirtual.com
- Cutillas B. Riñones (Sistema urinario)-Las nefronas. [Internet]. Enfermera virtual. Barcelona: Col·legi Oficial d'Infermeres i Infermers de Barcelona; 2009. [consultado 10 enero 2021]. Disponible en: www.infermeravirtual.com
- Cutillas B. Riñones (Sistema urinario)-Inervación e irrigación. [Internet]. Enfermera virtual. Barcelona: Col·legi Oficial d'Infermeres i Infermers de Barcelona; 2009. [consultado 11 enero 2021]. Disponible en: www.infermeravirtual.com
- Rouviere H.; Delmás A. Anatomía Humana: descriptiva, topográfica y funcional. 9a ed. Masson, 1988. Williams P. L.; Warwick R. Anatomía de Gray. Salvat, 1992.
- Manzanedo J.D. Alteraciones renales. Màster en cures d´Infermeria al malalt crític. Universitat de Barcelona. 20019-2020.
- Andrés E. Prevención primaria y secundaria del fracaso renal agudo. En: Net À, Roglán A, editores. Disfunción renal aguda en el paciente crítico. Barcelona: Ars Medica; 2009. p. 31---53.
- Torras A. Fisiopatología y diagnóstico del fracaso renal agudo. En: Net À, Roglán A, editores. Fracaso renal agudo. Barcelona: Springer-Velarg Ibérica; 1999. p. 1---19.
- Montoliu J. Prevención y tratamiento del fracaso renal agudo. En: Net À, Roglán A, editores. Fracaso renal agudo. Barcelona: Springer-Velag Ibérica; 1999. p. 59---65.
- Romero M.; Delgado P.; De la Cueva L. Revisión de conocimientos sobre el fracaso renal agudo en el contexto del paciente crítico. Enfermería intensiva. [Internet] 2013 [ Consultado 15 marzo 2021]; 11. Disponible en www.elsevier.es/ei.
- Francisco Javier Gaínza. Nefrología al día. Insuficiencia Renal Aguda. Disponible en: https://www.nefrologiaaldia.org/317. Consultado 2 de marzo 2021.
- Gutiérrez Rodríguez P. TÉCNICAS CONTINUAS DE DEPURACIÓN RENAL EXTRACORPÓREA EN EL PACIENTE CRÍTICO: FUNDAMENTOS Y COMPONENTES DEL SISTEMA DE TERAPIA. TEYS [Internet]. 19 de diciembre de 2020 [citado 31 de marzo de 2021];2(9):14-9. Disponible en: https://tiemposdeenfermeriaysalud.es/journal/article/view/101
- Pérez. A. Técnicas continuas de depuración extracorpórea (TCDE). Màster en cures d´Infermeria al malalt crític. Universitat de Barcelona. 20019-2020.
- Muñoz M. Técnicas continuas de depuración extracorpórea para enfermería. Ed. Elsevier. Barcelona. España. 2012.
- Catalán R.M. Indicaciones de las Técnicas Continuas de Depuración Extrarenal. EUE Bellvitge, UB, 13 y 14 de marzo, 2013.
- Sánchez C. Componentes I: Catéteres, cuidados y manipulación del acceso venoso. EUE Bellvitge, UB, 13 y 14 de marzo, 2013.
- Mateos A. Componentes II: Circuitos, membranas y líquidos. EUE Bellvitge, UB, 13 y 14 de marzo, 2013.
- Ortuño M.; Vallès C. CUIDADOS DE ENFERMERÍA Y COMPLICACIONES MÁS FRECUENTES. EUE Bellvitge, UB, 13 y 14 de marzo, 2013.
- Muñoz M. Optimización de las Técnicas de Depuración Continuas. EUE Bellvitge, UB, 13 y 14 de marzo, 2013.
- Muñoz M. Optimización de las Técnicas de Depuración Continuas. EUE Bellvitge, UB, 13 y 14 de marzo, 2013.
- Camacho F. Anticoagulación del circuito con Citratos. EUE Bellvitge, UB, 13 y 14 de marzo, 2013.
- Catalán M.; Nuvials X. “PROYECTO ITU-ZERO” Prevención de la infección urinaria relacionada con la sonda uretral en los pacientes críticos ingresados en las unidades de cuidados intensivos. Ministerio de Sanidad, Semicyuc, SEEIUC. España. 2018-2020
- Ortuño M. Protocolo “Maneig de Tècniques Contínues de Reemplaçament Renal amb el monitor Multifiltrate Fresenius amb citrat”. Hospital Universitari Joan XXIII. Tarragona. 2020.
- Ortuño M. Protocolo “Maneig de TCRR amb el monitor Prismaflex. Hospital Universitari Joan XXIII. Tarragona. 2019.
