En muchas ocasiones los pacientes posoperados precisan ser ingresados en la Unidad de Cuidados Intensivos. Pueden ser diferentes los motivos que lleven al paciente a ingresar a la unidad. Grandes cirugías como la cardíaca, la pulmonar o una gastrectomía, entre muchas otras, que por su complejidad y el elevado riesgo de complicaciones precisan un control estricto del estado del paciente y una vigilancia constante por parte de enfermería serán criterio de ingreso en UCI para realizar el postoperatorio.
Por ello es de vital importancia conocer los cuidados necesarios para este grupo de pacientes que estarán basados en el cuidado integral de la persona.
1. CONCEPTOS DE LA ANESTESIA
Fue en 1844 donde Horace Wells, dentista de Connecticut, Estados Unidos, utilizó por primera vez el óxido nitroso como anestésico para extraer piezas dentarias. Fue seguido del éter en 1846 y posteriormente el cloroformo en 1847 los que marcaron el inicio de la Anestesiología.
En España la Anestesia se fue desarrollando a partir del año 1950. En 1953 se creó la Sociedad Española de Anestesia y Reanimación, S.E.D.A.R.
La definición de anestesia es la perdida temporal y reversible de las sensaciones de tacto y dolor producidas por un medicamento.
La elección del tipo de anestesia a utilizar se hace en el preoperatorio, dónde el médico anestesista valorará los antecedentes del paciente y la intervención y técnica a realizar.
Para determinar el riesgo anestésico según el estado físico del paciente, se utiliza la Escala ASA (American Society of Anesthesiologists), clasificándolo en diferentes grados y relacionándolo con la posibilidad de muerte perioperatoria.

Tabla 1 Tabla adaptada de Departamento de Salud Clínico Malvarrosa. Clasificación ASA del estado físico de los pacientes
Entre ellas distinguimos la anestesia general, la anestesia espinal, la anestesia plexular, la anestesia local y la anestesia tópica. Destacamos la anestesia general y la espinal para cirugías del paciente crítico y semicrítico.
1.1 Anestesia general
Como hemos dicho anteriormente, la anestesia general es un estado temporal y reversible de hipnosis, analgesia, y relajación muscular. Con los fármacos vamos a conseguir un efecto de hipnosis, es decir, vamos a impedir que el paciente tenga algún tipo de recuerdo de la fase intraoperatoria. Con los analgésicos conseguiremos reducir o impedir el dolor y con los relajantes musculares conseguiremos una parálisis de la musculatura lisa y estirada que impida la movilidad del paciente y su respiración, pero preservaremos el funcionamiento neurovegetativo para que los órganos sigan funcionando de forma fisiológica. Se utiliza en la mayoría de las cirugías mayores.
En ella destacamos tres fases:
- Inducción: Es la fase donde se induce el sueño al paciente. Se puede hacer con fármacos intravenosos (propofol, etomidato, midazolam, etc.), inhalatorios (sevoflurano, isoflurano, gas de óxido nitroso, etc.), o la combinación de ambos. Se utilizan fármacos que inducen de forma rápida. Se debe controlar la vía aérea del paciente y el estado hemodinámico.
- Mantenimiento: En ella se desarrolla todo el acto quirúrgico. Se mantendrá el estado de hipnosis según requerimientos del paciente. Nos podemos ayudar con el Índice bispectral (BIS) para saber el estado de sedación del paciente, también se deberá controlar el nivel de analgesia y la relajación neuromuscular si es necesaria.
- Despertar: Al finalizar la cirugía se procede a despertar el paciente, estado de vigilia. Se debe revertir el efecto de los sedantes y los relajantes musculares, pero mantener la analgesia. Extubación del paciente y control hemodinámico y del dolor.
Las complicaciones de la anestesia general pueden ser:
- Alteración hemodinámica: bradicardia, arritmias, hipotensión, por efecto de los fármacos o de la propia cirugía. Será importante la toma de constantes vitales cada 5 minutos según estándares del ASA.
- Pulmonares: broncoaspiración, infección, imposibilidad de ventilar, hipoxia
- Rotura de piezas dentales, laceraciones, sangrado y edema.
- Laringoespasmo, broncoespasmo, aumento de la PIC, aumento de la presión intragástrica debido a la alteración de los reflejos parasimpáticos, simpáticos y espinales.
- Alteración del sistema fisiológico de la termorregulación: hipotermia intraoperatoria
- Propias de la medicación empleada: hipotensión, bradicardia, hipertermia maligna, infección, náuseas, vómitos, íleo paralitico, delirium o depresión respiratoria
- Manipulación errónea del paciente en la mesa de quirófano: UPP, lesiones oculares, caídas, etc.
1.2 Anestesia espinal
Este tipo de anestesia permite al cirujano realizar la intervención con el paciente despierto, consciente, pero sin dolor. Consiste en la punción de anestésico local (p.ej. lidocaína 2%) en el espacio intradural o epidural con la finalidad de bloquear el estímulo nervioso. Se utiliza para cirugías de abdomen inferior (ginecológicas, urológicas…) y de extremidades inferiores.
- Intradural: el anestésico local actúa en el espacio subaracnoideo produciendo un bloqueo nervioso con la perdida de la actividad sensitiva, motora y vegetativa. Efecto anestésico. Cuando se localiza el espacio hay salida de LCR. La zona más habitual a pinchar es L3-L4.
- Epidural o peridural: el anestésico local actúa en el espacio epidural. Se puede hacer con una única punción o con la colocación y mantenimiento de un catéter. El inicio de acción es más lento que en la punción intradural. Con ella conseguimos efecto anestésico y/o analgésico. Normalmente el bloqueo motor de ésta permite mover las EEII al paciente. Muy usada para el control del dolor.
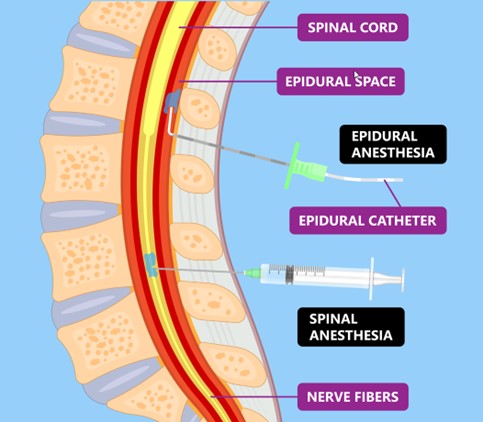
Imagen 1: Punción epidural y punción espinal.
Las complicaciones de la anestesia espinal pueden ser debidas a la punción o debidas al fármaco. Las más habituales son:
- Punción hemática
- Parestesias
- Hipotensión arterial
- Náuseas y vómitos
- Retención urinaria
- Lumbalgia
- Cefalea post punción
2. MANEJO DEL DOLOR EN UCI
Definición
El dolor fue definido por la Asociación Internacional para el Estudio del dolor como “una experiencia sensorial y emocional desagradable asociada a una lesión tisular real o potencial”.
Los pacientes críticos experimentan dolor durante su estancia en la UCI ya sea por su enfermedad de base, por los procedimientos que se les realizan o por la movilización que requieren, es por ello que es de vital importancia la administración de analgesia para un buen manejo del dolor. El tratamiento del dolor es considerado un derecho del paciente, así como un buen indicador de buena práctica clínica y calidad asistencial.
El dolor puede generar alternaciones hemodinámicas, respiratorias, psicológicas, metabólicas y neuroendocrinas como taquicardia, delirium, ansiedad, desorientación o insomnio.
Para evaluar el dolor del paciente crítico disponemos de diferentes escalas de evaluación, para ello, debemos tener en cuenta a los pacientes conscientes i orientados y a los pacientes con limitación de la comunicación como pueden ser los pacientes sedados y conectados a ventilación mecánica.
Para los pacientes conscientes se recomienda la utilización de la escala visual analógica (EVA) o la escala numérica del dolor, ya que son fáciles de aplicar y son adecuadas para la evaluación y monitorización del dolor.
Para los pacientes inconscientes se puede utilizar la escala Richmond Agitation-Sedation (RASS) o la Behavioral Pain Scale (BPS), en ellas se valoran las expresiones faciales, la agitación o la postura y la sincronía con el respirador.
Estas escalas deben formar parte de un protocolo para la evaluación de dicho dolor, evaluándolas mínimo cada 4 horas, o antes y después de procedimientos invasivos que puedan provocar o aumentar el dolor.
2.1 Clasificación del dolor
Tenemos diferentes formas de clasificar el dolor:
Duración:
- Dolor agudo: es de corta duración y su intensidad se relaciona con la gravedad del estímulo que lo produce. Suele estar localizado. Se acompaña de reflejos protectores del mismo organismo.
- Dolor crónico: tiene una duración de más de 3 o 6 meses, por ello se asocia a una afección crónica. No se asocia a factores protectores. El dolor crónico puede interferir en la vida cotidiana de la persona y se asocia a síntomas psicológicos.
Origen
- Nociceptivo: es causado por la activación de los receptores del dolor, los nociceptores, como respuesta del organismo ante un estímulo. Como ocurre en el dolor agudo, suele relacionarse la intensidad con la gravedad del estímulo.
- Neuropático: se asocia al daño directo a los nervios periféricos o al sistema nervioso central (SNC), por lo que no se relaciona con las terminales sensitivas.
- Psicógeno: tiene una causa psíquica o factores psicológicos (depresión, hipocondría).
Localización
- Somático: se origina en la piel, músculos, tendones, ligamentos o en el sistema vascular. Generalmente está localizado.
- Visceral: se origina en los órganos internos: riñón, hígado, pulmones… es profundo, continuo y generalmente mal localizado. Puede irradiarse e incluso percibirse a otra zona del dolor de origen.
Fisiología del dolor
Los nociceptores o receptores del dolor son terminaciones periféricas de las fibras aferentes sensoriales primarias y son los que desencadenan la respuesta al estímulo doloroso. Son estimulados como respuesta a la inflamación de la lesión tisular.
Se diferencian tres tipos según localización; los nociceptores cutáneos, los nociceptores musculo-articulares y los nociceptores viscerales. Además, existen dos tipos de receptores del dolor, los de conducción rápida que responden a estímulos térmicos y mecánicos, y otros de conducción más lenta que responden a la presión, temperatura y otros tipos de estímulo.
El estímulo del dolor es percibido por los nociceptores, estos reciben y transforman los estímulos en potencial de acción que son transmitidos a través de las fibras aferentes a un nervio raquídeo de la medula espinal. Allí, en contacto con neuronas de segundo orden (medulares) cruzan al lado contrario de la médula. Después asciende hasta el sistema de activación reticular (RAS) y el tálamo. La localización y percepción del dolor se da a nivel de la corteza somatosensorial, en las regiones cerebrales.
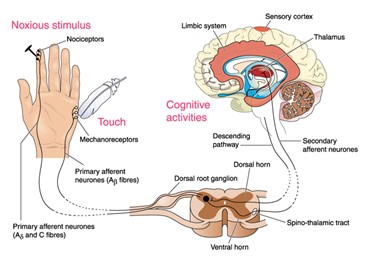
Imagen 2: Fisiología del dolor.
2.3 Un acercamiento a la analgesia multimodal
La analgesia multimodal es utilizada sobre todo en el paciente post quirúrgico. Después de una intervención, el dolor se considera agudo, y, por lo tanto, produce un importante estrés al paciente con la consecuencia de alterar su estado hemodinámico el cual recae en la elevación de la morbi-mortalidad en el periodo postoperatorio.
El objetivo de la analgesia multimodal es reducir los efectos secundarios derivados de los fármacos o técnicas empleadas para mejorar dicho dolor, y potenciar la analgesia administrada para obtener una mayor efectividad del tratamiento.
En el dolor postoperatorio intervienen la fuente nociceptiva, la inflamatoria y la neuropática, por lo que implica la necesidad de administrar de forma combinada diferentes fármacos que actúen sobre las diferentes vías causantes del dolor a nivel del SN central y periférico para evitar su estimulación y transmisión.
Las asociaciones de medicamentos más utilizados son el paracetamol asociado con antinflamatorios no esteroides (AINEs) o los opioides asociados con AINEs. Se combina la vía endovenosa, con la epidural y los bloqueos de los nervios periféricos o la infiltración de heridas.
La pauta de analgesia multimodal produce mayor alivio del dolor y reduce la administración de opioides, por lo que se traduce en una recuperación más placentera para el paciente, una disminución de los efectos secundarios causados por los opioides, y un mejor resultado del posoperatorio.
3.VALORACIÓN Y CUIDADOS DE ENFERMERÍA EN EL PACIENTE POSTQUIRÚRGICO EN UCI
3.1 Primer contacto
A la llegada del paciente proveniente de quirófano nos podemos encontrar con dos situaciones diferentes, el paciente aún bajo los efectos de la sedo analgesia, intubado y conectado al respirador, o un paciente ya consciente, es decir, que ya ha despertado del coma inducido en el quirófano y que respira por sí solo. Son situaciones diferentes pero las dos nos exigirán unos cuidados intensivos por nuestra parte.
- En primer lugar, debemos presentarnos e identificar al paciente que tenemos delante. Confirmaremos con la pulsera identificativa que el nombre y la historia clínica sean correctas y coincidan con los que tenemos en nuestra gráfica, si el paciente está consciente y orientado, podemos pedir su colaboración.
- El equipo que acompaña al paciente a la UCI nos deberá poner en situación explicándonos la intervención que se le ha practicado, y si ha habido incidencias durante el acto quirúrgico como puede ser inestabilidad hemodinámica, sangrado, o cualquier otra incidencia importante para el correcto cuidado postoperatorio. Por otro lado, debemos de ser informados de los antecedentes del paciente y de si existen alergias medicamentosas y cuales son.
- En este instante debemos estar valorando el nivel neurológico, puede ser que el paciente nos llegue despierto, pero debemos evaluar si realmente está consciente y orientado. Podemos ayudarnos de las escalas. Debemos ubicar al paciente del cambio de sala y del día y hora que es. En caso de que el paciente se desoriente o se agite, se puede valorar la presencia y acompañamiento por parte de la familia.
- Como se ha comento antes, el paciente puede ser portador de TOT con ventilación mecánica y deberá mantenerse la sedación hasta que el equipo médico decida despertar y extubar al paciente. Deberemos monitorizar la saturación de oxígeno periférico (SpO2). La mayoría llegan con algún aporte de oxígeno siendo lo más habitual cánulas nasales de bajo flujo o mascarilla ventimask. Es importante recordar que para proceder a la extubación debemos tener al paciente completamente despierto, y, además, asegurarnos que ha recuperado los reflejos de defensa laríngeos y faríngeos (deglución y tusígeno) y mantiene una adecuada conexión con el entorno: apertura espontánea de ojos, responde a ordenes verbales sencillas, etc.
- Vamos a monitorizar la hemodinamia del paciente para poder controlar la frecuencia cardíaca y el ritmo. Debemos monitorizar la tensión arterial, ya sea de forma invasiva o no invasiva dependiendo del estado hemodinámico en el que llegue. El paciente puede estar monitorizado con otros dispositivos como Swan Ganz, PICCO, balón de contrapulsación, Vigileo, PIC o PPC que también deberemos identificar y controlar. En caso de que el paciente lleve marcapasos, se deberá monitorizar y comprobar su funcionalidad.
- Se revisarán los accesos venosos sean vías periféricas o catéter venoso central. Comprobaremos la función de las luces y la medicación que pueda llevar en ellas. En caso de precisar NPT se deberá iniciar por una luz sellada.
- Será importante el control del dolor, muchas veces llegan con catéter epidural con perfusión continua de analgesia que deberemos revisar. En otros casos llevan perfusión continua de analgesia endovenosa o analgesia a demanda endovenosa. En cualquiera de los casos anteriores, deberemos asegurarnos de que la analgesia sea efectiva y suficiente. Puede ser que el/la paciente aun no haya recuperado la movilidad si se le ha practicado una anestesia espinal. Deberemos anotar cuando revierta completamente.
- El control de la diuresis también es de vital importancia para orientarnos sobre el estado hemodinámico del paciente. Deberá hacerse de forma horaria y adecuar el objetivo volumen según el peso del paciente, con uso de urinometer.
- Miraremos temperatura ya que muchas veces llegan hipotérmicos a causa de la baja temperatura dentro de quirófano, si es así deberemos termorregular al paciente ya sea con mantas de ropa o manta térmica. En caso de fiebre, deberemos consultar si son indicados los hemocultivos, y procederemos a bajar la temperatura con medidas físicas o fármacos prescritos por el equipo médico.
- Control de la SNG o sonda nasoyeyunal en declive o aspiración suave según indicación. La aparición de náuseas y vómitos a causa de la medicación anestésica es frecuente en el postoperatorio, y puede ser una causa de complicación por lo que deberemos revisar la medicación pautada para que en caso de que se presenten estos síntomas, se pueda administrar de forma precoz. La SNG o nasoyeyunal no debe de movilizarse ni hacer lavados si no es con orden estricta del médico.
- Control de los apósitos quirúrgicos. En caso de que el apósito llegue manchado, deberemos rotularlo para poder detectar si este augmenta de cantidad.
- Los drenajes deben numerarse si llevan más de uno y conocer donde están situados para saber si el débito que sale es el correcto o no, y valorar la cantidad de este.
- En las primeras horas el paciente deberá permanecer en reposo absoluto con el cabezal a 30º (posición de Fowler) siempre que sea posible y hasta indicación médica.
- Es posible que el equipo médico nos pida extracción de analíticas de sangre para la valoración de diferentes parámetros como bioquímica, hemograma coagulación y gases arteriales o venosos, la realización de un electrocardiograma o la realización de una radiografía.
3.2 Control posterior
Dolor:
Para la valoración del dolor empelaremos la escala EVA en caso de pacientes conscientes y en caso de pacientes bajo efectos de sedación la escala que utilice el hospital, como puede ser la escala ESCID que valora la expresión facial, la tranquilidad, el tono muscular, la adaptación a la VM y la confortabilidad.
Utilizaremos analgesia mediante catéter epidural, infusión continua endovenosa o analgesia sistémica endovenosa. Comprobaremos su efectividad y la necesidad de la misma ya que seguramente no será la misma demanda a la llegada del paciente a la UCI que al 4º día del postoperatorio.
Herida quirúrgica:
Se realizará la cura de la misma según el protocolo de cada hospital, generalmente por las mañanas coincidiendo con la higiene del paciente y de forma estéril en grandes cirugías. Se valorará el aspecto y características para detectar posibles infecciones. Es importante que en caso de algún cambio se anote a la gráfica y se comunique.
El equipo médico puede valorar el uso de faja abdominal en algunas cirugías.
Drenajes:
Podemos encontrarnos con diferentes tipos de drenaje según la cirugía realizada: Penrose, Redón, Jackson Pratt, tubo de Kehr, sonda Nelaton, drenajes tipo Saratoga, drenajes torácicos pleurales o drenajes ventriculares.
Se valorarán de forma continua para detectar sangrado o cambios en el débito. Valoraremos la pérdida del vacío. En caso de drenajes torácicos también debemos revisar el sello de agua, posibles fugas y comprobaremos la conexión a la aspiración si esta está indicada.
La cura se realizará también cada 24 h, normalmente por las mañanas cuando se realiza la higiene del paciente y la cura de la herida. En caso de los drenajes ventriculares, deberán hacerse de forma aséptica y con riguroso cuidado.
Serán retirados según indicación médica al cabo de unos días.
En el siguiente QR podrás obtener más información sobre la función, utilidad y cuidado de los drenajes:

DRENAJES QUIRÚRGICOS: Penrose, Kher, Tira de gasa, Redón, Pleur-Evac: https://www.youtube.com/watch?v=9dD3TIb1aoU
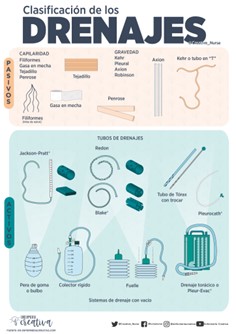
Imagen 3. Clasificación de los drenajes. Fuente: Enfermería creativa
Riesgo de hemorragia:
Clínica como sudoración excesiva, palidez cutánea, piel fría, relleno capilar de más de 3 segundos, nerviosismo, confusión o somnolencia serán indicativos de hemorragia.
Se deben monitorizar las constantes vitales: la FC, tensión arterial, PVC, gasto cardiaco o diuresis horaria para detectar signos de inestabilidad tales como, taquicardia, bradicardia, hipotensión u oliguria.
Se realizarán controles analíticos de hemograma, y si procede, se administrarán hemoderivados.
El paciente debe estar en reposo absoluto con el cabezal de la cama incorporado 30-45º hasta indicación médica.
Riesgo de complicaciones pulmonares:
Cuando el paciente sea portador de TOT se deben valorar los parámetros del respirador, el aspirado de secreciones, la saturación de oxígeno, etc.
Cuando del paciente esté extubado se debe vigilar el patrón respiratorio, la FR, la saturación, fisioterapia respiratoria y movilización precoz.
Riesgo de trombosis:
Estarán indicadas las medias de compresión neumáticas intermitente después de la cirugía o en su ausencia serán medias de compresión en EEII.
Generalmente, a las 8 h post cirugía y según indicación médica, se inicia la profilaxis antitrombótica con heparina de bajo peso molecular.
Nutrición
Dependiendo de la intervención quirúrgica que se haya realizado al paciente se deberá mantener un reposo del tracto gastrointestinal, o por el contrario podrá seguir con la dieta.
El ayuno prolongado en el paciente crítico se relaciona con mayor morbimortalidad por el estado hipermetabólico como respuesta a la agresión recibida.
Debemos conocer las diferentes vías de administración para la alimentación para reducir este tiempo.
La nutrición que podemos ofrecer es:
- Por vía oral: después de 6 horas de ayuno post intervención, el paciente podrá iniciar dieta progresiva según el protocolo del hospital.
- Por vía entérica: se inicia nutrición enteral, generalmente, por sonda nasogástrica.
- Por vía parenteral central. Generalmente, se deja una luz del catéter venoso central sellada para poder iniciar nutrición por ella. Debe ser un procedimiento estéril.
Íleo paralítico:
Se controlará el peristaltismo mediante auscultación de ruidos intestinales.
No se deben realizar lavados ni movilizar la SNG o sonda nasoyeyunal si no es con indicación médica específica.
Fisioterapia respiratoria:
No ha sido hasta los años 90-2000 cuando han aparecido las técnicas de fisioterapia respiratoria que se basan en la modificación del flujo inspiratorio y espiratorio.
La rehabilitación pulmonar después de una intervención quirúrgica torácica o gastrointestinal minimiza las complicaciones de la operación, puede contribuir a reducir la hipoxemia o el riesgo de aparición de atelectasias y ayuda en el manejo de secreciones. Por lo que se traduce en una reducción de infecciones, reducción en la estancia hospitalaria y una rehabilitación más temprana.
Se conocen diferentes procedimientos terapéuticos para hacer rehabilitación pulmonar: clapping, vibraciones, presión espiratoria positiva, espirometría incentivada, respiración con labios fruncidos, ventilación dirigida, ventilación torácica localizada, etc. Seguidamente, nos centraremos en la espirometría incentivada, ya que los dispositivos utilizados permiten que sea el personal de enfermería el que explique y ayude al paciente a realizarlo, sin necesidad de ser un fisioterapeuta.
La reexpansión pulmonar inspiratoria máxima es el objetivo principal de la fisioterapia respiratoria. La espirometría incentivada es una de las más utilizadas en la UCI después de algunas cirugías y en el paciente crítico. Es una técnica de inspiración lenta, profunda y larga que bien utilizada, mejora la función ventilatoria, reduce el trabajo respiratorio y ayuda a un mejor intercambio gaseoso.
Los incentivadores espirométricos por volumen, están orientados a aumentar el volumen pulmonar con la inspiración del paciente.
Se trata de un dispositivo de una sola cámara con un embolo unidireccional. Con un pequeño marcador, permite al paciente objetivar el volumen conseguido. A través de una manguera, el paciente hace una inspiración lenta y el embolo sube indicando el volumen movilizado.

Imagen 4: Incentivador espirométricos por volumen. Fuente propia
Por otro lado, el Triflow, utiliza la técnica de espirometría inspiratoria de flujo. No es el más recomendado para esta técnica, pues un mal uso puede derivar a una alcalosis respiratoria. Requiere mayor trabajo de los músculos respiratorios por parte del paciente y generalmente se consiguen volúmenes pulmonares más bajos. Es un aparato con tres cámaras comunicadas y una bola en cada una de ellas, el hecho de tener que elevar las tres bolas al máximo con la inspiración a través de una pequeña manguera, hacen que ésta sea rápida, no controlada y lenta por el paciente.
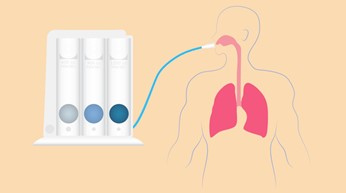
Imagen 5: Espirometría inspiratoria de flujo (Triflow)
Los dos son de uso individual y permiten que el paciente ser autónomo a la hora de realizar los ejercicios.
Será el equipo médico el que nos indicará el inicio de la rehabilitación. En cirugías como la pulmonar o bariátrica, la fisioterapia respiratoria se inicia, generalmente, en el posoperatorio inmediato.
BIBLIOGRAFÍA
- Hinkle JL, Cheever KH. Enfermería medicoquirúrgica Volumen 1. 14ª Edición. Philadelphia: Wolters Kluwer; 2018
- Aragonés Manzanares R, de Rojas Román JP, Aguiar Flores E, Alcalá Peña MM, Alcalde Perez D, Aldana Díaz EM et all. Cuidados Intensivos: Atención integral al paciente crítico. España: Editorial Médica Panamericana S.A.; 2016
- Grupo de shock. Actualización en Shock: atención del paciente en shock en urgencias [internet]. 3ª edición. España: Bubok Publishing S.L; 2014 [citado 2021 Marzo 2]. Disponible en: actualizacion-de-manejo-del-paciente-en-shock-tercera-edicion.pdf (sborl.es)
- Navío Serrano AM, Abad Esteban F, Aguiló Mir S, Alonso Llasheras JE, Afonso Rivero D, Aragón Leal MA et all. Manejo del paciente en shock en urgencias [internet]. Barcelona: Edikamed S.L; 2011 [citado 2021 Marzo 2]. Disponible en: SHOCK2ED.pdf (grupodeshock.info)
- Camacho JM, Calvo C. Shock: etiología y diagnóstico. An Pediatr Contin. 2003; 1 (3): 119-24
- Avilés García M, Figueira Iglesias JC, Agrifoglio Rotaeche A, Sánches Sánchez M. Bacteriemia, sepsis y shock séptico. Medicine. 2018; 12 (52): 3066-75
- Yébenes JC, Lorencio C, Estebanc E, Espinosa L, Badia JM, Capdevilaf JA et all. Código Sepsis Interhospitalario en Catalunya: modelo organizativo territorial para la atención inciial al paciente con sepsis. Med Intensiva. 2020; 44 (1): 36-45
- Aboal J. Reposición de volumen: ¿Cristaloides o coloides?. Rev Esp Cardiol Supl. 2015; 15 (D): 15-19
- Banchón Alvarado JD, Camacho García DE, Fernández Saquicela CA, Villacís Nieto JM. Conceptos actuales de sepsis y shock séptico. Journal of America Health [Internet]. 2020 [citado 2021 Marzo 2]; 3 (2): 103-116. Disponible en: Conceptos actuales de sepsis y shock séptico | Journal of America health (jah-journal.com)
- Garnacho Montero J, Fernández Mondéjar E, Ferrer Roca R, Herrera Gutiérrez ME, Lorente JA, Ruiz Santana S et all. Cristaloides y coloides en la reanimación del paciente crítico. Med Intensiva. 2015; 39 (5): 303-315
- Levy M, Evans L, Rhodes A. The Surviving Sepsis Campaign Bundle: 2018 update. Intensive Care Med. 2018; 44: 925-928
- Vahdatpour C, Collins D, Goldberg S. Cardiogenic Shock. Journal of the American Heart Assocition [internet]. 2019 [citado 2021 Marzo 2]; 8. Disponible en: Cardiogenic Shock | Journal of the American Heart Association (ahajournals.org)
- Hotchkiss R, Moldawer L, Opal S, Reinhart K, Turnbull I, Vicent JL. Sepsis and septic shock. Nat Rev Dis Primers [internet]. 2016 [citado 2021 Marzo 2]; 2. Disponible en: Sepsis and septic shock - PubMed (nih.gov)
- Kislitsina O, Rich J, Wilcox J, Pham D, Churyla A, Vorovich E et all. Shock- Classification and Pathophysiological Priciples of Therapeutics. Current Cardiology Reviews. 2019; 15 (2): 102-113
- Hernández Palazón J, Fuentes García D, Burguillos López S, Domenech Asensi P, Sansano Sánchez TV, Acosta Villegas F. Análisis de la insuficiencia de órganos y mortalidad en la sepsis por peritonitis secundaria. Med Intensiva. 2013; 37 (7): 461-467
- Rodríguez Botoa G, Rivero Garvía M, Gutiérrez González R, Márquez Rivas J. Conceptos básicos sobre la fisiopatología cerebral y la monitorización de la presión intracraneal. Neurología. 2015; 30 (1): 16-22
- Romero Valdez JG, Pereira Q, Atilio Zini R, Canteros GE. Reacciones de hipersensibilidad. Revista de Posgrado de la Via Cátedra de Medicina [internet]. 2007 [citado 2021 Marzo 2]; 167: 11-16. Disponible en: Microsoft Word - 3_167.doc (unne.edu.ar)
- Sáez Lorenzo L, Sáez Lorenzo M, Sáez Martin V. Revisión y actualización de la fluidoterapia de reanimación en el paciente con shock hipovolémico de origen traumático. Rev enferm CyL. 2016; 8 (1): 3-23
- Carrillo Ramírez SC, Elguera Echavarría PA. Choque circulatorio. Estableciendo metas en la reanimación con líquidos. Acta Medica Grupo Ángeles. 2017; 15 (1): 78-82
- Alemparte Pardavila E, Aller Fernández V, Bouza Vieiro MT, Cortés Cañones JR, Galeiras Vázquez R, García Monge MJ et all. SHOCK: identificación y manejo [Internet]. A Coruña: Seteseis Comunicación Creatividade SL y Complexo Hospitalario Universitario A Coruña (CHUAC); 2011 [citado 2021 Marzo 2]. Disponible en: (PDF) SHOCK: Identificación y Manejo (researchgate.net)
- González Villavelázquez ML, García Gonzalez A. Traumatismo craneoencefálico. Revista Mexicana de Anestesiología. 2013; 36 (1): 186-193
- González Posada MA, Biarnés Suñe A, Naya Sieiro JM, Salvadores de Arzuaga CI, Colomina Soler MJ. Damage Control Resuscitation en el paciente traumático. Rev Esp Anestesiol Reanim. 2019; 66 (7): 394-404
- Narváez I, Canabal A, Martín C, Sánchez M, Moron A, Alcalá J et all. Incidencia y evolución de la miocardiopatía séptica en una cohorte de pacientes con sepsis y shock séptico. Med Intensiva. 2018; 42 (5): 283- 291
- Zariquiey Esteva G, Santa Candela P. A propósito de un caso: intervenciones enfermeras a una paciente con shock anafiláctico en la UCI. Enferm Intensiva. 2017; 28 (2): 80-91
- Sánchez D, Lara B, Clausdorff H, Guzmán A. Generalidades y manejo inicial del shock. ARS MEDICA Revista de Ciencias Medicas. 2018; 43 (3): 66-76
- López Cruz F, Reyes Barragán G, Tapia Ibáñez EX, Paz Cordero DC, Ochoa Morales X, Cano Esquivel AA et all. Choque hipovolémico. An Med (Mex). 2018; 63 (1): 48-54
- Galeiras Vázquez R, Ferreiro Velasco ME, Mourelo Fariña M, Montoto Marqués A, Salvador de la Barrera S. Actualización en lesión medular aguda postraumática. Parte 1. Med Intensiva. 2017; 41 (4): 237- 247
- Dave S, Cho JJ. Neurogenic Shock [internet].StatPearls Publishing; 2021 [citado 2021 Marzo 2]. Disponible en: Neurogenic Shock - StatPearls - NCBI Bookshelf (nih.gov)
- Rhodes A, Evans L, Alhazzani W, Levy M, Antonelli M, Ferrer R et all. Campaña para sobrevivir a la sepsis: recomendaciones internacionales para el tratamiento de la sepsis y el choque septicémico: 2016. Critical Care Medicine. 2017; 45 (3): 486-568
- Haseer Koya H, Paul M. Shock [internet] StatPearls Publishing; 2021 [citado 2021 Marzo 2]. Disponible en: Shock - StatPearls - NCBI Bookshelf (nih.gov)
- Velasco Zúñiga R. Shock. Unidad de Urgencias Pediátricas. Hospital Universitario Río Hortega Valladolid. 2020
- Sabatier C, Monge I, Maynar J, Ochagavia A. Valoración de la precarga y la respuesta cardiovascular al aporte de volumen. Med Intensiva. 2012; 36 (1): 45-55
- Diaztagle Fernández JJ, Rodríguez Murciaa JC, Sprockel Diaz JJ. La diferencia venoarterial de dióxido de carbono en la reanimación de pacientes con sepsis grave y shock séptico: una revisión sistemática. Med Intensiva. 2017; 41 (7): 401- 410
- Palencia Herrejón E, Bueno García B. Nuevas guías de práctica clínica de la «Campana˜ sobrevivir a la sepsis»: lectura crítica. Med Intensiva. 2013; 37 (9): 600-604
- Grupo de trabajo de sepsis. Documento de Consenso (SEMES-SEMICYUC). Recomendaciones del manejo diagnóstico-terapéutico inicial y multidisciplinario de la sepsis grave en los Servicios de Urgencias hospitalarios. Med Intensiva. 2007; 31 (7): 375-87
- Grupo de trabajo de enfermedades infecciosas y sepsis. Estudio nacional de vigilancia de infección nosocomial en servicios de medicina intensiva ENVIN HELICS Informe 2019 [Internet]. España: Sociedad Española de Medicina Intensiva Crítica y Unidades Coronarias (SEMICYUC); 2019 [citado 2021 Marzo 2]. Disponible en: ENVIN-UCI '14 (vhebron.net)
- Ochagavía E, Baigorri F, Mesquida J, Ayuela JM, Ferrándiz A, García X, et al. Monitorización hemodinámica en el paciente crítico. Recomendaciones del Grupo de Trabajo de Cuidados Intensivos Cardiológicos y RCP de la Sociedad Espanola ˜ de Medicina Intensiva, Crítica y Unidades Coronarias. Med Intensiva. 2014; 38 (3): 154-169
- Mateu Campos ML, Ferrándiz Sellés A, Gruartmoner de Vera G, Mesquida Febrer J, Sabatier Cloarec C, Poveda Hernández Y, et al. Técnicas disponibles de monitorización hemodinámica. Ventajas y limitaciones. Med Intensiva. 2012; 36 (6): 434-444
- Grupo código sepsis. Plan de asistencia a la sepsis de Galicia. CÓDIGO SEPSIS [Internet]. Galicia: Xunta de Galicia; 2018 [citado 2021 Marzo 2]. Disponible en: CODIGO_SEPSE_CASTELLANO_WEB.pdf (sergas.es)
- Bravo Jover R, Morcillo Huertas J, Candela AB, Marín Real S, Martínez Baltanás A, Pascual Pérez R. Sepsis en adultos. España: Fisterra; 2020 [citado 2021 Marzo 2]. Disponible en: Guía clínica de Sepsis en adultos (fisterra.com)
- Empendium. Manual panamericano de medicina interna. Shock [Internet]. Polonia: Empendium [citado 2021 Marzo 2]. Disponible en: Shock - Enfermedades cardiovasculares - Enfermedades - Medicina Interna Basada en la Evidencia (empendium.com)
- Gersch C, Heimgartner NM, Rebar CR, Willis LM. Enfermería medicoquirúrgica. 4ªed. Philadelphia: Wolters Kluwer; 2017
- Woodruff DW. Enfermería fácil: Enfermería del paciente en estado crítico. 4ªed. Philadelphia: Wolters Kluwer; 201
