1. ENTORNO QUIRÚRGICO
Entendemos como entorno quirúrgico al conjunto de las áreas por las que el paciente atravesará durante su proceso quirúrgico. Los riesgos de infecciones en esta zona se intensifican cuando el personal no es hábil, está mal adiestrado o no conoce los protocolos de funcionamiento del área. Hemos hablado y lo haremos en otras unidades, de las funciones y atribuciones de la enfermera en el quirófano, si bien en esta unidad, la limpieza, asepsia y esterilización recae en la mayoría de los centros en las TCAE, es necesario conocer los principios básicos que sustentan la asepsia del entorno quirúrgico.
Debido al incremento en los últimos años de aspergilosis en los centros sanitarios, en especial en las áreas quirúrgicas, en relación, en su mayor parte con el aumento de cirugías a pacientes inmunusuprimidos sometidos a quimioterapia o radioterapia inmunosupresoras, o candidatos a trasplante, toma especial relevancia que todo el personal involucrado en el proceso observe rigurosamente las normas de circulación, vestimenta y limpieza dentro del quirófano. Las medidas de prevención de las infecciones nosocomiales quirúrgicas son la mejor barrera de protección. Las características de la limpieza van más allá de aspectos estéticos o de comodidad del paciente (como podrían darse en hoteles, aviones o bibliotecas), es una limpieza que asegura el control de la población de microorganismos, entre otras características.
CARACTERISTICAS DE LA LIMPIEZA
En general la limpieza deberá hacerse de manera correcta y completa seguida, cuando precise de la desinfección o esterilización, por personal debidamente formado, si bien debe ser considerada una responsabilidad de todos los miembros del personal. Existirán protocolos claros de limpieza y desinfección elaborados en colaboración con el servicio de medicina preventiva del centro sanitario, si lo hubiera, o el personal asignado al control de infecciones.
En la sanidad de ámbito público, se adjudica mediante concurso, a la empresa que cumpla con determinados requisitos, nº de personal asignado, materiales, frecuencia de la limpieza y tratamiento de los residuos, entre otros.
La organización de la limpieza de un centro sanitario se divide habitualmente, en Áreas Generales o de Bajo Riesgo, Áreas Semicríticas o de Medio Riesgo y Áreas Críticas o de Alto Riesgo; esta clasificación se realiza en función de criterios asistenciales, por ejemplo, UCI, Reanimación, Unidades de Hemodiálisis o quirófanos, serían Áreas Criticas, mientras que zonas de administración, pasillos de las plantas, etc., serían Áreas Generales o de Bajo Riesgo.
Dadas las particularidades ya mencionadas del área quirúrgica, los productos más empleados generalmente son: alcoholes, aldehídos e hipocloritos, sabiendo que todo el material empleado, tanto productos como herramientas, NO pueden salir del quirófano para realizar la higiene de otras zonas.
Los momentos de limpieza dentro del quirófano se dividen en:
- Limpieza diaria.
- Limpieza entre intervenciones.
- Limpieza tras intervenciones contaminadas y/o contaminantes del área.
LIMPIEZA DIARIA: Se realizará al inicio de jornada y al final de esta (salvo en quirófanos de urgencia que mantienen actividad 24 horas, que se realizará al inicio de cada turno y al final si la actividad lo permite). Es importante recordar el carácter de acceso restringido que tiene el área, evitar que personal que no sea de la unidad, acceda a la misma si no es estrictamente necesario, si lo hiciera, debe hacerlo tras cambiarse de atuendo en las esclusas, colocación de gorro, mascarilla y calzado de quirófano, si lo hubiera, o en su defecto, calzas. Y siempre, con la explicación del personal de la unidad sobre cómo circular dentro del quirófano.
Es importante no relajarnos tras los años de práctica en este punto, en los quirófanos de grandes centros hospitalarios, los circuitos “limpio” y “sucio” conllevan protocolos de asignación de personal limpio y sucio que no debe olvidar el cambio de zuecos, el uso de mascarillas y gorros, asi como, restringir en lo estrictamente necesario el cruce de una zona a otra a través de los quirófanos, ya que las condiciones higiénicas están estrechamente ligadas al diseño arquitectónico. Para asegurar la asepsia, la humedad relativa ambiente, el circuito de aire, su renovación (alrededor de 15 a 20 veces por hora) y grado de presión positiva está estrictamente relacionado con la presencia de patógenos contaminantes y con nuestra responsabilidad en el cumplimiento de lo anteriormente explicado.
LIMPIEZA ENTRE INTERVENCIONES: Los protocolos de limpieza varían de un centro a otro, pero todos coinciden en unas premisas básicas y comunes:
- Las TCAE, o el personal de limpieza (depende de convenios) retira todas las sabanas, cobertores, tubuladuras coarrugadas de ventilación, rodetes desechables, empapadores y material no fungible de la mesa, las mesas auxiliares, etc. (salvo el material CORTANTE, bisturís, agujas, cuchilletes, ampollas de medicación, etc. los retirará la instrumentista de su mesa, la circulante y/ o la due de anestesia de la mesa de anestesia antes de la limpieza. Asi como de las bolsas de basura de los cubos de quirófano y antequirófano.
- Se limpiará en húmedo, con el desinfectante de elección (generalmente con productos en spray fungicidas, levaduricida, bactericida y con actividad antivírica a determinadas temperaturas antes algunos virus habituales como el rotavirus, el herpesvirus, VHB, HCV, VRS, coronavirus, por ejemplo, el Instrunet®) la mesa quirúrgica, la mesa de la instrumentista, la de anestesia y las auxiliares si se hubieran utilizado (mesas de Mayo, de mano, de intubación...).
- Se limpiarán y recolocarán todos los cables del aparato de anestesia, los latiguillos de los electrodos de EKG, el manguito de T/A, la entropía, el BIS®, y todos los aparatos de control de constantes utilizados y no utilizados pero que se hayan contaminado por contacto con productos desinfectantes de superficies como el anteriormente citado.
- Se procederá a la limpieza del pavimento mediante sistema de mopa en doble cubo, de tal forma que siempre se friega con la solución de agua-detergente limpia. Y NUNCA se seca el pavimento.
- NUNCA se debe empezar a meter cajas de instrumental o materiales de reposición (jeringas, medicación, tubuladuras o sondas de capnografía nuevas) sin acabar el proceso de limpieza, salvo casos de extrema urgencia vital del paciente, NUNCA para acelerar los tiempos y acabar la programación, pese a las presiones que puedan aparecer.
- Todo este proceso debe ser realizado con celeridad, para reducir al máximo posible las esperas entre cirugías, pero siempre de manera exhaustiva, siguiendo el orden establecido de más cerca de la mesa quirúrgica a más lejos, de más limpio a más sucio, siendo lo último el suelo, y cambiando de agua, de paños o balletas o compresas siempre que sea necesario, y respetando el tiempo de secado de las superficies antes de entrar de nuevo a preparar la siguiente cirugía.
LIMPIEZA TRAS INTERVENCIONES CONTAMINADAS O CONTAMINANTES: Siempre que la situación del paciente lo permita, las cirugías de pacientes colonizados por patógenos infecciosos (SARM, Cándida Albicans, Estreptococo, VHB, VHC, VIH, SARS CoV-2, etc.), se programarán la última del parte y ese quirófano se inutilizará hasta dos horas tras fin de cirugía, más concretamente, desde que el paciente abandone el quirófano, y hasta que se realice la limpieza completa. Existen muchos protocolos de limpieza de quirófano tras cirugías contaminantes, pero un sistema habitual es el siguiente:
- Limpieza de suelos: Siempre en húmedo, con fregona empapada en agua con detergente desinfectante y bactericida profesional. Tras esa primera limpieza, se friega de nuevo con agua e hipocloritos al 0,1%, si existen zonas metálicas, como el pie de la mesa quirúrgica o placas de acero es conveniente cambiar la lejía al 0,1% por aldehídos que no corroen el metal.
- Limpieza de paredes: se limpian con dilución de detergente más lejía al 0,1% o aldehídos. Esta limpieza de paredes exhaustiva se realizará una vez a la semana, si la ocupación quirúrgica es elevada (uso exhaustivo del mismo, 24h ininterrumpidas, o turnos de mas de 12h consecutivas al día) o al menos, cada quince días si el uso es sólo de un turno al día, y con cirugías potencialmente no contaminadas.
- Limpieza de la zona de ante-quirófano/lava-manos: se lavan con agua y detergente: grifos, lava-manos, dosificadores de jabón y porta cepillos de desinfección, tras ello se repite la operación con agua y lejía o aldehídos.
- Limpieza de las rejillas de aire acondicionado: en la mayoría de los centros, y debido a la altura a la que se encuentran, es el personal de mantenimiento os encargados de su limpieza periódica o puntual bajo solicitud de la supervisión del área. En su mayoría, se aspiran, revisan los filtros y se procede a su limpieza con aldehídos y/o derivados que evitan la corrosión.
2. MATERIAL QUIRÚRGICO E INSTRUMENTAL
La limpieza, desinfección y posterior esterilización del material quirúrgico debe eliminar todos los patógenos presentes, virus, bacterias, hongos, levaduras, etc. Para entender cómo funcionan los procesos químicos o físicos de desinfección/esterilización haremos un repaso a la fisiología de los microorganismos que pueden contaminar el instrumental.
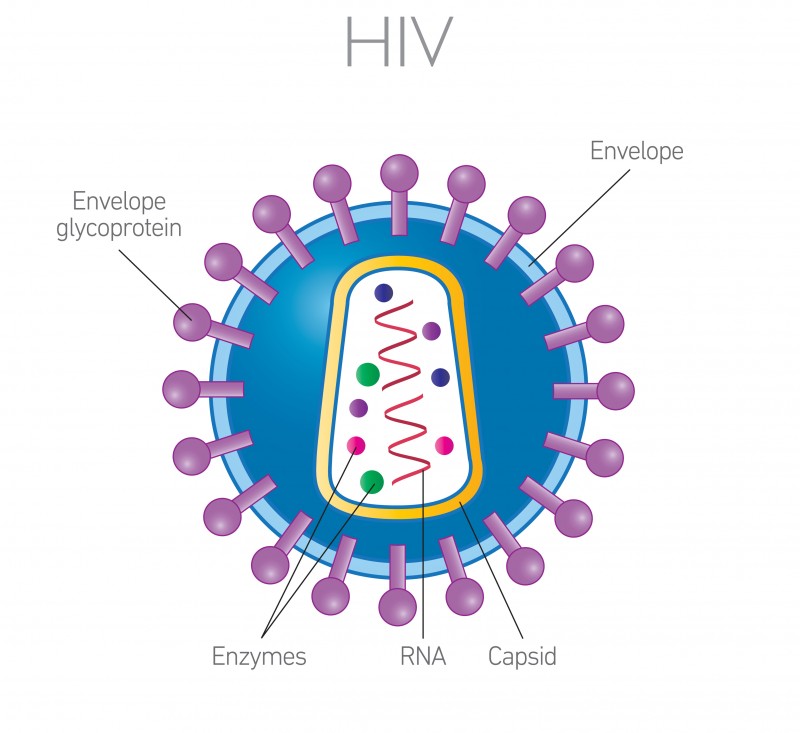
Imagen 40. Virus VIH
Los VIRUS son partículas de código genético, ADN o ARN, encapsuladas en una vesícula de proteínas, son acelulares, pequeños, que necesitan invadir una célula para replicarse en su interior. El virión, la parte infecto-contagiosa del virus, es una párticula compuesta por un ácido ribonucleico recubierto de una cápside proteica. Su mecanismo de acción es simple, el virus invade la célula, sus genes invaden el citoplasma y los ribosomas, “tomando el control” de tal manera que la célula comienza a producir nuevos ejemplares del virus hasta que ya no “caben” dentro de la célula, ésta se rompe con lo que se liberan al torrente sanguíneo y desde ahí se diseminan para colonizar el resto de las células del organismo o de otro huésped.
Las BACTERIAS son células procariotas que presentan un tamaño de unos pocos micrómetros y formas diversas, esferas (cocos), pequeñas barras (bacilos), filamentos curvos (vibrios), helicoidales (espirilos y espiroquetas) o irregulares. Poseen una membrana celular o plasmática que es una capa con permeabilidad selectiva para el intercambio de sustancias con el medio exterior, compuesta por una bicapa fosfolípida.
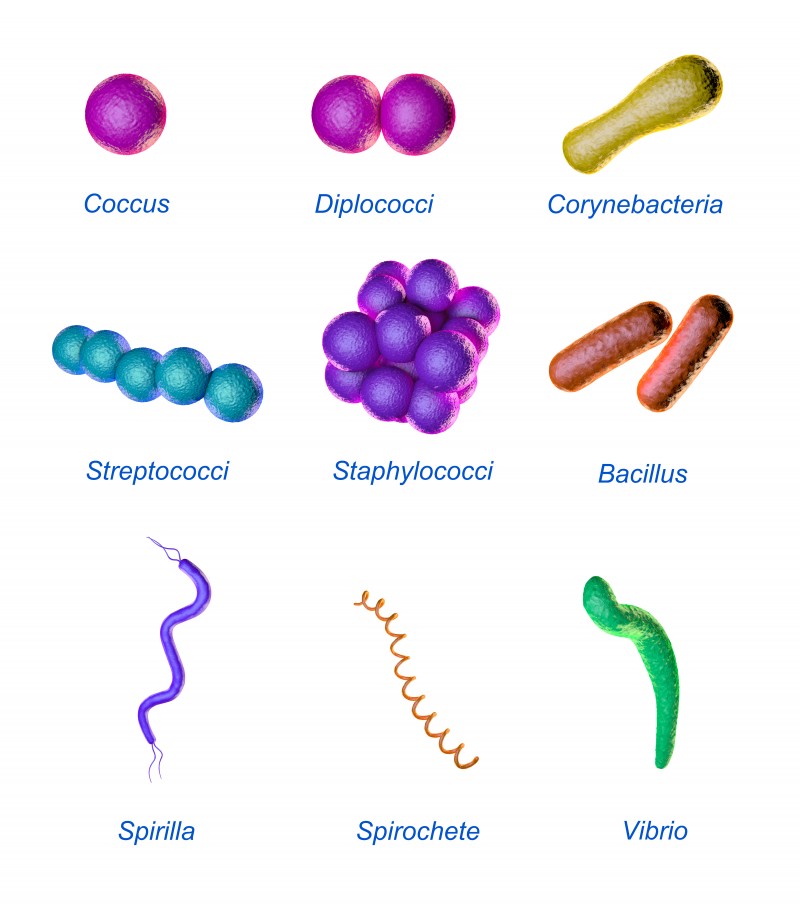
Imagen 41. Representación gráfica de bacterias
No presentan núcleo diferenciado como las eucariotas, pero si poseen, en su mayoría pared celular compuesta por peptidoglicanos, es una barrera rígida que la protege frente a diferencias de presión, según su estructura, las bacterias se clasifican en Gram+ y Gram-.
- Las Gram+ disponen de una pared celular con varias capas. Ej.: Staphylococcus Aureus.
- Las Gram- tienen una pared delgada y su parte externa está compuesta por glicoproteínas. Ej.: Esquerichia Coli.
Las que disponen de cápsula, ésta está situada por fuera de la pared, y su pérdida se relaciona con la disminución de infectabilidad bacteriana, ya que evita el ataque de antibióticos, la fagocitosis, ayuda a la adhesión y la protege de la desecación.
Algunas bacterias, disponen además, de flagelos, unos filamentos largos empleados como sistema de desplazamiento, fimbrias o filamentos cortos que emplean para adherirse al medio, y pilis, filamentos cortos y largos para el intercambio de ADN en la conjugación.
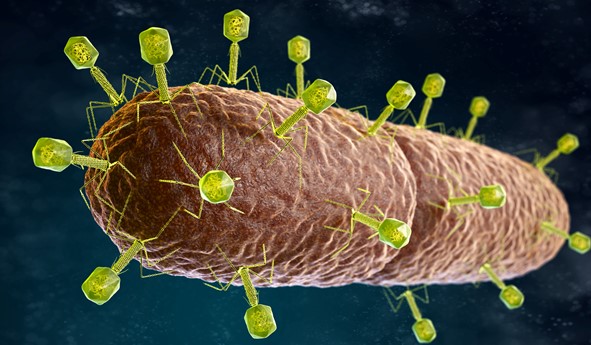
Imagen 42. Pilis
Algunas bacterias Gram+ desarrollan esporas o endosporas que son resistentes al calor, la desecación, los ácidos, los desinfectantes químicos o incluso la radiación ultravioleta. Las esporas se desarrollan por tanto, en circunstancias ambientales extremas, de ahí su importancia en nuestro medio. Las más esporas de bacterias GRAM+ más habituales son: Bacillus sp y Clostridium sp (C. Perfringens, causante de gangrena, C. Tetani, causante del tétanos C. Botulinum, responsable del botulismo y C. Difficile, causante de la colitis pseudomembranosa).
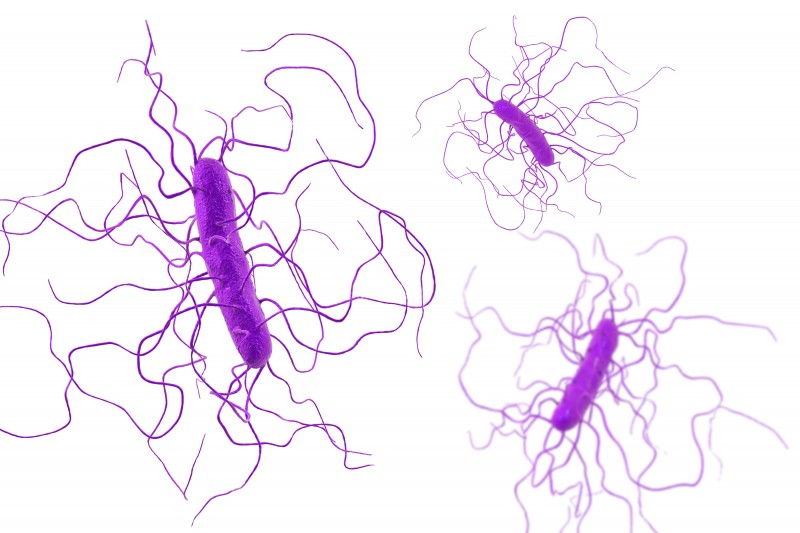
Imagen 43. Clostridium dificile en 3D aislado en fondo blanco
Los hongos o Eumycota son una clase de microorganismo eucariotas la mayoría, formas libres que actúan como putrefactores. De las 90000 especies conocidas menos de 200 son causantes de enfermedades en humanos, la mayoría necesitan para provocar la infección y enfermedad que el individuo esté inmunosuprimido. Son mas complejos biológicamente hablando que las bacterias, poseen un núcleo formado por varios pares de cromosomas de ADN envueltos por una membrana nuclear. El citoplasma contiene aparato de Golgi, mitocondrias y ribosomas, portan esporas y se dividen en:
- Hongos filamentosos (Aspergillus sp. o el Penicillium sp.), que son organismos pluricelulares, en la antigüedad se les llamaba mohos. Poseen pared celular polisacarida y protéica que regula el cambio de sustancias con el medio exterior y que es la principal responsable de la resistencia de los hongos a los desinfectantes y esterilizantes.
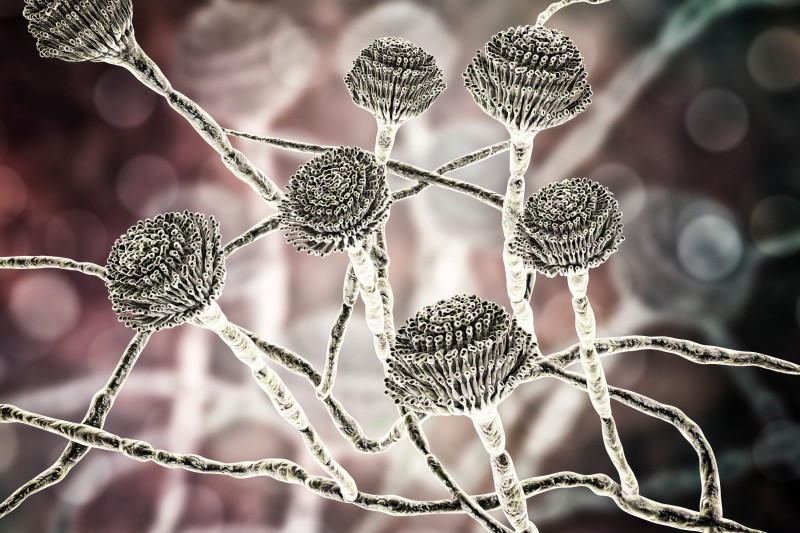
Imagen 44. Hongo Aspergillus
- Levaduras (Cándida sp.) que son hongos redondeados unicelulares y microscópicos que descomponen azucares e hidratos de carbono de sustancias orgánicas.
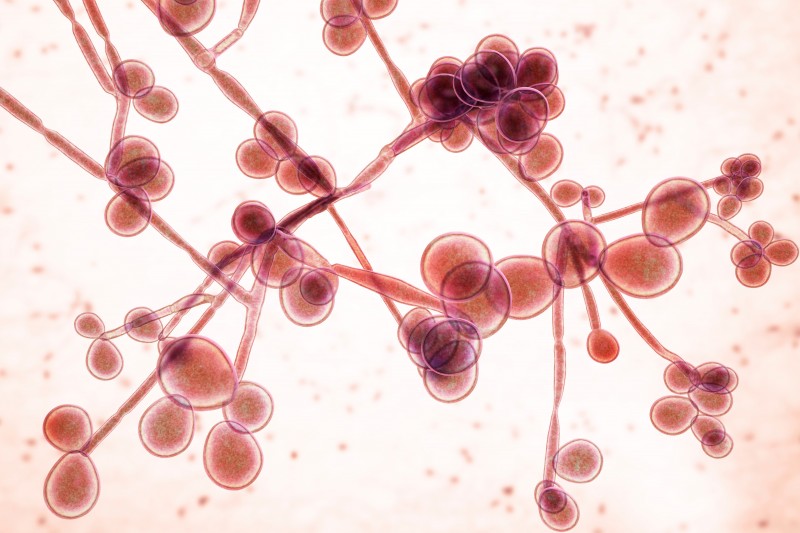
Imagen 45. Cándida Albicans
Los priones son agentes patógenos, en esencia, una proteína (PrPSc) sin un ácido nucléico específico, capaza de causar alteraciones, responsables de patologías neurodegenerativas letales como encefalopatías espongiformes transmisibles en una variedad de mamíferos, incluida la encefalopatía espongiforme bovina EEB, enfermedad de Creutzfeld-Jakob o “mal de las vacas locas”.
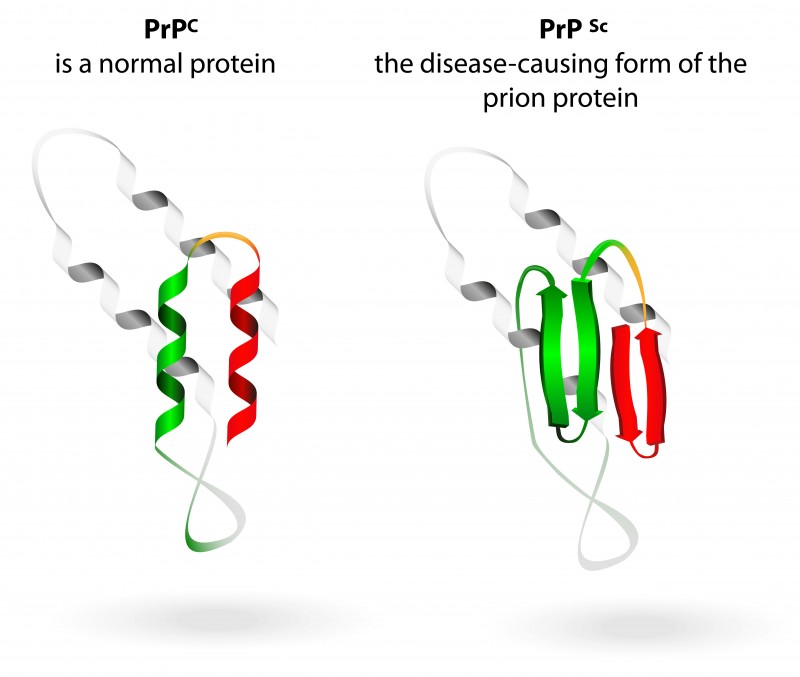
Imagen 46. Priones
La resistencia de todos los microorganismos mencionados a los distintos procesos de inactivación y/o destrucción depende, como ya hemos dicho, en la diferente composición de su pared celular, responsable de la permeabilidad de agentes desinfectantes y esterilizantes, siendo los priones, los más resistentes.

Tabla. Grado de resistencia a la inactivación, de mayor a menor
Todos los microorganismos presentes pueden colonizar el área quirúrgica, los aires acondicionados, el material, el instrumental, etc. Por eso es muy importante una buena limpieza, desinfección y esterilización. No solo se esteriliza el instrumental quirúrgico propiamente dicho, muchos objetos de uso quirúrgico requieren desinfección y, en ocasiones, esterilización, entre paciente y paciente como, por ejemplo, la sonda de capnografía, las palas de laringoscopio, la cánula de Vama, mascarillas laríngeas etc…
La limpieza previa de estos materiales antes de proceder a la desinfección y esterilización es importante, porque los restos biológicos pueden interferir en los procesos de desinfección y posterior esterilización.


Imagen 47. Cánula de Vama® Imagen 48. Mascarilla laríngea
Las características fundamentales de la desinfección de los materiales hospitalarios, y más concretamente quirúrgicos son:
- Posibilita la destrucción de microorganismos tanto patógenos como residentes, debe emplearse el producto adecuado para el instrumento o material a desinfectar y se de “amplio espectro”, actuar frente a bacterias, virus, levaduras, microorganismos y esporas.
- Se emplea tanto si es necesaria la posterior esterilización (como las mascarillas laríngeas) o no, por ejemplo, las palas de laringoscopio, que precisan estar desinfectados, pero no estériles.
- Que el producto posea propiedades humectantes, tensioactivas, de fácil manejo, pero sin ser corrosivo, alergénico, cancerígeno, toxico por absorción cutánea, ni toxicidad sistémica. Generalmente enzimáticos, proteasas, lipasas o amilasas.
- Debe poder realizarse la desinfección con máquina o a mano, en dilución y aplicación con trapo, bayeta o similar, o en pulverización con spray.
Una vez limpios y en la mayoría de los casos desinfectado, el material se envía a la unidad de esterilización. Para la limpieza del instrumental, se dispondrá en la zona de sucio de la unidad, de fregaderos con agua fría y caliente, pistolas de agua a presión y aire a presión para lavar, soplar y secar los instrumentales huecos. Debido a los riesgos de pinchazos, cortes y lesiones, sólo se limpiará a mano el instrumental delicado que se podría estropear en el lavavajillas, como por ejemplo el de microcirugía.
Para entender los diferentes tipos de limpieza, desinfección y esterilización del instrumental quirúrgico, debemos previamente entender la clasificación del material sanitario. Es en 1968, cuando Earle H. Spaulding, médico norteamericano, realiza el primer estudio racional sobre desinfección según el riesgo de infección en los pacientes derivado del uso del instrumento a desinfectar. No todos los instrumentos que usamos en la clínica deben estar estériles, unos están en contacto con la piel intacta, otros con mucosas, y otros con zonas estériles del cuerpo. De ahí que el uso del instrumento determine el grado de desinfección que requiere:
- Material crítico: aquel que usamos para acceder a zonas o cavidades estériles del organismo (vejiga, venas, arterias, pulmones…): instrumental quirúrgico, pinzas de biopsia endoscópica, etc. Dentro de esta clasificación incluimos también todo el material implantado en el cuerpo: prótesis vasculares, oftalmológicas, material de osteosíntesis o cualquier objeto que deba pasar más de 30 días insertado, como un reservorio. Requiere de una limpieza en profundidad una desinfección de alto nivel y la posterior esterilización (según pautas del fabricante).
- Material semicrítico: el que entra en contacto con piel no intacta o mucosas. Por ejemplo: endoscopios (colonoscopio, gastroscopio, broncoscopio), palas del laringoscopio, etc. Es material que, si bien no necesita esterilización, si requiere de una limpieza a fondo y una desinfección completa y en profundidad (desinfección de nivel medio).
- Material no crítico: el material o instrumental que SOLO entra en contacto con la piel intacta. Por ejemplo: fonendoscopio, aparato de ultrasonidos, termómetro, etc. Para este material debemos realizar una buena limpieza y una desinfección con antisépticos como el alcohol de 70o (desinfección de bajo nivel).
Tipos de desinfección:
- Desinfección de alto nivel: es aquella que consigue la destrucción de microorganismos vivos salvo algunas esporas.
- Desinfección de nivel medio: efectiva frente a formas bacterianas, el Mycobacterium tuberculosis, la mayor parte de los virus y algunos hongos.
- Desinfección de bajo nivel: Destruye gran parte de las bacterias, algunos virus y hongos. No es efectiva frente al Mycobacterium tuberculosis ni frente a esporas.
El inicio de la limpieza del instrumental quirúrgico se realiza con detergentes. En tendemos por detergente al producto químico que disuelto en agua modifica su tensión superficial (tensioactivos), de manera que esa solución se vuelve humectante y emulsionante para poder ejercer la función limpiadora. Existen detergentes aniónicos, compuestos mayoritariamente por sales sódicas compatibles con el uso de hipoclorito, y detergentes catiónicos, principalmente sales de amonio cuaternario, incompatibles con los anteriores.
Es importante leer las instrucciones del fabricante porque muchos detergentes son incompatibles con el desinfectante que vayamos a usar a posteriori. Los detergentes más utilizados son los neutros, con respecto al pH depiel (no válidos para el instrumental); alcalinos, los más utilizados (porque tienen pocas incompatibilidades con los desinfectantes); los detergentes-desinfectantes (se le añaden a la composición agentes desinfectantes compatibles); y enzimáticos, producto de elección en el medio quirúrgico.
Tras la limpieza manual del material pequeño o delicado, por inmersión, soplado, o con agua a presión, separando siempre que sea preciso, las partes desmontables para evitar que queden restos biológicos sin limpiar, o tras la limpieza en termodesinfectadoras (lavavajillas de instrumental) se procederá a su empaquetado para el envío a la central de esterilización.
3. ESTERILIZACIÓN DEL MATERIAL QUIRÚRGICO
Se define la esterilidad como el proceso por el cual se obtiene un producto libre de microorganismos. La esterilidad no se puede comprobar o demostrar de manera absoluta, asi que, en términos probabilísticos un elemento es estéril cuando la probabilidad de que un microorganismo siga presente en dicho elemento, bien activo, bien en forma latente es igual o menor a 1 en 1.000.000, conocido como coeficiente de seguridad de esterilidad 10^-6.
Existen diversos métodos de esterilización tanto físicos, como químicos, y dependiendo del objeto a esterilizar, la utilidad de este, o el ámbito del que hablemos, se empleará uno u otro. Dentro del ámbito de la sanidad, los más empleados son:
- METODOS FISICOS: CALOR Y RADIACIONES IONIZANTES (calor seco y húmedo, radiaciones ionizantes y no ionizantes).
- METODOS QUIMICOS: GASES Y LIQUIDOS (gases como el plasma gas, el oxido de etileno o el formaldehido al 2%; y líquidos, cada vez más en desuso, como el glutaraldehído al 2%).
Para no cometer errores en la elección del empaquetado del instrumental, el tipo de sistema de esterilización que soporta el material o el tiempo que estaremos sin el instrumental, es necesario conocer los conceptos clave de la esterilización y los métodos más habituales en el área quirúrgica.
- METODOS FISICOS: CALOR Y RADIACIONES
- METODOS QUIMICOS: GASES Y LIQUIDOS.
CALOR SECO:
Destruye los microorganismos patógenos por oxidación. Necesita más tiempo y mayor temperatura que la esterilización por calor húmedo por lo que hay muchos materiales que no soportan este sistema. Generalmente se emplea para esterilizar instrumental de vidrio y metal.
Consta generalmente de dos programas, en ambos, el material a esterilizar debe ir envuelto, o empaquetado en contenedores de materiales que soporten altas temperaturas.
- 160oC durante 130 a 160 minutos.
- 190oC durante 45 a 50 minutos.
Monitorización biológica mediante Bacillus subtilis.
Maquina esterilizadora: “Pupinel” o Estufa Pupinel.

Imagen 49. Estufa Pupinel
CALOR HÚMEDO:
El método de esterilización mas empleado en el campo de la sanidad. Es eficaz, eficiente y seguro. El vapor a altas presiones destruye los microorganismos y sus esporas mediante la coagulación de los ácidos nucléicos y proteínas del material genético de las células. No se puede esterilizar mediante calor húmedo materiales como las gomas, el teflón, el polietileno, el polipropileno o instrumental como sistemas ópticos (ópticas de laparoscopia) o instrumental eléctrico o con elementos electrónicos.
Consta de varios programas:
- 121oC y 1,03 bares durante 7 minutos para bolsas de papel mixto y contenedortes de hasta 10 kg.
- 132oC durante 20 minutos para plásticos, látex y gomas resistentes.
- 134oC durante 8 minutos para contenedores y cajas de instrumental de mas de 10kg.
- 134oC durante 18 minutos para instrumental que se sospeche ha estado en contacto con priones. Un prion es una partícula proteica, ni un virus, ni una bacteria, con gran capacidad infectiva en el tejido del SNC (mal de Creutzfeld-Jakob). Ante cualquier duda sobre la esterilización las páginas web de los CDC y de la AORN disponesn de recomendaciones sobre los procedimientos a seguir actualizados.
Monitorización biológica: Geobacillus stearotermophillus.
Maquina esterilizadora: Autoclave.

Imagen 50. Ejemplo de autoclave
RADIACIONES
R. ionizantes:
Las radiaciones ionizantes producen la ionización del ADN de los microorganismos, lo que conduce a la ruptura de cadenas y a la formación de enlaces transversales impidiendo la multiplicación celular. Se produce la esterilización a Tª ambiente, alterando la capacidad de reproducción de los patógenos. Instalación costosa, empleado para esterilizar material de 1 solo uso. El principal parámetro que hay que controlar en un sistema de esterilización por radiación es la dosis de radiación recibida por el producto, que depende de la actividad de la fuente de radiación, el tiempo de exposición y el poder de penetración de la radiación. Las formas vegetativas de los microorganismos, particularmente de los Gram negativos, son las más sensibles a las radiaciones, seguidas de hongos, levaduras, virus y formas esporuladas.
Monitorización biológica mediante tiras de Bacilluspumillus.
Ámbito de aplicación: envases y materiales plásticos, prótesis, productos desechables, suturas, ropa quirúrgica.
Si bien no se emplea este método en centros sanitarios, debido a la complejidad arquitectónica y económica de las instalaciones necesarias para emplear este método, queda añadido a este tema porque la mayoría de instrumental fungible quirúrgico (de un solo uso) se esteriliza en origen con este método.
- RAYOS GAMMA, ALFA y BETA: Destrucción de los microorganismos mediante desintegración del Cobalto 60, la radiación resultante de esa desintegración penetra los envases y esteriliza el material. Al absorber estas radiaciones el agua y otras sustancias se ionizan y generan radicales libres que provocan daños celulares y la muerte del microorganismo.
- ELECTRONES: Fuente de electrones que rompe la cadena de ADN y prodúcela muerte celular.
R. no ionizantes.
Producen excitación electrónica, pero no arrancan electrones a la materia.
- Infrarrojos. Radiación electromagnética con mayor longitud de onda que la luz solar. Alcanza los 180oC. Poco uso en el ámbito sanitario.
- Ultravioleta. Las proteínas y los ácidos Nucleicos absorben la rádiación Ultravioleta produciéndose mutaciones que provocan la muerte del microorganismo. Empleado para desinfección de aire y superficies, poseen poco poder de penetración y pueden provocar quemaduras en piel y ojos. Se utiliza principalmente para reducir la contaminación del aire, del agua y de superficies de zonas de trabajo limpias. Su aplicación a los productos sanitarios se reduce a la descontaminación superficial de productos o dispositivos que van a ser utilizados en zonas limpias de trabajo.
Es un método de esterilización menos eficaz que las radiaciones ionizantes. La acción letal sólo se produce sobre los microorganismos directamente expuestos a la radiación.

Imagen 51. Señal de aviso de zona con radiaciones no ionizantes
Las formas vegetativas de los microorganismos, particularmente de los Gram negativos, son las más sensibles a las radiaciones, seguidas de hongos, levaduras, virus y formas esporuladas.
Monitorización biológica mediante tiras de Bacilluspumillus.
Ámbito de aplicación: envases y materiales plásticos, prótesis, productos desechables, suturas, ropa quirúrgica.
Ventajas:
- Inducen menos alteración que el calor sobre los productos.
- Proceso fácil de controlar.
- Excelente capacidad de penetración en los materiales.
Inconvenientes:
- Requiere instalaciones para radioesterilización y ser realizada por profesionales especializados.
- No aptos para productos con teflón.
- Puede provocar cambios de color y aumento de fragilidad en vidrios y algunos plásticos.

Imagen 52. Señal de peligro ante radiaciones ionizantes
METODOS QUIMICOS. GASES:
Siempre es preferible la esterilización por métodos físicos, más controlables y con menos riesgo de contaminación del istrumental y de riesgos en el manejo. Pero existen en sanidad infinidad de materiales termosensibles. Para su esterilización emplearemos los métodos químicos, los más empleados son el óxido de etileno, el plasma-gas y el formaldehído a baja temperatura.
Oxido de etileno.
La capacidad del OE para esterilizar instrumental termosensible aceleró la fabricación de material de un solo uso (de plástico) para el ámbito sanitario. EL OE debe mezclarse con otros gases como el freón (CFC, en desuso por su gran capacidad de contaminación del medio ambiente), clorofluorocarbonos o, con hidroclorofluorocarbonos o dióxido de carbono.
Necesario emplear empaquetamientos muy porosos par que el OE penetre, el ideal, el papel mixto. Requiere de mucho tiempo de aireación.
Ventajas:
- Alta permeabilidad de los paquetes.
- Facil manejo y operatividad asi como de la mo nitorización de la efectividad.
- Util para numerosos materiales sensibles tanto al calor como a la humedad.
Inconvenientes:
- Requiere mucho tiempo de aireación.
- Muy inflamable.
- Las cámaras de esterilización son de pequeño volumen.
- Es necesario un control de residuos en el material debido a la toxicidad del OE.
- Si el OE está mezclado con Peróxido de hidrógeno (gas-plasma Sterrad 100S®), mezcla muy empleada en los hospitales, la penetrabilidad es baja, por lo que el empaquetamiento no admite papel mixto, sólo tipo Tyvek®, y sirve para esterilizar tela, celulosa ni líquidos.
Formaldehido al 2%:
Destrucción mediante solución de formaldehido con etanol al 3% vaporizada a baja temperatura en cámara de presión negativa. No necesita aireación. Poca penetración y alta acción corrosiva, por lo que poca utilidad en materiales metálicos. En su forma líquida (formalina 35-37%) se emplea, en ocasiones, para la desinfección de material no crítico y superficies, suelos y paredes, además de la función conservadora de tejidos para su envio a anatomía patológica.
Compuesto químico sencillo (CH2O) que se obtiene de la oxidación del metanol. Dos programas o ciclos:
- Ta 50oC durante 5h.
- Ta 60oC durante 3h.
Plasma-gas de peróxido de hidrogeno:
Además de su aplicación en medio líquido, la generación de gas plasma a partir de vapor peróxido de hidrogeno se patentó en 1968 (Menashi, 1968) para la esterilización de soluciones parenterales. En España, empleamos el sistema Sterrad 100S® desde 1997, que posee un ciclo largo para material de endoscopia de unos 74 minutos, otro de 54 minutos y otro de 20-25 minutos. La temperatura oscila entre 45oC y 50-60oC. Se inyecta el peróxido líquido a una cámara de vacío se expone a ondas de radiofrecuencia. No necesita airear.
Monitorización biológica: depende del fabricante.
Acido paracético:
Mezcla del ácido con anticorrosivos para pH 6,4. Oxida enlaces y destruye proteínas.
Para materiales sumergibles a Ta 50 a 56oC como endoscopios u ópticas.
LIQUIDOS
Glutaraldehído:
Se usa al 2% en soluciones alcalinas.
Para esterilización de instrumental. Poco uso porque precisa de 10 h para completar el ciclo de esterilización y la manipulación posterior del material es compleja.
Una vez entendidos los procesos de esterilización veremos el proceso de limpieza grosera del instrumental, su empaquetado y envío a la unidad de esterilización.
Salvo que el centro sea pequeño y no se realicen grandes cirugías, o se trate de poco instrumental, como en el caso del utilizado en la consulta de Cirugía Maxilofacial, por ejemplo, es en la propia unidad donde se disponen de maquinas lavavajillas y selladoras de papel para empaquetar material para su esterilización y máquinas de esteril más pequeñas, adecuadas al uso menos exigente en cuanto volumen de material y su propio tamaño.

Imagen 53. Termodesinfectadora
Si existe la unidad de esterilización, la definiríamos como el servicio encargado de procesar todo el instrumental de las áreas quirúrgicas, y de cualquier otra área que requiera material o instrumental estéril para su funcionamiento.
Recibe, registra, esteriliza y valida el proceso para, posteriormente, reenviarlo a sus unidades de origen. Para que el envío del material sea correcto debemos saber las características generales del proceso de esterilización (sea cual sea). El instrumental debe colocarse en sus contenedores (sean cuales sean) de tal manera que el agente esterilizante penetre a todos los resquicios y su posterior manipulación sea sencilla (fácil apertura del paquete o contenedor una vez esterilizado para su uso en otra cirugía):
- El embalaje debe aislar el material durante todo el proceso, permitir el paso del agente esterilizante y evitar roturas del embalaje (protección de instrumental agudo).
- Elegir el sistema de empaquetado no es en función del tamaño o de la comodidad sin no del método de esterilización a emplear. Debe permitir el sellado y/o precinto, ser permeable al agente, y a la evaporación de la condensación resultante. Es importante diferenciar los sistemas de empaquetado dependiendo del sistema para evitar errores y destrucción del instrumental (muchos materiales no soportan el calor y pierden elasticidad o incluso se derriten).
- Controles: el embalaje debe llevar indicadores visibles y fáciles de interpretar que atestigüen que el proceso se ha completado.
Debemos conocer también, cómo se envía el instrumental a dichas unidades de esterilización.
Contenedores: son cajas de instrumental metálicas, de plásticos resistentes o ABS (termoplástico muy utilizado por su durabilidad cuyo acrónimo deriva de los tres monómeros empleados en su construcción: acrilonitrilo, butadieno y estireno) con tapa perforada, con contenedor perforado, con filtros de un solo uso, o con filtros con duración temporal (generalmente de 1 a 3 meses). Dentro de los mismos, o adheridos al exterior, se introducirá “testigos” que viren de color al completar el ciclo de esterilización:


Imágenes 54 y 55. Tira reactiva para plasmagas y tira reactiva para autoclave.
Imagen 56. Contenedor para instrumental pequeño.
Cajas de instrumental con filtro de duración establecida (generalmente entre 1 y 3 meses) vacía, y con instrumental sucio rociado con detergente enzimático para su envío a la central de esterilización:
Imágenes 57 y 58. Caja de instrumental tras uso.
Imagen 59. Sello inviolable colocado tras esterilización.
Contenedor perforado de sostén de piezas delicadas (Imagen a), requieren ir introducidos en otros contenedores, y en ocasiones, si el contenedor también es perforado, precisan de envoltura en papel de esterilización (Imagen b).
Imágenes 60 y 61. Opticas de endoscopia sin empaquetas y tras empaquetado.
Si las piezas a enviar tienen que ir de manera individual, o son pocas, se procederá a su limpieza y empaquetado, el empaquetado de un solo uso se realiza en:
- Papel grado médico, bolsas de papel. Embalaje de un solo uso, termorresistente y poroso para que penetre el agente esterilizador. Compatible con vapor, óxido de etileno y formaldehido. Prácticamente en desuso por la mala apertura al campo estéril que tiene, hay que rasgarlo o cortarlo con tijeras.
Imágenes 62 y 63. Ejemplo de sobres de papel de grado médico.
- Tejido sin tejer. Se emplea para envoltura de cajas perforadas, o para determinados procesos de esterilización.
Imagen 64. Rollo de papel sin tejer para envoltura y envío a esterilizar.
- Papel mixto. Embalaje de un solo uso, termorresistente, tiene una capa de papel de grado médico porosa por donde penetra el agente esterilizador, y otra de polipropileno transparente. Existen sobres preparados, con un extremo termosellado y el otro pre-engomado para cerrar tras llenado), papeles termo-sellado por un lado, una vez introducido el material a esterilizar, se envía a termosellar el otro extremo, a la unidad de estéril, o se sella en la propia unidad, o se usan cintas de sellado.
Imagen 65. Sobre pre-engomado de papel mixto
Imágenes 66 y 67. Rollos de papel mixto y cinta adhesiva con marcas testigo.
Descripción del papel de grado médico mixto:
Imagen 68. Papel mixto y su descripción.
Conceptos clave del proceso de limpieza / desinfección / esterilización:
- Antes del proceso de desinfección/esterilización, se efectúe en el propio quirófano, o en la unidad de estéril, es necesaria una LIMPIEZA grosera del instrumental, eliminando restos biológicos del paciente, lo antes posible para evitar la corrosión. Dicha limpieza respetará los tiempos de actuación y el % de concentración de los detergentes elegidos.
- Los instrumentos NO deben sumergirse en suero fisiológico al 0,9% porque provoca corrosión y oxidación.
- Lavado a mano del material más delicado y a máquina del resto. PRECAUCION UNIVERSAL.
- Se comprueba que el material esté SECO, con trapos, bayetas que no suelten pelusa, pistolas de aire a presión, etc. antes de empaquetar, en contenedor, papel mixto, o bolsa de papel de grado médico.
- Se anotará en una hoja (con copia al servicio de estéril si existiera):
o Nombre y cantidad del instrumental. Ejemplo: 2 disecciones finas sin dientes.
o Fecha de envío a esterilización.
- Proceso al que va a someterse. Ejemplo: “Se envían 2 óptica de 30oC a plasma gas”. Para evitar destrucción o daño del material por someterlo a sistemas no adecuados como enviar a aesterilizar mediante calor húmedo (autoclave) gomas o plásticos termosensibles. TODO el instrumental enviado portará visible indicador de resultado adecuado para el proceso de la esterilización. Y si ese contenedor, incluyera bolsas con instrumental más pequeño (bolsa para mangos de bisturí y disecciones), otro dentro de ese paquete.
- PROTEGER las puntas del instrumental para que no se estropeen durante el proceso y no atraviesen las envolturas.
- Comprobar que todo el material que se envía dentro de un contenedor es el correcto, está en perfecto estado y seco. Para facilitar la tarea, la unidad dispondrá de leyendas (con foto a poder ser) con todo el instrumental que tiene que incluir el contenedor.
- Ejemplo: Caja de apendicetomía
o 1 mango de bisturí del 23 y 1 del 15.
o 5 disecciones: 2 sin dientes, 2 con dientes y 1 de Bakey.
o 2 Farabeuf.
o 4 mosquitos.
o 6 Crille.
o Etc.
- Cuando el instrumental regresa de la unidad de estéril debe ser visible la fecha de caducidad de la esterilidad. Para que se efectúen revisiones de caducidades programadas dentro de la unidad quirúrgica que eviten errores.
BIBLIOGRAFÍA
- Agra, Y., E. Terol. «La seguridad del paciente: una estrategia del Sistema Nacional de Salud». Anales del Sistema Sanitario de Navarra, vol.29, nº3, diciembre de 2006, pp. 319-23.
- Canales Carmona, Fresia, & Salazar Campos, María de los Ángeles (2013). Efectividad del lavado de manos prequirúrgico con cepillo y sin cepillo. Enfermería Actual en Costa Rica, (25). Accedido 1 de marzo de 2020.
- Serjan, María A., Saraceni, Liliana, Higiene en manos. Revista del Hospital Materno Infantil Ramón Sardá [Internet]. 2005;24(4):158-163. Recuperado de: https://www.redalyc.org/articulo.oa?id=91204104
- Angeles Garay, Ulises et al. «Efectividad de la aplicación de alcohol gel en la higiene de manos de las enfermeras y médicos». Revista de Enfermería del Instituto Mexicano del Seguro Social, vol.13, nº 1, 2005, pp.15-22.
- OMS. «OMS/ Material y documentos sobre la higiene de manos». WHO, http://www.who.int/gpsc/5may/tools/es/? Accedido 3 de marzo de 2020
- Acevedo Díaz, José Antonio, et al. «Un caso de Historia de la Ciencia para aprender Naturaleza de la Ciencia: Semmelweis y la fiebre puerperal». Revista Eureka sobre Enseñanza y Divulgación de las ciencias – 2016, 13(2) – pp. 408-422, abril de 2016. rodin.uca.es, https://rodin.uca.es/xmlui/handle/10498/18297
- Lyons, Albert S., et al. «Historia de la medicina». Ediciones Doyma, 1980.
- Henao, Guillermo. La fiebre puerperal: La lucha de IF Semmelweis en la génesis de un nuevo paradigma. Iatreia, 1999, vol. 12, nº3, p. 149-156.
- A55/13 – Quality of Care: Patient Safety. Report by the Secretariat, World Health Assembly, 2002. https://apps.who.int/medicinedocs/es/m/abstract/Js16002e/. Accedido 1 de marzo de 20202
- Aranaz-Andrés J.M., et al. Los sucesos adversos en los hospitales españoles: resultado del estudio ENEAS. Med. prev, 2007, p. 64-70
- Aranaz-Andrés, Jesús M., et al. «Luces y sombras en la seguridad del paciente: estudio y desarrollo de estrategias. Informe SESPAS 2008». Gaceta Sanitaria, vol. 22, abril de 2008, pp.198-204. ScienceDirect, doi: 10.1016/S0213-9111(08)76093-X
- Vazquez-Espinosa, E. et al. «Evaluación de la calidad de las guías y protocolos de lavado de manos existentes en España». Medicina Clínica, vol.135, julio de 2010, pp. 67-72.DOI.org (Crossref), doi: 10.1016/S0025-7753(10)70023-3.
- Quiroz-Romero, Fernando. «Mascarillas quirúrgicas a propósito del COVID-19: Algunos aspectos técnicos». Revista Colombiana de Cirugía, vol 35. Nº2, abril de 2020, pp. 200-02. DOI.org (Cfrossref), doi: 10.30944/20117582.620.
- «OMS Material y documentos sobre la higiene de manos». WHO, http://www.who.int/gpsc/5may/tools/es/? Accedido 15 de julio de 2020.
- «Mejoramiento de Los Procesos En El Quirófano mediante La Aplicación de La Metodología Lean de Toyota». Revista Colombiana de Anestesiología, vol. 42, nº3, julio de 2014, pp. 220-28. www.sciencedirect.com, doi: 10.1016/j.rca.2014.02.007.
- Hospital de Galdakao Manual de Enfermería Quirúrgica. https://www.google.com/search?client=safari&rls=en&q=hospital+de+galdakao+manual+de+enfermeria+quirurgica&ie=UTF-8&oe=UTF-8. Accedido 1 de diciembre de 2020.
- Grupo de trabajo de la Guía de Práctica Clínica para la Seguridad del Paciente Quirúrgico. Centro Cochrane Iberoamericano, coordinador. Guía de Práctica Clínica para la Seguridad del Paciente Quirúrgico. Plan de Calidad para el Sistema Nacional de Salud del Ministerio de Sanidad, Política Social e Igualdad. Agència d ́Informació, Avaluació i Qualitat en Salut (AIAQS) de Cataluña; 2010. Guías de Práctica Clínica en el SNS: AATRM No 2007/24.
- «Vía clínica de Recuperación Intensificada en Cirugía Abdominal (RICA)». GuíaSalud, https://portal.guiasalud.es/opbe/via-clinica-recupercaion-intensificada-cirugia-abdominal-rica/.
- Haynes AB, Weiser TG, Berry WR, Lipsitz SR, Breizat AH, Dellinger EP, et al. Safe Surgery Saves Lives Study Group. A surgical safety checklist to reduce morbidity and mortality in a global population. N Engl J Med. 2009; 360:491–9. [PubMed] [Google Scholar]
- Arribalzaga, E. B., Lupica, L., Delor, S. M., & Ferraina, P. A. (2012). Implementación del listado de verificación de cirugía segura. Revista argentina de cirugía, 102(1), 8-12.
- ES Yip. Accommodating latex allergy concerns in surgical settings. AORN J 2003;78(4):595-603. En: Mota ANB, Turrini RNT. Periopera- tive latex hypersensitivity reactions: an integrative literature review. Rev. Latino-Am. Enfermagem 2012;20(2):1-10.
- Fuller, Joanna Kotcher, y Joanna Ruth Fuller. Instrumentación quirúrgica/ Surgical Technology: Teoría, técnicas y procedimientos/Principles and Practice. Ed. Médica panamericana, 2007.
