1. CIRCULACIÓN EXTRACORPÓREA
El corazón junto con los pulmones, es el encargado de transportar oxígeno a todas las células del cuerpo, bombea sangre desoxigenada a los pulmones, y de los pulmones al corazón para luego distribuir por todo el cuerpo la sangre oxigenada.
Cualquiera de las múltiples patologías que puede sufrir el músculo cardíaco pueden requerir intervenciones quirúrgicas, gracias al avance de la técnica de acceso endovascular radioguiada, a cargo de radiología intervencionista, muchas de las intervenciones de realizan accediendo desde la arteria femoral, o arteria radial, para llegar hasta la zona del corazón lesionada, lo que genera múltiples beneficios para los pacientes, como por ejemplo, menor tiempo operatorio, ausencia de incisiones, menor tiempo de ingreso hospitalario, del dolor intra y post operatorio.
Pero en ocasiones, algunos procedimientos, requieren de cirugía “a corazón abierto” como, por ejemplo: recambio valvular, bypass coronario, disecciones aórticas, malformaciones del tabique, pericarditis congestiva, etc.
En 1893, el Dr. Ludwig Rehn, cirujano en la ciudad de Frankfurt, fue el primero en suturar con éxito un corazón, el de un paciente de 22 años que había sido apuñalado.
En 1908, Frederic Trendelenburg fue el primero en realizar una embolectomía pulmonar, la realizó en tres pacientes (los tres fallecieron, uno en la intervención, el segundo 15 h después de IC, y el tercero 37 horas después tras una hemorragia de la arteria mamaria izquierda) realizaba una incisión en T sobre la 2ª costilla accedía a través de la pleura al pericardio y una vez abierto exponía la aorta y el tronco de a pulmonar. Extraía los coágulos con pinza y aspiración y suturaba. Esto es lo que se conocería como operación de Trendelenburg. Posteriormente, en los años 30-40 comenzó el tratamiento de las cardiopatías congénitas, fundamentalmente el cierre de ductus y la coartación de aorta.
El desarrollo posterior de la circulación extracorpórea y medidas de protección cardiaca, el descubrimiento de la heparina, y el avance en las técnicas quirúrgicas, han permitido llegar a la cirugía cardiaca moderna. Entender el funcionamiento de la Bomba de circulación extracorpórea es básico para la enfermera quirúrgica, si bien su manejo y control recae sobre la perfusionista, entender el proceso hará que la colaboración interpersonal del equipo mejore la calidad asistencial:
- Perfusionista.
Las bombas de CEC son manejadas por la figura de la perfusionista, profesionales diplomados en enfermería cuyo trabajo consiste en: “Proporcionar los cuidados asistenciales necesarios, para mantener y controlar una adecuada circulación de la sangre, en aquellos pacientes intervenidos quirúrgicamente de lesiones cardio circulatorias, y en los cuales es necesario sustituir la función cardiaca y pulmonar, así como la puesta en marcha, el mantenimiento y el control de las técnicas de circulación artificial, derivadas de un procedimiento médico quirúrgico, que requiere circulación extracorpórea (CEC)” (Manual de Calidad en Perfusión. Asociación Española de Perfusionistas).
Se convertirán en percusionistas aquellas profesionales que hayan superado: el programa de estudios acreditado por la AEP, que posean el Certificado Europeo de Perfusión Cardiovascular (BOARD), el Curso de Posgrado en “Técnicas de Perfusión y Oxigenación Extracorpórea “acreditado por la Universidad de Barcelona, la Asociación Española de Perfusionistas, la Sociedad española de Cirugía Cardiovascular y The European Board of Cardiovascular Perfusion.
- Bomba de circulación extracorpórea.
Los pacientes que van a ser intervenidos bajo CEC requieren ser sometidos a monitorización invasiva de la presión arterial (generalmente a través de la canalización de la arteria radial) y a la monitorización del GC a través de sistema PiCCO®, así como la monitorización de la presión de la aurícula derecha.
El sistema PiCCO® es un método de monitorización hemodinámica, capaz de medir el GC por termodilución transpulmonar, estimar la precarga por medio del volumen sanguíneo intratorácico, el agua extravascular, el índice de función cardiaca y la variación del volumen sistólico. Este método requiere un catéter venoso central convencional (yugular, subclavia o femoral) al que se conecta externamente un sensor capaz de medir la temperatura de la solución inyectada, y un catéter arterial (femoral, axilar o radial), el cual además de permitir la medición de la presión arterial, posee un sensor de temperatura en su extremo distal. Este método alternativo de monitorización hemodinámica invasiva del gasto cardíaco tiene tanta validez como el obtenido por el catéter de Swan-Ganz (para ello se emplea el sensor ProAQT®).

Imagen 2. PiCCO® Pulsion.
Una vez realizada la apertura del tórax mediante esternotomía media, básicamente la técnica del bypass cardiopulmonar, consiste en la canulación de las venas cavas superior e inferior junto a la aurícula derecha, y de la aorta ascendente o la arteria femoral.
La sangre venosa procedente de las cavas entra por el circuito de CEC, donde es movilizada y propulsada por la bomba de rodillos, peristáltica o centrífuga, para pasar a través de un intercambiador térmico que permita inducir la hipotermia (y calentar la sangre antes de salir de CEC) y posteriormente, ese flujo de sangre venosa pasa por un oxigenador de membrana o de burbuja, que posee un “filtro de aire” que evita el paso de burbujas antes de entrar al paciente por la cánula situada en la aorta.
La CEC requiere que el paciente esté anti coagulado con heparina, proceso que será revertido con protamina. Una vez que el paciente entra en CEC, generalmente se infunde una solución cardioplégica por la raíz aórtica o directamente sobre las arterias coronarias (seno coronario).
o Cardioplegia:
La Cardioplegia es una solución para perfusión intracardiaca, que se utiliza combinada con la isquemia, para inducir la parada cardíaca durante la cirugía con CEC.
El objetivo principal es la ralentización de la velocidad de la reacciones celulares, con lo que se retrasa el desgaste de la energía y otros procesos perjudiciales para el miocardio durante la isquemia cardiaca (también evita el edema intracelular mediante la adicción de elementos hiperosmolares como el Manitol®), la hipotermia (cada vez se tiende a emplear cardioplegias menos frías) y la administración de sustancias energéticas para cubrir las necesidades metabólicas del miocardio durante el clampaje aórtico (generalmente glucosa). La Cardioplegia puede tener dos composiciones, cristaloides y sanguínea.
- Cardioplegia sanguínea es la que se utiliza con mayor frecuencia en la cirugía cardiaca de adultos, se produce al mezclar sangre con cristaloideas en una proporción determinada, debido a la hemoglobina, esta solución puede administrarse fría o caliente.
A esta solución se le añaden infinitos aditivos y variaciones de la misma para combatir los daños tisulares provocados por la isquemia-reperfusión (HCO3, K+, Na+, glucosa, magnesio, calcio...). El pH y la osmolaridad de la Cardioplegia también es muy importante para limitar el edema del miocardio que puede ser perjudicial para la recuperación ventricular.
- Cardioplegia fría: genera un ahorro de energía por la detención diastólica inducida químicamente y por la hipotermia añadida, que reduce la demanda de oxígeno del miocardio en casi un 95 % por lo que también se reduce la degeneración de las reacciones celulares durante la isquemia.
- Cardioplegia caliente: la Cardioplegia caliente si bien, se puede usar antes del inicio de la isquemia como inducción cálida, no puede realizarse toda la operación con Cardioplegia caliente.
El miocardio se mantiene la temperatura caliente, es decir la actividad metabólica continúa (en menor grado porque se suprime la actividad mecánica del corazón) por lo que los requerimientos de O2. Sin embargo, la Cardioplegia tibia, administrada generalmente a 29 °C, proporciona algunos de los beneficios de la Cardioplegia caliente mientras que minimiza los efectos de la hipotermia en el miocardio.
- Cardioplegia cristaloide: es la más empleada para la conservación del corazón del donante durante el trasplante cardíaco (Celsior®). Esta solución no contiene hemoglobina, por lo que liberan solamente oxígeno disuelto, suficiente para mantener la oxigenación miocárdica a temperaturas frías, por lo que la Cardioplegia cristaloide se puede usar solo en el contexto de hipotermia miocárdica.
- Cardioplegia anterógrada: se administra a través de una cánula que se inserta en la raíz aórtica salvo en el caso de insuficiencia valvular aórtica. Se administra a un flujo y presión determinados para conseguir la distribución homogénea.
- Cardioplegia retrógrada: se emplea como ruta primaria de protección del miocardio o como un complemento a la cardioplegia anterógrada, se administra a través de las venas coronarias (seno coronario) se realiza un pequeño orificio en la aurícula derecha y se introduce una cánula que se dirige al seno coronario. Se administra a una presión menor de 40 mm H.G. porque una presión más alta o una colocación incorrecta del catéter puede lesionar el seno coronario. La principal ventaja de la administración de cardioplegia retrógrada es la realización de procedimientos valvulares.
- Máquinas o bombas de circulación extracorpórea:
Las bombas están formadas por unidades modulares integradas, cada módulo tiene un motor eléctrico acoplado a un cabezal regulable conformado por dos rodillos metálicos, que giran contra una “pista”, por donde se instala un tubo colapsable por el que circula la sangre. Cada giro del cabezal desplaza un volumen de sangre que, al multiplicarlo por el número de vueltas, permite determinar el flujo generado por la BCE. La calidad mecánica de la BCE influye en la facilidad y la persistencia de la regulación efectuada. En los equipos disponibles en la actualidad, con sensores, se puede observar en pantalla el volumen eyectado expresado en litros por minuto. La función de oxigenación la realiza un componente que contiene un reservorio para la sangre y una membrana artificial plegada, micro porosa, con la superficie equivalente al pulmón, de aproximadamente 1.8 m2. El equipo posee, además, un orificio para entrada y salida de gases (aire comprimido y oxígeno) y un sistema de batería propia por si hubiera un fallo en la red eléctrica, y con rotadores manuales, para accionar los rodillos en caso de emergencia. Poseen:
-. Un monitor donde se pueden observar las alarmas de las que dispone: detección de burbujas en el circuito y de nivel, así como, la temperatura, la presión, cronómetros, e indicadores del funcionamiento de cada rodillo. A su vez estos datos quedan registrados y grabados para poder exportarlos a una base de datos.
-. Sistemas de gases: las bombas de CEC deben disponer de mangueras o tubuladuras con conexiones al sistema de aire y oxigeno de los quirófanos, mezcladores, vaporizadores y flujómetros. Todas las tubuladuras y conexiones de aire y oxígeno deberán ir identificadas con colores diferentes y no intercambiables. Aún así, como medida de seguridad deberá existir en la unidad quirúrgica balas de oxígeno y aire ante un fallo del sistema de gases del hospital.
-. Sistema de medición del tiempo de coagulación activada (Hemochrom®). El paciente esta “heparinizado” para garantizar la inhibición del proceso de coagulación de la HepNa y minimizar el riesgo de coagulación intravascular diseminada este tiempo de coagulación activada deberá mantenerse >400 segundos.
-. Intercambiador de temperatura: sistemas que permiten bajar la temperatura y posteriormente “calentar” al paciente para recuperar Normotermia. Esto se consigue al pasar la sangre por un circuito lleno de agua que calienta o enfría la sangre a su paso.
-. Sistemas de seguridad:
- Filtro en la línea arterial. Tras la salida del oxigenador, para proporcionar protección frente a embolismos
- Alarma de Presión de la línea. Tanto en la línea arterial como en la cardioplegia, audibles y visibles.
- Detector de nivel bajo. Que avisa de que el nivel de sangre en el reservorio es bajo y detiene el cabezal arterial de la bomba para evitar embolismos.
- Detector de burbujas.
- Monitorización de presión transmembrana. Que mide la presión de entrada de la sangre al oxigenador y la de salida. El gradiente de ambas delata el buen funcionamiento del oxigenador.
- Válvula unidireccional en el aspirador Vent. Asegura que la presión de aspiración es correcta y constante.

Imagen 3. Cánula de CEC arterial.
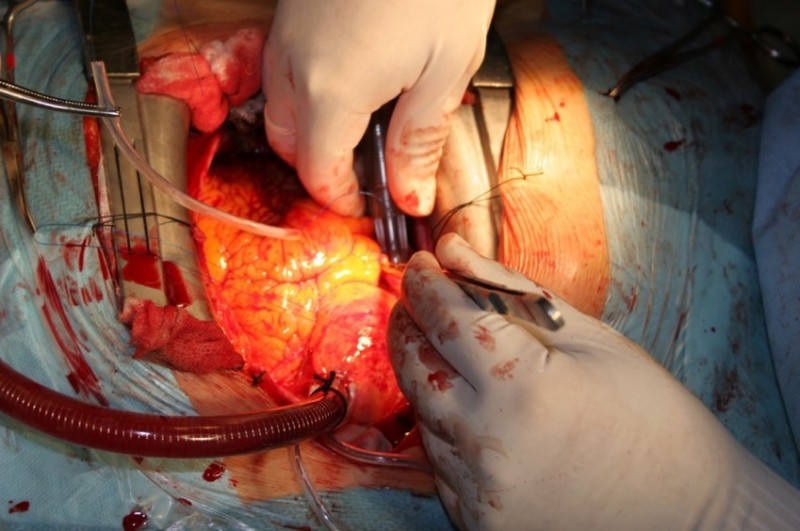
Imagen 4. Inserción de cánula venosa.

Imagen 4 bis. Inserción cánula en Arteria femoral.
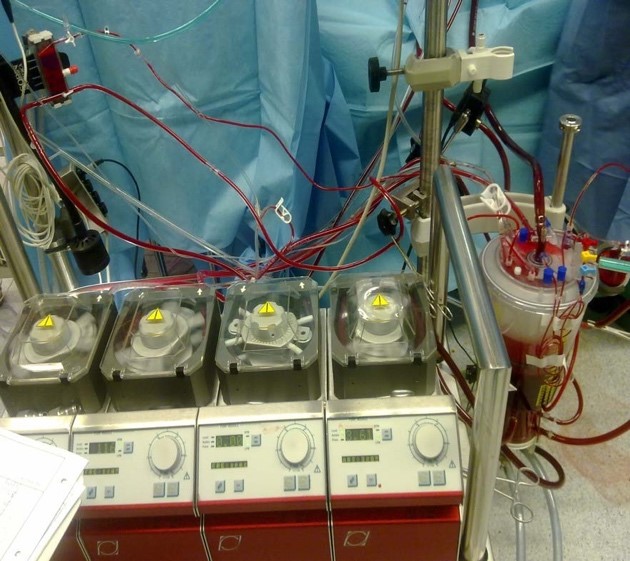
Imagen 5. Rodillos de bomba de CEC.
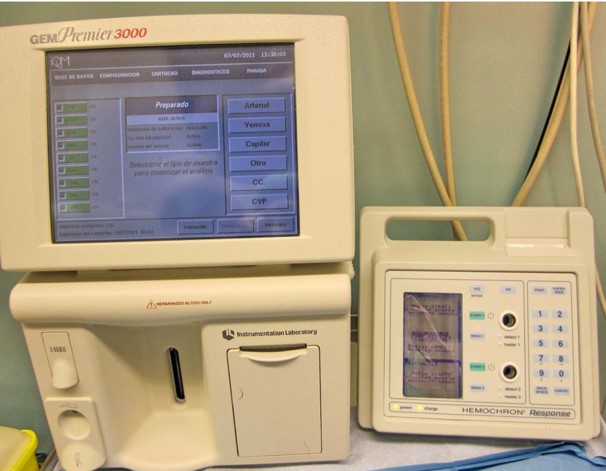
Imagen 6. Hemochrom®.

Imagen 7. Cardioplegia anterógrada y retrógrada.
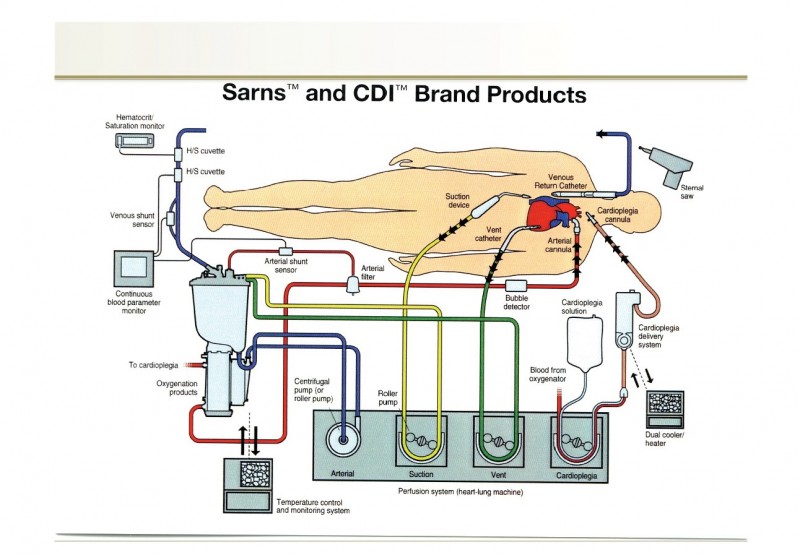
Imagen 8. Esquema de funcionamiento de bomba de CEC.
2. ENTRADA EN CEC CON ESTERNOTOMÍA MEDIA
La cirugía que requiere circulación extracorpórea y que es a corazón abierto mediante esternotomía media tiene un protocolo de apertura disección preparación de la canulación y la canulación común a todas ellas, para no repetirlo en todas y cada una de las intervenciones queda recogida en este apartado:
- Apertura de piel mediante incisión con bisturí frío.
- Disección y bisturí eléctrico para control de hemostasia y avance por planos hasta el esternón.
- Mientras eso ocurre, la perfusionista facilita el circuito arteriovenoso (CC) re circulado con suero a la instrumentista, esta lámpara el tubo arterial y el tubo venoso a 2 cm de la conexión y corta mediante una tijera fuerte.
- Apertura del esternón mediante sierra eléctrica de esternotomía.
- Colocación del separador esternal con valvas.
- Apertura del pericardio con bisturí eléctrico y tracción del mismo con puntos de seda generalmente del cero.
- La instrumentista facilita la sutura para que el cirujano realice la bolsa de tabaco en aorta. Generalmente tipo Ethibond 2/0, pasa hilos Rummel (dos suturas).
- Bolsa de tabaco en Cava superior. Mismo proceder.
- Bolsa de tabaco para la retroplegia, la instrumentista facilita Prolene de 3/0 de aguja grande con teflón, pasa hilos Rummel y mosquitos para marcar la sutura.
- Bolsa de tabaco para la cardioplegia anterógrada.
- Y bolsa de tabaco para la espirador Vent en aurícula izquierda (Prolene de 4/0 apoyado con teflón).
- Canulación:
o Aorta: con las bolsas de tabaco ya realizadas, se humedece la cánula y se facilita al cirujano bisturí, generalmente del número 11, con pinza de Back y Creel o tijera, en el momento en el que el cirujano introduce la cánula se le facilita clamp de tubo. El reflujo de sangre arterial en la aorta es muy potente por eso hay que campar la cánula para no perder sangre. Seda del 6 y Rochester Pean para fijar la cánula del campo. Conectar circuito arterial de la bomba de CEC.
o Cava superior: mismo procedimiento que en la aorta, pero el bisturí es del número 12 y se facilita la tubuladura venosa.
o Cardioplegia anterógrada: inserción en la raíz aórtica de la aguja de Cardioplegia anterógrada, a través del ostium coronario. Fijación con seda del 6. Conexión a la línea de infusión previamente purgada. A través de esta cánula introducimos la cardioplegia tanto por la rama de la arteria coronaria izquierda como por la derecha.
o Cánula de retroplegia: con bisturí del 11 se hace la incisión en el seno coronario, se introduce la cánula se fija con seda del número seis y se facilita una conexión en Y (para conectar cardioplegia anterógrada y retrograda) y una alargadera M-M para medir las presiones. El objetivo de esta cánula es la introducción de la cardioplegia en sentido contrario, desde el seno coronario hasta los ostium coronarios, cuya finalidad, como ya hemos comentado, es la protección miocárdica.
o Aspirador Vent, que aspira las cavidades izquierdas a través de una cánula en la vena pulmonar, que extrae la sangre procedente de las arterias bronquiales, que podría dilatar el corazón o bloquear la visión del cirujano. Facilitar bisturí nº 11, crile, clamp de tubo, seda del 6 para fijación y se conecta a la goma de aspiración. Su finalidad es la aspiración de las cavidades izquierdas
- Una vez colocadas las cánulas y el aspirador de ventosas, se coloca el clamp de aorta ascendente para ocluir el ingreso de sangre en las arterias coronarias y se procede a inyectar la cardioplegia. Una vez terminada la intervención, el clamp aórtico se retira mientras el organismo está perfundido por la bomba de CEC, con el corazón y los pulmones detenidos. Al ingresar sangre a las coronarias, el corazón empieza a latir o a presentar FV; en caso de esta última, se procede a la desfibrilación eléctrica con las palas internas en la superficie cardíaca. El corazón todavía está asistido por la CEC en su función contráctil. Cuando todos los parámetros vitales tengan valores correctos, el perfusionista disminuye el caudal de la CEC; si el corazón mantiene la circulación y la saturación sin problemas, se detiene la BCE. Se calcula la cantidad de heparina circulante y se inicia la infusión de protamina para su inactivación.
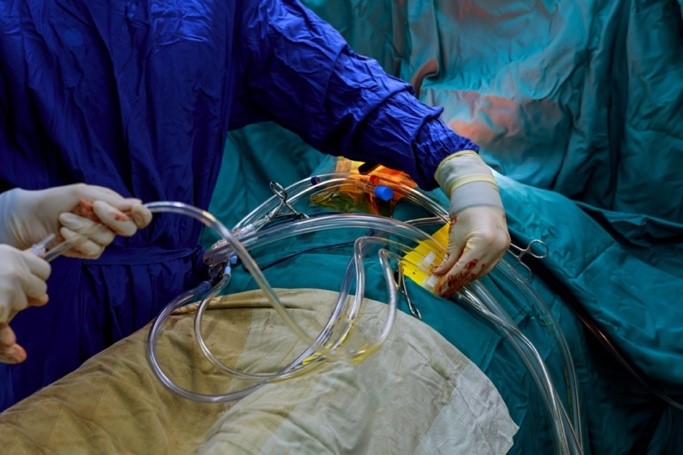
Imagen 9. Instrumentista fijando al campo con velcros las tubuladuras de la CEC.
A continuación, detallaremos algunas de las cirugías más habituales en una unidad de cirugía cardiotorácica: un bypass de las arterias coronarias bajo circulación extracorpórea, un recambio valvular aórtico tipo Bentall y David, y un coronario sin bomba.
Las intervenciones a realizar son decenas, y sería imposible y contraproducente representarlas todas en este módulo, entendiendo la base anatómica, la fisiología del sistema cardiocirculatorio, el funcionamiento de la circulación extracorpórea y las intervenciones más habituales con su preparación anestésica, los materiales y la técnica quirúrgica se adquiere la base necesaria para comprender una unidad quirúrgica tan especial como la cirugía cardiotorácica.
3. BYPASS CORONARIO EN CEC

Imagen 10. Bypass coronario bajo CEC.
La cirugía de bypass coronario es una de las más habituales en cirugía cardiaca, cuando existe una obstrucción de las arterias y venas coronarias que requieren tratamiento quirúrgico la solución radica en la revascularización del lecho miocárdico, bien mediante endarterectomía de la placa de ateroma (radiología intervencionista, acceso endovascular por arteriografía) o revascularización mediante bypass con injerto.
Las arterias mamarias internas son la primera lección para la realización de dichos injertos, cuando no es posible se tiende a emplear las venas safenas, o la arteria radial.
- Preparación del paciente: en ayunas, con todos los CI firmados y con el protocolo pre quirúrgico del centro hospitalario realizado (ducha con clorhexidina al día anterior, rasurado de todo el cuerpo, retirada de objetos metálicos, etc.). Si el quirófano de cirugía cardiaca dispone de una sala de preanestesia, se canalizan dos vías periféricas de gran calibre y se conectan a equipo de cinco llaves de tres vías más alargadera a un suero, generalmente Ringer lactato, para mantener vía.
Pasa a quirófano para anestesia general. La postura del paciente será en decúbito supino con los brazos pegados al cuerpo. Si se sospecha que el injerto de mamaria no va a ser factible, se dejan preparadas ambas piernas con sendos campos quirúrgicos para extracción de vena safena.
- Anestesia: si bien la anestesia es general, con intubación orotraqueal, tanto la medicación como las bobas de infusión continua, las concentraciones y diluciones variarán en función del anestesista responsable, el estado del paciente e incluso, los protocolos de la unidad, pondremos a continuación un ejemplo que sirva como guía, de las medicaciones, vías y bombas de perfusión más habituales en las cirugías bajo CEC:
o Adrenalina: 1 amp. y 9 cc de suero en jeringa de 10 cc.
o Atropina: 1 amp.
o Cloruro cálcico: 1 amp
o Lidocaína 1%. 1 amp.
o Fenilefrina: 1 amp. en 10 cc de suero para concentración 100 mg/ml
- De esa dilución: cargar una jeringa de 10 cc (sigue siendo 100 mg/ml)
-. Cargar 1 cc de la dilución de 100 mg/ml con 9 cc de suero fisiológico para dilución de 10 mg/ml.
o Drogas de anestesia (hipnosis, analgesia y relajación muscular):
-. Etomidato 1 amp.
-. Midazolam: 10 mg. (1 mg/ml).
-. Fentanest: 3 ampollas.
-. Anectine: 1 amp.
-. Cisatracurio (Nimbex® 5 mg/ml) 2 amp en inducción y en bomba de infusión en una concentración: 5 ampollas (50 mg) en 100 cc de suero fisiológico (extraer el volumen de la dosis del medicamento antes de introducirlo en los 100 ml de suero fisiológico para mantener concentraciones).
o Medicación en bomba de infusión continua (jeringa o tipo Braun®):
-. Noradrenalina: 20 mg en 10 cc de suero fisiológico.
-. Dobutamina: 400 mg. en 100 cc de suero fisiológico.
-. Solinitrina 50 mg (5 amp) en 100 cc de suero fisiológico. (extraer volumen para mantener concentración).
o Monitorización de presiones centrales y sus transductores:
-. Las vías centrales, el aparataje para su monitorización y la cantidad de vías centrales varía mucho dependiendo de los centros, pero generalmente en las intervenciones de cirugía cardiaca se monitoriza la presión en la aurícula derecha, la presión venosa central y la presión arterial central. Se pueden canalizar la arteria radial y/o la femoral, una vía yugular interna.
o Antibióticos: si es cirugía coronaria: puede emplearse curoxima (1,5 gr) y si es valvular, vancomicina (1 gr).
o Heparina Na para la CEC y protamina para la salida de CEC.
o Sueros:
-. Salinos, Ringer lactato y los necesarios para los equipos de monitorización de presiones.
- Materiales e instrumental: equipo de ropa para cirugía cardiaca.
o Caja de instrumental para cirugía cardiaca.
o Caja de instrumental de coronaria.
o Caja de instrumental para disección de mamaria
o Separador de mamaria.
o Caja de instrumental de disección de vena (si el injerto es de arteria radial).
o Medidores de flujo con sondas (nº 2, 3).
o Desfibrilador con cable y palas externas e internas.
o Pila de marcapasos.
o Ioban®
o Campo 3M para piernas, paño grande en forma de sábana y 4 paños pequeños. Para preparar los campos de las safenas.
o Equipo de varias cápsulas con jarra.
o Hemoclips pequeños y medianos.
o Bulldogs grises (2 o 3) y blancos.
o Bisturí Deaver.
o Bisturí oftalmológico o cuchillete.
o Protectores de mosquitos, cera de hueso, surgicel, cintas de nilón, teflón, y vessel-loop de varios calibres.
o Electrodos bipolares y monopolares con cables de marcapasos.
o Bisturí es eléctricos (dos) + varias lijas.
o Goma de aspirador + terminal tipo yankauer, dos gruesos y uno fino.
o Material estéril del recuperador de sangre y el recuperador de sangre.
o Solución preservadora de endotelio tipo DuraGraft® (seguir las instrucciones de dilución).
o Gasas y compresas.
- Técnica quirúrgica: tras la anestesia del paciente y la realización de la primera ecografía transesofágica (la sonda transesofágica queda en el esófago del paciente para controles ecográficos a lo largo de la cirugía, siempre que sea necesario), se inicia la intervención.
Una vez preparado campo quirúrgico que abarca todo el tórax desde clavículas hasta unos 10 cm por debajo de apófisis xifoides, se procede a la incisión con bisturí frío, hemostasia con bisturí eléctrico has hasta llegar al periostio esternal, se reseca con eléctrico y periostótomo. La instrumentista facilita la Sierra de esternotomía y se abre el tórax. Hemostasia del esternón incluyendo cera de hueso se colocan compresas húmedas a ambos lados del esternón y se colocan las palas del retractor o separador esternal.
Los cirujanos disecan toda la zona por planos hasta llegar al pericardio, la instrumentista facilita puntos de pericardio, se abre pericardio y se pasan puntos a su través, de tal manera que quede expuesto el campo.
Si el injerto arterial elegido ha sido la arteria mamaria izquierda (AMI), existen dos maneras de anastomosar, una, empleando la AMI como injerto in situ (se conserva el origen de la arteria subclavia), como injerto libre (no se respeta su origen en la arteria subclavia y se anastomosa proximal mente a la Aorta ascendente) o, una tercera opción, anastomosada en T o en Y a la AMD para constituir un injerto compuesto cuando por ejemplo, se precisa revascularizar todo el territorio coronario izquierdo con dos arterias mamarias izquierdas.
El cirujano diseca la AMI de la pared torácica y procede a su anastomosis de la manera elegida antes de entrar en CEC, de tal manera que se reduce el tiempo que el paciente pasa en CEC.
Entrada en CEC y comienzan a hacer el bypass, voltean el corazón con el Janke-Barron, emplean bisturí de ojos, Deaver y Pott para preparar el lecho de la anastomosis. Tras anastomosar todos los puentes, el cirujano comprueba el flujo de las arterias con los medidores de flujo, revisión de hemostasia, salida de bomba, colocación de electrodos de marcapasos, drenajes de Blake y cierre de esternotomía y piel.
*Si para el bypass se emplea la vena safena, hay que recordar que se coloca “al revés” en cuanto a direccionalidad de flujo, para que las válvulas no interfieran, y se anastomosa directamente a la aorta.

Imagen 11. Retractor esternal.

Imagen 12 Mesa de instrumental para coronario bajo CEC.
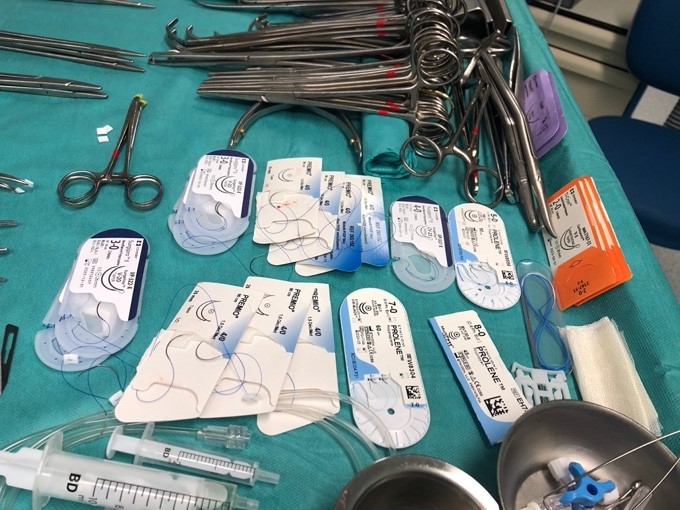
Imagen 13. Detalle de mesa de instrumental: suturas para coronario.


Imagen 14. Malla de volteo cardiaca tipo Janke-Barron. / Imagen 15. Separador de mamaria.

Imagen 16. Hemoclip pequeño Ligaclip®MCA Multiple Clip Applier. (extraída del catálogo online de ©2020 Johnson & Johnson Medical Devices & Diagnostics Group – Latin America, L.L.C.. Disponible en: https://www.ethicon.com/latam/es/epc/code/msm20?lang=es-default.
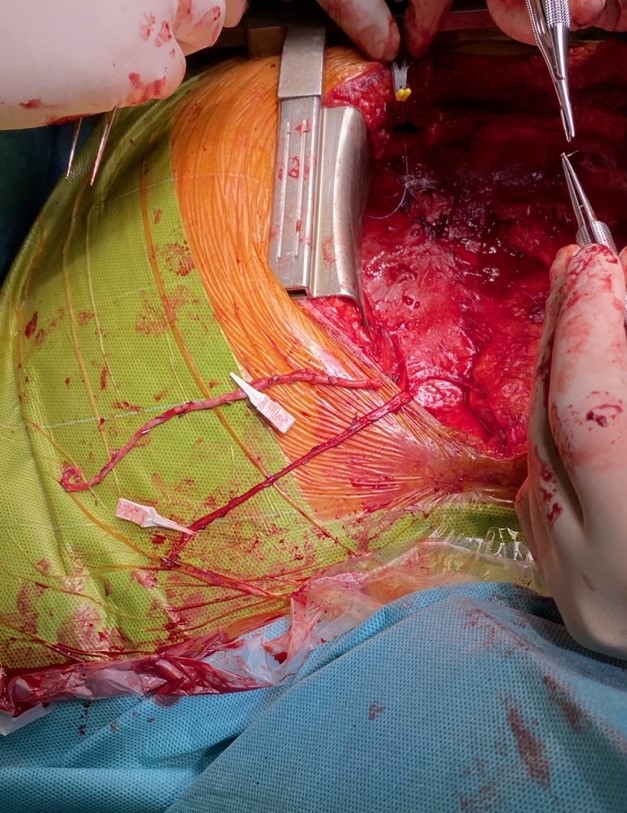
Imagen 17. Suturas marcadas con Bulldogs blancos para anastomosis.

Imagen 18. Ejemplo de caja de coronarias.
4. DISECCIÓN AÓRTICA SIN RECAMBIO VALVULAR (DAVID) Y CON RECAMBIO VALVULAR (BENTALL) BAJO CEC.
La válvula aórtica es una válvula tricúspide, es la encargada de que la sangre oxigenada fluya del corazón hacia la Orta e impide que esa sangre retroceda hacia la cámara cardíaca cuando el ventrículo izquierdo está en diástole. Múltiples patologías pueden requerir un recambio valvular, una válvula aórtica bicúspide, una estenosis, una dilatación de la raíz aórtica, un prolapso de velos, una regurgitación, etc.
La patología valvular puede requerir una reparación valvular, es decir, una comisurotomía o una Valvuloplastia, pero si lo que precisa es el recambio valvular tenemos existen dos tipos de válvulas:
- Válvulas mecánicas, fabricadas generalmente en plástico, carbono o metal. Éstas son resistentes y duraderas, pero en contrapartida, la sangre se adhiere, tiende a adherirse a las válvulas mecánicas por lo que los pacientes deberán ser anticoagulados de por vida.
- Válvulas biológicas, éstas pueden ser de tejido humano (aló injerto de corazón humano de donante), o de tejido Animal (seno injerto). Los pacientes portadores de válvulas biológicas no siempre requieren de anticoagulación, pero en contrapartida requieren un recambio aproximadamente, cada 10 años.
Existen gran variedad de técnicas quirúrgicas de válvula aórtica cada una de ellas con una indicación específica, en general si el paciente tiene un anillo aórtico
- Plastia valvular.
- Intervención de Ross o de Ross-Konno.
o Reemplazo valvular con prótesis mecánica.
Si, por el contrario, el diámetro del anillo aórtico es >19-21 mm, las técnicas son:
o Plastia valvular.
o Intervención de David.
o Intervención de Bentall.
o Reemplazo valvular con prótesis mecánica o biológica.
A continuación, detallaremos las técnicas de Bentall Y David, dos de las más habituales en patología aórtica que requiere de tratamiento quirúrgico.
La preparación del quirófano, del paciente y la anestesia, así como los materiales e instrumental, son muy similares, por lo que hasta la técnica quirúrgica no haremos diferenciaciones.
La diferencia entre David (o Yacoub o David II) y Bentall radica en que en la técnica de David la prótesis de Dacron no es valvular, es decir, el paciente mantiene su propia V.A. Mientras que en la técnica de Bentall, el conducto protésico si es valvulado, es decir, el paciente no conserva su V.A.
- Preparación del paciente: paciente en ayunas, con tórax y abdomen rasurado. En la preanestesia de la unidad se canalizan dos vías venosas de gran calibre (Abocath® 16 o 14) en ambas EESS. Y se coloca suero tipo Ringer Lactato con cinco o seis llaves de tres vía y alargadera.
El paciente se coloca en decúbito supino con los brazos pegados al cuerpo ya que el cirujano principal (lado izquierdo) y el ayudante (lado derecho) se colocan a la altura del tórax, uno a cada lado. La instrumentista dispone de dos mesas de instrumental, ella se colocará a la derecha del ayudante, en el lado derecho, e introduce la mesa de instrumental sobre las piernas del paciente, y la segunda mesa justo a continuación.
- Anestesia: general con intubación orotraqueal.
o Ver apartado de anestesia del punto 2.2.
o Equipo de sondaje vesical.
o Mesas preparadas para canalización de vías venosas centrales y arteriales con sensores de monitorización de presión (suero de 500 blando, equipo de PVC y camisa de presión).
- Materiales e instrumental. Equipo de paños de cirugía cardiaca.
o Caja de instrumental de cirugía cardiaca.
o Caja de instrumental de coronarias.
o Sierra de esternotomía y batería (pila).
o Caja de cirugía de mitral.
o Si precisa: medidores de aorta (depende de la casa comercial), pinza para retirar placas de calcio valvulares (Loop o de disco) y equipo de CO2.
o La perfusionista: facilitará las tubuladuras de la bomba de CEC y las cánulas elegidas una vez esté la cirugía en marcha.
o Prótesis de Dacron:
- Si técnica de David, el conducto de Dacron es diferente si la válvula aórtica del paciente es bicúspide o tricúspide).
o Palas internas de desfibrilador con cable conector al desfibrilador.
o Pila de marcapasos. Electrodos bipolares y monopolares + cable de marcapasos.
o Equipo del aspirador-recuperador de sangre.
o Bisturí eléctrico y punta larga. Lijas
o Goma de aspirador + terminal Yankauer grueso y fino (varios).
o Equipo de suero. (para recortar y fabricar las vainas del estilete Rummel pasa hilos).
o Ioban.
o Hoja de bisturí frío del 23 (3), 11 (3)y 12(1).
o Equipo de varias cápsulas.
o Hemoclips de varios tamaños.
o Cintas de nylon, cera de hueso, surgicel y teflón.
o Alforjas.
o Jeringas de 20 cc y agujas I.M. y de carga (rosa y verde).
o 2 drenajes tipo Blake® con conexión en Y para conectarlos al Pleur-evac®.
o Suturas más empleadas (varían según preferencias del cirujano):
- Ligadura seda 6 (4).
- Seda 0 triangular (6).
- Seda 2/0 triangular (6).
- Prolene 3/0 aguja grande (6).
- Prolene 4/0 aguja grande (6).
- Prolene 4/0 aguja pequeña (2).
- Prolene 5/0 (1).
- Ti-cron 2/0 aguja grande para sutura valvular.
- Polisorb 0 triangular (2).
- Sutura metálica de esternón (2).
- Grapas para cierre de piel.
- Apósitos.
- Técnica quirúrgica: tras la reparación del campo quirúrgico que abarca todo el tórax desde clavículas hasta unos 10 cm por debajo de apófisis xifoides, se procede a la incisión con bisturí frío, hemostasia con bisturí eléctrico has hasta llegar al periostio esternal, se reseca con eléctrico y periostótomo. La instrumentista facilita la Sierra de esternotomía y se abre el tórax. Hemostasia del esternón incluyendo cera de hueso se colocan compresas húmedas a ambos lados del esternón y se colocan las palas del retractor esternal.
Los cirujanos disecan toda la zona por planos hasta llegar al pericardio, la instrumentista facilita puntos de pericardio, se abre pericardio y se pasan puntos a su través, de tal manera que quede expuesto el campo. Se expone el campo quirúrgico, es decir el corazón y los grandes vasos, donde prepararán las zonas de canulación.
o Si el reemplazo de la aorta ascendente (AA) afecta a la válvula y al osteum coronario será la técnica de Bentall:
La canulación para entrar en CEC se realiza en la aorta si la disección no es muy amplia, si, por el contrario, la AA está disecada hacia muy arriba, se cánula la femoral, por lo que, en la preparación del campo quirúrgico, se ha añadido el campo de la femoral para la canulación. En ocasiones, incluso, se prepara un campo quirúrgico en las carótidas (perfusión cerebral).
El proceso de canulación de la femoral sigue los pasos de cualquier cirugía general, disección por planos, control de la hemostasia y exposición de la arteria femoral.
El cirujano hace una resección alta de aorta ascendente (ortotomía), con tijeras, generalmente de Metzembaun, disecciones, etc. Realiza la medición de la raíz aórtica con los medidores específicos para el tipo de conducto de Dacron valvular a implantar, y selecciona el tamaño adecuado (prueba y definitivo). Las coronarias se desinsertan para su posterior anastomosis sobre la prótesis de Dacron (parada cardiaca mediante hipotermia profunda).
Si la válvula es biológica, la instrumentista procede al LAVADO de la misma con suero fisiológico (varios lavados en cápsula con recambio del suero fisiológico). Se colocan los organizadores de suturas y se comienza a facilitar al cirujano puntos de sutura.
Reactivación del corazón, en ocasiones es necesario el empleo de las palas internas de DF, salida de bomba EC, control de hemostasia y cierre por planos.
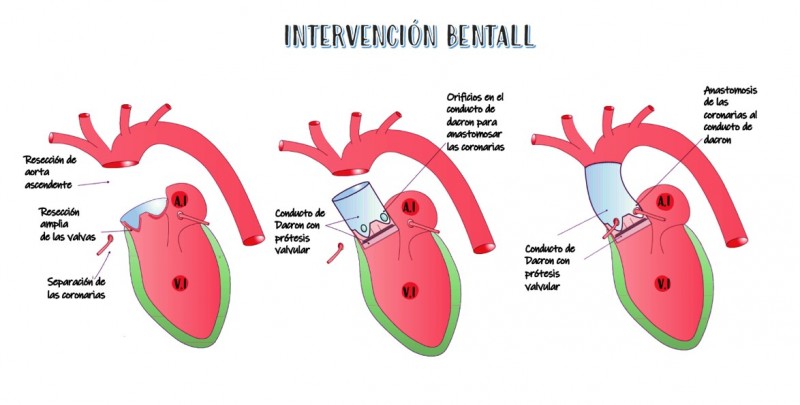
Imagen 19. Intervención Bentall. Recambio aórtico con prótesis valvulada.
- Si el reemplazo de la aorta disecada no afecta a la válvula aórtica: técnica de David:
Si la disección de AA no requiere de recambio valvular el conducto de Dacron se anastomosa “envolviendo” la válvula para asegurar que los velos coaptan y no se produce una IA. Y en este caso la apertura y disección de planos hasta llegar al corazón y grandes vasos es la misma técnica, la diferencia radica en que tras la resección de la Aorta ascendente y de los senos coronarios se comprueba la situación de los senos de Valsalva, pinza para retirar placas de calcio (Loop) que pudiera haber en las valvas y se anastomosa la prótesis sobre la raíz aórtica en su borde inferior y superior de tal manera, que la válvula aórtica del paciente queda “recogida” dentro del conducto de Dacron asegurando así, la captación correcta de los velos. Se anastomosa en las coronarias sobre ese conducto de Dacron, se revisa hemostasia, activación cardiaca y salida de bomba, cierre por planos.
La inserción de las coronarias sobre el tubo de Dacron, se hace recortando éste en forma de pétalos para que case exactamente con la V.A. La inserción de las coronarias, con la colocación o no, de anillo coronario de fijación, puede realizarse con modificaciones como la técnica de Jacoub.
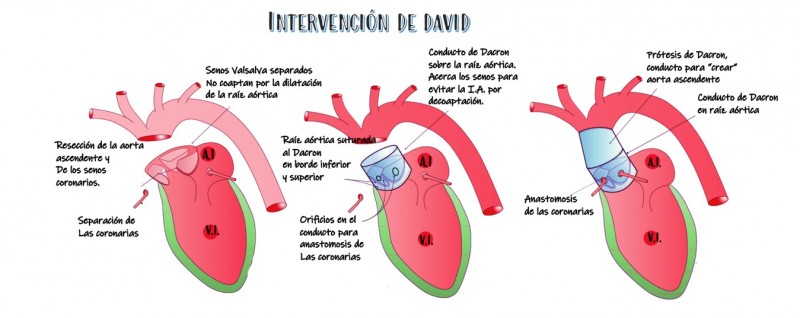
Imagen 20. Recambio de raíz aórtica preservando la válvula en Insuficiencia Aórtica.
5. RECAMBIO VÁLVULA AÓRTICA TÉCNICA DE ROSS
Anestesia, preparación del paciente y del quirófano, materiales e instrumental prácticamente igual que en las disecciones de aorta. El recambio de válvula aórtica se realiza generalmente siguiendo la técnica de Ross, tanto en niños como en adultos. La técnica de Donald Ross (1967) consiste en un homoinjerto. Se realiza con tejido vivo de la válvula pulmonar del propio paciente por lo que presenta la ventaja de que no precisa anticoagulación, o con tejido de donante cadáver.
- Técnica quirúrgica de Ross bajo CEC: apertura esternal y canulación según el protocolo anteriormente visto. Si el cirujano procede abrir las cavidades derechas, realiza con un bisturí del nº 11 una aortotomía y revisión o examen de la válvula aórtica. La instrumentista facilita bisturí del 11 y disecciones tipo de Bakey para abrir la arteria pulmonar y que el cirujano pueda examinar la situación de la válvula para decidir si realiza o no el auto trasplante.
Si se decide que sí, es el momento de preparar el homoinjerto, con pinza DeBakey y tijera de Metzembaum extirpa la válvula pulmonar con toda la arteria hasta su bifurcación. Extirpa la raíz aórtica y los primeros cm de AA (con los ostium coronarios).
o El homoinjerto homoinjerto viene congelado en nieve carbónica. Abrir cuidadosamente el precinto de la caja aislante utilizada para el transporte y almacenamiento.
o Verter un poco de nieve en la tapa hasta localizar la bolsa del homoinjerto.
o Con unas pinzas extraer la bolsa del homoinjerto y depositarla en la primera mesa, no es necesario que esta pinza esté estéril ya que la bolsa externa del homoinjerto no lo está́.
o Volver a verter la nieve de la tapa dentro de la caja, taparla, precintarla y entregarla para su retirada advirtiendo que no se debe desprecintar. La nieve carbónica produce quemaduras muy fácilmente.
La Enfermera Instrumentista tendrá́ preparada en su mesa una batea con suero frío, y la circulante colabora en la preparación de dos mesas auxiliares estériles para descongelar el injerto por fases, cuando se derrite el hielo de la primera bolsa se corta y se extra la siguiente, se disponen de varias bateas con suero fisiológico a 40 0C para ir descongelando. Cuando el último envase se abre y se vierte el homoinjerto y el líquido de conservación en una batea de 2-3 litros hasta que se descongela del todo (2-3 minutos). Se pasa a una cápsula de suero frio para facilitársela al cirujano.
El cirujano implanta la válvula pulmonar sobre el anillo aórtico (generalmente con puntos de Prolene 4/0 sin teflón). Hay que anastomosar los ostiums coronarios al autoinjerto (Prolene 6/0), realizar la anastomosis distal del autoinjerto con la aorta ascendente, con el ventrículo derecho (ambas anastomosis con mismo calibre, generalmente Prolene 4/0) y con la bifurcación pulmonar (Prolene 5/0).
La instrumentista debe conocer las suturas que va a emplear el cirujano de antemano, y tener una o dos de cada calibre en la mesa esta técnica con lleva muchas anastomosis, por lo que la instrumentista debe de tener en su mesa varios portaagujas de diferentes larguras y tamaños de boca.
Revisión de hemostasia, colocación de electrodos de marcapasos drenajes, salida de CEC, decanulación y cierre esternal según protocolo.

Imágenes 21 y 22. Sutura metálica para cierre esternal.

Imagen 23. Mesa de instrumental en cirugía cardiaca.
Imagen 24. Situación de la segunda mesa de instrumental.
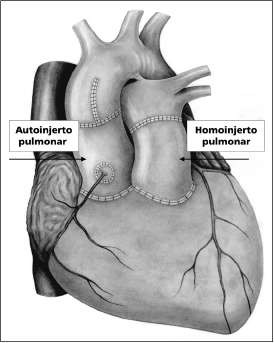
Imagen 25. Técnica de Ross.

Imagen 26. Desplazamiento sobre las suturas de válvula aórtica para su colocación.
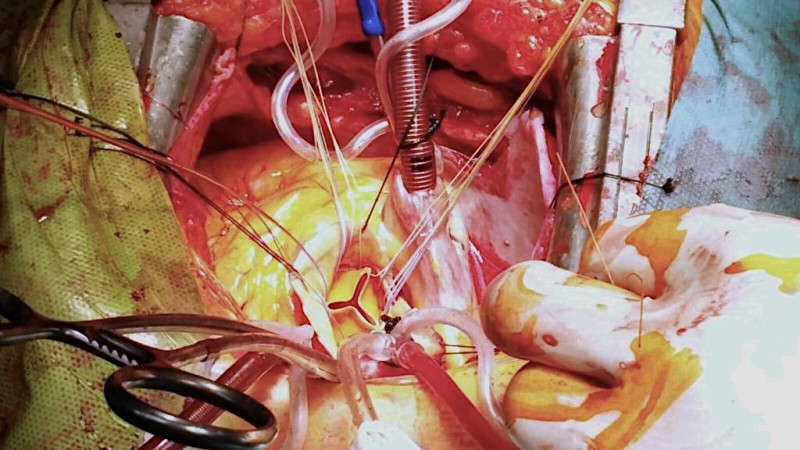
Imagen 27. Válvula aórtica alojada en su posición final.
BIBLIOGRAFIA
- Calavia Galé, Pablo; Gascón Catalán, Ana María. Protocolo de Circulación Extracorpórea: el rol de la Enfermera Perfusionista en Cirugía Cardíaca.
- Hornero Sos F, Centella Hernández T, Polo López L, López Menéndez J, Mestres Lucio C-A, Bustamante Munguira J, et al. Recomendaciones de la SECTCV para la cirugía cardiovascular. 2019 actualización de los estándares en organización, actividad profesional, calidad asistencial y formación en la especialidad. Cirugía Cardiovascular 2019;26:104–23. https://doi.org/10.1016/j.circv.2018.10.001.
- Margarit, Juan A., et al. Vía clínica de recuperación intensificada en cirugía cardiaca. Documento de consenso de la Sociedad Española de Anestesiología, Reanimación y Terapéutica del Dolor (SEDAR), la Sociedad Española de Cirugía Cardiovascular y Endovascular (SECCE) y la Asociación Española de Perfusionistas (AEP). Cirugía Cardiovascular, 2021, vol. 28, p. 1-40.
- López Gómez A, Rodríguez R, Zebdi N, Ríos Barrera R, Forteza A, Legarra Calderón JJ, et al. Guía anestésico-quirúrgica en el tratamiento de la cirugía de la aorta ascendente y del arco aórtico. Documento de consenso de las Sociedades Española de Cirugía Cardiovascular y Endovascular y la Sociedad Española de Anestesiología, Reanimación y Terapeútica del Dolor. Cirugía Cardiovascular 2020;27:47–74. https://doi.org/10.1016/j.circv.2020.02.004.
- Castillo-Martín R, Rubio-Lobato L, Martín-Manzano JA, Zabala-Argüelles JI, Calleja-Rosas F. Evolución natural de la enfermedad aneurismática aórtica. Cirugía Cardiovascular 2016;23:268–9. https://doi.org/10.1016/j.circv.2016.07.007.
- Sualís A, Carreras F, Borrás X, García-Picart J, Montiel J, Pons-Lladó G. Evaluación de la permeabilidad de los injertos de arteria mamaria interna izquierda mediante análisis de la velocidad del flujo por técnica Doppler transcutánea. Revista Española de Cardiología 1999;52:681–7. https://doi.org/10.1016/S0300-8932(99)74989-4.
- Legarra JJ. Anastomosis coronaria. Técnica quirúrgica. Endarterectomía coronaria. Cirugía Cardiovascular 2011;18:283–7. https://doi.org/10.1016/S1134-0096(11)70046-8.
- Álvarez, Prudencio Díaz-Agero. Y TERAPÉUTICA.
- Bejarano B, Manrique M. Simpatectomía toracoscópica: una revisión de la literatura. Neurocirugía 2010;21:5–13. https://doi.org/10.1016/S1130-1473(10)70048-8.
- Protocolo de Neumotórax del Hospital de Donostia. Accesible en : https://www.euskadi.eus/contenidos/informacion/hd_publicaciones/es_hdon/adjuntos/Protocolo25NeumotoraxC.pdf
- Aguinagalde B, Aranda JL, Busca P, Martínez I, Royo I, Zabaleta J. Guía de práctica clínica de la SECT sobre el manejo de pacientes con neumotórax espontáneo. Cirugía Española 2018;96:3–11. https://doi.org/10.1016/j.ciresp.2017.11.005.
- Celis López A. Enfermedad inflamatoria pélvica: tratamiento médico y quirúrgico. Rev Peru Ginecol Obstet 2015;53:240–7. https://doi.org/10.31403/rpgo.v53i1049.
- De tecnologías sanitarias, Informes de Evaluación. Mallas transvaginales en la reparación del prolapso de órganos pélvicos. Axencia de Avaliación de Tecnoloxías Sanitarias de Galicia, avalia-t. Consellería de Sanidade. Ministerio de Sanidad, Servicios Sociales e Igualdad, 2014.
- DÍAZ, Cristóbal Rengel. La maniobra de Kristeller: revisión de las evidencias científicas. Matronas prof, 2011, vol. 12, no 3, p. 82-89.
- Hernández Durán D, Diaz Mitjans O. Enfermedad inflamatoria pélvica. Revista Cubana de Obstetricia y Ginecología 2010;36:613–31
