INTRODUCCIÓN
La investigación cuantitativa está directamente basada en la corriente conocida como positivismo. El paradigma positivista sostenía que todas las “cosas” o fenómenos que estudiaban las ciencias eran medibles. Este paradigma utiliza preferentemente información cuantitativa o cuantificable para describir o tratar de explicar los fenómenos que estudia. Usa la recolección de datos para probar hipótesis, con base en la medición numérica y el análisis estadístico para establecer patrones de comportamiento y probar teorías.
Este paradigma sostiene que existe una realidad objetiva (estática), que puede ser estudiada por parte del investigador que tiende a comprender las causas de los fenómenos naturales. Los positivistas tratan de ser tan objetivos como sea posible en la búsqueda del conocimiento, para lo que emplean procedimientos ordenados y disciplinados que les permitan probar las ideas del investigador acerca de la naturaleza de los fenómenos que son objeto de estudio, así como las relaciones existentes entre ellos.
El enfoque cuantitativo es secuencial y probatorio. Cada etapa precede a la siguiente, no podemos definir y seleccionar la muestra si aún no hemos establecido las hipótesis. Tampoco es posible recolectar o analizar datos si previamente no hemos desarrollado el diseño o definido la muestra. El orden es riguroso, aunque desde luego, podemos redefinir alguna fase. Parte de una idea que va acotándose y una vez delimitada se derivan objetivos y preguntas de investigación, se revisa la literatura y se construye un marco o una perspectiva teórica. De las preguntas se establecen hipótesis y determinan variables. Se desarrolla un plan para probarlas (diseño), se miden las variables en un determinado contexto, se analizan las mediciones obtenidas (con frecuencia utilizando métodos estadísticos), y se establece una serie de conclusiones respecto de las hipótesis.
1.1 CARACTERÍSTICAS DEL ENFOQUE CUANTITATIVO
La investigación cuantitativa permite producir y analizar datos numéricos en relación a unas determinadas variables, que han sido previamente establecidas para poder interpretar los resultados obtenidos.
Las principales características del enfoque cuantitativo son:
- Sus preguntas de investigación versan sobre cuestiones específicas.
- Se construye un marco teórico (la teoría que habrá de guiar el estudio mediante una revisión de la literatura previa), del cual deriva una o varias hipótesis (cuestiones que va a examinar si son ciertas o no) y las somete a prueba mediante el empleo de los diseños de investigación apropiados.
- Si los resultados corroboran las hipótesis o son congruentes con éstas, se aporta evidencia en su favor y se genera confianza en la teoría que las sustenta. Si se refutan, se descartan en busca de mejores explicaciones y nuevas hipótesis y se descarta eventualmente la teoría, generándose por tanto evidencia en contra de la misma.
- La recolección de los datos se realiza con herramientas de medición mediante procedimientos estandarizados y aceptados por la comunidad científica. Se busca que los estudios efectuados puedan replicarse.
- Los datos son producto de mediciones y se representan mediante números (cantidades). Se deben analizar a través de métodos estadísticos.
- En el proceso se busca el máximo control de las variables para lograr que otras posibles explicaciones o causas del problema distintas a la propuesta del estudio (hipótesis), sean desechadas y se excluya la incertidumbre y así minimizar el error.
- Los análisis cuantitativos deben interpretarse en base a las predicciones iniciales (hipótesis) y de estudios previos (teoría). Las conclusiones constituyen una explicación de cómo los resultados encajan en el conocimiento existente
- La investigación cuantitativa debe ser lo más “objetiva” posible. Los fenómenos que se observan y/o miden no deben ser afectados por el investigador.
- En una investigación cuantitativa se pretende generalizar los resultados encontrados en un grupo o segmento (muestra) a una colectividad mayor (universo o población).
- Al final, con los estudios cuantitativos se intenta explicar y predecir los fenómenos investigados, buscando regularidades y relaciones causales entre elementos. Los datos generados poseen los estándares de validez y confiabilidad, y las conclusiones derivadas contribuirán a la generación de conocimiento.
- Esta aproximación utiliza la lógica o razonamiento deductivo, que comienza con la teoría y de ésta se derivan expresiones lógicas denominadas hipótesis que el investigador busca someter a prueba.
- La investigación cuantitativa pretende identificar leyes universales y causales.
1.2 DISEÑOS CUANTITATIVOS
La elección del tipo de diseño es una fase fundamental del proceso de investigación que estará determinada por la pregunta de investigación. La naturaleza o enfoque de la pregunta indicará cuál será el tipo de estudio más adecuado para contestarla. Es decir, la pregunta nos dirigirá hacia un estudio cuantitativo, cualitativo o mixto, considerando siempre la pregunta junto a las consideraciones bioéticas, para delimitar cuál debe ser el tipo de estudio a desarrollar.
Los estudios se pueden clasificar según diferentes criterios:
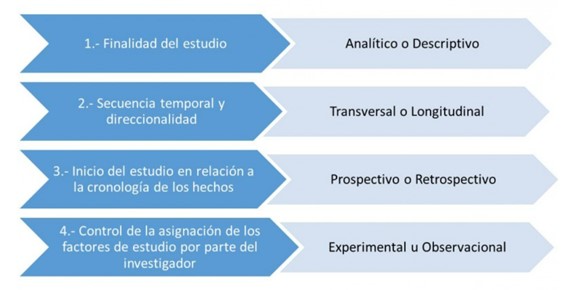
A) Según su finalidad:
- Descriptivos: se limitan a describir determinadas características del grupo de elementos estudiados.
- Analíticos: son aquellos que pretenden evaluar una presunta relación causa efecto.
B) Según secuencia temporal:
- Transversales: estudian las variables de forma simultánea en un momento de tiempo determinado.
- Longitudinales: estudian las variables a lo largo de un periodo de tiempo. Las mediciones se realizan en, al menos, dos momentos en el tiempo.
C) Según la cronología del proceso:
- Prospectivos: el inicio del estudio es anterior a los efectos estudiados. Los datos se recogen según se van sucediendo en el tiempo.
- Retrospectivos: el inicio del estudio es posterior a la aparición de los hechos estudiados.
- *Estudio ambispectivo: Se realiza un histórico de los hechos pasados y se continúan recogiendo medida que van sucediendo.
D) Según la asignación de los factores de estudio:
- Experimentales: el investigador manipula la variable independiente, puesto que establece los valores que esta va a tomar, la controla de forma deliberada o introduce un elemento nuevo en la realidad que estudia. Son los que mayor evidencia de causalidad aportan entre una exposición y un efecto.
- Observacionales: el investigador no manipula, solo se limita a observar lo que ocurre de forma natural, sin que intervenga más allá de describir o analizar.
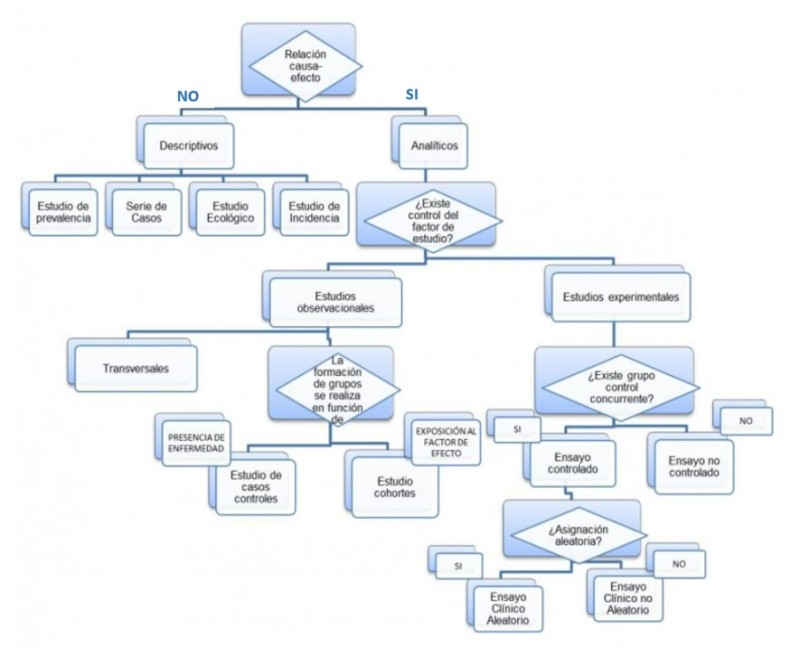
1.2.1 Estudios Descriptivos
Son estudios que tratan de conocer las características de una población determinada, describen la frecuencia y las características más importantes de un problema de salud. Este tipo de diseño se centra en conocer qué es lo que pasa, pero sin llegar a profundizar en el por qué ocurre eso.
En estos estudios se aplican únicamente estadísticos descriptivos, como la media aritmética, la desviación estándar, la moda o conocer cómo se reparten las frecuencias sin la realización de análisis más profundos, que supongan conocer cómo se relacionan estas variables o si alguna de estas variables es capaz de ser predicha por otra.
Estos estudios se distinguen según sea su unidad de estudio.
- Estudio Ecológico estudia a una población en su conjunto. En estos estudios no es posible identificar a un individuo dentro del grupo estudiado, son estudios que utilizan datos a nivel poblacional ya publicados, como las encuestas del INE o el Censo, y sirven para generar hipótesis. Pueden ser:
o Series temporales.
o Mapas o estudios descriptivos de patrones geográficos de salud.
o Estudios de correlación ecológica.
Si se estudia a individuos, podemos encontrar:
- Informes de caso (descripciones de un único caso clínico señalado)
- Informes de series de casos. Estos estudios describen la experiencia de un paciente o un grupo de pacientes con un diagnóstico similar. En estos estudios frecuentemente se describe una característica de una enfermedad o de un paciente, que sirven para generar nuevas hipótesis. Muchas veces documentan la presencia de nuevas enfermedades o efectos adversos y en este sentido sirven para mantener una vigilancia epidemiológica.
En este tipo también se encuadran los Estudios de prevalencia, que recogen información de forma simultánea de un conjunto de pacientes buscando los factores de exposición y las patologías que padecen. Son útiles en la planificación y para la evaluación de intervenciones. Su ejemplo es el EPINE (Estudio de prevalencia de infección hospitalaria en España).
Los diseños descriptivos pueden ser transversales o longitudinales.
Los diseños transversales son aquellos que tratan de medir unas determinadas características de una muestra en un momento concreto únicamente. Hacen una fotografía de la realidad de la muestra que estudian.
Los diseños longitudinales son aquellos en los que, respetando una misma muestra, se toma mediciones de una determinada característica en dos o más de dos momentos de la historia. Hay estudios longitudinales de incluso años, donde los mismos sujetos han sido estudiados para conocer la evolución de una determinada característica.
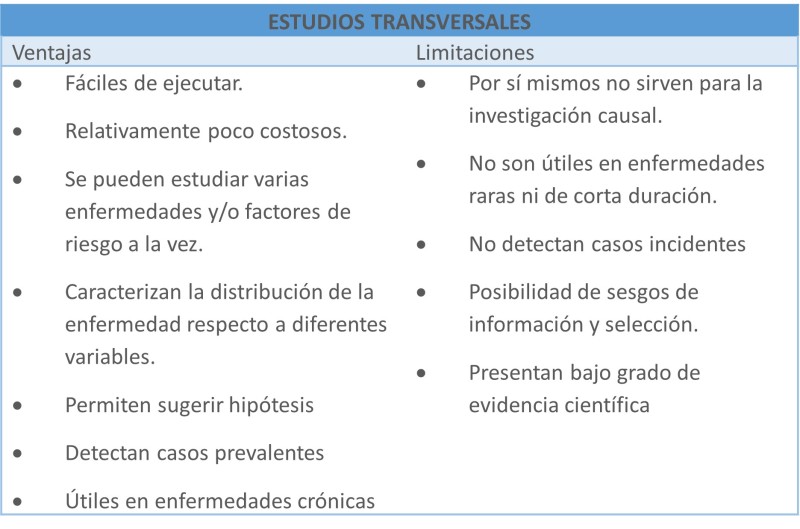
1.2.2 Estudios Analíticos
Analizan la realidad trazando relaciones entre las variables estudiadas. Pueden ser Observacionales (No existe control del factor de estudio) y Experimentales.
1.2.2.1 Analíticos observacionales
Los diseños Analíticos Observacionales se realizan cuando ya existe cierto conocimiento de la distribución de un fenómeno y se busca una explicación de este (conocer su causa o sus factores asociados).
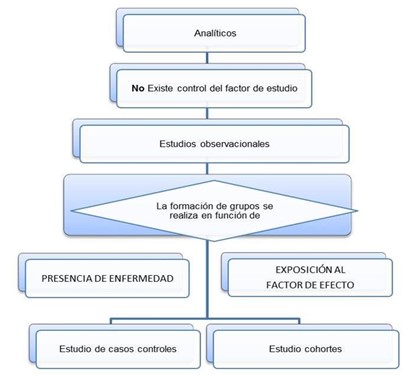
Estudios de cohortes: En epidemiología, el término “cohorte” sirve para referirse a un conjunto de personas que comparten una determinada exposición y/o “evolucionan” juntas a lo largo del tiempo.
Por tanto, los estudios de cohortes valoran el estado de exposición antes de que se produzca la enfermedad y permiten registrar los cambios ocurridos en el tiempo a nivel individual.
La esencia de los estudios de cohortes es el seguimiento. Realizan el seguimiento a lo largo del tiempo de grupos de individuos seleccionados que presentan una diferencia entre sí, la exposición o no a un factor de riesgo, estudiándose la aparición o no de un efecto (enfermedad). El seguimiento sirve para cuantificar no sólo la frecuencia de enfermedad en las distintas cohortes (incidencia acumulada), sino el ritmo o dinámica de la enfermedad en cada una de ellas (tasa de incidencia). Además, durante el seguimiento es posible considerar e incorporar en el análisis los cambios en el nivel de exposición, así como las variaciones del resto de factores de riesgo relevantes.
La cuantificación de esta asociación la podemos calcular construyendo una razón entre la incidencia del fenómeno en los expuestos a la variable (le) y la incidencia del fenómeno en los no expuestos (lo). Esta razón entre incidencias se conoce como riesgo relativo y su cálculo se estima como se ve en la siguiente tabla:
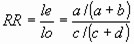

Este tipo de estudio permite el examen de múltiples efectos ante una exposición determinada.

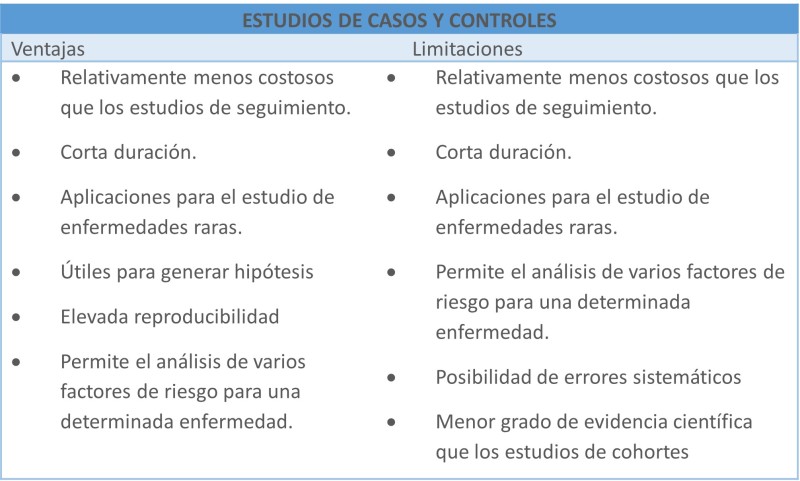
Estudios de casos y controles: Los estudios de casos y controles son un tipo de estudios observacionales, analíticos y retrospectivos en el tiempo, en los que se identifican dos grupos:
- Un grupo con un desenlace especificado (casos), presentan la enfermedad o el efecto a estudio.
- Un grupo sin ese desenlace especificado (controles o grupo de referencia).
Un estudio de casos y controles es un estudio analítico observacional que comienza con la identificación de un grupo de casos (individuos con una particular enfermedad o condición) y un grupo de controles (individuos sin la enfermedad o condición). Entonces, el nivel o prevalencia de la exposición a un factor se mide en los dos grupos y se compara. Básicamente, si la prevalencia de la exposición es mayor en casos que en controles, la exposición podría ser un factor de riesgo, mientras que si es menor, la exposición podría ser un factor protector. Luego, los investigadores comparan el grado en que cada persona estuvo expuesta con anterioridad a la variable de interés, por ejemplo, un factor de riesgo, un tratamiento o una intervención.
Se estudia retrospectivamente la aparición de los factores de riesgo (o de protección), obteniéndose los datos mediante entrevista o registros ya existentes. La relación entre uno o varios factores relacionados con la enfermedad se examina comparando la frecuencia de exposición a éste u otros factores entre los casos y los controles.
En los estudios de casos y controles tenemos casos expuestos (a), casos no expuestos (c), controles expuestos (b) y controles no expuestos (d). En este estudio la frecuencia de exposición a la causa entre los casos (a/c) se compara con la frecuencia de exposición en una muestra que represente a los individuos en los que el efecto no se ha producido y entre los que la frecuencia de exposición es (b/d).

La medida de asociación que permite cuantificar esta asociación se llama "odds ratio" (razón de productos cruzados, razón de disparidad, razón de predominio, proporción de desigualdades, razón de oposiciones, oposición de probabilidades contrarias, cociente de probabilidades relativas, oportunidad relativa).
La selección de los casos debe establecer de forma clara y explícita la definición de la enfermedad y los criterios de inclusión.
La selección del grupo control debe tener en cuenta:
- La función del grupo control es estimar la proporción de exposición esperada en un grupo que no tiene la enfermedad.
- Los controles deben ser representativos de la población de donde provienen los casos. Los casos y los controles no deben entenderse como dos grupos representativos de dos poblaciones distintas, sino como dos grupos que proceden de una misma población.
- Los controles deben ser comparables a los casos en el sentido de haber tenido la misma probabilidad de haber estado expuestos.
Los estudios de casos y controles son útiles para estudiar afecciones raras y afecciones con intervalos prolongados entre la exposición y el desenlace. Un ejemplo sería el desarrollo de enfermedades crónicas (cáncer, enfermedades cardiovasculares), aunque cada vez son más utilizados también en el estudio de enfermedades transmisibles y en la evaluación de intervenciones y programas de salud. En estos casos, un estudio prospectivo sería difícil. Aunque los estudios de casos y controles pueden ser eficaces y económicos, no tienen la robustez de las pruebas científicas de un estudio prospectivo.
1.2.3 Declaración STROBE
En el marco de la iniciativa STROBE (Strengthening the Reporting of Observational Studies in Epidemiology), se formularon recomendaciones sobre lo que debería contener una notificación precisa de un estudio observacional. La Declaración STROBE está constituida por una lista de puntos a tener en cuenta en la comunicación de los estudios realizados con los tres diseños más importantes de la epidemiología analítica observacional: los estudios de cohortes, los estudios de casos y controles y los estudios transversales.
1.2.3.1 Analíticos experimentales
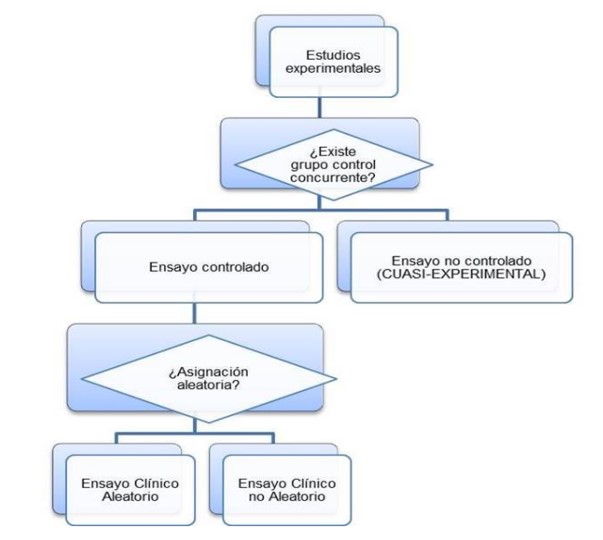
Los estudios experimentales son aquellos en los que el investigador controla la asignación de la exposición a estudio. Todos ellos son de tipo analítico, longitudinales y prospectivos, y por razones éticas, suelen limitarse exclusivamente a evaluar intervenciones terapéuticas o preventivas. Se utilizan para comprobar los efectos de una intervención o actuación específica, mientras se trata de mantener controladas otras variables que pudieran influir en el resultado, los sujetos son distribuidos en grupo(s) de intervención y control.
Aunque el elemento central que define un estudio experimental sea la introducción de una intervención que altera las condiciones de este y es asignada a los participantes por el investigador, para que podamos hablar de un experimento válido desde el punto de vista científico, es preciso que además se cumplan las siguientes condiciones:
- La única razón por la que los sujetos reciben la intervención bajo estudio es el cumplimiento del protocolo del estudio.
- En el estudio existe una serie de sujetos, denominados grupo control, que no reciben la intervención cuyo efecto se desea analizar.
- La asignación de la intervención a una serie de sujetos, grupo de intervención, se lleva a cabo por un mecanismo debido al azar.
Un grupo control es un conjunto de personas que comparte con el grupo de sujetos tratados todos los predictores de las variables, excepto el tratamiento a evaluar. Por tanto, su papel consiste en controlar la acción de los otros predictores en el efecto de la intervención que se está ensayando. Es decir, el grupo control informa del resultado en ausencia de intervención.
El grupo control podrá recibir una intervención activa, que habitualmente será la utilizada en condiciones normales para la condición bajo estudio, inactiva e inocua (placebo) o simplemente no recibir intervención alguna.
1.2.3.2 Ensayos Clínicos Controlados
Para lograr este objetivo es necesario controlar todos los factores que pueden afectar de forma relevante la condición bajo estudio. Es decir, necesitamos crear unas condiciones tales que el único factor que presente variación entre los grupos de comparación sea la intervención cuyo efecto pretendemos evaluar. Puede afirmarse que un experimento es aceptable si la variación de los factores extraños es demasiado pequeña como para afectar la condición bajo estudio de forma importante en comparación con el efecto de la intervención bajo estudio.
Su paradigma es el Ensayo Clínico Aleatorizado (ECA). El ECA está considerado como el diseño más idóneo para evaluar la eficacia de las intervenciones sanitarias.
1.2.3.3 Ensayo Clínico Aleatorizado
Según el Real Decreto de Ensayos Clínicos (RD 1090/2015) se refiere a toda investigación clínica relativa a personas y destinada a descubrir o comprobar, estudiar o identificar efectos clínicos, farmacológicos y reacciones adversas.
Un ensayo clínico es un experimento planificado en el que, de forma prospectiva, se comparan dos o más intervenciones (o intervención y placebo) preventivas, curativas o rehabilitadoras, que son asignadas de forma individualizada y aleatoria a un grupo de pacientes para determinar su eficacia. Además, tanto la selección de los sujetos como los períodos de tratamiento y seguimiento han de tener lugar simultáneamente en todos los grupos. Dado que los participantes en un ensayo clínico son, por definición, sujetos enfermos (pacientes), las intervenciones preventivas a las que nos referimos son secundarias, dirigidas a evitar las secuelas de la enfermedad, incluyendo la muerte.
El diseño de este estudio debe contemplar básicamente:
- La ética y justificación del ensayo. Todos los ECAs deben haber sido aprobados por el comité de ética de su institución, para lo que es necesario presentar protocolo completo según rige en el RD. Es imprescindible que el sujeto otorgue libremente su consentimiento informado antes de poder ser incluido en un ensayo clínico y así debe constar en todo ensayo publicado. El consentimiento informado es el procedimiento formal para aplicar el principio de autonomía y debe reunir, al menos tres elementos: voluntariedad, información y comprensión. Decidir libremente si quieren o no participar en un proyecto de investigación. Ello implica que no exista ningún tipo de presión externa ni influencia indebida, cada sujeto debe recibir la información mínima necesaria, adaptada a su nivel de entendimiento, sobre el objetivo, procedimiento del estudio, beneficios esperados y riesgos potenciales, posibles alternativas, etc., así como la posibilidad de retirar su consentimiento, sin perjuicio alguno. Se debe comprobar que se ha comprendido la información proporcionada. Hablaremos ampliamente de los aspectos éticos en temas posteriores.
- La población susceptible de ser estudiada. Un aspecto a tener en cuenta al definir el perfil de los participantes es el de la representatividad de la muestra. Deseamos demostrar la eficacia de la intervención en los pacientes del ensayo, y que pueda ser extensible a todos aquellos sujetos o pacientes susceptibles de recibir la intervención en el futuro. Por ello, es necesario intentar que la muestra sea lo más representativa posible.
- La selección de los pacientes con su consentimiento a participar. Hay que empezar por definir de forma precisa el perfil de los sujetos susceptibles de participar en el estudio. A continuación, se deben definir los criterios de exclusión, en función de aspectos que pudieran comprometer la participación en el estudio (p. ej. enfermedades incapacitantes física o mentalmente) o que pudieran interaccionar con la intervención bajo estudio y afectar la variable de interés. En cualquier caso, hemos de intentar ser lo menos restrictivos posible a la hora de establecer los criterios de inclusión y exclusión.
- El proceso de Aleatorización. Los participantes deben ser asignados a uno de los dos grupos utilizando un procedimiento de aleatorización correcto, de forma que todos los sujetos tengan la misma probabilidad de acceder a cualquiera de los dos grupos.
La aleatorización elimina el sesgo del investigador en la asignación de los sujetos, garantiza la validez de los niveles de significación de las pruebas estadísticas que se aplicarán en el análisis de los datos y tiende a producir grupos comparables respecto de características conocidas y desconocidas que pudieran afectar al desenlace de interés (factores pronósticos).
Secuencia de aleatorización. Debe ser oculta para que no se vea interferida por la acción consciente o inconsciente de investigadores o participantes. Debe resultar impredecible, es decir, el investigador debería ser incapaz de adivinar con antelación el grupo al que va a ser asignado el próximo sujeto. En ciertas ocasiones, adivinar la secuencia de aleatorización se convierte en un reto para la investigación.
El proceso debe estar basado en propiedades matemáticas conocidas y ser reproducible. Los métodos de aleatorización sistemáticos (asignación según el orden de incorporación al estudio, la fecha de nacimiento, etc.) no son válidos ya que, aunque son aleatorios, también son predecibles y además no están basados en un modelo matemático ni son reproducibles.
Herramientas en versión española y gratuita que puede servir en este proceso: OxMaR para minimización y aleatorización de estudios clínicos.
- La descripción minuciosa de la intervención: El ECA debe haber sido diseñado para responder a una pregunta clínica en la que estén bien definidos sus componentes habituales: población, intervención, comparación y resultado.
La descripción de la intervención debe ser una descripción minuciosa de los beneficios para el sujeto del ensayo o para la salud pública esperados justifican los riesgos y los inconvenientes previsibles, y se supervisa de forma constante el cumplimiento de esta condición. No obstante, los derechos, la seguridad, la dignidad y el bienestar de los sujetos prevalecen sobre cualquier otro interés.
- Enmascaramiento. o carácter ciego de un ensayo clínico, es el conjunto de medidas o precauciones que se toman con el fin de que los que intervienen en el mismo (paciente, médico, evaluador, etc.) desconozcan el tratamiento al que el paciente ha sido asignado, ya que este conocimiento podría introducir sesgos en el desarrollo, análisis y evaluación de un ensayo clínico.
En función del grado de enmascaramiento decimos que un ensayo clínico es:
- abierto cuando el paciente y el investigador conocen la intervención asignada
- simple ciego cuando el paciente es el único que desconoce la intervención asignada
- doble ciego, cuando el paciente y el evaluador de la variable respuesta (investigador) desconocen el grupo de tratamiento asignado. Aunque en el doble ciego hay en realidad tres agentes implicados (paciente, equipo de tratamiento y evaluador), se mantiene esa denominación porque en muchas ocasiones el médico que trata al paciente es asimismo el responsable de la evaluación de la variable respuesta.
- A veces se habla de triple ciego cuando la persona que analiza los resultados es distinta al investigador que lleva a cabo la intervención y ninguno de ellos (paciente, investigador, analista) conoce la intervención
El enmascaramiento del responsable de evaluar la respuesta a la intervención es particularmente importante cuando la variable de resultado es subjetiva (p. ej. valoración de la intensidad del dolor, análisis de una radiografía, etc.), ya que el conocimiento de la intervención asignada puede afectar la percepción sobre la
El seguimiento exhaustivo que contemple las pérdidas y los no cumplidores debe ser completo e igual en los dos grupos. Se debe tratar de evitar que se produzcan pérdidas excesivas, además de valorar el posible efecto de las pérdidas sobre los resultados del ECA.
- Análisis de los resultados. El análisis y la presentación de los resultados deben realizarse de forma correcta. Los sujetos deben ser preferiblemente analizados según el grupo al que fueron inicialmente asignados (análisis por intención de tratar) y no según el grupo en el que finalmente participaron (análisis por protocolo) ya que, en caso contrario, se pierden los beneficios de la aleatorización.
El análisis por intención de tratar incluye a cada paciente en su grupo de aleatorización independientemente de los cambios que pudieran ocurrir a posteriori: incumplimiento de la intervención, cambio de tratamiento, etc.
Aunque este tipo de análisis tiene una mayor tendencia a obtener resultados nulos, aumentando las dificultades para demostrar la eficacia de cualquier nueva intervención, existen dos poderosas razones para llevarlo a cabo. Por un lado, con este tipo de análisis se pretende preservar lo conseguido con la aleatorización, que los grupos sean comparables, lo cual constituye el fundamento para poder obtener conclusiones válidas (no sesgadas) sobre la eficacia de una intervención. Por otro lado, se trata de evaluar el efecto de la intervención en condiciones lo más parecidas posibles a las de la vida real (efectividad) y no sólo teniendo en cuenta las condiciones ideales (eficacia) que proporcionan el subgrupo de pacientes que han seguido el protocolo de forma estricta.
La medición del efecto de una intervención podría llevarse a cabo mediante
- medidas absolutas, como la reducción del riesgo atribuible, la diferencia de riesgos en este supuesto, conocida como reducción absoluta del riesgo (RAR), se calcula restando del riesgo en el grupo control el riesgo en el grupo de intervención.
Cálculo de RAR:
Incidencia grupo control – Incidencia grupo experimental
- medidas relativas, como la reducción porcentual del riesgo relativo o Reducción Relativa del Riesgo (RRR), es el complemento del Riesgo Relativo (RR). Se interpreta como el porcentaje de reducción del riesgo de eventos en el grupo expuesto con respecto al riesgo de eventos en el grupo control.
Cálculo de RRR: (1 - RR) x 100
La presentación de los resultados mediante un único indicador, como la reducción porcentual del riesgo relativo, puede producir una impresión magnificada sobre el efecto del tratamiento, por lo que actualmente se recomienda que al presentar los resultados de un ensayo clínico se utilice la reducción porcentual del riesgo relativo acompañada de alguna magnitud que mida la reducción del riesgo en términos absolutos, particularmente el Número Necesario a Tratar (NNT). El NNT constituye el número de pacientes que tendríamos que tratar para evitar que se produjera un caso con la enfermedad o condición estudiada y se calcula como el inverso de la reducción del riesgo atribuible.
NNT = (1 / RAR) x 100
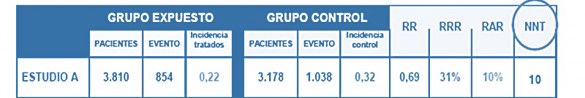
- La medición de la variable final. Evaluación de la respuesta y presentación de los resultados. Los ensayos clínicos son la mejor herramienta para evaluar si un medicamento es seguro y efectivo.
Los ensayos clínicos evalúan las intervenciones en condiciones óptimas diferentes a las de su aplicación habitual, ya que los pacientes están sometidos a un estrecho seguimiento y vigilancia médica y no suelen ser representativos de todo el espectro de posibles sujetos que padecen la enfermedad en cuestión. Los pacientes seleccionados para realizar un ensayo suelen estar más motivados y representan habitualmente al grupo más accesible al equipo investigador, con menos patologías asociadas y con mayores probabilidades de cumplir con el protocolo del estudio. Un ensayo está evaluando el efecto de la intervención en condiciones ideales (eficacia). Sin embargo, no puede evaluar cómo se comportará esa misma intervención en condiciones reales de uso (efectividad), ni su relación coste-beneficio (eficiencia), aspectos que se contemplan en el marco de la investigación de resultados.
La legislación española ha establecido mediante Real Decreto el procedimiento a seguir y los apartados que se deben incluir en el protocolo: Real Decreto 1090/2015, de 4 de diciembre, por el que se regulan los ensayos clínicos con medicamentos, los Comités de Ética de la Investigación con medicamentos y el Registro Español de Estudios Clínicos.
FASES DE UN ENSAYO CLÍNICO
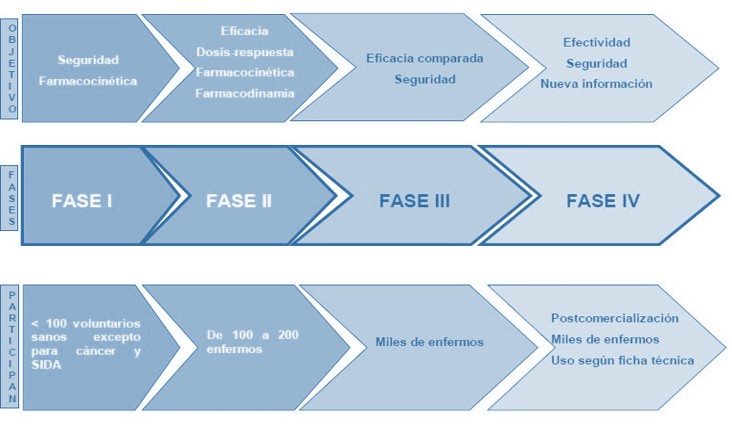
Placebo
El efecto global de cualquier intervención tiene dos componentes, el efecto placebo y el efecto específico de la misma. La administración de una intervención produce un efecto terapéutico sobre el individuo denominado efecto placebo, independientemente del principio activo que contenga la misma. Es decir, incluso la administración de un principio inactivo inocuo produce un efecto medible. El simple hecho de ser observado, de participar en un estudio, produce una modificación positiva en el estado clínico de los pacientes, denominada “efecto Hawthorne”. A esto hay que añadir el poder de sugestión derivado del hecho de recibir una terapia, aunque ésta sea farmacológicamente inactiva, y el de la presencia de un investigador que aplica la misma. La razón principal para utilizar el placebo consiste en conseguir que la actitud de los individuos ante la investigación en los grupos de intervención y control sea la misma. Asimismo, proporciona la oportunidad de realizar ensayos doble ciegos y evitar de esa forma que se produzcan sesgos en el desarrollo, análisis y evaluación del ensayo.
Por ello, al estudiar la eficacia de una nueva terapia es preciso aplicar una intervención alternativa al grupo control, que permita controlar el efecto placebo y discernir el efecto específico de la nueva terapia. Por razones éticas, cuando exista una terapia eficaz disponible para la condición bajo estudio no aplicaremos un placebo a los pacientes del grupo control, sino ese tratamiento habitual.
- Tipos de Ensayos Clínicos Aleatorizados
o Ensayo clínico de grupos paralelos
El ensayo de grupos paralelos constituye por su sencillez, el diseño básico para realizar un ensayo clínico. En este modelo, cada paciente es asignado al mismo tiempo y de forma aleatoria a una intervención diferente y tras un período de seguimiento variable, se procede a medir la respuesta. En general, se incluyen dos grupos de comparación, dada la dificultad de reclutar suficiente número de pacientes por grupo cuando se aumenta el número de tratamientos a comparar.
El problema principal de los ensayos de grupos paralelos es que habitualmente los pacientes presentan una gran variación en el estado inicial de la enfermedad, las variables pronósticas y en su respuesta a la intervención. Esto implica que se necesita un número importante de pacientes en cada brazo del ensayo para poder estimar de forma fiable la magnitud de la diferencia de efecto de las intervenciones estudiadas
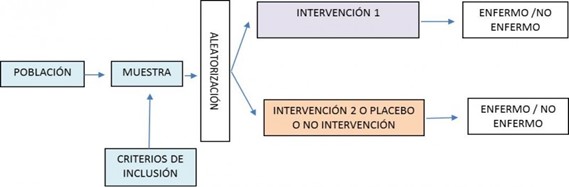
o Ensayo clínico cruzado
En este diseño cada individuo es asignado aleatoriamente a una secuencia temporal de dos o más tratamientos, al objeto de controlar el posible efecto período derivado de posibles cambios en otras variables predictoras a lo largo del tiempo. Es decir, lo que se aleatoriza no es el grupo de intervención al que va a ser asignado el paciente, sino el orden en el que va a recibir las intervenciones del estudio.
Cada paciente es sometido a todas las intervenciones durante periodos de tiempo sucesivos, realizándose después una comparación de tratamientos intrapaciente. Estas comparaciones son más eficientes, ya que se reduce la variablilidad intragrupo al servir cada individuo como su propio control, por lo que se obtienen resultados más precisos con tamaños muestrales reducidos. Como contrapunto, una muestra pequeña puede condicionar la eficacia de la aleatorización para distribuir las variables de interés de forma homogénea en los grupos a comparar.
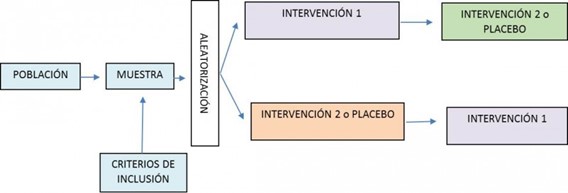

1.2.4 Consort
La “Declaración CONSORT”, es un informe con recomendaciones para mejorar la calidad de la presentación de los resultados de ensayos clínicos La declaración recoge los aspectos (22 ítems) que han de ser contemplados y la forma de presentarlos.
Ensayos controlados no aleatorizados
En este tipo de estudios, la asignación de los sujetos participantes a los grupos de comparación se realiza siguiendo un mecanismo no aleatorio, que puede ser sistemático (en función del orden de entrada en el estudio o de la fecha de nacimiento) o simplemente a criterio del investigador. En ambos casos, el investigador conoce a priori la intervención que recibirá el individuo, lo que puede afectar tanto su decisión de incluirlo en el estudio, como la de asignarlo a uno u otro grupo. La presencia de grupos de tamaño muy desequilibrado nos debería hacer sospechar de la existencia de intencionalidad a la hora de ubicar los sujetos en uno u otro grupo y de un posible sesgo de asignación asociado.
Declaración TREND (Transparent Reporting of Evaluations with Non-Randomized Designs) para estudios de intervención no aleatorizados.
1.2.4.1Ensayos No Controlados o Cuasiexperimentales
Para algunos autores, únicamente podemos hablar con propiedad de estudio experimental cuando existe un grupo control que no recibe la intervención bajo estudio y sirve como grupo de referencia para establecer las comparaciones, siempre que la asignación de los participantes en el estudio a uno u otro grupo se haya llevado a cabo mediante un mecanismo debido al azar.
Sin embargo, existen muchas situaciones en las que nos encontramos con que el investigador manipula las condiciones del estudio (introduce una intervención) sin que se den las condiciones previamente mencionadas. son diseños muy utilizados en el ámbito de la enfermería. Este tipo de estudios son muy similares a los estudios experimentales, pero con la desventaja de que se asume de antemano que el investigador no tiene el control total de todas las variables que rodean al sujeto. Se tratan de casi (cuasi) experimentos. P. ej. a la hora de evaluar una intervención que no pueda cegarse (Educación para la salud, utilización de algún tipo de tecnología, materiales para curas etc.) El problema con este tipo de estudios es que carecen del grado de validez interna que se precisa para atribuir el efecto observado a la intervención bajo estudio.
Algunos tipos de estudios cuasiexperimentales son:
- Estudios pre-post. Comparan los resultados del efecto estudiado en el mismo grupo de individuos antes y después de recibir la intervención. En este tipo de investigación no existe ninguna garantía de que el efecto observado sea debido a la intervención bajo estudio, también puede ser un debido a un efecto placebo, a un efecto período, a la propia historia natural de la enfermedad o a fenómenos puramente estadísticos, como la regresión a la media. El efecto período se refiere a todos aquellos factores que pudiendo tener alguna influencia sobre la condición de interés (clima, hábitat, estilos de vida, etc.), se hayan modificado a lo largo del período de estudio. El efecto placebo consiste en que el sólo hecho de administrar una intervención produce un efecto sobre el individuo, independientemente del principio activo que contenga la intervención.
- Estudios con controles históricos. En este tipo de estudio, se compara un grupo de pacientes que están recibiendo la intervención cuyo efecto se pretende determinar, con pacientes que recibieron una intervención diferente en el pasado. En este caso, el problema es que no podemos garantizar la comparabilidad entre los dos grupos, es decir, no podemos asegurar que los sujetos de ambos grupos son similares en todo, excepto en la intervención estudiada. Con el paso del tiempo, nos podemos encontrar con diferencias en los procedimientos de selección de los pacientes susceptibles de ser intervenidos (edad, estadío clínico o anatomo-patológico, gravedad, patologías asociadas, etc.), en los tratamientos auxiliares aplicados, en los criterios diagnósticos y de valoración de la respuesta al tratamiento, etc. En estos casos, nada nos permite afirmar que el efecto observado sea debido a la intervención estudiada y no a cualquier otra característica en la que difieren los grupos comparados. Los estudios no controlados o con controles históricos tienden a exagerar el valor de un nuevo tratamiento.
- Ensayos de campo: valoran la eficacia de una medida preventiva primaria en la población. Tratan con sujetos que aún no han adquirido la enfermedad o con aquéllos que estén en riesgo de adquirirla y estudian factores preventivos de enfermedades como pueden ser la administración de vacunas o el seguimiento de dietas.
- Ensayos comunitarios: Incluyen intervenciones sobre bases comunitarias amplias. Este tipo de diseños suelen ser cuasiexperimentales (existe manipulación, pero no aleatorización), en los que una o varias comunidades recibirán la intervención, mientras que otras servirán como control.
1.2.4.2 Registro de Ensayos Clínicos
Los ensayos clínicos con resultados negativos tienen el doble de posibilidades de no ser publicados frente a aquellos que tienen resultados positivos. Esto implica que las personas que toman decisiones no tienen toda la información completa sobre los riesgos y beneficios de los tratamientos que usamos cada día. Todos los ensayos clínicos, pasados y presentes, deberían ser registrados y sus resultados publicados.

Para que esto sea así existe una plataforma AllTrials sobre la premisa de “Todos los ensayos registrados | Todos los resultados informados”
En España el RD obliga al registro de todos los Ensayos Clínicos, el Registro Español de estudios clínicos (REec) es una base de datos pública, de uso libre y gratuito para todo usuario, accesible desde la página web de la AEMPS, cuyo objetivo es servir de fuente de información primaria en materia de estudios clínicos con medicamentos.

A nivel mundial, podemos estar informados e informar a nuestros pacientes de los ECAs finalizados, en curso o abiertos para reclutamiento de pacientes desde la plataforma Clinicaltrials.gov
1.3 GUÍAS DE COMPROBACIÓN DE DOCUMENTOS CIENTÍFICOS
Las listas guía de comprobación de diseño de estudios son herramientas diseñadas para ayudar a alcanzar ciertos estándares de calidad, ética y rigor científico, al proporcionar un conjunto de recomendaciones que orientan hacia una conducta adecuada. Su propósito es obtener de los autores una exposición transparente de la investigación para que tanto sus lectores como sus evaluadores comprendan su diseño, realización, análisis e interpretación. Estas listas definen iniciativas para mejorar la realización y publicación de estudios experimentales, observacionales, de precisión diagnóstica, pronóstico, evaluación económica, guías de práctica clínica, etc. Cada tipo de estudio tiene su propia guía identificada por unas siglas (AGREEE, CONSORT, COREQ, QUOROM, MOOSE, PRISMA, REMARK, SQUIRE, STARD, STROBE, TREND, etc.)
EQUATOR Network, siglas de Enhancing the QUAlity and Transparence Of health Research, es una iniciativa internacional cuyo objetivo es mejorar la confiabilidad y el valor de la bibliografía de investigación médica por medio de la promoción de prácticas claras y precisas para la presentación de informes sobre estudios de investigación.
Este enlace da también acceso a estas guías: https://www.goodreports.org/
La asociación española de pediatría ha recopilado y traducido estas listas: LISTA DE GUÍAS DE COMPROBACIÓN
BIBLIOGRAFÍA
- Asociación Médica Mundial.Declaración de Helsinki de la Asociación Médica Mundial. Principios éticos para las investigaciones médicas en seres humanos. Anales del Sistema Sanitario de Navarra. 2008; 24(2):209-212.
- Casado M., Vilà A. Declaración Universal sobre Bioética y Derechos Humanos de la Unesco y la discapacidad, 1ª ed. Barcelona: Edicions Universitat Barcelona; 2014.
- Consejo de Organizaciones Internacionales de Ciencias Medica. International Ethical Guidelines for Biomedical Research Involving Human Subjects. Ginebra: CIOMS; 2002
- Sinobas P E. Manual de investigación cuantitativa para enfermería. Oviedo: Federación de Asociaciones de Enfermería Comunitaria y Atención Primaria; 2011.
- Fathalla Mahmoud F. Guía práctica de investigación en salud. Vol. 620. Washington DC: Organización Panamericana de la Salud, 2008. 247 p.
- Galindo-Domínguez, H. Estadística para no estadísticos: una guía básica sobre la metodología cuantitativa de trabajos académicos. 1ªed. Alicante:3ciencias, 2020. DOI: https://doi.org/10.17993/EcoOrgyCso.2020.59
- Grupo de trabajo sobre GPC. Elaboración de Guías de Práctica Clínica en el Sistema Nacional de Salud. Actualización del Manual Metodológico. Madrid: Ministerio de Sanidad, Servicios Sociales e Igualdad; 2016
- Hernández Sampieri R, Fernández Collado C BLP. Metodología de la investigación. 5a ed. México, D.F: McGraw-Hill; 2010. 613 p.
- Mirón Canelo JA, Alonso Sardón M I. Metodología de investigación en Salud Laboral. Med y Segur del Trab. 2010;56(221):347–65.
- Instituto Aragonés de Ciencias de la Salud. Manual Metodológico. Madrid: Plan Nacional para el SNS del MSC.
- Instituto Aragonés de Ciencias de la Salud-I+CS; 2016.
- Ochoa Sangrador C., Molina Arias M., Ortega Páez E. Inferencia estadística: contraste de hipótesis. (Internet) Evid Pediatr, 2020; 16:11. Disponible en: https://evidenciasenpediatria.es/articulo/7537/inferencia-estadistica-contraste-de-hipotesis (consultado 20 agosto 2024)
- Parreño Urquizo A. Metodología de investigación en salud. Instituto de Investigaciones. Riobamba: Escuela Superior Politécnica de Chimborazo; 2016.
- Pita Fernández, S. Epidemiología. Conceptos básicos. En: Tratado de Epidemiología Clínica. Madrid; DuPont Pharma, S.A.; Universidad de Alicante: 1995.
- Royo Bordonada M.Á, Damián Moreno J. Método epidemiológico. Madrid: ENS Instituto Salud CarlosIII;2009.
- Salamanca Castro AB. El AEIOU de la investigación. Enero 2013. Madrid: FUDEN; 2013. 494 p.
- Vicente Edo, MJ., Gavín Benavent, P., Cantero Muñoz, P., Novella Arribas, B., Reviriego Rodrigo, E., Toledo Chávarri, A., Triñanes Pego, Y. Evaluación de Tecnologías Sanitarias. Material de Formación para Pacientes y Ciudadanía. Versión completa. Madrid: Ministerio de Sanidad; Zaragoza: Instituto Aragonés de Ciencias de la Salud; 2020. 113 p.
