1. Concepto y clasificación
La diabetes mellitus (DM) es una alteración metabólica multicausal caracterizada por hiperglucemia crónica asociada a alteraciones del metabolismo hidrocarbonado, lipídico y proteico que se manifiesta como consecuencia de defectos en la secreción, en la acción, o en ambas, de la hormona insulina (secretada en las células β del páncreas).
La clasificación de la DM ha ido sufriendo modificaciones, y se ordena de la siguiente manera:
- Diabetes de tipo 1: también conocida como insulinodependiente o de comienzo juvenil. Presenta las siguientes características:
- 5-10 % de la DM.
- Su causa es la destrucción de las células β del páncreas.
- Se incluyen casos de:
- Patogenia autoinmunitaria: destrucción rápida de células β en niños y más lenta en adultos.
- Patogenia idiopática.
- Cetoacidosis como primera manifestación.
- Comienzo antes de los 30 años.
- Tendencia a la cetosis.
- Ausencia de obesidad.
- Asociada con endocrinopatías.
- Diabetes de tipo 2: también conocida como no insulinodependiente o de inicio en edad adulta. Sus características son las siguientes:
- Forma más prevalente de DM: 90-95 %.
- Aumentan la probabilidad de sufrirla la obesidad, el sedentarismo y la edad.
- Se produce insulinorresistencia y secreción deficiente compensatoria de insulina (ambas son necesarias, aunque predomine una sobre otra).
- Inicio progresivo después de los 40 años.
- No hay tendencia a la cetosis.
- Presencia de obesidad o mayor proporción de grasa abdominal.
- Diabetes gestacional: se diagnostica en el 2.º o 3.er trimestre del embarazo y se regresa a la normalidad tras el parto. Debe tenerse presente la posibilidad de este tipo de DM debido a la morbimortalidad fetal asociada. La posibilidad de desarrollar algún otro tipo de DM con posterioridad al parto (hay que reclasificar a la paciente) se eleva con la edad.
- Otros tipos específicos; dentro de este grupo existen subgrupos:
- Síndromes de diabetes monogénica:
o MODY (maturity-onset diabetes of the young) o diabetes del adulto de inicio juvenil. Es una alteración de la secreción de insulina. Autosómica dominante. Suele aparecer antes de los 25 años.
o Diabetes neonatal.
- Enfermedades del páncreas (pancreatitis, fibrosis quística).
- Inducida por medicamentos (glucocorticoides), por agentes químicos o después de trasplante de órganos.
Además de la clasificación expuesta y de las diferencias entre los dos tipos fundamentales de DM (de tipo 1 y de tipo 2) que se recogen en la tabla 1, se emplea el concepto de prediabetes (u homeostasis alterada de la glucemia) para casos que sin cumplir criterios de diabetes presentan niveles de glucosa demasiado altos para ser catalogados como normales. Engloba tres situaciones:
- Tolerancia anormal a la glucosa (TAG): respuesta patológica a la sobrecarga de glucosa sin llegar a niveles de DM. Parte de los pacientes con TAG pueden evolucionar a DM como tal o no si pierden peso y realizan ejercicio.
- Glucosa en ayunas anormal (GAA): se revisa el dato de la glucemia en ayunas, pues tienden a mantener niveles normales de glucemia en su vida normal. Suele asociarse (como ocurre también en TAG) a obesidad, dislipemia e hipertensión arterial (HTA), por lo que a pacientes con estas patologías es útil hacerles control glucémico y descartar la presencia de estados prediabéticos.
- Riesgo elevado de desarrollar diabetes: con niveles de hemoglobina glucosilada (HbA1c) entre 5,7 y 6,4 %.
Tabla 1
Principales diferencias entre DM de tipo 1 y de tipo 2
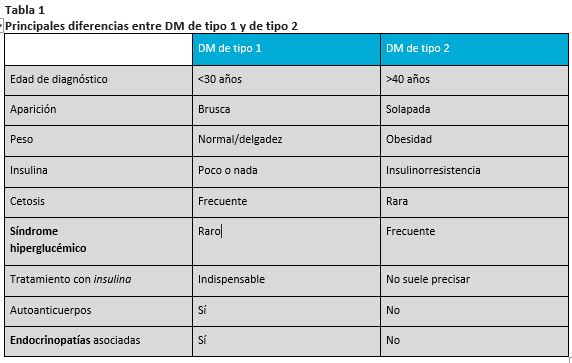
2.Clínica y diagnóstico
La DM suele ser asintomática y detectarse en análisis rutinarios, aunque en ocasiones puede darse una cetoacidosis grave. Los patrones de presentación se clasifican de la siguiente manera:
- Presentación metabólica, forma clásica sobre todo en DM de tipo 1:
- Poliuria.
- Polidipsia.
- Polifagia.
- Enuresis en niños.
- Si el déficit de insulina es grave: náuseas, vómitos, respiración de Kussmaul, deshidratación.
- Presentación no metabólica, en glucemias inferiores a 200-250 mg/dl la presentación metabólica es poco común, por lo que debe sospecharse por fenómenos asociados:
- Infecciones: sobre todo genitourinarias, respiratorias y periodontales.
- Complicaciones de la enfermedad:
o Retinopatía diabética.
o Dermopatía diabética.
o Patología vascular: claudicación intermitente, disfunción eréctil.
- Presentación asintomática: la forma más común de diagnóstico de DM de tipo 2 tras analíticas por parte de servicios médicos laborales, compañías de seguros y chequeos. Es recomendable hacer un cribado sistemático de DM en cierto tipo de personas:
- >45 años.
- Índice de masa corporal (IMC) >25 y 1 o más factores de riesgo:
- Inactividad física.
- Familiares diabéticos en primer grado.
- Pertenecer a etnias de riesgo .
- Mujeres que han tenido recién nacido >4 kg o con diagnóstico de diabetes gestacional.
- Presentan factores de riesgo cardiovascular:
- HTA >140/90 mmHg o en tratamiento.
- HDL 250 mg/dl.
- Niveles previos de Hb1c >5,7 % o TAG o GAA en análisis previos.
- Historia de enfermedad cardiovascular.
Para realizar el diagnóstico de la DM se necesita hacer determinación glucémica. Esta puede ser de 2 tipos:
- Glucemia basal: la obtenida tras ayuno nocturno de 8-12 h. Hay que conocer la procedencia de la muestra (venosa o capilar, sangre total, plasma o suero).
- Curva de glucemia o prueba de tolerancia a la glucosa oral (PTGO): se trata de administrar una cantidad de glucosa y obtener distintas muestras de sangre. Solo vale para realizar el diagnóstico, es decir, en los casos en los que ya esté establecido no se debe emplear. Según la Organización Mundial de la Salud (OMS), los criterios que hay que seguir son los siguientes:
- Administrar 75 g de glucosa disuelta en 375 ml de agua y tomada en 5-10 min.
- Extracciones sanguíneas a los 0 min y a los 120 min (opcionalmente a los 60 min y a los 90 min).
- Ayunas 12 h antes de la prueba, reposo físico y no fumar.
- Dieta libre los 3 días previos (no limitar los glúcidos a
- La persona no debe padecer enfermedad intercurrente, estar convaleciente o tomar medicación.
La DM se diagnostica por 1 de las siguientes opciones:
- Síntomas típicos (poliuria, polidipsia o pérdida de peso no explicada) y glucemia plasmática al azar ≥200 mg/dl. Basta con una determinación.
- Glucemia plasmática (venosa) basal de 8 h o más ≥126 mg/dl.
- Debe confirmarse con otra determinación.
- Glucemia plasmática (venosa) a las 2 h de la PTGO ≥200 mg/dl.
- Debe confirmarse con otra determinación.
- HbA1c ≥6,5 %. Debe confirmarse con otra determinación.
Para poder considerar GAA y TAG los valores serían los siguientes:
- GAA: glucemia plasmática (venosa) basal ≥100 y
- TAG: glucemia plasmática (venosa) a las 2 h de la PTGO ≥140 y
3. Tratamiento
El paradigma de tratamiento en la DM debe ser multifocal y perseguir determinados objetivos:
- Corregir los valores de glucosa para que se acerquen a la normalidad.
- Prevenir o retrasar el desarrollo de complicaciones.
- Tratar trastornos asociados (dislipemia y HTA).
- Evitar conductas de riesgo (fumar).
- Preservar la calidad de vida del paciente.
3.1 Dieta
Sobre las recomendaciones en la dieta, estas deben consensuarse con el paciente para poder alcanzar un régimen dietético que permita lograr los objetivos. Hay que componer una dieta que mantenga o alcance el peso normal. Se pueden distinguir 3 situaciones:
- DM de tipo 2 con exceso de peso: corregir el peso debe ser lo prioritario; producirá mejoras en la resistencia a la insulina, en el perfil lipídico y en la apnea del sueño. Se propugna reducir la cantidad de hidratos de carbono (menos de 100 g/día) en vez de la de grasas, pero hay que monitorizar la función renal y vigilar la posible cetosis. Así mismo, se deben reducir las grasas saturadas y se debe aumentar la ingesta de fibra.
- DM de tipo 2 con peso normal y reserva insulínica: se podría recomendar una ingesta de principios inmediatos similar a la de la población no diabética, pero se tiende a disminuir los hidratos de carbono y se propugna la dieta mediterránea como la base de alimentación.
- DM insulinopénica: se debe instruir al paciente sobre las cantidades de alimentos que hay que ingerir, ya que deben ir en relación con las dosis de insulina. Se habla de unidades-ración, que pueden ser intercambiadas en función de la comida.
Como consideraciones genéricas se deben mencionar las siguientes:
- El consumo de alcohol debe moderarse debido a su absorción por delante de otros nutrientes (no requiere insulina para ello) y a que en grandes cantidades se puede convertir en grasas, con lo que aumenta el riesgo de cetosis.
- Hay que prestar atención a ciertos productos etiquetados como bajos en azúcar o libres de azúcar, ya que las cantidades calóricas que aportan, fundamentalmente a base de hidratos de carbono (miel, jarabe de maíz) o grasas vegetales saturadas (aceite de coco o palma), podrían elevar las concentraciones de lípidos en sangre.
- Los edulcorantes de tipo natural aportan 4 kcal/g y los artificiales depende del tipo: los polioles (sorbitol, manitol, xilitol…) aportan 2,4 kcal/g y los sintéticos (aspartamo, sacarina, acesulfamo-K, sucralosa, ciclamato…) ninguna.
3.2 Ejercicio
Es un pilar importante en el tratamiento de la diabetes debido a sus efectos hipoglucemiantes (existe mayor captación de la glucosa por parte de las células musculares) y reductores de los factores de riesgo cardiovascular (a nivel lipídico se consiguen elevar las cantidades de lipoproteínas de alta densidad y decrecer las de colesterol y triglicéridos). Se deben tener en cuenta una serie de premisas:
- La recomendación básica (evidencia A) consiste en:
- 150 min a la semana.
- Ejercicios aeróbicos de intensidad moderada (70 % FC máxima).
- Al menos 3 días a la semana.
- En pacientes con factores de riesgo cardiovascular y >30-35 años sería conveniente realizar prueba de esfuerzo previa.
- No realizar ejercicio en ayunas, ni en el pico de acción de fármacos hipoglucemiantes.
- Cuando el paciente esté capacitado, puede ajustar la insulina (no administrar en zonas de roce que incrementarían su absorción) al tipo de ejercicio que realice, así como aportar de manera extra hidratos de carbono.
3.3 Insulina
Principal fármaco empleado en el control de la DM de tipo 1. En la DM de tipo 2 puede ser necesaria cuando el uso de antidiabéticos orales, la dieta y el ejercicio no sean suficientes. Puede clasificarse en función de 2 factores:
- Origen:
- Insulina humana: similar a la humana. Obtenida por ingeniería genética.
- Análogos de insulina: obtenidos por recombinación de ADN (se sustituyen o modifican determinados aminoácidos).
- Farmacocinética (ver tabla 2):
- Rápida (simple o regular): de aspecto transparente, se puede mezclar con otros tipos. Administración s.c. (subcutánea) o i.v.
- Análogos de acción rápida (lispro, aspart y glulisina): efecto más rápido y corto que la rápida. Se puede inyectar justo antes, durante o después de la ingesta. Menor riesgo de hipoglucemia posprandial. Vía s.c. o i.v.
- Acción retardada (NPH y NPL): empleada en control basal de glucemia al poseer liberación más lenta. Vía s.c. Puede mezclarse con rápida.
- Análogos de acción retardada (glargina, detemir, degludec): su objetivo es mantener la insulinemia basal, ayudan a pacientes con riesgo de hipoglucemias (y de predominio nocturno) dado que suelen inyectarse una vez al día. Vía s.c. Se pueden poner junto a otras insulinas, pero no mezclarse con ellas.
- Premezcladas o bifásicas: son mezclas de rápida o análogo de acción rápida con retardadas o análogos de acción retardada con la ventaja de cubrir necesidades basales y prandiales. Existen diversas mezclas. Vía s.c.
Tabla 2
Características de los diferentes tipos de insulinas
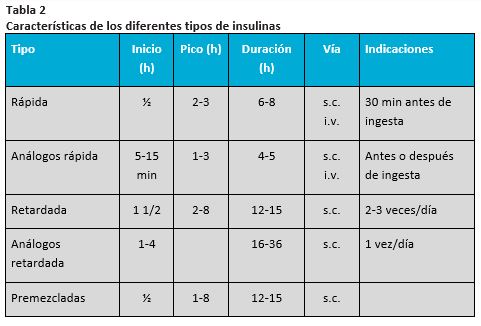
A la hora de manejar la insulina hay una serie de aspectos que conviene tener presentes:
- Zonas de inyección: la absorción varía dependiendo de diversos factores:
- Lugar, de mayor a menor absorción: abdomen, deltoides, muslo, glúteo. Por tanto, insulinas prandiales en zonas de absorción rápida y basales en zonas de absorción lenta.
- Dosis: a mayor dosis, absorción más irregular.
- Riego sanguíneo de la zona: masajear la zona de inyección aumenta la absorción. Por el contrario, la vasoconstricción (tabaco, frío) la reducen.
- Se debe rotar la zona de inyección.
- Conservación y consideraciones sobre la inyección:
- La insulina almacenada debe estar en frío entre 2-8 °C.
- La insulina en uso puede estar a temperatura ambiente (25-30 °C), protegida de luz y calor directo.
- La dosis depende del paciente y de las circunstancias, como base se calcula:
o DM de tipo 1 0,6-0,9 U/kg peso.
o DM de tipo 2 0,3-0,4 U/kg peso.
- Si se mezclan insulinas, cargar primero la rápida.
- Aguja nueva y estéril para cada inyección.
- Tamaño de aguja 6-8 mm para adultos y 4-5 mm para niños.
- Inyectar en tejido celular subcutáneo (no en músculo o en vaso sanguíneo).
- Variar ángulo según zona de inyección (pellizco optativo).
- No sacar la aguja inmediatamente.
- No masajear.
- Se puede inyectar la insulina de 2 maneras:
- Convencional: en DM de tipo 2 suele ser suficiente administrar 1 vez, y si se hiciera en 2 suelen inyectarse ⅔ de la dosis en el desayuno y ⅓ en la cena.
- Intensivo: suele ser de elección en DM de tipo 1. A su vez, puede ser:
o Pauta de inyección múltiple: requiere de 3-4 inyecciones según el control glucémico.
o Bomba de inyección s.c. de insulina: se administra insulina de forma continua, con una dosis basal y bolos previos a comidas. Deben realizarse controles de glucemia.
En ambos métodos es necesaria la monitorización de niveles de glucosa en sangre, y en ese sentido se pueden emplear, o bien dispositivos de tiras reactivas con información puntual, o bien dispositivos de monitorización continua a través de sensores subcutáneos con lecturas a tiempo real.
- El empleo de insulina puede conllevar una serie de efectos secundarios:
- Hipoglucemia: principal complicación, en especial en DM de tipo 1 con tratamiento intensivo. De causa variada (exceso de dosis, cambios en hábitos del paciente —deporte excesivo, baja ingesta de hidratos, etc.—) se trata, si está consciente, con aporte oral de hidratos de carbono (2-3 terrones de azúcar, 150 ml de zumo de naranja) y, si está inconsciente, con glucosa hipertónica i.v. o glucagón i.m. (intramuscular).
- Problemas locales como lipohipertrofia (pequeñas tumoraciones), que altera la absorción de la insulina (se deben rotar las zonas de inyección), o la lipoatrofia (desaparición de tejido celular subcutáneo), que ya es casi inexistente.
- Edema insulínico: edema generalizado presente en pacientes que han recibido corrección insulínica tras descompensación hiperglucémica. Benigno y con resolución pronta y espontánea.
- Hiperglucemia basal persistente, que puede aparecer de dos formas:
- Fenómeno del alba: hiperglucemia matutina secundaria a elevación de glucemia en las últimas horas de la madrugada (cuando nace el sol).
o Causa: elevación de hormonas contrainsulínicas (cortisol, hormona del crecimiento) al amanecer.
o Detección: glucemia entre 2 h y 6 h normal o alta.
o Tratamiento: aumento de dosis de insulina antes de cenar.
- Fenómeno de Somogyi: hiperglucemia matutina de rebote, secundaria a hipoglucemia en la madrugada.
o Detección: glucemia entre 2 h y 6 h baja.
o Tratamiento: reducir dosis de insulina antes de cenar.
3.4 Antidiabéticos orales (ADO)
Aunque se emplean en el tratamiento de la DM de tipo 2, un porcentaje de estos pacientes suelen requerir insulina con el paso del tiempo. Según el mecanismo de acción, los ADO pueden clasificarse en diferentes grupos:
- Secretagogos de insulina: estimulan secreción endógena de insulina. Existen:
a) Sulfonilureas: inducen liberación insulínica. Derivadas de las sulfamidas, las más empleadas son glibenclamida, clorpropamida, glipizida, gliclazida, tolbutamida, gliquidona. Puede presentarse hipoglucemia con su uso. No asociar con alcohol por la posibilidad de presentar efecto Antabus. No deben ser la primera línea de tratamiento.
b) Glinidas: secretagogos de acción rápida. Son la repaglinida y nateglinida. Se administran antes de las comidas. Tendencia a hipoglucemia leve. Escasa repercusión terapéutica.
- Sensibilizadores de la acción de la insulina: mejoran la utilización de la insulina por parte de los tejidos sensibles a ella. Existen:
a) Biguanidas (metformina): favorece el consumo celular de glucosa, disminuye la gluconeogénesis, la glucogenólisis, los triglicéridos y la lipoproteína de baja densidad (LDL, por sus siglas en inglés). Los efectos secundarios más frecuentes son de tipo gastrointestinal, y el más grave (y raro) es la acidosis láctica. Se considera el fármaco de elección en DM de tipo 2 y sobre todo en estados de GAA, ya que reduce la progresión a DM.
b) Glitazonas o tiazolidinedionas: agonistas PPARγ, aumentan la sensibilidad tisular a la insulina. Comercializada la pioglitazona. Sus efectos secundarios incluyen retención hídrica, insuficiencia cardiaca y cáncer de vejiga.
- Modificadores de la absorción de hidratos de carbono: reducen la hidrolisis y la absorción de los hidratos de carbono. Existen:
- Inhibidores de las alfa-glucosidasas (acarbosa y miglitol): al impedir la acción de las alfa-glucosidasas, los hidratos de carbono complejos y disacáridos tardan en ser metabolizados a monosacáridos absorbibles, con lo que disminuye la hiperglucemia postprandial. Efectos secundarios digestivos. En caso de hipoglucemia, emplear glucosa.
- Aumentadores de eliminación renal de glucosa:
a)Inhibidores de la SGLT-2: al bloquear este transportador se produce natriuria y glucosuria. Son la canagliflozina, la empagliflozina y la dapagliflozina. Posible efecto cardiorrenoprotector, y como efecto secundario, cetoacidosis.
- Moduladores de las incretinas: existen dos hormonas incretinas (GIP y GLP-1) que se secretan como respuesta a la ingesta de alimentos, y producen el llamado efecto incretina (respuesta secretora de insulina mayor tras administración oral de glucosa que tras administración intravenosa de esta). Existen dos tipos de fármacos:
a) Inhibidores de la dipeptidil peptidasa 4 (DPP-4): es la enzima metabolizadora de las incretinas, por lo que su bloqueo aumenta la concentración y actividad de estas. Son la sitagliptina, la vildagliptina, la saxagliptina y la linagliptina.
b) Agonistas del receptor de GLP-1: análogos de GLP-1 que impiden su rápida degradación por la DPP-4. Son la exenatida, la liraglutida, la lixisenatida y la exenatida LAR (acción prolongada). De uso s.c. Efectos secundarios a nivel gastrointestinal.
4. Complicaciones agudas
Son fundamentalmente las siguientes:
- Hipoglucemia: complicación más frecuente y principal factor a la hora del manejo de la DM. Según la tríada de Whipple existe hipoglucemia cuando:
- Hay un nivel bajo de glucemia plasmática.
- Hay síntomas clínicos indicativos de hipoglucemia.
- Se produce mejoría de los síntomas al elevarse la glucemia.
Se puede producir por diversas causas: exceso de insulina o ADO, retrasos en la ingesta, ejercicio físico intenso o prolongado y consumo de alcohol. La clínica que se produce cursa con síntomas:
- Adrenérgicos: por activación compensatoria del sistema nervioso simpático (SNS) con ansiedad, inquietud, irritabilidad, taquicardia, palidez, sudoración, náuseas y debilidad.
- Neuroglucopénicos: debido a la falta de glucosa en el sistema nervioso central (SNC). Son cefalea, hambre, lentitud, lenguaje incoherente, alteraciones visuales, somnolencia, confusión, desorientación y convulsiones.
- El tratamiento variará en función de:
- Si está consciente: aportar hidratos de carbono v.o., mejor en forma líquida (zumos, bebidas azucaradas…) y repetir en 15 min si persisten los síntomas.
- Si está inconsciente: no usar la v.o. y administrar glucagón i.m. o s.c. o solución hipertónica de glucosa i.v. La mejor prevención es un buen control con ajuste de dieta y medicación.
- Cetoacidosis diabética (CAD): complicación hiperglucémica más frecuente en DM de tipo 1. Puede darse debido a omisiones del tratamiento con insulina o ADO, al ayuno, a enfermedades intercurrentes (sobre todo infecciones) y a fármacos como los glucocorticoides. La no disponibilidad de insulina conlleva hiperglucemia, y una activación de lipólisis y cetogénesis que acaba desembocando en acidosis metabólica.
Las manifestaciones clínicas comprenden náuseas, vómitos y dolor abdominal (debidos a los cuerpos cetónicos), deshidratación e hipotensión, poliuria, polidipsia, fetor cetósico (olor a manzanas) y respiración de Kussmaul (respiraciones profundas y rápidas para compensar el exceso de ácidos).
Entre los datos de laboratorio destacan hiperglucemia, cetonemia (cuyos valores se clasifican mmol/l, de forma que <0,6 es normal, entre 0,6 y 1,0 ligeramente elevado, 1,1 y 3,0 riesgo de cetoacidosis y >3 se debe acudir a Urgencias), cetonuria, acidosis metabólica, hiponatremia e hiperpotasemia.
En el tratamiento es básica la reposición hídrica: comenzar con sueros salinos para pasar a glucosados cuando las glucemias sean
- Síndrome hiperglucémico hiperosmolar: complicación hiperglucémica más frecuente en DM de tipo 2, sobre todo en ancianos. En este caso no hay acidosis ni cetosis, pues sí hay insulina. La causa subyacente es una deshidratación profunda que puede obedecer o estar asociada a infección intercurrente, a enfermedades cuyos vómitos y diarreas sean marcados o a ingestas insuficientes de líquidos.
Se caracteriza por presentar hiperglucemia elevada (>600 mg/dl), hiperosmolaridad (>350 mmol/l) y sin cetoacidosis. Suele cursar de manera insidiosa con poliuria, deshidratación y alteraciones neurológicas (desde el estupor al coma).
El tratamiento consiste en reponer líquidos, administrar insulina y potasio junto a heparina para prevenir eventos trombóticos. Tiene peor pronóstico que la CAD y mortalidad entre un 5-20 %.
5. Complicaciones crónicas
Representan la principal causa de morbimortalidad en la DM. Dependiendo del tiempo de evolución de la DM, y de su control, las complicaciones crónicas serán más o menos graves. El endotelio vascular es el sustrato más afectado por la hiperglucemia; se pueden diferenciar 2 grandes grupos:
- Microangiopatía diabética: la afectación se produce en capilares esenciales para la función del órgano. Son de especial relevancia:
a) Retinopatía diabética: es la primera causa de ceguera en países occidentales. Más frecuente en DM de tipo 1, en diagnósticos tardíos de DM de tipo 2 no es infrecuente observar daño retiniano. Su presencia implica mayor probabilidad de complicaciones cardiovasculares.
Evoluciona desde una fase no proliferativa (existen pequeños microaneurismas y hemorragias, con posterior edema macular) hacia una proliferativa (con neoangiogénesis con tendencia al sangrado y posibilidad de hemovítreo y desprendimiento de retina).
Se deben hacer controles oculares que incluyan revisión de fondo de ojo.
Las lesiones se tratan con fotocoagulación.
b) Nefropatía diabética: representa la principal causa de muerte en la microangiopatía diabética, y es factor de riesgo para complicaciones cardiovasculares. Su clínica incluye la tríada: proteinuria, HTA y deterioro progresivo de la función renal. Se clasifica en 5 estadios:
- Hiperfiltración.
- Silente.
- Lesión inicial (albuminuria elevada, antes microalbuminuria).
- Lesión progresiva (albuminuria muy alta, antes macroalbuminuria).
- Insuficiencia renal crónica establecida (ERC).
La prueba analítica de diagnóstico y seguimiento clásica era la determinación de albuminuria en orina de 24 h, pero cada vez más se emplea la relación albúmina-creatinina (RAC) en orina de primera hora de la mañana.
Hay que controlar la glucemia y la TA para evitar la progresión a ERC.
c) Neuropatía diabética: se debe a una degeneración axonal y desmielinización (neuropatía mixta). Es una enfermedad heterogénea con distintas presentaciones clínicas, de las que la más frecuente es la polineuropatía simétrica distal con hipoestesias y parestesias (distribuciones en guante o calcetín) además de dolor y trastornos motores.
- Macroangiopatía diabética: la afectación endotelial se localiza a nivel de arterias de mayor tamaño que irrigan órganos vitales como corazón o cerebro.
Entre las afecciones principales cabe destacar el accidente cerebrovascular, la enfermedad vascular periférica y la enfermedad arterial coronaria, que a su vez es la principal causa de mortalidad en la DM (síntomas de infarto como el dolor pueden enmascararse en pacientes diabéticos).
Se deben controlar la TA y la glucemia, así como los factores de riesgo asociados.
- Mixta: se considera pie diabético aquel que presenta una alteración anatómica o funcional causada por anomalías neurológicas y/o ciertos grados de enfermedad vascular periférica en diabéticos, y que supone mayor riesgo de padecer infección, ulceración o destrucción de tejidos profundos.
La valoración de la sensibilidad neurológica se realiza mediante el monofilamento de Semmes-Weisntein aplicando presión en 3 puntos plantares de cada pie (falange distal del 1.er dedo, base del 1.er y 5.º metatarsiano) y la vascular con la presencia de pulsos distales y el índice tobillo-brazo.
Las úlceras suelen generarse por determinados traumatismos menores repetidos, como uso de calzado inapropiado, caminar descalzo, o cambios en los apoyos que propicien la aparición de callos que sangren subcutáneamente y den lugar a una úlcera plantar. Existen varias formas de clasificar las úlceras, entre las que destaca la úlcera de Wagner:
- Grado 0: sin úlcera, pie de riesgo.
- Grado 1: úlcera superficial.
- Grado 2: úlcera profunda.
- Grado 3: úlcera aún más profunda, absceso.
- Grado 4: gangrena limitada.
- Grado 5: gangrena extensa.
Es básica la prevención de aparición de lesiones, y se debe recomendar:
- Inspección ocular diaria con palpación de pulsos.
- Higiene diaria con agua templada, sin inmersión prolongada, y con secado (sin frotar) que incluya espacios interdigitales.
- Cortar las uñas en forma recta.
- No usar fuentes de calor como braseros, estufas o bolsa de agua.
- Usar calzado adecuado: cómodo, ancho sin ser excesivo, sin costuras internas, flexible y transpirable. Comprarlo al final del día. No ir descalzo. Usar con calcetines y cambiar estos a diario.
- No autotratar callos y durezas, revisión por podólogo.
BIBLIOGRAFÍA
- Berman A, Snyder S. Kozier y Erb. Fundamentos de enfermería. Madrid: Pearson Educación; 2013.
- Domarus A, Farreras Valentí P, Rozman C, Cardellach López F. Medicina interna. Barcelona: Elsevier; 2020.
- Hinkle J, Cheever K. Brunner y Suddarth. Enfermería medicoquirúrgica. 14 ed. Barcelona: Wolters Kluwer; 2019.
- Berman A, Snyder S. Kozier y Erb. Fundamentos de enfermería. Madrid: Pearson Educación; 2013.
- Domarus A, Farreras Valentí P, Rozman C, Cardellach López F. Medicina interna. Barcelona: Elsevier; 2020.
- Hinkle J, Cheever K. Brunner y Suddarth. Enfermería medicoquirúrgica. 14. ed. Barcelona: Wolters Kluwer; 2019.
