La intervención quirúrgica que da lugar al trasplante renal no es sino la piedra de toque a partir de la cual debe construirse un ambiente propicio para la homeostasis entre receptor e injerto. Para ello, no solo la operación debe haber salido con éxito, sino que requiere un seguimiento postquirúrgico en el largo plazo, basado en el manejo de una medicación inmunosupresora específica y la detección precoz de complicaciones. A lo largo de este capítulo comentaremos los aspectos más relevantes de dicho seguimiento.
4.1 Rechazo del injerto
El rechazo del injerto ocurre principalmente debido a una respuesta inmunitaria celular dirigida contra los antígenos presentes en las células del trasplante, especialmente las moléculas del HLA, como vimos atrás en uno de los capítulos iniciales donde comentamos la afinidad entre donante y receptor.
De entre todas las células y elementos del sistema inmunitario que intervienen en la respuesta contra el injerto, los linfocitos T son las células prioritarias en el establecimiento del rechazo. Estas células pueden reconocer de forma directa (a través de células dendríticas, que presentan los antígenos a células efectoras linfocitos CD8+) o indirecta (mediante macrófagos, que presentan los fragmentos de HLA de las células del donante a linfocitos moduladores CD4+, amplificando la respuesta inmunitaria), por lo que el papel de los fármacos inmunosupresores estará focalizado en la inhibición de sus vías de actuación.
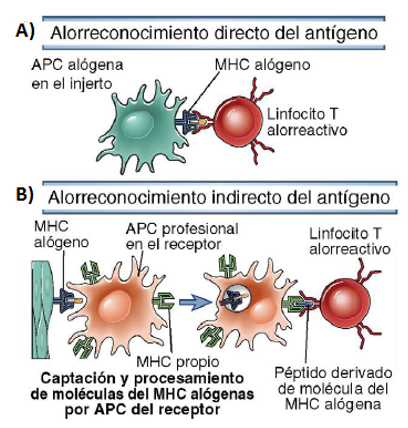
Ilustración 42: Reconocimiento y sensibilización de linfocitos T tras presentación de antígenos procedentes del injerto. A) Reconocimiento directo; B) Reconocimiento indirecto. Fuente: Inmunología celular y molecular. Abbas AK et al, 2009
Tras esta primera fase sensibilizadora, se produce la respuesta inmunitaria, en la que tanto linfocitos T como el resto de células y elementos del sistema inmunitario (anticuerpos, sistema de complemento…) atacan al injerto, pudiendo provocar rechazo en el mismo.
En la siguiente imagen se observa cómo a partir de la presentación de antígenos por una célula especializada, los linfocitos T colaboradores (CD4+) amplifican la señal a través de las distintas interleucinas proinflamatorias, facilitando la llegada de elementos citotóxicos que, en primer lugar, atacan la membrana externa y, posteriormente, logran infiltrar el riñón, provocando la destrucción del parénquima en el medio-largo plazo.
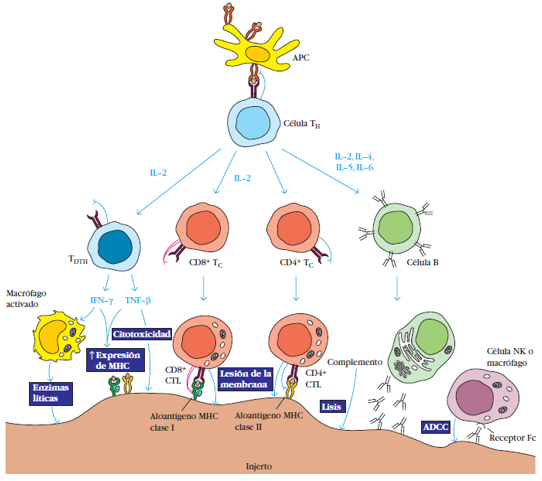
Ilustración 43: Mecanismos efectores que participan en el rechazo del injerto. ADCC: células dependientes de anticuerpo. Fuente: Inmunología de Kuby. Kindt T et al, 2007
4.1.1 Tipos de rechazo
Así, el rechazo del injerto renal es una de las principales complicaciones tras un trasplante y ocurre cuando el sistema inmunológico del receptor reconoce los aloantígenos del donante como extraños, activando una respuesta inmune que puede comprometer la función y viabilidad del órgano trasplantado. Dependiendo del mecanismo inmunológico implicado y las características histopatológicas, el rechazo se clasifica en tres tipos principales: hiperagudo, agudo y crónico.
Rechazo hiperagudo
El rechazo hiperagudo ocurre minutos u horas después del trasplante y se caracteriza por una oclusión trombótica de los vasos del injerto, causada por anticuerpos preexistentes en el receptor que se unen a los antígenos endoteliales del donante. Esta unión activa el complemento, promoviendo la lesión endotelial, la agregación plaquetaria y la activación de la coagulación, lo que conduce a una isquemia irreversible del injerto.
Inicialmente, estos anticuerpos son IgM naturales, generados en respuesta a antígenos bacterianos y responsables del rechazo mediado por incompatibilidad ABO, aunque este es raro gracias a la compatibilización previa de donante y receptor. Actualmente, el rechazo hiperagudo es más comúnmente mediado por anticuerpos IgG dirigidos contra moléculas del HLA del donante, adquiridos por transfusiones, embarazos o trasplantes previos.
Si el nivel de anticuerpos es bajo, el rechazo puede desarrollarse en varios días, denominándose rechazo acelerado, puesto que el inicio es más temprano que el rechazo agudo que ahora veremos.
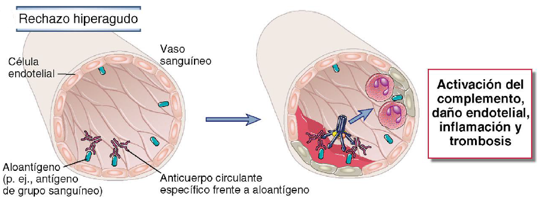
Ilustración 44: Mecanismo de rechazo hiperagudo. Fuente: Inmunología celular y molecular. Abbas AK et al, 2009
Rechazo agudo
El rechazo agudo es un proceso de lesión del parénquima del injerto y de los vasos sanguíneos mediado por los linfocitos T y los anticuerpos alorreactivos. Puede ocurrir desde los primeros días hasta varios meses postrasplante y es el tipo más común en la práctica clínica. Se debe a la activación de la inmunidad adaptativa del receptor contra los antígenos del injerto, pudiendo ser mediado por células T (rechazo celular) o por anticuerpos (rechazo humoral).
- Rechazo agudo celular: El rechazo agudo celular es mediado principalmente por linfocitos T citotóxicos (CTL CD8+), que atacan y destruyen las células del injerto. Como veremos más adelante cuando hablemos de la biopsia del injerto renal, en el estudio histológico se observa un infiltrado linfocitario que invade y daña los tejidos trasplantados. La presencia de perforina y granzima B, moléculas clave en la citotoxicidad de los CTL, es un marcador sensible del rechazo agudo. Además de la citotoxicidad directa, los linfocitos T CD4+ liberan citoquinas proinflamatorias, promoviendo la activación de otras células inmunitarias que amplifican el daño. Además, las células endoteliales son las principales dianas, y el rechazo suele manifestarse con endotelitis microvascular y arteritis de la íntima en la arteria renal, señales de un rechazo grave que, si no se trata, puede provocar el fracaso agudo del injerto.
- Rechazo agudo humoral: El rechazo agudo humoral es mediado por anticuerpos dirigidos principalmente contra moléculas HLA en las células endoteliales vasculares del injerto. Estos anticuerpos desencadenan lesión endotelial, activación del complemento y formación de trombos, lo que compromete la perfusión y provoca la destrucción del injerto. Histológicamente, se caracteriza por necrosis de la pared vascular con inflamación aguda, a diferencia del rechazo hiperagudo, que presenta trombosis sin necrosis. Un marcador clave en el diagnóstico es la presencia de C4d en los capilares del injerto, indicador de activación del complemento. Sin embargo, en algunos casos, el daño endotelial ocurre independientemente del complemento, por lo que no se detecta C4d en la biopsia.
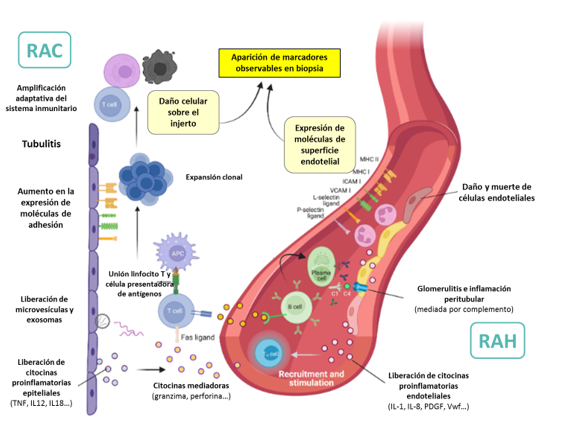
Ilustración 45: Mecanismos fisiopatológicos del rechazo agudo celular (RAC) y humoral (RAH). Fuente: modificado de Chancharoenthana W et al. 2023. Disponible en: doi.org/10.3389/fimmu.2023.1206929
Rechazo crónico
Se desarrolla de forma progresiva en meses o años y es la principal causa de pérdida tardía del injerto. Su lesión dominante es la oclusión arterial progresiva debido a la proliferación de células musculares lisas en la íntima, lo que provoca isquemia y fibrosis intersticial. En el riñón, este proceso se conoce como vasculopatía del injerto, y conlleva el deterioro gradual de la función renal.
Los mecanismos involucrados incluyen la activación de linfocitos T, la secreción de citocinas, la reparación fibrótica tras brotes repetidos de rechazo y factores no inmunológicos como isquemia perioperatoria, toxicidad inmunosupresora e infecciones virales crónicas.

Ilustración 46: Mecanismo de rechazo crónico. Fuente: Inmunología celular y molecular. Abbas AK et al, 2009
4.1.2 Biopsia renal
Como ya vimos en capítulos anteriores, la biopsia renal constituye uno de los métodos diagnósticos de elección más utilizados no solo de patología renal en general, sino también de rechazo de trasplante. Sin embargo, a pesar de tratarse de un procedimiento seguro, conlleva ciertos riesgos, por lo que su indicación debe cumplir condiciones específicas.
Antes de realizarla, se deben agotar métodos no invasivos, asegurarse de que su resultado proporcionará un diagnóstico preciso y útil para el tratamiento y garantizar un análisis por un patólogo experto con técnicas avanzadas. Por tanto, no debe realizarse sin relevancia clínica o con fines meramente docentes.
La indicación de biopsia se da en casos de aumento inexplicado de creatinina, función retardada del injerto, ausencia de recuperación funcional en los primeros 1-2 meses y presencia de proteinuria nueva o inexplicada. Además, la biopsia de protocolo es útil en el primer año post trasplante para detectar daño inmunológico subclínico y optimizar la terapia inmunosupresora, mejorando la supervivencia del injerto.
Preparación y procedimiento
Antes de realizar la biopsia, es fundamental evaluar las condiciones clínicas del paciente para minimizar riesgos. Se debe verificar que el paciente no presente alteraciones de la coagulación, ya que la biopsia puede aumentar el riesgo de sangrado. Para ello, se requiere: suspender antiagregantes plaquetarios (aspirina, clopidogrel) 5-7 días antes, o anticoagulantes orales como warfarina o heparina según protocolos específicos, así como realizar pruebas de coagulación (TP, INR, TTPa, recuento plaquetario…). Debe evaluarse la función renal y la presencia de hipertensión no controlada, puesto que puede aumentar el riesgo de complicaciones. Además, se debe informar al paciente sobre el procedimiento, sus riesgos y beneficios, obteniendo su consentimiento informado.
La biopsia renal se realiza generalmente bajo control ecográfico para guiar la punción y reducir complicaciones. El procedimiento se desarrolla en los siguientes pasos:
Posicionamiento del paciente: Si bien es cierto que en caso de riñón nativo el paciente se coloca en decúbito prono, en caso de biopsia de injerto renal, el paciente se posiciona en decúbito supino, ya que el injerto se encuentra en la fosa ilíaca.
- Localización del riñón: Se emplea ecografía Doppler para identificar la estructura renal, la vascularización y el punto de punción óptimo.
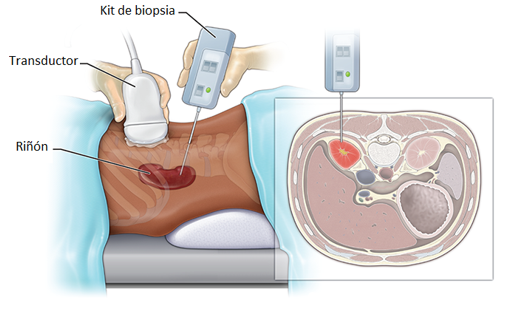
Ilustración 47: Biopsia renal. Localización ecográfica. Fuente: Temple Health, 2021. Fuente: https://www.templehealth.org/services/transplant/kidney-transplant/rejection
- Asepsia y anestesia: Se desinfecta la piel con antiséptico y se infiltra anestesia local en el área de punción.
- Punción y obtención de la muestra: Se introduce una aguja de biopsia tipo Monoptype a través de la piel hasta el riñón, guiándose con ecografía. Las sondas ecográficas con adaptador para la aguja permiten la visualización del riñón en tiempo real y permite guiar la progresión de la aguja, consiguiendo un ángulo entre 50-70º de la aguja respecto a la cortical para obtener material suficiente con un riesgo más bajo de complicaciones. Se extraen 1-2 cilindros de tejido renal, procurando que incluyan glomérulos para un estudio adecuado. No se recomienda la punción a ciegas.
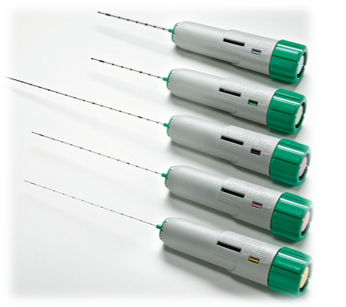
Ilustración 48: Agujas Monopty. Fuente: https://www.bd.com/en-ca/products-and-solutions/products/product-page.121820
- Verificación de la muestra: Se evalúa macroscópicamente para confirmar la presencia de tejido renal adecuado. Debe contener, al menos, 50 túbulos renales para ser significativo. Si es necesario, se obtiene una muestra adicional.
Tras el procedimiento, se aplica presión local sobre el sitio de punción para minimizar el riesgo de sangrado (15-20 minutos). Además, es necesario monitorizar (si no está en intensivos, controles cada 15-30 minutos) la presión arterial, frecuencia cardiaca y signos de hemorragia durante, al menos 6 horas, aunque ciertas guías aconsejan alargar hasta las 24 horas (cuando el paciente acude de forma ambulatoria y no hay sintomatología asociada puede hacerse durante un turno de trabajo, pero al tratarse de un posible rechazo renal el control es más estrecho). Se aconseja reposo absoluto en cama durante este periodo, fomentando la hemostasia de la zona puncionada.
Complicaciones derivadas
Aunque la biopsia renal es un procedimiento seguro, presenta complicaciones en un 6-8% de los casos, con eventos mayores (descenso significativo de hemoglobina y necesidad de transfusión) en un 1-3% y menores en un 2-7%. La mortalidad es baja (0,02-0,1%).
Entre las complicaciones a destacar encontramos:
- Hematuria macroscópica: Hasta en un 12%, generalmente autolimitada, pero en casos graves puede provocar coágulos y obstrucción urinaria.
- Hematoma retroperitoneal: Puede generar anemia e hipotensión arterial. Se diagnostica con ecografía y puede requerir embolización selectiva.
- Taponamiento renal (riñón de Page): Acumulación de sangre en la cápsula renal con activación del sistema renina-angiotensina, causando hipertensión arterial.
- Fístula arteriovenosa: ocurre de manera mucho más frecuente a la imaginada, pero su resolución es espontánea en la mayoría de los casos y no supone efectos adversos sobre el paciente. Cuando son de mayor entidad pueden generar hematuria e hipotensión.
- Otras: aunque en mucha menor prevalencia, la punción de otros órganos como hígado, pulmón, páncreas o intestino (en función de la localización del injerto) podría darse. No hay que descartar el desarrollo de infecciones pues, aunque la punción se realiza mediante técnica estéril, en la práctica puede haber errores en la realización.
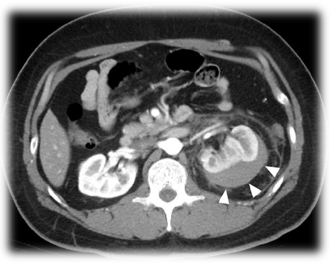
Ilustración 49: Riñón de Page. Las flechas muestran el evidente hematoma que se observa en el riñón derecho en esta imagen de tomografía. Fuente: Teruya H et al, 2020. Disponible en: https://www.ccjm.org/content/87/5/271
Anatomía patológica
Una vez obtenida la muestra por biopsia renal, es necesario analizarla mediante técnicas de histología que permitan dilucidar la presencia de lesiones o eventos negativos en el riñón, no solo en caso de rechazo, sino también pretrasplante procedente del donante.
Durante el apartado anterior no hemos precisado la técnica de extracción del donante, puesto que la única puntualización es que se realiza en el momento de la extracción cuando es cadavérico; en caso de donante vivo, sigue los mismos pasos que los ya descritos con la consideración de que, al estar en la zona anatómica nativa, la punción se realiza en decúbito contralateral al riñón a evaluar.
- Valoración del rechazo - Clasificación de Banff: La clasificación de Banff es un sistema de consenso internacional para la evaluación de biopsias de injertos de órganos sólidos, con un enfoque inicial en los trasplantes renales. Fue desarrollada en 1991 en Banff, Alberta, Canadá, por un grupo de patólogos y clínicos de trasplante liderados por Kim Solez y Lorraine Racusen. Desde entonces, se ha revisado y actualizado cada dos años en conferencias internacionales, incorporando nuevos conocimientos y tecnologías emergentes.
La clasificación de Banff proporciona criterios estandarizados para el diagnóstico de rechazo de injertos renales, incluyendo el rechazo mediado por células T (TCMR) y el rechazo mediado por anticuerpos (ABMR). Los criterios incluyen la evaluación de lesiones histológicas específicas, como la tubulitis, la arteritis, la inflamación intersticial, y la presencia de anticuerpos específicos del donante (DSA). En la siguiente tabla se muestran los criterios posteriormente utilizados para otras distintas clasificaciones.
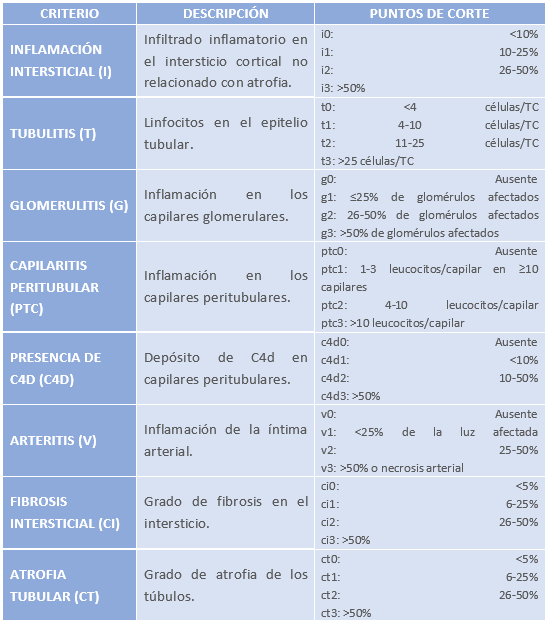

Tabla 9: Criterios de lesión de distintas estructuras renales según clasificación de Banff
Tras el estadiaje a partir de la histología de las muestras obtenidas, es posible definir no solo el rechazo agudo, sino también el rechazo crónico y las lesiones asociadas a infecciones virales como la nefropatía por poliomavirus BK. A grandes rasgos, la clasificación de Banff divide los distintos tipos de rechazo en:
- Rechazo celular agudo mediado por linfocitos T (TCMR): Se caracteriza por infiltración de linfocitos T en el injerto y daño tisular. Se clasifica en:
- Grado IA: Infiltración de linfocitos en el intersticio renal con tubulitis leve (1-4 linfocitos por túbulo).
- Grado IB: Tubulitis moderada-severa (>4 linfocitos por túbulo).
- Grado II (Rechazo Vascular): Compromiso de las arterias renales. - IIA: Arteritis de la íntima (inflamación en la pared de las arterias).
- IIB: Arteritis más severa con inflamación transmural.
- Grado III (Rechazo Necrotizante): Necrosis fibrinoide de la pared arterial con inflamación intensa. - Rechazo agudo mediado por anticuerpos (ABMR): Implica la presencia de anticuerpos donante-específicos (DSA) y daño endotelial mediado por el complemento. Se diagnostica no solo por la evidencia histológica de inflamación en distintas estructuras (endotelio, glomérulo, capilares peritubulares…) y presencia de la proteína CD4 del complemento, sino también por la presencia de anticuerpos contra el donante del receptor. Clasifica a grandes rasgos:
- ABMR Agudo Activo: Daño activo con inflamación.
- ABMR Crónico Activo: Fibrosis y atrofia progresiva del injerto.
- ABMR Crónico Inactivo: Cambios fibróticos sin signos de inflamación aguda. - Otras categorías de clasificación Banff: valora la presencia de cambios llamados “borderline” (indeterminados) donde aparece inflamación leve sin criterios claros de rechazo, así como lesiones crónicas no inmunológicas (nefropatía crónica del injerto, atribuida a daño isquémico o toxicidad por fármacos, entre otras).
Debido a la complejidad y constante actualización del tema en cuestión, se emplaza al estudiante al seguimiento de posibles cambios y mejoras del conocimiento en la página de la Fundación Banff: https://banfffoundation.org/, así como al trabajo de Roufosse C y colaboradores en el que hacen una profunda revisión del tema, con imágenes histológicas asociadas, y al que se puede acceder libremente a partir del siguiente enlace: https://journals.lww.com/transplantjournal/fulltext/2018/11000/a_2018_reference_guide_to_the_banff_classification.14.aspx.
4.2 Fármacos inmunosupresores
Tras recibir un trasplante renal, el cuerpo del paciente reacciona ante el nuevo órgano como si fuera un elemento extraño, activando su sistema inmunológico en un intento de rechazarlo. Para evitar este proceso, es necesario administrar un tratamiento inmunosupresor que permita modular la respuesta del organismo, manteniendo un equilibrio entre la protección del injerto y la preservación de las defensas naturales del paciente.
El desafío principal de la terapia inmunosupresora radica en lograr una inhibición efectiva del sistema inmunológico sin aumentar en exceso el riesgo de infecciones oportunistas, neoplasias o efectos adversos graves. Aunque se han desarrollado múltiples combinaciones de fármacos para este propósito, aún no existe un consenso universal sobre cuál es la mejor estrategia terapéutica. Cada paciente requiere un enfoque individualizado, considerando la eficacia y toxicidad potencial de los diferentes tratamientos.
El uso de inmunosupresores ha permitido mejorar significativamente la supervivencia del injerto, inhibiendo la respuesta inmunitaria adaptativa en distintos niveles. Para minimizar los efectos adversos, muchas unidades de trasplante han optado por estrategias de combinación de fármacos, lo que permite reducir la dosis de cada uno y disminuir su toxicidad global.
En los últimos años, han surgido estrategias de "minimización" inmunosupresora, con el objetivo de reducir la carga medicamentosa y sus efectos secundarios. No obstante, todavía no se puede predecir con certeza qué pacientes pueden beneficiarse de estas estrategias sin poner en riesgo la viabilidad del injerto. Por ello, se están desarrollando líneas de investigación centradas en biomarcadores que permitan identificar con seguridad a aquellos pacientes que podrían requerir menores dosis sin comprometer la función renal trasplantada.
Para entender el mecanismo de acción de los fármacos inmunosupresores es imprescindible conocer el papel de los linfocitos T en el rechazo del injerto. La respuesta inmunitaria mediada por linfocitos T contra el injerto implica la activación de linfocitos T vírgenes y de memoria, algunos de los cuales pueden haber sido estimulados previamente por antígenos virales que reaccionan de forma cruzada con los antígenos HLA del donante.
Las células dendríticas (células presentadoras de antígenos) del donante y del receptor desempeñan un papel clave al captar y presentar los aloantígenos en los órganos linfoides secundarios, donde activan a los linfocitos T específicos del injerto. La activación ocurre mediante tres señales:
- Señal 1: La interacción entre los antígenos presentados por las células dendríticas y los receptores de los linfocitos T (TCR) a través del complejo CD3.
- Señal 2: La coestimulación mediante la interacción entre CD80/CD86 de las células dendríticas y CD28 de los linfocitos T.
- Señal 3: La activación por citocinas, como la interleucina-2 (IL-2), que desencadena la proliferación de los linfocitos T mediante la vía de mTOR.
Esta activación genera una expansión clonal (proliferación) de linfocitos T efectores que atacan el injerto. Además, los linfocitos B también se activan, produciendo anticuerpos contra los antígenos HLA del donante, lo que contribuye al rechazo.
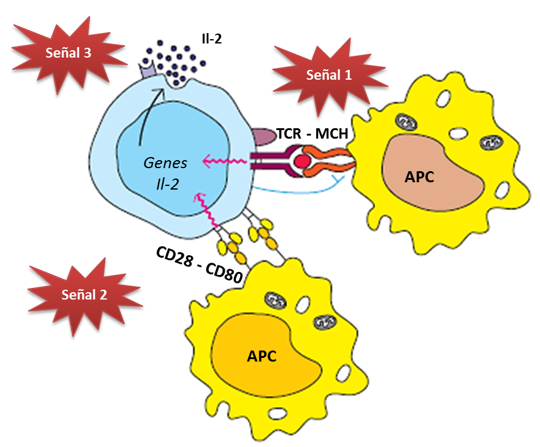
Ilustración 50: Activación de linfocitos T mediante las tres señales. APC: Célula presentadora de antígenos. Señal 1: Unión TCR (Linfocito T) y B7 (APC); Señal 2: Unión CD28 (linfocito T) y CD80 (APC); Señal 3: producción de Il-2 y estimulación de respuesta pro-inflamatoria. Fuente: modificado de Inmunología de Kuby. Kindt T et al, 2007
Son muchos los fármacos inmunosupresores destinados a la prevención del rechazo en el trasplante renal. A grandes rasgos, podemos dividirlos en moléculas pequeñas y agentes biológicos.
4.2.1 Pequeñas Moléculas
- Corticosteroides: como la prednisona y la metilprednisolona. Son componentes esenciales de la inmunosupresión en el trasplante renal. Actúan mediante la modulación de la transcripción génica en linfocitos y macrófagos, inhibiendo la expresión de citoquinas proinflamatorias como IL-1, IL-6 y TNF-α. Además, su administración en altas dosis puede inducir apoptosis de linfocitos T.
- Antimetabolitos: los antimetabolitos son fármacos que se usan comúnmente para interferir la síntesis de ADN y, de este modo, la proliferación celular. En ocasiones pueden ser utilizados como agente antibióticos o antivirales, pues su estructura química les asemeja a nucleótidos, pero sin capacidad de alargamiento de la cadena de ADN, por lo que -como decimos- inhiben su síntesis. Los más importantes son:
- Azatioprina: Análogo de purinas que inhibe la síntesis de ADN y la proliferación linfocitaria, disminuyendo la respuesta inmune.
- Micofenolato mofetil (MMF) y micofenolato sódico: Inhiben la inosina monofosfato deshidrogenasa, impidiendo la síntesis de guanosina en los linfocitos, lo que reduce su proliferación y activación. - Inhibidores de la calcineurina (CNI): La calcineurina es una fosfatasa proteica dependiente de calcio y calmodulina que desempeña un papel clave en la activación de los linfocitos T. Su principal función es desfosforilar el factor nuclear de células T activadas (NFAT), lo que permitiendo la transcripción de genes proinflamatorios, especialmente la interleucina-2 (IL-2), crucial para la proliferación y diferenciación de los linfocitos T, facilitando la respuesta inmune adaptativa. En el contexto del trasplante renal, la inhibición de la calcineurina impide la activación de NFAT y, por tanto, la producción de IL-2, reduciendo la respuesta inmune y previniendo el rechazo del injerto. Los dos más importantes son:
- Ciclosporina A (CsA): Peptído cíclico lipofílico que se une a la ciclofilina, bloqueando la actividad de la calcineurina y evitando la transcripción de IL-2.
- Tacrolimus (TAC): Macrólido que se une a FKBP-12, inhibiendo la calcineurina y reduciendo la proliferación de linfocitos T. Presenta mayor potencia inmunosupresora y menor nefrotoxicidad que CsA. - Inhibidores de mTOR: mTOR (mammalian target of rapamycin) es una quinasa clave en la regulación del crecimiento celular, la proliferación y la supervivencia. En el contexto del sistema inmunológico, mTOR juega un papel fundamental en la activación del sistema inmunitario, aumentando la producción de citoquinas proinflamatorias, y permitiendo la regulación y expansión de linfocitos T, así como su diferenciación hacia células más maduras. Los fármacos inhibidores de mTOR actúan bloqueando dicha proliferación. Los más conocidos son:
- Sirolimus (SRL) y Everolimus (EVL): Se unen a FKBP-12 y bloquean la vía de mTOR, impidiendo la transición del ciclo celular de G1 a S en linfocitos T. Se asocian con menor nefrotoxicidad en comparación con los CNI.
4.2.2 Agentes biológicos
- Globulina antitimocítica (ATG): la ATG, comúnmente conocida como timoglobulina, derivada de sueros de conejos inmunizados contra timocitos humanos, produce depleción masiva de linfocitos T, reduce la capacidad de maduración de células dendríticas y de migración de linfocitos y monocitos, y regula la respuesta inmune en la fase de inducción del trasplante renal. ATG es una de las estrategias más efectivas para la inmunosupresión tanto en la inducción en receptores de alto riesgo inmunológico como en el tratamiento del rechazo.
- Inmunoglobulina intravenosa (IGIV): Compuesta por inmunoglobulinas humanas. Ejercen un efecto inmunomodulador mediante la regulación de receptores Fc (fracción común de anticuerpos), la neutralización de autoanticuerpos y la inhibición de la activación del complemento.
- Bloqueadores de la coestimulación: como hemos visto anteriormente, tras el reconocimiento de antígenos de linfocitos T mediante su receptor (TCR), es imprescindible que se produzca una coestimulación entre su proteína CD28 y la CD80/86 de las células presentadoras de antígeno para que se transcriban los genes de citoquinas proinflamatorias y se amplifique la respuesta inmunitaria. Los inhibidores de esta segunda señal (unión CD28-CD80/86) provocan que esta no se produzca, deprimiendo la actividad de dichos linfocitos T. El representante más conocido de los fármacos inmunosupresores de esta categoría es el belatacept.
- Bortezomib: se trata de un inhibidor del proteasoma en células plasmáticas (linfocitos B maduros encargados de la producción de anticuerpos), bloqueando la degradación de proteínas reguladoras de la apoptosis, lo que provoca la apoptosis de las células productoras de anticuerpos. Se utiliza en casos de rechazo humoral refractario o desensibilización previa al trasplante en pacientes con anticuerpos preformados contra el injerto.
- Anticuerpos monoclonales: son proteínas diseñadas para unirse a dianas específicas del sistema inmunológico, modulando su función. En el contexto del trasplante renal, los anticuerpos monoclonales se utilizan para bloquear la activación de linfocitos (no solo los T, sino también los B), inducir su eliminación o modular señales inmunológicas clave, reduciendo así el riesgo de rechazo del injerto. Entre los más conocidos encontramos:
- Basiliximab: Anticuerpo monoclonal contra la subunidad α del receptor de IL-2 (CD25), bloqueando la activación de linfocitos T.
- Alemtuzumab: Se une a CD52 en linfocitos T y B, induciendo su eliminación por citotoxicidad mediada por complemento (CMC) y apoptosis.
- Rituximab: Anticuerpo contra CD20 que media la depleción de linfocitos B, utilizado en rechazo mediado por anticuerpos. Uso habitual en la preparación del trasplante renal en presencia de incompatibilidad AB0.
- Tocilizumab: Antagoniza el receptor de IL-6, modulando la inflamación en el rechazo crónico.
- Eculizumab: es un anticuerpo monoclonal anti-C5, que impide la escisión de C5 en C5a y C5b, bloqueando la formación del complejo de ataque a la membrana que permite la perforación de la membrana celular. Al inhibir la activación terminal del sistema del complemento, previene el daño endotelial y la inflamación en el injerto. Se ha utilizado con éxito en casos de rechazo mediado por anticuerpos (AMR) agudo severo, particularmente en pacientes con alto riesgo de daño mediado por complemento.
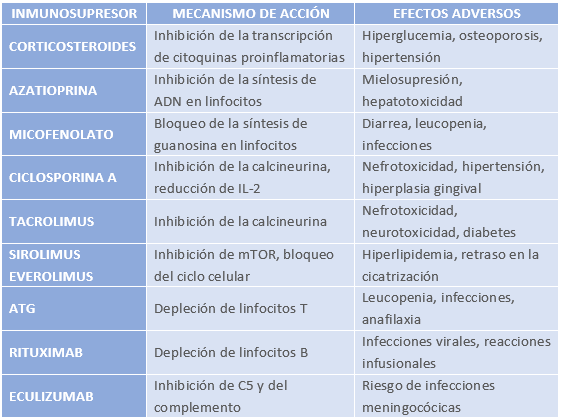
Tabla 10: Resumen de inmunosupresores más habituales usados en trasplante renal
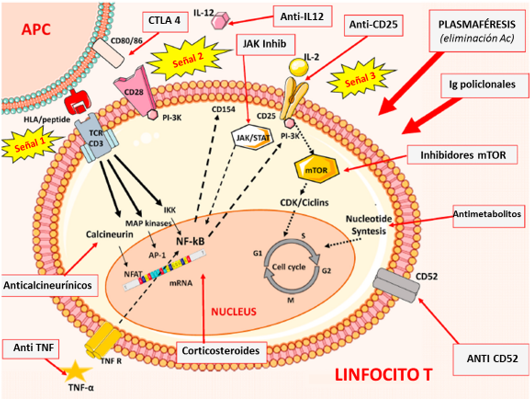
Ilustración 51: Dianas terapéuticas contra las que se diseñan los distintos fármacos inmunosupresores. Fuente: modificado de Meneghini M et al. 2021; disponible en: https://doi.org/10.1016/j.bpg.2021.101757
4.2.3 Plasmaféresis
La plasmaféresis con recambios plasmáticos es un procedimiento terapéutico extracorpóreo utilizado en diversas condiciones inmunomediadas, incluyendo el trasplante renal. Su principal objetivo es la eliminación de sustancias patogénicas presentes en el plasma, como autoanticuerpos, inmunocomplejos o mediadores inflamatorios, mediante su separación y sustitución por soluciones alternativas.
Con el mismo fin que es utilizada en otras patologías autoinmunes (miastenia gravis, lupus, púrpura trombocitopénica o Guillem-Barré, entre otras) en el contexto del trasplante renal, esta técnica es especialmente útil en:
- Prevención y tratamiento del rechazo mediado por anticuerpos: El rechazo humoral está caracterizado por la presencia de DSA y daño endotelial mediado por el complemento. La plasmaféresis facilita la eliminación rápida de estos anticuerpos, reduciendo el daño inflamatorio y favoreciendo la recuperación del injerto. Su uso se combina con terapias inmunomoduladoras como eculizumab (anti-C5), IVIG y rituximab (anti-CD20).
- Desensibilización pretrasplante para pacientes altamente sensibilizados: Pacientes con alto grado de sensibilización HLA pueden desarrollar anticuerpos donante-específicos, lo que incrementa el riesgo de rechazo hiperagudo o temprano tras el trasplante.
La plasmaféresis se lleva a cabo mediante dispositivos de aféresis, los cuales extraen la sangre del paciente a través de un acceso vascular robusto (salvo que el paciente sea portador de fístula arteriovenosa previa, se realizará por catéter venoso central) y la someten a un proceso de separación a través de membrana, eliminando el plasma patológico y reemplazándolo por un fluido de sustitución. Los elementos celulares de la sangre (glóbulos rojos, blancos y plaquetas) se reincorporan al paciente junto con el nuevo plasma. Por su parte, el plasma eliminado se reemplaza con albúmina 5% o plasma fresco congelado.
A pesar de su eficacia, la plasmaféresis no está exenta de riesgos. Entre los principales efectos adversos se incluyen:
- Hipotensión y reacciones vasovagales: Por la rápida extracción de plasma o secundaria a reacción de hipersensibilidad.
- Trastornos de la coagulación: Reducción de factores de coagulación, fibrinógeno y plaquetas, aumentando el riesgo de sangrado. Aumentar recambios con plasma respecto a la proporción del albúmina.
- Mayor susceptibilidad a infecciones: Debido a la pérdida de inmunoglobulinas y factores del complemento.
- Alteraciones metabólicas: Hipocalcemia por la eliminación de calcio junto con el plasma, debido a la presencia de citrato como conservante del plasma fresco.
- Reacciones alérgicas: Asociadas a la administración de plasma fresco congelado.
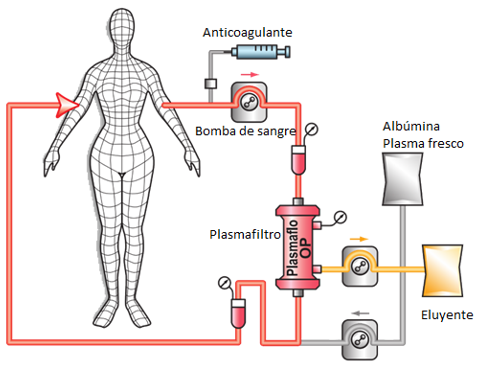
Ilustración 52: Esquema de plasmaféresis. Fuente: Izasa Medical ®; disponible en: https://www.izasamedical.es/es/productos/plasmaferesis-pe
4.3 Protocolos clínicos de inmunosupresión
A lo largo de este capítulo se ha expuesto que existen diversos fármacos inmunosupresores con mecanismos de acción distintos, los cuales deben combinarse estratégicamente para prevenir tanto el rechazo agudo como el crónico, minimizando al mismo tiempo los efectos adversos, en especial los de tipo cardiovascular, infeccioso y neoplásico en el paciente trasplantado. El esquema inmunosupresor en el trasplante renal se fundamenta en la combinación de tres clases de fármacos: 1) inhibidores de la calcineurina (ciclosporina o tacrolimus), 2) agentes antiproliferativos (derivados del ácido micofenólico o inhibidores de mTOR) y 3) corticosteroides.
No existe un consenso absoluto sobre el protocolo terapéutico óptimo, por lo que la estrategia más adecuada es la personalización del tratamiento. Para ello, es fundamental considerar diversas características del donante y del receptor, incluyendo no solo el riesgo inmunológico basado en la compatibilidad HLA, sino también factores como la edad, el tipo de donante y la fragilidad del receptor, entre otros. Teniendo en cuenta el grado de riesgo inmunológico del receptor, encontramos dos estrategias fundamentales a la hora de abordar el tratamiento:
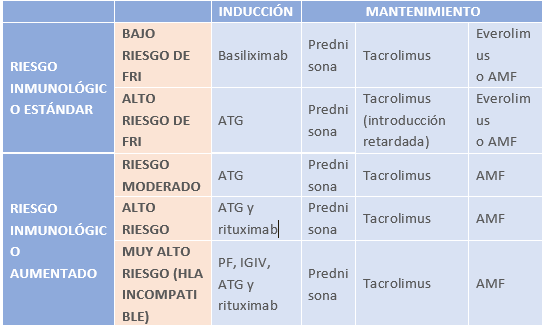
Tabla 11: Protocolo clínico estándar de inmunosupresión. FRI: Función retrasada del injerto; AMF: ácido micofenólico; PF: plasmaféresis; IGIV: inmunoglobulinas intravenosas; ATG: timoglobulina. Fuente: Crespo M et al, 2023; disponible en: https://nefrologiaaldia.org/es-articulo-inmunosupresion-en-el-trasplante-renal-602
BIBLIOGRAFÍA
- Abbas, A. K., Lichtman, A. H., & Pillai, S. (2022). Inmunología Celular Y Molecular (10a ed.). Elsevier.
- Arias, L. F. (s/f). Enf_tubulointert. Kidney Pathology. Recuperado el 2 de marzo de 2025, de https://kidneypathology.com/Enf_tubulointerst.html
- Arias, M., Campistol, J. M., & Morales, J. M. (2012). Manual de trasplante renal.
- Arrunátegui, A. M., Ramón, D. S., Viola, L. M., Olsen, L. G., & Jaramillo, A. (2022). Aspectos técnicos y clínicos de la prueba cruzada de histocompatibilidad en el trasplante de órganos sólidos. Biomedica: Revista Del Instituto Nacional de Salud, 42(2), 391–413. https://doi.org/10.7705/biomedica.6255
- Caballero, F., & Matesanz, R. (2023). ABC de la Donación y Trasplante de Órganos Humanos.
- Crespo, M., Diekmann, F., Redondo-Pachón, D., & Sancho, A. (2023). Inmunosupresión en el Trasplante Renal. Nefrologiaaldia.org.
https://nefrologiaaldia.org/es-articulo-inmunosupresion-en-el-trasplante-renal-602 - Feifer, A., & Anidjar, M. (2007). Nefrectomía laparoscópica en donante vivo. EMC - Urología, 39(4), 1–12. https://doi.org/10.1016/s1761-3310(07)70058-0
- Gutiérrez de la Fuente, C., López Jiménez, V., Pérez Flores, I., Ruíz San Millán, J. C., & Sánchez Fructuoso, A. I. (2012). Trasplante renal. En G. Fernández Fresnedo (Ed.), Algoritmos en nefrología. Grupo Editorial Nefrología.
- Halloran, P. F. (2004). Immunosuppressive drugs for kidney transplantation. The New England Journal of Medicine, 351(26), 2715–2729.
- https://doi.org/10.1056/NEJMra033540
- Kukla, A., Ventura-Aguiar, P., Cooper, M., de Koning, E. J. P., Goodman, D. J., Johnson, P. R., Han, D. J., Mandelbrot, D. A., Pavlakis, M., Saudek, F., Vantyghem, M.-C., Augustine, T., & Rickels, M. R. (2021). Transplant options for patients with diabetes and advanced kidney disease: A review. American Journal of Kidney Diseases: The Official Journal of the National Kidney Foundation, 78(3), 418–428. https://doi.org/10.1053/j.ajkd.2021.02.339
- Leeson, S., & Desai, S. P. (2015). Medical and ethical challenges during the first successful human kidney transplantation in 1954 at Peter bent Brigham hospital, Boston. Survey of Anesthesiology, 59(3), 119.
https://doi.org/10.1097/sa.0000000000000131 - Liverman, R., Chandran, M. M., & Crowther, B. (2021). Considerations and controversies of pharmacologic management of the pediatric kidney transplant recipient. Pharmacotherapy, 41(1), 77–102. https://doi.org/10.1002/phar.2483
- López Del Moral, J. L. (2010). Regulatory bases of living-donor kidney transplantation. Nefrologia: publicacion oficial de la Sociedad Espanola Nefrologia, 30 Suppl 2, 23–29.
https://doi.org/10.3265/Nefrologia.pre2010.Nov.10688 - López-Hoyos, M., Ruiz-San Millán, J. C., San Segundo-Arribas, D., & Rodrigo-Calabria, E. (2021). Inmunobiología del Trasplante. Estudios inmunológicos del donante y del receptor del trasplante renal. Nefrologiaaldia.org.
https://nefrologiaaldia.org/es-articulo-inmunobiologia-del-trasplante-estudios-inmunologicos-del-donante-y-del-146 - Matensanz, R. (2024). La pequeña - gran historia del trasplante renal en España. Grupo Editorial Nefrología de la SEN.
- Matesanz, R. (2008). El modleo español de la coordinación de trasplantes. Aula Médica.
- McAlister, V. C. (2005). Clinical kidney transplantation: a 50th anniversary review of the first reported series. American Journal of Surgery, 190(3), 485–488. https://doi.org/10.1016/j.amjsurg.2005.04.016
- Meneghini, M., Bestard, O., & Grinyo, J. M. (2021). Immunosuppressive drugs modes of action. Best Practice & Research. Clinical Gastroenterology, 54–55(101757), 101757. https://doi.org/10.1016/j.bpg.2021.101757
- Ministerio de Sanidad, Global Observatory on Donation and Transplantation, & World Health Organization. (2023). International report on organ donation and transplantation activities.
- Ministerio de Sanidad, & Organización Nacional de Trasplantes. (2011). Guía de buenas prácticas en el modelo de donación de órganos.
- Ministerio de Sanidad, Organización Nacional de Trasplantes, Sociedad Española de Trasplante, & Grupo de Histocompatibilidad. (2024). Guía Española para el Trasplante Renal en Pacientes Altamente Sensibilizados con Anticuerpos anti‑HLA Donante‑Específicos.
- Nagendra, L., Fernandez, C. J., & Pappachan, J. M. (2023). Simultaneous pancreas-kidney transplantation for end-stage renal failure in type 1 diabetes mellitus: Current perspectives. World Journal of Transplantation, 13(5), 208–220. https://doi.org/10.5500/wjt.v13.i5.208
- Organización Nacional de Trasplantes, & Ministerio de Sanidad. (2024). Informe de actividad 2024.
- Pérez-Sáez, M. J., Francés, A., & Pascual-Santos, J. (2023). Técnicas quirúrgicas en donante vivo y fallecido. Complicaciones. Indicaciones de embolización y nefrectomía del injerto. Nefrologiaaldia.org.
https://nefrologiaaldia.org/es-articulo-tecnicas-quirurgicas-en-donante-vivo-y-fallecido-complicaciones-indica-309 - Pérez-Tamajón, L., & Hernández-Marrero, D. (2024). Evaluación del receptor de trasplante renal. Nefrologiaaldia.org.
https://www.nefrologiaaldia.org/es-articulo-evaluacion-del-receptor-de-trasplante-renal-62 - Roach, J. P., Bock, M. E., & Goebel, J. (2017). Pediatric kidney transplantation. Seminars in Pediatric Surgery, 26(4), 233–240.
https://doi.org/10.1053/j.sempedsurg.2017.07.006 - Semenova, Y., Bayanova, M., Rakhimzhanova, S., Altynova, S., Sailybayeva, A., Asanova, A., & Pya, Y. (2024). Understanding pediatric kidney transplant rejection: Its pathophysiology, biomarkers, and management strategies. Current Medicinal Chemistry, 31.
https://doi.org/10.2174/0109298673333693240806160544 - Thongprayoon, C., Hansrivijit, P., Leeaphorn, N., Acharya, P., Torres-Ortiz, A., Kaewput, W., Kovvuru, K., Kanduri, S. R., Bathini, T., & Cheungpasitporn, W. (2020). Recent advances and clinical outcomes of kidney transplantation. Journal of Clinical Medicine, 9(4), 1193. https://doi.org/10.3390/jcm9041193
- Vazquez Martul, E. (2018). Anatomía patológica del trasplante renal. Revista española de patología: publicación oficial de la Sociedad española de anatomía patológica y de la Sociedad española de citología, 51(2), 110–123. https://doi.org/10.1016/j.patol.2017.10.001
- Vijayan, M., & Pavlakis, M. (2017). Pregnancy and the kidney transplant recipient. Current Opinion in Nephrology and Hypertension, 26(6), 494–500.
https://doi.org/10.1097/mnh.0000000000000363
