La enfermedad vascular Incluye enfermedades linfáticas, venosas, arteriales y se denomina periférica cuando los vasos afectados aparecen, en mayor frecuencia, en extremidades inferiores pudiendo ser de aparición repentina, aguda, o progresiva, crónica.
La enfermedad vascular afecta al flujo sanguíneo, ya sea bloqueando o debilitando los vasos sanguíneos, y por continuidad los órganos y estructuras corporales como resultado de la disminución o el bloqueo total del flujo sanguíneo.
3.1 CIRCULACIÓN LINFÁTICA
El sistema linfático es una red de vasos junto con pequeños órganos, los ganglios linfáticos colaborando con el sistema venoso en la recuperación del excedente filtrado a nivel tisular y, consecuentemente, en el mantenimiento delequilibrio hídrico en el organismo.
La linfa de la parte inferior del cuerpo accede al conducto torácico y se vacía en el sistema venoso en la unión de la yugular interna izquierda con la vena subclavia.
El líquido linfático de la mitad izquierda de la cabezay el cuello, del brazo izquierdo y partes del tórax desembocan también al conducto torácico.
La linfa procedente de la mitad derecha de cabeza y cuello, brazo derecho es conducida por el conducto linfático derecho desembocando en la confluencia de la vena yugular interna derecha y la subclavia.
3.1.1 Estructura y función de los vasos linfáticos
Los capilares linfáticos comienzan en fondos de saco, y van uniéndose y estableciendo anastomosis, formando vasos linfáticos cada vez mayores que se dirigen hacia ganglios linfáticos para terminar en los conductos torácico y linfático derecho.
Al igual que los capilares sanguíneos, están formados por una capa de células endoteliales diferenciándose de ellos, por la cantidad de canales (o hendiduras intercelulares) que presenta la pared.
3.1.2 Formación de la linfa
La linfa es líquido del intersticio que accede y recorre los vasos linfáticos.
Se compone del líquido intersticial de la parte anatómica del cuerpo de la que provienen. Es una solución que varía en composición dependiendo del espacio anatómico donde se forme.
La linfa tiene un color amarillento y capacidad de coagularse ya que contiene fibrinógeno.
3.1.3 Flujo linfático
El sistema linfático carece de bomba impulsora dependiendo el flujo de las interacciones externas.
Los mecanismos que definen el flujo de linfa son varios divididos en intrínsecos (propios del sistema linfático) y otros extrínsecos (relacionados con el sistema venoso).
- a) Bomba linfática capilar. El incremento de entrada de líquido intersticial produce un aumento concomitante de flujo linfático.
- b) Bomba linfática vascular. Las fibras musculares lisas ejercen una acción de bombeo por las contracciones rítmicas y espontáneas.
- c) Bomba muscular y respiratoria. La contracción de la musculatura esquelética corporal comprime los vasos linfáticos actuando como una bomba externa para la movilización del flujo linfático.
- d) Compresiones externas. La compresión de vendajes o medias facilita el flujo linfático.
3.2. ENFERMEDAD VASCULAR VENOSA
La enfermedad venosa crónica (EVC) o insuficiencia venosa crónica (IVC), (en sus últimas fases evolutivas), es una afección que ocurre cuando la pared venosa y / o las válvulas en las venas de las piernas no funcionan de manera efectiva, lo que dificulta que la sangre regrese al corazón desde el sistema venoso de las extremidades inferiores.
El fracaso del aparato valvular constituye el mecanismo fundamental de la EVC.
La IVC hace que la sangre se "acumule" o se acumule en estas venas, y esta acumulación se denomina estasis.
El funcionamiento correcto para el retorno de la sangre venosa al corazón precisa de una adecuada actividad de las válvulas venosas, que evitan el retorno descendente y favorecen el sentido ascendente.
El ejercicio físico y la ergonomía en la actividad laboral son factores que influyen en el desarrollo de la EVC siendo aquellos trabajos con un ortostatismo prolongado manteniendo la bipedestación más de 4 hs./día favoreciendo la aparición y severidad EVC.
3.2.1 Reflujo
La presencia de reflujo sanguíneo mantenido a través de válvulas incompetentes provoca un incremento de la presión venosa durante la deambulación siendo el factor fisiopatológico fundamental de la EVC.
Existe un flujo retrógrado, en condiciones fisiológicas, hasta producirse el cierre valvular.
Se considera un reflujo “normal” si se produce y controla por debajo de medio segundo (medido con eco-Doppler) en el sistema venoso superficial y venas profundas de la pantorrilla y menor de un segundo en el tramo femoropoplíteo.
Si existe una degradación valvular o ya instaurada, la contracción muscular que se produce en la deambulación, no solo no reduce la presión venosa distal, sino que la incrementa de forma progresiva.
La hipertensión venosa distal que genera la deambulación en pacientes con fallo valvular constituye la clave fisiopatológica en la progresión de la EVC.
La hipertensión venosa mantenida genera cambios en la tensión endotelial que es reconocida como una afectación lesiva produciendo la adhesión y activación leucocitaria, como cuadro inflamatorio de pared y tejidos perivasculares, a través de mediadores inflamatorios y quimiotácticos liberados.
3.2.2 Respuesta inflamatoria luminal
Las variaciones hemodinámicas en la luz venosa producen la liberación de factores proinflamatorios y elementos vasoactivos que aumentan la permeabilidad de pared enlenteciendo el flujo primero por el aumento de la presión relacionado con el reflujo venoso.
Estas alteraciones hemodinámicas lesionan la pared endotelial y su funcionamiento, permitiendo la fijación leucocitaria y produciendo una disminución en la síntesis de óxido nitroso.
La hipertensión venosa, como comentábamos en el apartado anterior, genera cambios en la tensión endotelial y el proceso inflamatorio mantenido degrada el glucocáliz de la pared venosa, con mayor énfasis en el sistema superficial, más descubierto y sin la protección muscular que sí poseen las venas del sistema profundo.
El glucocáliz endotelial está constituido por glucosaminoglicanos, proteoglicanos y glucoproteínas que cubren y protegen el endotelio vascular en su parte interna o luminal.
Asume diferentes funciones protectoras:
- ante las fuerzas mecánicas de tensión
- regula la permeabilidad vascular de líquidos y moléculas
- equilibra la activación de la coagulación y la fibrinólisis
- protege de la adhesión de leucocitos y plaquetas al endotelio
En una situación normal, los leucocitos se desplazan por la luz mediante un movimiento de rodamiento.
Si se ve alterada esta traslación al presentarse la activación endotelial inflamatoria que disminuye la función del glucocáliz, se favorece la fijación de los leucocitos a la superficie endotelial mediante moléculas de adhesión, perpetuando la inflamación e incrementando los mediadores proinflamatorios.
Los mediadores proinflamatorios, (interleucinas (IL-1, IL-6), citocinas (TNF-a, TGF-ß1), metaloproteinasas (MMP-2, MMP-3, MMP-9), factores de crecimiento (plaquetas-PDGF-, factor de crecimiento vascular endotelial -VEGF-, endotelial -EGF-, etc.) producen modificaciones en la estructura venosa y la dermis, consistentes en la disminución de elasticidad por la reducción de fibras elásticas (elastina y laminina).
Esta disminución de fibras elásticas unido al incremento total de colágeno tipo I (produce la rigidez tisular) y la disminución del colágeno tipo III (favorece la respuesta elástica) hacen más rígidos y frágiles tanto la pared venosa como la dermis perilesional favoreciendo en endurecimiento y dilatación de las venas y la perpetuación del reflujo.
La actividad inflamatoria en el entorno perivascular va a provocar alteraciones del tejido cutáneo con la sintomatología clave que define a este tipo de lesiones:
- atrofia blanca
- celulitis
- dermatitis de estasis
- eccema venoso
- lipodermatoesclerosis
- Úlcera venosa, ulcera flebostática.
A este acumulo de sangre por reflujo, aumento de la presión e inflamación mantenida en la pared venosa le sumamos la agregación plaquetaria y la formación de trombos en venas de pequeño calibre se nos presenta en EVC la trombosis venosa que en función de su presentación será superficial (TVS) o profunda (TVP).
La insuficiencia venosa crónica que se desarrolla como resultado de la TVS/TVP también se conoce como síndrome postrombótico.
Las válvulas pueden verse afectadas de forma indirecta en el proceso de recanalización de los trombos venosos o ser secundarias a una obstrucción crónica del sistema venoso que dilata las venas distales a la obstrucción.
La insuficiencia venosa primaria o esencial constituye la causa más frecuente de la EVC.
3.3. ENFERMEDAD VASCULAR ARTERIAL
El grado de isquemia producido por la obstrucción está determinado por el calibre arterial, la localización, la extensión y la velocidad de instauración, relacionada con el desarrollo de circulación colateral, cuya sintomatología varía en función del estadio evolutivo de la enfermedad.
La enfermedad arterial periférica o arteriopatía periférica se define como un conjunto de síndromes arteriales no coronarios causados por una alteración en su estructura y el funcionamiento de las arterias (cerebro, órganos y miembros superior e inferior). El término enfermedad arterial periférica suele referirse a la presencia de estenosis, oclusiones y/o enfermedad aneurismática siendo la enfermedad más común es la arteriosclerosis.
En el estadio inicial, el paciente se encuentra asintomático.
Progresivamente aparece la claudicación intermitente, (sensación dolorosa en la extremidad, calambres o cansancio en los músculos de la pierna con la actividad física), pudiendo aliviarse con el reposo.
La distancia que se puede caminar sin presencia de dolor, a medida que la enfermedad se agrava, sé hace más corta hasta que éste aparece incluso en reposo.
La isquemia crítica es una manifestación de la patología arterial periférica que incluye dolor isquémico crónico de reposo o lesiones isquémicas de la piel, tanto úlceras como gangrena.
La afectación cutánea producida por la disminución del flujo en la luz arterial puede producirse por diferentes trastornos: oclusivos y funcionales.
- Trastornos arteriales oclusivos.
o Oclusión arterial aguda.
o Enfermedad de Buerger o Tromboangitis obliterante.
o Oclusión arterial crónica.
- Trastornos arteriales funcionales.
o Fenómeno de Raynaud.
o Vasculitis.
3.4 FACTORES DE RIESGO RELACIONADOS CON LA ENFERMEDAD VASCULAR
La causa más frecuente de la enfermedad vascular y dentro de la enfermedad vascular arterial, la Isquemia crónica de extremidad inferior, es la arteriosclerosis.
La arterioesclerosis es una acumulación progresiva de sustancias (grasas, colesterol, calcio, fibrina) en la capa interna de la arteria.
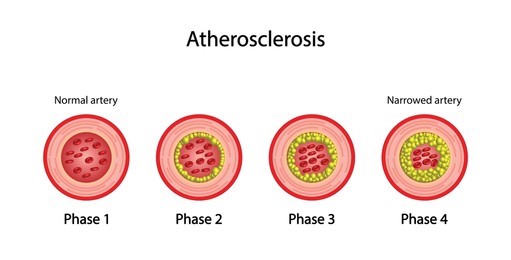
Imagen 3. Fases ocupación placa luz arterial
La progresión vascular del cierre de la luz vascular es lenta y progresiva pudiendo comenzar en la niñez.
Si la placa ateromatosa se desarrolla y engrosa, provoca una disminución de flujo o bloquearlo completamente con la afectación isquémica de órganos o tejidos.
La búsqueda de factores de riesgo que faciliten la aparición de la arteriosclerosis es esencial para el diagnóstico precoz y prevención de futuras lesiones isquémicas cutáneas.
Los factores de riesgo para la anamnesis del paciente con enfermedad vascular son modificables y no modificables:
- Modificables
- Alteraciones de la coagulación.
- Diabetes.
- Dislipemia.
- Hiperhomocisteinemia
- Hipertensión arterial.
- Insuficiencia renal crónica.
- Tabaco.
- Obesidad.
- Sedentarismo.
- No Modificables:
- Edad.
- Sexo.
- Genéticos.
3.4.1. Factores de riesgo modificables
Los factores de riesgo mayores (diabetes, hipertensión, tabaquismo e hiperlipemia) están implicados en un 80-90% de las enfermedades cardiovasculares
3.4.1.1 Alteraciones de la coagulación
Nuestro cuerpo en respuesta fisiológica forma un coágulo sanguíneo para detener las hemorragias. En estas situaciones es necesario disponer de plaquetas y proteínas sanguíneas que se denominan factores de coagulación.
Si la persona padece una alteración de la coagulación no dispone de suficientes factores de coagulación o que estos factores no funcionan correctamente.
Las alteraciones de coagulación pueden ser consecuencia de otras enfermedades, hereditarios o por efecto secundario de algunos medicamentos.
Normalmente, los trastornos de coagulación incluyen:
- Coagulación Intravascular Diseminada. CID.
- Defectos adquiridos de la función plaquetaria.
- Defectos congénitos de la función plaquetaria.
- Deficiencia de la proteína C o S de forma congénita.
- Deficiencia del factor II de coagulación.
- Deficiencia del factor V de coagulación.
- Deficiencia del factor VII de coagulación.
En la coagulación sanguínea intervienen principalmente plaquetas y hasta 20 proteínas plasmáticas distintos llamados factores de coagulación.
A los factores de coagulación se les asignó un número romano según el orden correlativo en el cual fueron descubiertas. Las proteínas o factores de la coagulación, en condiciones fisiológicas normales, se encuentran en forma inactiva. Para indicar la forma activa de los factores de la coagulación se adiciona el sufijo -a- después del número romano. Varios factores de la coagulación, como la precalicreína (PK), (Factor Fletcher), y los quininógenos de alto peso molecular (QAPM), no poseen ningún número romano.
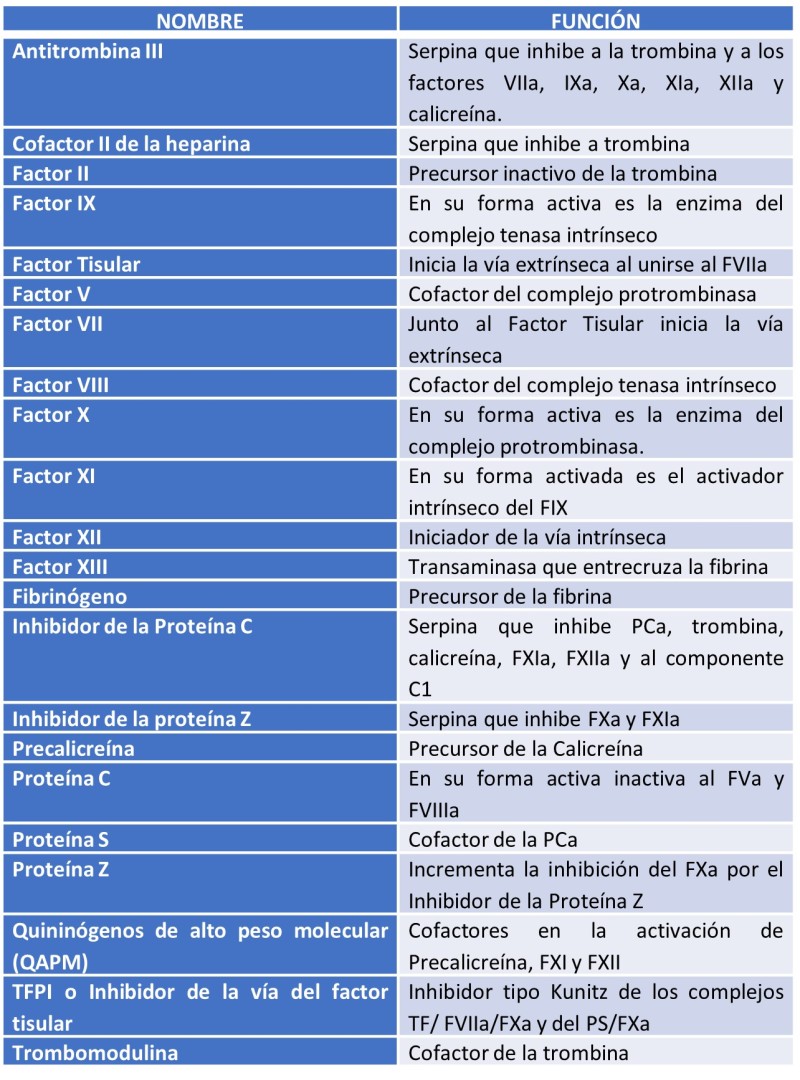
Tabla 1. Nombre y Función de los factores de coagulación.
En ausencia de factores de coagulación o están en niveles bajos, el proceso hemostático se ve impedido.
Los trastornos de coagulación tienen habitualmente una causa hereditaria siendo otros producidos por:
- Enfermedades con deficiencia de vitamina K
- Enfermedad hepática grave
- Tratamientos que utilizan medicamentos anticoagulantes
- Uso prolongado de antibióticos
La deficiencia congénita de la mayoría de las proteínas anticoagulantes como ATIII, PC y PS está asociada a la aparición de un estado de hipercoagulabilidad, protrombótico o trombofilico, sin embargo, en estos casos no se observan alteraciones en las pruebas clásicas, por lo que estas no se emplean en el estudio de pacientes con trombofilias primarias.
3.4.1.1.1Teoría clásica: la cascada de la coagulación
Entre 1960 y 1970, se propuso el modelo de la Cascada de la Coagulación, valorando este mecanismo como un proceso enzimático secuencial y limitado a la superficie de las plaquetas favoreciendo la generación de trombina.
Este modelo se explica a través de dos vías: Intrínseca y Extrínseca.
La vía intrínseca se inicia tras un daño vascular exponiendo superficies cargadas
negativamente y la interacción que produce en los factores de contacto (FXII, FXI, PK y QAPM) iniciándose el proceso de activación secuencial, donde el FXII funciona como verdadero iniciador.
La vía extrínseca se inicia con la formación del complejo conformado por el factor tisular (FT), el Factor VIIa circulante, iones de Ca++ y fosfolípidos.
La vía común se unen las dos vías anteriores conformando el complejo “Protrombinasa”, encargado de generar trombina, que actúa sobre el fibrinógeno transformándolo en monómeros de fibrina formando junto con los elementos formes de la sangre, el tapón hemostático o coágulo.
El modelo clásico es útil en las pruebas de laboratorio para la evaluación de desórdenes en la coagulación. Entre estas pruebas están el Tiempo de Protrombina (TP), para evaluar la vía extrínseca; el Tiempo de Tromboplastina Parcial activado (TTPa) para la víaintrínseca y el Tiempo de Trombina (TT), en la vía común.
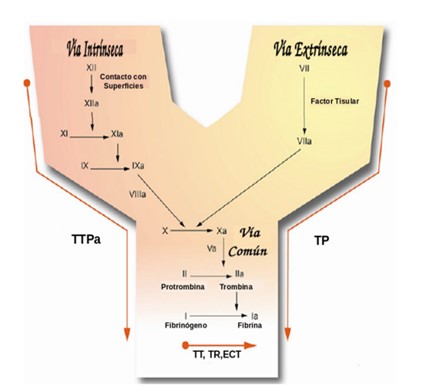
Imagen 4. Cascada de la Coagulación
3.4.1.1.2.Modelo Celular de la Coagulación
Según este modelo, la coagulación ocurre en tres fases:
La primera de ellas, Fase de Iniciación: tras la exposición del Factor Tisular, una proteína transmembrana que se expresa constitutivamente en los fibroblastos expuestos luego de una lesión vascular, en células musculares lisas y que puede ser inducida en células endoteliales, monocitos y macrófagos, por acción de estímulos proinflamatorios.
Luego, se inicia la Fase de Amplificación, que es dependiente de la adhesión de las plaquetas al colágeno subendotelial y su activación por las trazas de trombina que se forman durante la fase de iniciación. Las plaquetas activadas experimentan un cambio morfológico, con la subsecuente exposición de fosfolípidos cargados negativamente y, además, liberan el contenido de sus gránulos, los cuales almacenan sustancias que inician el proceso de la agregación y la formación del tapón hemostático primario.
En la Fase de Propagación, el FIXa generado en la fase de iniciación, forma junto con el FVIIIa, sobre una superficie fosfolipídica y en presencia de iones de calcio forma el complejo “Protrombinasa” que activa a la protrombina y asegura la generación de grandes cantidades de trombina, fenómeno denominado “explosión de trombina”. La activación del fibrinógeno genera un coágulo de fibrina estable y resistente a una lisis prematura. Una vez cumplida su función hemostática, la generación de trombina es atenuada y neutralizada por la acción de inhibidores.
El modelo celular de la coagulación asegura que la hemostasia se localice en el sitio donde ocurre la lesión vascular y que este proceso ocurra sobre superficies celulares esenciales para el ensamblaje de las diversas reacciones enzimáticas que modulan la formación del coágulo.
La trombina tiene numerosas funciones dentro de la hemostasia, las cuales pueden ser clasificadas como:
- Procoagulantes
- Anticoagulantes
- Profibrinolíticas
- Antifibrinolíticas
La trombina induce las agregaciones plaquetarias representando un sistema de retroalimentación positiva que favorece la generación de más trombina.
El sistema de la coagulación es finalmente regulado por mecanismos que aseguran que la generación de trombina y la posterior formación de la fibrina sean procesos localizados. Bajo condiciones fisiológicas, el mantenimiento del flujo sanguíneo adecuado y la actividad anticoagulante del endotelio vascular, limitan la acumulación local de factores de la coagulación activados y la formación de los complejos procoagulantes, evitando así que se active el sistema de la coagulación y ocurra la oclusión de algún vaso sanguíneo.
3.4.1.2. Diabetes
En pacientes diabéticos el riesgo de padecer una enfermedad vascular periférica es cuatro veces mayor respecto al resto de la población.
Un incremento de 1% en la hemoglobina glicosilada provoca un incremento del 25% en el riesgo de enfermedad arterial periférica.
Este riesgo vascular en la diabetes es debido a que mantener valores de glucemia elevados a lo largo del tiempo producen cambios que generan complicaciones macro y microvasculares.
Si a esto le añadimos la neuropatía característica de los diabéticos, tenemos como consecuencia una respuesta insuficiente a la infección y un trastorno de la cicatrización, lo que aumenta el riesgo de amputación hasta 10 veces más que los pacientes no diabéticos.
El control de la diabetes se basará en:
- Tratamiento farmacológico. Ya sea antidiabéticos orales e insulina para mantener niveles de glucemia adecuados.
- Control de dieta.
- Ejercicio físico.
- Programas de educación sanitaria que permitan al paciente comprender y gestionar su propio tratamiento.
3.4.1.3. Hiperlipemi
La dislipidemia, hiperlipemia o hiperlipidemia agrupa niveles de grasa altos en nuestra sangre. La relación de aterosclerosis con el colesterol es directa.
El colesterol es necesario para mantener los procesos bioquímicos naturales.
Un alto contenido en esta sustancia en la dieta produce hipercolesterolemia que predispone a enfermedades cardíacas y vasculares.
El incremento de los niveles de colesterol total y de lipoproteínas de baja densidad. (LDL) Incrementa la permeabilidad de las células endoteliales, lo que aumenta el riesgo de arteriosclerosis, mientras que las lipoproteínas de alta densidad (HDL) actúan como inhibidoras de la placa aterosclerótica.
Niveles de colesterol total por encima de 270 miligramos/decilitro se asocia al doble de incidencia de claudicación cómo uno de los principales signos de la enfermedad arterial periférica.
3.4.1.4. Hiperhomocisteinemia
La homocisteína es un aminoácido sintetizado en el organismo a partir de la metionina(aminoácido esencial).
La única fuente de metionina es la ingesta, principalmente de proteínas animales para producir creatina.
El metabolismo de la homocisteína está muy relacionado con las vitaminas B6, B12 y ácido fólico.
Los niveles plasmáticos de Homocisteína provocan un aumento del riesgo de arteriosclerosis y en especial, de enfermedad arterial periférica. Los niveles de homocisteína en plasma están elevados en el 60% de las personas con arteriosclerosis en la extremidad inferior, frente al 1% de la población sin enfermedad. El mecanismo de acción de la Homocisteína podría ser doble:
- Provoca oxidación del LDL que provoca cambios estructurales.
- Inhibe la síntesis de óxido nítrico. Que posee un efecto dilatador de los vasos sanguíneos provocando Un endurecimiento de la arteria y disminución del calibre del vaso.
3.4.1.5. Hipertensión arterial
El riesgo de padecer enfermedad arterial periférica es de 2,5 a 4 veces mayor en pacientes hipertensos que en los no hipertensos.
La enfermedad arterial hipertensiva se define como la presión arterial superior a 140/90 mmHg en dos o más lecturas de la presión sanguínea; se describen dos etapas: la etapa I, con presión arterial sistólica de 140 a 159 mmHg y la presión diastólica en 90 a 99 mmHg, y la hipertensión en etapa II que presenta una presión arterial sistólica de 160 o más mmHg y una presión arterial diastólica de 100 o más mmHg. La hipertensión esencial está presente en el 90 % de las personas que padecen esta enfermedad, no se identifica su causa ni tiene síntomas específicos.
Por el contrario, la hipertensión secundaria sí tiene causa identificada, entre las que se describen: la estenosis de la arteria renal, el feocromocitoma, la nefropatía diabética, la enfermedad renal poliquística, entre otras
Con la edad, aumenta la prevalencia de la enfermedad arterial hipertensiva, y esta adquiere una serie de características clínicas que la diferencian de la hipertensión en el joven y en edades medias de la vida. En su patogenia intervienen mecanismos que conducen a la vasoconstricción por disfunción endotelial, o bien por mecanismos independientes del endotelio, y es interesante observar que muchos de estos mecanismos son similares a los que aparecen en el envejecimiento e idénticos a los que conducen a la arteriosclerosis; ejemplo de ello es la producción de radicales libres y especies reactivas del oxígeno, elevados ambos en la enfermedad arterial hipertensiva y en el envejecimiento. La hipótesis de los telómeros (son los extremos de los cromosomas) en la teoría del envejecimiento, son complejos de proteínas y ADN no nucleosómico que se localizan en los extremos de los cromosomas, y se ha descrito que las alteraciones de su integridad conducen a la disfunción endotelial, propia de la hipertensión y la arteriosclerosis. El estrés oxidativo causa, además, el acortamiento de los telómeros y acelera el inicio del envejecimiento celular.
La relación de riesgo frente al tabaco o con la diabetes es más débil en la hipertensión en la enfermedad vascular arterial.
3.4.1.6. Insuficiencia renal crónica
La insuficiencia renal crónica consiste en el deterioro progresivo e irreversible de la función renal en el filtrado glomerular.
El filtrado va disminuyendo en su capacidad absoluta iniciándose un acumulo sanguíneo de urea y creatinina.
La persona puede estar relativamente asintomática o presentar anemia, hipertensión arterial, poliuria y nicturia.
Las causas más comunes de ERC son la nefropatía diabética, hipertensión arterial, y glomerulonefritis.
En la práctica clínica, la mayoría de las nefropatías progresan lentamente hacia la pérdida definitiva de la función renal.
Se han clasificado según la relación anatómica que producían la enfermedad renal crónica como:
- Vascular: por enfermedades de grandes vasos (estenosis arteria renal bilateral), enfermedades de pequeños vasos (nefropatía isquémica, síndrome urémico hemolítico y vasculitis)
- Glomerular: Enfermedad glomerular primaria, secundaria.
- Túbulo intersticial, enfermedad poliquística renal, nefritis tubulointersticial crónica inducida por drogas o toxinas, y nefropatía de reflujo
- Obstructiva: piedras del riñón bilaterales.
Las alteraciones más significativas que se producen en la enfermedad renal crónica son:
- Cardiovasculares: hipertensión arterial
- Dermatológicas: color pajizo de la piel por la anemia, prurito.
- Electrolíticas: niveles de potasio y bicarbonato.
- Gastrointestinales: anorexia, náuseas y vómitos.
- Hematológicas: anemia,
- Hormonales: impotencia y oligospermia, alteraciones en ciclo menstrual amenorrea.
- Neurológicas: encefalopatía urémica, polineuropatía sensitiva y motora.
- Osteomusculares: dolores óseos, deformidades en dedos, fracturas y retraso del crecimiento en niños.
3.4.1.7. Tabaco
El tabaco es el principal factor de riesgo modificable de las enfermedades del aparato circulatorio y de la arteriopatía periférica. Está presente en el 90% de los pacientes diagnosticados.
El tabaquismo favorece el desarrollo de la aterosclerosis en la aorta, las carótidas y las arterias de las extremidades inferiores, que da lugar a la claudicación intermitente y progresa a isquemia en reposo, ulceración y gangrena.
El tabaco altera los componentes celulares de la sangre coma los factores de coagulación, el sistema inmunitario y las paredes de las arterias. La nicotina tiene un factor vasoconstrictor que aumenta la frecuencia cardíaca y la tensión arterial.
Las sustancias directamente relacionadas con el progreso de las lesiones vasculares son el monóxido de carbono (CO) y la nicotina.
El CO en la sangre se une a la hemoglobina y da lugar a la carboxihemoglobina, que desplaza las moléculas de O2, con lo que se reduce su concentración y se produce la consiguiente hipoxemia. La hipoxemia modifica los sistemas enzimáticos que regulan la respiración celular y favorece la disfunción endotelial y el desarrollo precoz de la aterosclerosis.
El monóxido de carbono influye sobre la íntima de las arterias y favorece la hipoxia de los tejidos.
El tabaco produce alteraciones de la estructura de las células endoteliales, lo que ocasiona cambios en su función.
Las dos principales sustancias sintetizadas por el endotelio, el monóxido de nitrógeno (NO) y la prostaciclina, (vasodilatadores, antiaterogénicas e inhibidoras de la agregación plaquetaria) disminuyen y reducen la migración de los leucocitos hacia el músculo liso vascular, disminuyen en su concentración incrementándose la síntesis de endotelina, que es un potente vasoconstrictor con efectos opuestos a los del NO.
El tabaco aumenta el riesgo de esta enfermedad de 2 a 7 veces, siendo el riesgo de hasta 16 veces más elevado en fumadores activos. El abandono del tabaco ha demostrado una reducción de riesgo de enfermedad arterial periférica, siendo el riesgo proporcional al número de cigarrillos consumidos por día y al número de años.
Los fumadores más severos no solo tienen un mayor riesgo de enfermedad arterial periférica, sino que presentan las formas más graves que ocasionan la isquemia crítica.
3.4.2. Factores de riesgo no modificables
En los factores de riesgo no modificables destacan la importancia de la prevención y el manejo temprano de la EAP mediante cambios en el estilo de vida y el control de los factores de riesgo modificables.
3.4.2.1. Edad
La cicatrización de heridas en personas mayores sanas se retrasa; no es que la piel sea defectuosa, sino que las alteraciones cutáneas relacionadas con la edad pueden predisponer a los ancianos a los efectos de diversos factores que afectan al proceso de cicatrización de heridas y subyacen a las heridas crónicas.
3.4.2.2. Sexo
El 80% de la enfermedad arterial periférica afecta principalmente a varones.
Las mujeres desarrollan enfermedades vasculares a edades más avanzadas que los hombres, aproximadamente una década más tarde siendo peor el pronóstico.
Las mujeres en edad fértil tienen cierto grado de “protección” por efecto de los estrógenos que ejercen efectos beneficiosos sobre el sistema cardiovascular en situaciones normales ni patología asociada.
3.4.2.3 Factores genéticos
Ciertas condiciones del sistema vascular se heredan de padres a hijos.
La genética es una de las ramas de conocimiento que va poco a poco abarcando todas las disciplinas y en parte de ellas, centrándose en su análisis para la detección precoz de patologías y potenciales riesgos.
Los estudios genéticos debieran ser una herramienta habitual en la práctica clínica evitando las complicaciones futuras desde un abordaje preventivo tras sucesos familiares abruptos que nos aportaran una información para el manejo de los pacientes.
BIBLIOGRAFÍA
- Adrián Fuentes Agúndez, Gonzalo Esparza Imas, Morales J, Lucía Crespo Villazán, Manuel J. “Dominate”. Acrónimo de apoyo en la valoración de heridas. Enfermería Dermatológica. 2016 Jan 1;10(29):7–11.
- Armstrong, Ehrin J., and David G. Armstrong. "Critical limb ischemia." Vascular Medicine 26.2 (2021): 228-231.
- Azzopardi EA, Boyce DE, Dickson WA, Azzopardi E, Laing JH, Whitaker IS, Shokrollahi K. Application of topical negative pressure (vacuum-assisted closure) to split-thickness skin grafts: a structured evidence-based review. Ann Plast Surg. 2013; 70(1):23-29.
- Budino D. Índice Tobillo-Brazo. Disponible en: https://www.google.com/search?sxsrf=ALiCzsb0evBrBQfZdLZegiA7cnpVyAzD-Q:1657128363529&q=Budino+DE.+%C3%8Dndice+Tobillo-Brazo.&spell=1&sa=X&ved=2ahUKEwiS_9Gb5OT4AhUExoUKHdeaDOEQBSgAegQIARA4&biw=1821&bih=876&dpr=0.75
- CHEN, Ju-Yi. Thromboangiitis obliterans. Anatolian journal of cardiology, 2021, vol. 25, no 2, p. E-8.
- Conte MS, Bradbury AW, Kolh P, et. al, Global Vascular Guidelines on the Management of Chronic Limb-Threatening Ischemia. Eur J Vasc Endovasc Surg. 2019 jul;58(1S): S1-S109.e33. doi: 10.1016/j.ejvs.2019.05.006.
- Esparza Imas G. Indicación, uso y autorización de dispensación de medicamentos sujetos a prescripción médica: heridas. Rev. enferm. vasc. [Internet]. 15 de julio de 2023 [citado 12 de octubre de 2023];5(8):3-. Disponible en: https://revistaevascular.es/index.php/revistaenfermeriavascular/article/view/129.
- Fourgeaud C, Mouloise G, Michon-Pasturel U, Bonhomme S, Lazareth I, Meaume S et al. Interest of punch skin grafting for the treatment of painful ulcers. J Mal Vasc. 2016; 41:323-328.
- Fowkes FG, Rudan D, Rudan I, Aboyans V, Denenberg JO, McDermott MM, Norman PE, Sampson UK, Williams LJ, Mensah GA, Criqui MH. Comparison of global estimates of prevalence and risk factors for peripheral artery disease in 2000 and 2010: a systematic review and analysis. Lancet. 2013; 382:1329–1340. doi: 10.1016/S0140-6736(13)61249-0.
- Fowkes, F. G. R., Housley, E., Cawood, E. H. H., Macintyre, C. C. A., Ruckley, C. V., & Prescott, R. J. (1991). Edinburgh Artery Study: prevalence of asymptomatic and symptomatic peripheral arterial disease in the general population. International journal of epidemiology, 20(2), 384-392.
- Gabel, Josué y col. "El enfoque multidisciplinario logra la salvación de la extremidad sin revascularización en pacientes con isquemia y pérdida de tejido de leve a moderada". Revista de cirugía vascular 71.6 (2020): 2073-2080.
- Gómez Gutiérrez, N. "Valoración, prevención y tratamiento de las heridas de difícil cicatrización." (2023).
- Guerrero Belsy, López Mercedes. Generalidades del sistema de la coagulación y pruebas para su estudio. Invest. clín 56(4): 432-454. Disponible en: http://ve.scielo.org/scielo.php?script=sci_arttext&pid=S0535-51332015000400010&lng=es.
- Joosten MM, Pai JK, Bertoia ML, Rimm EB, Spiegelman D, Mittleman MA, Mukamal KJ. Associations between conventional cardiovascular risk factors and risk of peripheral artery disease in men. JAMA. 2012; 308:1660–1667. doi: 10.1001/jama.2012.13415
- Lahoz C. Mostaza J. Índice tobillo-brazo: una herramienta útil en la estratificación del riesgo cardiovascular. Rev Esp Cardiol; 59:647-9. Disponible en: https://www.revespcardiol.org/es-indice-tobillo-brazo-una-herramienta-util-articulo-13091364
- Levin, Scott R., Nkiruka Arinze, and Jeffrey J. Siracuse. "Lower extremity critical limb ischemia: a review of clinical features and management." Trends in cardiovascular medicine 30.3 (2020): 125-130.
- Medlineplus.gov. [Internet]. Rockville Pike: Información de Salud de la Biblioteca Nacional de Medicina. Enfermedad arterial periférica; 2017. Disponible en: https://medlineplus.gov/spanish/peripheralarterialdisease.html
- Melon Lozano O, Miñana Climent J, and San Cristóbal Velasco E. Patología Vascular Periférica. Tratado de geriatría para residentes. 2007. P: 355-361.
- Mills JL, Conte MS, Armstrong DG, et al. The Society for Vascular Surgery Lower Extremity Threatened Limb Classification System: Risk stratification based on Wound, Ischemia, and foot Infection (WIfI). J Vasc Surg. 2014;59(1): 220034.e1-2.
- Ministerio de Sanidad y Consumo; Instituto de Salud Carlos III, Agencia de Evaluación de Tecnologías Sanitarias (AETS). Prótesis endovasculares (stents) en el tratamiento de la arteriopatía periférica de los miembros inferiores. Madrid: AETS, Instituto de Salud Carlos III; 1996.
- Murabito, J. M., D’Agostino, R. B., Silbershatz, H., & Wilson, P. W. (1997). Intermittent claudication: a risk profile from the Framingham Heart Study. Circulation, 96(1), 44-49.
- Natarajan, B., Patel, P., & Mukherjee, A. Acute Lower Limb Ischemia—Etiology, Pathology, and Management. International Journal of Angiology, 29(03), (2020). 168-174.
- O´Donell CJ, Elosua R. Factores de riesgo cardiovascular. Perspectivas derivadas del Framingham Heart Study. Rev Esp Cardiol 61 (6): 299-310. Disponible en: https://www.revespcardiol.org/es-factores-riesgo-cardiovascular-perspectivas-derivadas-articulo-13116658
- Roldán Valenzuela A, Pérez Barreno D, Ibáñez Clemente P, Navarro Caballero M, Alba Moratilla C, Esparza Imas G et al. Guía de práctica clínica- Consenso sobre Úlceras Vasculares y Pie Diabético de la AEEVH [Internet]. 3rd ed. Madrid: Asociación Española de Enfermería Vascular y Heridas; 2017. Disponible en: https://www.aeev.net/pdf/GuiadePractica-Clinica-web.pdf
- Romero JM. Enfermedad arterial periférica. Barcelona: Medical Dosplus; 2010 Disponible en: https://docplayer.es/7345384-Enfermedad-arterial-periferica-dr-jose-m-romero.html
- Rozman C, Cardellach F. Medicina Interna. Volumen I. 18 Ed. Elsevier; 2016.
- Serrano FJ, Martín A. Enfermedad Arterial Periférica: aspectos fisiopatológicos, clínicos y terapéuticos. Rev Esp Cardiol 60 (9): 969-82. Disponible en: https://www.revespcardiol.org/es-enfermedad-arterial-periferica-aspectos-fisiopatologicos-articulo-13109651
- Suárez C, Lozano F. Documento de consenso multidisciplinar en torno a la enfermedad arterial periférica. 1ºed. Madrid: Luzán; 2012.
- Teot, Luc, and Norihiko Ohura. "Challenges and management in wound care." Plastic and Reconstructive Surgery 147.1S-1 (2021): 9S-15S.
- Torrealba, J. Ignacio, et al. "Manejo endovascular de la isquemia crítica distal: análisis de una serie contemporánea." Revista médica de Chile 148.12 (2020): 1734-1741.
- Urits I, Seifert D, Seats A, Giacomazzi S, Kipp M, Orhurhu V, et al. Treatment Strategies andEffective Management of Phantom Limb-Associated Pain. Curr Pain Headache Rep. 29 de julio de 2019;23(9):64.
- Villaescusa J. Enfermedad Aterosclerótica. Fisiopatología y factores de riesgo. Disponible en: https://www.google.com/search?q=7.+Villaescusa+J.+Enfermedad+Ateroscler%C3%B3tica.+Fisiopatolog%C3%ADa+y+factores+de+riesgo.&oq=7.%09Villaescusa+J.+Enfermedad+Ateroscler%C3%B3tica.+Fisiopatolog%C3%ADa+y+factores+de+riesgo.+&aqs=chrome..69i57.830j0j15&sourceid=chrome&ie=UTF-8
- Yara Sánchez JE. Enfermedad arterial periférica. En: Lic. Dilayddis Cardero Montoya. Enfermedades vasculares periféricas. Santiago de Cuba: Ciencias Médicas; 2008.: 56-58.
