2.1 INTRODUCCIÓN
Los trastornos cardiovasculares en los niños se dividen en dos grandes grupos: cardiopatías congénitas y trastornos cardíacos adquiridos. Las cardiopatías congénitas (CC) son principalmente anomalías anatómicas presentes al nacer que provocan una función cardíaca anómala. Las consecuencias clínicas de los defectos cardíacos congénitos confluyen en dos amplias categorías, insuficiencia cardíaca (IC) e hipoxemia. Los trastornos cardíacos adquiridos son enfermedades o anomalías que ocurren después del nacimiento y pueden observarse en corazones normales o en presencia de defectos cardíacos congénitos. Estos resultan de varios factores, incluidos infecciones, respuestas autoinmunitarias, factores ambientales y predisposiciones familiares.
En el adulto la causa más frecuente de IC es la cardiopatía isquémica y la hipertensión arterial (HTA), siendo la revascularización y el control de la HTA el tratamiento inicial. Una vez tratada la causa, si persiste la IC existe un amplio arsenal farmacológico, protocolizado en guías clínicas, para tratar grupos de pacientes relativamente homogéneos con disfunción sistólica, diastólica, izquierda o derecha.
En el niño la causa más frecuente son las CC, cuyo principal tratamiento es la cirugía. Existe una gran variedad de CC, varias clasificaciones y multitud de cirugías posibles, lo que condiciona un sustrato muy heterogéneo de pacientes; desde aquellos corregidos totalmente sin lesiones residuales que no precisan tratamiento, hasta el paciente con ventrículo derecho (VD) sistémico con circulación un ventricular. Esta heterogeneidad de la afección y la baja incidencia de la misma dificultan la estandarización del tratamiento de la IC pediátrica.
La segunda causa de IC son las miocardiopatías, fundamentalmente la dilatada (MCD). Estos pacientes constituyen un grupo más homogéneo, con disfunción sistólica del ventrículo izquierdo (VI), sobre los que se realizan la mayoría de los ensayos clínicos con fármacos que en adultos han demostrado efectividad en IC.
2.2 ANATOMÍA
Anatomía torácica relacionada:
MEDIASTINO
El mediastino es la zona central amplia que separa las dos cavidades pleurales situadas lateralmente. Se extiende:
- Desde el esternón hasta los cuerpos vertebrales.
- Desde la abertura torácica superior hasta el diafragma.
El mediastino contiene la glándula del timo, el saco pericárdico, el corazón, la tráquea y las arterias y venas principales. Además, el mediastino sirve como vía de paso a estructuras tales como el esófago, el conducto torácico y a diversos componentes del sistema nervioso cuando traspasan el tórax en su camino hacia el abdomen.
El mediastino medio se localiza centralmente en la cavidad torácica. Contiene el pericardio, el corazón, el origen de los grandes vasos, diversos nervios y pequeños vasos.
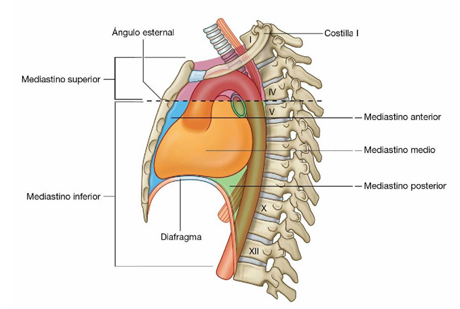
Ilustración 10.Fuente: Drake R, Vogel W, Mitchell A. Subdivisiones del mediastino. GRAY. 2015
PERICARDIO
El pericardio es un saco fibroseroso que rodea al corazón y a la raíz de los grandes vasos. Tiene dos componentes, el pericardio fibroso y el pericardio seroso.
El pericardio fibroso es una capa externa de tejido conjuntivo resistente que establece los límites del mediastino medio. El pericardio seroso es fino y está formado por dos partes:
La capa parietal que recubre la superficie interna de la lámina fibrosa.
La capa visceral (epicardio) de pericardio seroso que se adhiere al corazón y forma su cubierta externa.
Las capas visceral y parietal del pericardio seroso son continuas en la raíz de los grandes vasos. El estrecho espacio creado entre las dos capas de pericardio seroso que contiene una pequeña cantidad de líquido se llama cavidad pericárdica. Este espacio potencial permite el movimiento prácticamente sin restricciones del corazón.
- Pericardio fibroso
El pericardio fibroso es una bolsa en forma de cono con su base en el diafragma y cuyo vértice se continúa con la adventicia de los grandes vasos. La base está unida al tendón central del diafragma y a una pequeña zona muscular del diafragma en el lado izquierdo. Anteriormente, se une a la superficie posterior del esternón a través de los ligamentos esternopericárdicos. Estas inserciones ayudan a mantener la posición del corazón en la cavidad torácica. El saco también limita la distensión cardíaca.
Los nervios frénicos que inervan el diafragma y se originan en los niveles espinales de C3 a C5 atraviesan el pericardio fibroso y lo inervan en su recorrido entre su punto de origen y su destino final. Su localización en el pericardio fibroso está directamente relacionada con el origen embrionario del diafragma y los cambios que se producen durante la formación de la cavidad pericárdica. De igual modo, los vasos pericardiofrénicos también se localizan en el interior del pericardio fibroso proporcionándole inervación en su paso a través de la cavidad torácica.
- Pericardio seroso
La capa parietal del pericardio seroso se continúa con las capas viscerales del pericardio seroso en torno a la raíz de los grandes vasos. Estas reflexiones del pericardio seroso se producen en dos zonas:
- Una superior, rodeando a las arterias, la aorta y el tronco pulmonar.
- La segunda más posterior rodea a las venas, la vena cava superior e inferior y a las venas pulmonares.
El pericardio está irrigado por ramas de las arterias torácica interna, pericardiofrenica, musculofrénica y frénica inferior y la aorta torácica. Las venas del pericardio entran en el sistema de la vena ácigos y en las venas torácica interna y frénica inferior.
Los nervios del pericardio nacen del nervio vago (X), de los troncos simpáticos y de los nervios frénicos. Es importante observar que la fuente de sensibilidad somática (dolor) del pericardio parietal es conducida por el nervio frénico. Por esta razón, el “dolor” referido de la patología pericárdica puede localizarse en la región supraclavicular del hombro.
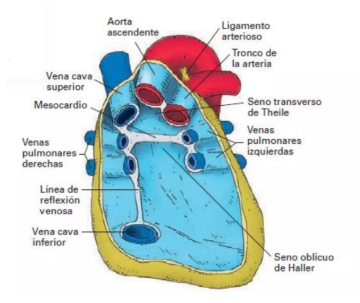
Ilustración 11. Fuente: https://es.slideshare.net/slideshow/corazn-y-pericardio-233021748/233021748#5
Anatomía cardíaca
El corazón es un órgano musculoso con 4 cavidades situado en el mediastino, detrás del cuerpo del esternón. Tiene forma de cono invertido, cuyo borde inferior, denominado ápex, descansa sobre el diafragma, dirigido hacia la izquierda. El borde superior se encuentra por debajo de la segunda costilla. El corazón tiene su propia envoltura, un saco inextensible llamado pericardio, que a su vez tiene dos partes, una fibrosa y otra serosa (epicardio). La pared cardiaca está formada por 3 capas distintas de tejido:
- Epicardio: la más externa (pericardio seroso).
- Miocardio: tejido muscular del corazón.
- Endocardio: membrana que reviste el interior del corazón.
El interior del corazón está dividido en 4 cámaras o cavidades cardiacas, dos en el lado izquierdo y dos en el derecho. Las cavidades situadas en la parte superior son las aurículas, y las situadas en el inferior, los ventrículos.
Corazón derecho: a la aurícula derecha (AD) llega la sangre venosa (no oxigenada) de todo el cuerpo a través de las venas cavas, que desembocan en ella. También desemboca en la aurícula derecha el seno venoso, conducto que recoge la sangre venosa del corazón. La AD se comunica con el ventrículo derecho (VD) a través de la válvula tricúspide. Esta válvula permite el paso de sangre de la aurícula al ventrículo, pero no en sentido contrario (flujo unidireccional). Cuando el corazón se contrae (sístole), la sangre sale del ventrículo derecho a través de la válvula pulmonar, pasa a la arteria pulmonar y ésta la lleva a los pulmones para que se oxigene.
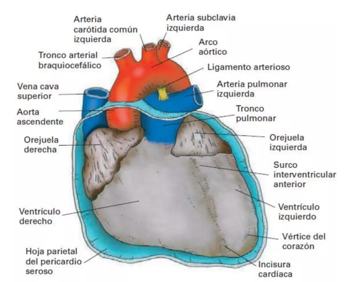
Ilustración 12. Fuente: Drake R, Vogl W, Mitchell A. Superficie anterior del corazón. GRAY. 2015
Corazón izquierdo: en la aurícula izquierda (AI) desembocan cuatro venas pulmonares, responsables de llevar la sangre oxigenada desde los pulmones hasta el corazón. La AI se comunica con el ventrículo izquierdo (VI) a través de la válvula mitral, que permite el paso de la sangre desde la AI hasta el VI, pero no en sentido contrario. Cuando se produce la sístole, la sangre pasa del ventrículo a la arteria aorta a través de la válvula aórtica y es distribuida por todo el organismo. El ventrículo izquierdo es más largo y estrecho que el derecho, de tal forma que la punta del corazón (ápex) está formada por ese ventrículo. El miocardio de los ventrículos es más grueso que el de las aurículas, debido a que se requiere más fuerza para bombear la sangre más lejos.
Tras el nacimiento este recorrido se realiza mediante dos circuitos en serie. La circulación pulmonar es muy compliante y tiene unas resistencias y presión bajas, mientras la circulación sistémica es de presión y resistencias altas.
Fisiología del sistema circulatorio
La actividad eléctrica cardiaca se produce como resultado del movimiento de iones a través de la membrana de las células del miocardio. Los iones que influyen en la actividad eléctrica cardiaca fundamentalmente son el potasio (K+), el sodio (Na+) y el calcio (Ca2+).
El sistema eléctrico o de conducción del corazón da lugar al ritmo sinusal. Este sistema está formado por el nodo sinusal, el nodo auriculoventricular y el haz de His y las fibras de Purkinje.
Nodo sinusal: situado en la aurícula derecha en la desembocadura de la vena cava superior. Inicia cada latido cardiaco y establece su ritmo, por lo que es considerado el marcapasos natural del corazón. Genera los impulsos eléctricos que se extienden por las aurículas hasta el nodo auriculoventricular. La generación de impulsos da lugar a la contracción de las aurículas.
Nodo auriculoventricular (AV): situado también en la pared posterior de la aurícula derecha, próximo al anillo de la válvula tricúspide. Retrasa los impulsos eléctricos, de tal forma que los ventrículos se contraigan después de las aurículas.
El nodo AV recoge el impulso eléctrico y lo proyecta por el Haz de His a las paredes ventriculares, a través de las ramas derecha e izquierda (fibras de Purkinje), de forma que la contracción de ambos ventrículos, el VD y el VI, se realice coordinadamente, impulsando la sangre con fuerza hacia las arterias aorta y pulmonar (AP) que salen del corazón. A la vez, las aurículas se relajan preparándose para la siguiente contracción y admiten sangre que les llega de las venas cavas (aurícula derecha) y de las venas pulmonares (aurícula izquierda). Cuando las aurículas están llenas, el nodo sinusal lanza un nuevo estímulo eléctrico provocando una nueva contracción auricular para llenar otra vez los ventrículos, reanudando así el proceso.
Electrocardiograma
El electrocardiograma (ECG) es el registro gráfico de la actividad eléctrica del corazón, de la conducción de sus impulsos. Las ondas que se observan en el registro son las siguientes:
- Onda P: despolarización auricular, paso de la corriente de despolarización desde el nódulo sinusal por la musculatura de ambas aurículas.
- Complejo QRS: despolarización ventricular. Al tiempo que se despolarizan los ventrículos, las aurículas se repolarizan.
- Onda T: repolarización ventricular.
Ciclo cardiaco
Es la secuencia de elementos eléctricos, mecánicos y sonoros que ocurren durante un latido cardíaco completo. En el ciclo cardiaco existen dos acciones principales, la contracción o sístole y la relajación o diástole de las aurículas y ventrículos.
- Despolarización: Sístole o contracción.
- Repolarización: Diástole o relajación miocárdica.
2.3 VALORACIÓN DE ENFERMERÍA
Semiología cardiovascular:
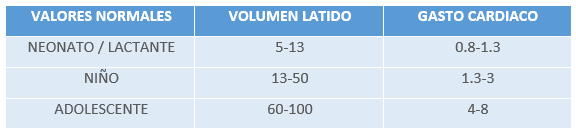
El gasto cardíaco o volumen minuto se define como la cantidad de sangre bombeada cada minuto por cada ventrículo. Se calcula mediante el producto del volumen sistólico, (volumen impulsado en cada latido cardíaco) por la frecuencia cardíaca (número de latidos por minuto).
- Gasto cardiaco (L/min): Volumen de sangre expulsada por el corazón en 1 minuto.
- Volumen sistólico (VS): El volumen de sangre que expulsa el corazón en cada latido.

En un adulto en reposo el gasto cardíaco es de 4-7 L/min, sin embargo, este varía continuamente de acuerdo con las necesidades de oxígeno de los tejidos corporales.
Regulación del gasto cardíaco
La regulación de la función de bombeo del corazón depende de forma directa de los valores de la frecuencia cardíaca y del volumen sistólico. En el estudio de la regulación se diferencian dos tipos:
- Regulación intrínseca, en la que intervienen factores exclusivamente cardíacos
- Regulación extrínseca, determinada por la acción de factores externos.
Regulación de la frecuencia (efecto cronotrópico)
Aunque el corazón tiene una actividad rítmica intrínseca, existen factores externos a la estructura cardíaca que pueden alterar esta frecuencia basal de contracción. Estos factores son de naturaleza nerviosa y hormonal. El sistema nervioso autónomo, a través de sus dos divisiones, simpático y parasimpático, modifica la frecuencia cardíaca.
En un adulto normal la frecuencia cardiaca es de unos 70 latidos/minuto, si ese mismo corazón se le aísla separándose de sus conexiones nerviosas, pasa a realizar 100 latidos/minuto, que es la frecuencia intrínseca de las fibras del nodo sinusal. De esta forma la frecuencia disminuye (bradicardia, o efecto cronotrópico negativo), e incluso si la estimulación parasimpática es muy fuerte puede llegar a pararse el corazón. La bradicardia que se produce durante el sueño, se basa en el incremento de la actividad parasimpática y en la disminución de la actividad simpática.
La estimulación del nervio vago también disminuye la velocidad de conducción del impulso cardíaco, efecto conocido con el término de dromotrópico negativo.
En sentido opuesto se encuentra la acción del sistema simpático, la estimulación simpática que puede aparecer en situaciones de intenso ejercicio físico o de estrés, aumentan la frecuencia cardíaca (taquicardia, o efecto cronotrópico positivo) hasta alcanzar frecuencias de 200-220 latidos/minuto. La velocidad de conducción también se incrementa por la estimulación simpática (dromotrópico positivo).
Además de las acciones debidas a la actividad del sistema nervioso autónomo, existen otros factores que tienen influencia sobre la frecuencia cardíaca. Así, la temperatura, cuyo aumento tiene un efecto cronotrópico positivo. Este efecto, puramente físico, es debido simplemente al hecho de que el aumento de energía térmica da lugar a una mayor movilidad iónica.
Por último, también la concentración de potasio extracelular juega un papel importante sobre la frecuencia. Los incrementos de potasio producen disminuciones de frecuencia y también de la velocidad de conducción del potencial de acción cardíaca.
Regulación del volumen sistólico (efecto inotrópico)
El volumen sistólico es el volumen de sangre impulsado por el ventrículo en cada latido, su valor viene determinado principalmente por la fuerza de contracción (contractilidad) del músculo cardíaco. Los factores que afectan a esta propiedad se denominan factores inotrópicos, y como en la frecuencia, se consideran positivos cuando aumentan la contractilidad y negativos cuando la disminuyen.
A diferencia de la frecuencia que sólo estaba influenciada por factores extrínsecos, el volumen sistólico dispone de dos tipos de mecanismos de regulación diferenciados por su origen. Existen dos factores importantes en la forma de regulación intrínseca que influyen en la respuesta táctil del músculo cardíaco. Estos factores son:
- La precarga. Definida como la tensión pasiva que determina, en el músculo cardíaco, la longitud inicial de las fibras antes de la contracción; es decir, la distensión de las fibras (o volumen diastólico final). Dentro de ciertos límites, existe una relación proporcional entre el incremento de la precarga y la respuesta táctil del músculo cardíaco, representada por la curva de Starling. A mayor volumen diastólico final, mayor volumen sistólico, lo cual garantiza que una mayor afluencia o entrada de sangre al corazón se va a ver compensada por una contracción más enérgica y una salida proporcionalmente también mayor; o, en otros términos, el corazón bombea toda la sangre que recibe sin permitir acumulación y ajusta el retorno venoso con el gasto cardíaco. Este comportamiento se conoce como ley de Frank-Starling y una de las funciones que explica es el equilibrio de gasto cardíaco de los ventrículos derecho e izquierdo.
- La poscarga. Es la carga frente a la que deben acortarse las fibras miocárdicas durante la sístole, dicho de otro modo, la carga que debe desplazar el músculo después de iniciarse la contracción. Para el ventrículo izquierdo, la poscarga viene dada por la presión en la aorta.
Regulación extrínseca del volumen sistólico:
Existen una serie de factores extrínsecos que pueden modificar la contractilidad del corazón. El sistema nervioso autónomo es uno de los reguladores principales en la contractilidad de las fibras miocárdicas. En condiciones basales la influencia predominante es simpática, y su efecto es un aumento de la contractilidad (efecto inotrópico positivo) aumentando el vaciado del ventrículo y el incremento de presión sistólica.
Otros factores son las concentraciones iónicas de potasio, calcio, un aumento de la concentración de potasio extracelular o una disminución de la concentración de calcio tienen un efecto inotrópico negativo, al igual que los descensos de pH sanguíneo.
Signos y síntomas frecuentes en pacientes con alteraciones cardiovasculares:
Aunque el soplo en un niño asintomático puede deberse a una cardiopatía, hay que recordar que la inmensa mayoría de los soplos en la infancia son inocentes. Por otra parte, cabe subrayar que no toda cardiopatía asocia soplo.
En cuanto a las cardiopatías congénitas sintomáticas, las manifestaciones clínicas de las innumerables formas heterogéneas de cardiopatías congénitas se resumen en 2 cuadros:
- Cianosis
- Insuficiencia cardíaca
Habitualmente las cardiopatías que dan cianosis no dan insuficiencia cardíaca y viceversa. Excepciones a esta regla son, por ejemplo, el ventrículo izquierdo hipoplásico y el drenaje venoso pulmonar anómalo total obstructivo que asocian ambos cuadros clínicos.
2.4 CLASIFICACIÓN DE LA PATOLOGÍA PEDIÁTRICA
Manifestaciones clínicas de las cardiopatías congénitas:
Las cardiopatías congénitas se manifiestan fundamentalmente por cianosis, soplos cardíacos, disnea, palpitaciones, dolor precordial, pobre desarrollo ponderal, síncope, hipertensión sistémica, estridor laríngeo o disfagia y shock cardiogénico. Se requiere de una orientación diagnóstica clínica que permita llegar, con el apoyo de métodos diagnósticos disponibles como la electrocardiografía, la radiografía, el ecocardiograma en sus diversas modalidades, el cateterismo cardíaco, la tomografía computarizada helicoidal y la resonancia magnética, a un diagnóstico preciso que dé sustento al plan terapéutico.
- La cianosis se define como la coloración azul de las mucosas, secundario a la presencia de más de 5 g/dL de hemoglobina reducida en la sangre, de modo que la aparición de cianosis depende fundamentalmente de la concentración de hemoglobina reducida en sangre. Si la concentración de hemoglobina es inferior a 10 g/dL, la cianosis no será detectada clínicamente, ya que con saturaciones arteriales de oxígeno de 80% no habrá la suficiente hemoglobina reducida para que se manifieste la cianosis. Con sustento en lo anterior, es muy importante una evaluación clínica completa, puesto que la ausencia de cianosis no descarta necesariamente la presencia de una cardiopatía congénita cianosante.
Respecto del valor de la cianosis como signo, se debe de tener en cuenta el hecho de que muchas cardiopatías congénitas presentan una saturación de oxígeno a niveles en los que la cianosis no es detectada, como ya fue mencionado. Otras veces, niños portadores de cardiopatías congénitas no cianosantes muestran cianosis por la presencia de insuficiencia cardíaca o infecciones pulmonares intercurrentes. También puede existir cianosis secundaria al llanto, por la exposición al agua, al frio, hipoglucemia, sepsis, entre otras, siendo más evidente en el recién nacido y en el lactante.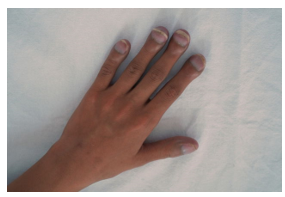
Ilustración 13. Fuente: Bezerra C. Acropaquia. Tua Saúde. 2024.
- Se considera al hipocratismo digital, o dedos en "palillo de tambor", como uno de los signos clínicos más antiguamente referidos. Si bien presente en diversas patologías, entre ellas algunas neoplásicas, es un hallazgo común en los pacientes con cardiopatías congénitas cianosantes. El signo es consecutivo a cortocircuitos extrapulmonares que ocasionan que grandes fragmentos de megacariocitos accedan a la circulación sistémica, provocando la liberación de factores de crecimiento endotelial y activación plaquetaria a nivel de la circulación distal, lo que condiciona osteoartropatía hipertrófica. La expresión del factor de crecimiento endotelial vascular (VEGF, por sus siglas en inglés) se encuentra elevada en una proporción de 10 a 50 veces en los pacientes con hipoxia; este factor ocasiona hiperplasia vascular, edema y proliferación de fibroblastos y osteoblastos.
Las alteraciones más importantes que pueden explicar el porqué de la desaturación arterial se encuentran en el sistema respiratorio, hematológico y cardiovascular. La historia clínica puede orientar hacia un problema pulmonar como explicación de la cianosis si se encuentra taquipnea, tiraje intercostal, hipoventilación o presencia de ruidos respiratorios anormales. Una etiología cardíaca puede ser sospechada ante la presencia de shock, insuficiencia respiratoria, soplo cardíaco, si bien debemos de recordar que diversas cardiopatías congénitas complejas tienen poca expresión acústica en el período neonatal. En el terreno hematológico, el registro de un PO2 normal con bajas saturaciones arteriales obliga a sospechar la presencia de metahemoglobinemia, y un hematocrito elevado, la posibilidad de policitemia.
- En ocasiones, la realización de la prueba de hiperoxia puede dilucidar entre una patología pulmonar con alteración en la difusión y una cardiopatía congénita con cortocircuito de derecha a izquierda. El uso de oxígeno al 100%, ya sea por tubo endotraqueal o mascarilla por 10 minutos, puede permitir observar cambios en cuanto a la disminución en el grado de cianosis. Si obtenemos mejoría en forma ostensible, el problema es a nivel pulmonar, mientras que, si el cambio es ligero, nos encontramos ante una cardiopatía. La elevación de la PO2≥ 300 mmHg se orienta a un problema de difusión pulmonar.
- Otro procedimiento consiste en medir la PCO2, que está elevada en procesos pulmonares, mientras que en las cardiopatías puede ser normal o estar disminuida. Los riesgos de la prueba de hiperoxia, fundamentalmente en neonatos, incluyen el peligro de provocar el cierre del conducto arterioso en pacientes con cardiopatías congénitas conducto-dependientes y condicionar hipoxia y shock. Aun con la adecuada elaboración de la historia clínica y de las pruebas diagnósticas mencionadas, en muchas ocasiones no es posible dilucidar si la desaturación es secundaria a cardiopatía congénita o bien a un patrón fetal persistente o a hipertensión pulmonar, membrana hialina, malformaciones arteriovenosas, por mencionar las más habituales, por lo cual resulta primordial para establecer un diagnóstico de certeza la realización de un ecocardiograma por personal experimentado.
- La presencia de soplo en el área cardíaca en muchos casos es el signo pivote que conduce a sospechar la posibilidad de una cardiopatía congénita. Por definición, los soplos son manifestaciones auscultatorias de turbulencia del flujo sanguíneo; sus características dependen del radio del vaso sanguíneo o la estructura cardíaca, de la velocidad del flujo y del grado de viscosidad sanguínea. La presencia de soplo no implica en forma necesaria patología cardíaca. Un estado hiperdinámico condicionado por anemia, infección, ansiedad extrema, fiebre o hipertiroidismo, entre otros, se asocia a la presencia de soplo cardíaco.
- El pulso yugular como signo de incremento en la presión auricular derecha y de insuficiencia congestiva-venosa es de muy difícil evaluación en los pacientes recién nacidos, lactantes y preescolares; en estos grupos etarios el tamaño del hígado es un signo más confiable para la evaluación de congestión venosa. En el recién nacido en condiciones clínicas normales se puede palpar el borde hepático a 2.5 cm por debajo del reborde costal, y en los lactantes menores es en promedio de 2 cm. En todo paciente con soplo cardíaco y síndrome febril, además, se deberá explorar la posibilidad de crecimiento del bazo ante el riesgo de endocarditis bacteriana.
- Las palpitaciones son un síntoma común en la edad pediátrica y pueden estar o no acompañadas de otros síntomas como dolor precordial, síncope o visión borrosa, por mencionar algunas. Se refiere una frecuencia de hasta 16%, pero sólo en un bajo porcentaje de estos pacientes (≤10%) están asociados a una verdadera arritmia. Es de suma importancia la realización de una historia clínica cuidadosa para definir la frecuencia, duración y asociación con síncope o con los esfuerzos. Se deberá indagar insistentemente el antecedente de muerte súbita en la familia.
- El dolor precordial es motivo frecuente para llevar pacientes pediátricos a un servicio de urgencias o referirlos con el cardiólogo pediatra. En un estudio se relata que el dolor precordial representó 6 de cada 1000 consultas en un servicio de urgencias y fue la segunda indicación de envío para el cardiólogo pediatra. En aproximadamente el 75% de los casos el dolor es idiopático o explicado por una alteración músculo-esquelética o costocondral.
Cardiopatías congénitas:
Las cardiopatías congénitas son lesiones anatómicas de una o varias de las cuatro cámaras cardíacas, de los tabiques que las separan, o de las válvulas con origen congénito (de nacimiento) cuya causa exacta se desconoce. A día de hoy se detectan durante la vida fetal en su mayoría o en los primeros días, semanas o meses del nacimiento. Sin embargo, no todas las cardiopatías, aunque sean congénitas, están presentes en el momento de nacer. Algunas se manifiestan días, semanas, meses o incluso años después, y sin embargo su origen es también congénito, pues al nacer existía ya la tendencia o predisposición a que se generará posteriormente esa cardiopatía.
Actualmente se desconoce la verdadera causa de las anomalías o deficiencias del desarrollo cardíaco, pero se cree que en la génesis de las cardiopatías congénitas se hallen implicadas alteraciones genéticas, la mayoría de las cuales aún no están identificadas.
INCIDENCIA:
En la población general aparecen 8 cardiópatas por cada 1.000 nacidos vivos. Y en España nacen al año 5.000 niños con algún tipo de cardiopatía. La mayoría son cardiopatías leves que desaparecen espontáneamente con el tiempo. Sin embargo, alrededor de 2.000 niños son operados al año en nuestro país, y al menos 6.500 niños en Europa, a causa de una cardiopatía congénita.
CLASIFICACIÓN:
Existen numerosas cardiopatías congénitas y también diversas formas de clasificarlas tanto por su fisiopatología como por su presentación clínica o su anatomía.
Relacionada con las aurículas y de sus conexiones venosas:
DRENAJE VENOSO PULMONAR ANÓMALO TOTAL (DVPAT):
El drenaje venoso pulmonar anómalo total (DVPAT) es una cardiopatía congénita caracterizada por la ausencia de conexión directa entre todas las venas pulmonares y la aurícula izquierda del corazón. El retorno venoso pulmonar confluye entonces en la aurícula derecha o en alguna de sus venas tributarias.
La existencia de una comunicación interauricular (CIA) o de un foramen oval permeable que precargue la aurícula izquierda es imprescindible para asegurar la supervivencia posparto de estos pacientes.
La frecuencia de presentación de la conexión venosa pulmonar anómala total es baja. Supone el 1-3% del total de cardiopatías congénitas en corazones con concordancia auriculoventricular y ventrículo-arterial.
El diagnóstico de DVPAT es por sí mismo indicación de cirugía reparadora. El momento de realizarla lo condiciona la presencia o no de clínica obstructiva. Esta última situación se considera una urgencia quirúrgica. En neonatos críticos con obstrucción exclusivamente a nivel auricular, puede contemplarse la maniobra de Rashkind (auriculoseptostomía percutánea) y diferir la cirugía reparadora 24-48 h, una vez conseguida la estabilización clínica del paciente.
El principal problema hemodinámico en el postoperatorio inmediato de estos pacientes son las crisis de hipertensión pulmonar. Según las series, la incidencia de hipertensión pulmonar tras la cirugía del DVPAT obstructivo está cifrada en torno al 45%. Estas crisis van a venir determinadas clínicamente por la aparición brusca de hipotensión arterial, hipoxemia, acidosis y disminución brusca del gasto cardíaco.
La mortalidad hospitalaria es, según la escala de riesgo quirúrgico RACHS-1, del 3,4% (categoría 2) para los DVPAT reparados fuera del período neonatal, mientras que en aquellos que se corrigen antes del primer mes de vida se eleva al 19,4% (categoría 4).
Aquellos pacientes que sobreviven los 2 primeros años después de la cirugía tienen una expectativa de vida desde el punto de vista cardiológico similar a la población normal, con excelente grado funcional y sin necesidad de medicación. Los marcapasos ectópicos auriculares sin repercusión clínica son muy frecuentes, afectando entre el 50 y el 80% de los pacientes intervenidos. La principal causa de reintervención (5-20% de los pacientes que sobreviven a la cirugía) es la obstrucción del retorno venoso pulmonar. Cuando aparece, suele hacerlo en los primeros 6-12 meses posquirúrgicos.
DRENAJE VENOSO PULMONAR ANÓMALO PARCIAL (DVPAP):
En el drenaje venoso pulmonar anómalo total (DVPAT), las cuatro venas pulmonares drenan equivocadamente en la aurícula derecha. En el drenaje venoso pulmonar anómalo parcial (DVPAP) algunas de las venas pulmonares, habitualmente las derechas, en vez de desembocar en la aurícula izquierda, conectan con la aurícula derecha de forma directa o a través de alguna de las venas que llegan a ésta. Suele asociarse con una comunicación interauricular (CIA).
La clínica del paciente va a depender del número de venas que drenan anómalamente. Los pacientes con una sola vena anómala, están, en la mayoría de los casos, asintomáticos, mientras que aquellos que presenten 3 venas conectadas de forma anómala presentarán una clínica muy similar al DVPAT.
La forma más frecuente de DVPAP es el drenaje anómalo de las dos venas derechas y cursan con:
- La mayoría están asintomáticos o tienen síntomas leves de catarros frecuentes, curva de peso lenta, etc.
- Menos frecuentemente presentan síntomas de insuficiencia cardíaca en edad temprana.
- Los pacientes con síndrome de la cimitarra presentan con frecuencia síntomas de inicio precoz con escasa ganancia ponderal, sudoración y fatiga. En ocasiones pueden presentar cianosis y episodios de neumonía de repetición (en relación con anomalías pulmonares asociadas a esta malformación).
El diagnóstico se establece en la mayor parte de los casos mediante ecocardiografía. En casos más complejos puede ser necesario realizar resonancia magnética o cateterismo.
El tratamiento es quirúrgico. El cirujano redirige las venas pulmonares afectadas hacia la aurícula izquierda, y cierra la CIA, si existe.
No se indica cirugía si únicamente hay una vena anómala, pues es escasa la sangre que drena anómalamente y no justifica el riesgo de una intervención.
COMUNICACIÓN INTERAURICULAR (CIA):
Es un defecto a nivel del tabique interauricular. Se distinguen varios tipos:
- Ostium Secundum: Se localiza en la porción central del tabique interauricular. Es el más común.
- Ostium Primum: Solo asocia el defecto a nivel de las aurículas y de las válvulas.
- Seno venoso: Se localiza en la porción posterior del tabique a nivel de la desembocadura de venas cavas (superior e inferior).
- Foramen oval permeable: Es el defecto que de forma normal (fisiológica) se tienen todos intraútero y que puede persistir hasta los 18 meses abierto de forma no patológica.
Son asintomáticos en su mayoría. Suelen diagnosticarse por un soplo cardiaco a partir de los 2-3 años, aunque muchos ya son vistos en época neonatal de forma no patológica. Produce sobrecarga de volumen de cavidades derechas (AD y VD) con ligero hiperaflujo pulmonar. A la auscultación, cuando el defecto es moderado-grande suelen ocasionar un soplo sistólico. El ECG puede ser normal o dar datos de crecimiento de ventrículo derecho y la radiografía tórax suele ser normal.
El tratamiento puede demorarse hasta épocas superiores a los 3 años de vida y dependiendo del tamaño y de los bordes del defecto (para lo cual se requerirán generalmente otras exploraciones complementarias como ecocardiografía transesofágica o resonancia magnética en el caso de CIAs tipo seno venoso para valorar el defecto y los drenajes de las venas pulmonares) se elegirá tratamiento quirúrgico (cirugía bajo CEC con cierre del defecto mediante sutura directa o con un parche de pericardio generalmente, de elección en los defectos tipo ostium primum y seno venoso) o cierre mediante cateterismo percutáneo (solo posible en defectos tipo ostium secundum o foramen oval permeable con buenos bordes para el implante del dispositivo) con la implantación de diversos dispositivos que se colocaran en el defecto ocluyendo el paso de sangre a su través.
A nivel de la conexión auriculoventricular:
INSUFICIENCIA MITRAL CONGÉNITA:
La insuficiencia mitral consiste en el retroceso de la sangre del ventrículo izquierdo a la aurícula izquierda y pulmones cada vez que late el ventrículo izquierdo. La insuficiencia mitral puede ser de origen congénito, en cuyo caso se debe a malformaciones de la propia válvula, incluyendo dilatación del anillo mitral, lesiones de las valvas o malformaciones de las cuerdas y músculos papilares.
La sangre que se escapa por un cierre inadecuado de la válvula retrocede a la aurícula izquierda; el exceso de sangre en esta cámara provoca su dilatación y el aumento de presión en su interior, impidiendo el drenaje adecuado de las venas pulmonares. Retrógradamente, ocasiona la acumulación de sangre en los pulmones. Este exceso de líquido en el pulmón es el responsable de la aparición de dificultad respiratoria y el aumento de infecciones respiratorias.
En los casos leves de insuficiencia mitral no se desarrollan síntomas, y los moderados también pueden ser asintomáticos o presentar fatiga con el esfuerzo. De hecho, la insuficiencia mitral es muy bien tolerada durante años por los pacientes. Si la insuficiencia mitral es severa aparecerá dificultad para la alimentación, retraso ponderal, sudoración aumentada, respiración rápida y cuadros infecciosos respiratorios de repetición.
El ecocardiograma es una prueba fundamental para el diagnóstico y seguimiento de la insuficiencia mitral. Si no se visualiza adecuadamente la válvula mitral mediante el ecocardiograma transtorácico, se puede recurrir a la ecografía transesofágica.
La reparación valvular quirúrgica está indicada en los casos de insuficiencia mitral severa con síntomas sin respuesta al tratamiento, o edema pulmonar con hipertensión pulmonar. También se debe indicar la cirugía si tiene insuficiencia mitral severa con disfunción ventricular, aunque el paciente esté asintomático.
No es infrecuente la doble lesión mitral, es decir, estenosis e insuficiencia a la vez, que hace más difícil la reparación conservadora, siendo el implante de prótesis artificial más frecuente en estos casos.
ESTENOSIS MITRAL CONGÉNITA:
Es una malformación cardíaca rara que aparece en el 0,5% de los pacientes con cardiopatías congénitas. En la estenosis mitral, la sangre oxigenada que llega a la AI se encuentra con un obstáculo que impide su paso al ventrículo izquierdo. Dada esta dificultad al paso de la sangre, se reparte menos sangre oxigenada al cuerpo y se acumula en la AI, que se hace más grande de lo normal. Como la aurícula izquierda no puede acumular todo el exceso de sangre que recibe, ésta se queda estancada en los pulmones, ocasionando dificultad respiratoria. La obstrucción al flujo puede producirse por afectación de las valvas, del anillo (el tejido fibroso que soporta la válvula), del aparato subvalvular o por tejido accesorio.
Existen varios tipos:
- Estenosis supramitral.
- Anillo mitral pequeño o hipoplásico.
- Las valvas son displásicas o anómalas.
- Las cuerdas que fijan la válvula al músculo papilar son gruesas, rígidas y cortas.
En caso de estenosis grave, los síntomas aparecen durante los dos primeros años de vida y consisten en escasa ganancia de peso, respiración rápida, cansancio y sudoración con las tomas. Los niños mayores presentan intolerancia a los esfuerzos físicos y desarrollan hipertensión pulmonar. En algunos niños aparecen arritmias como consecuencia del crecimiento de la aurícula izquierda.
En los niños que tienen lesiones leves y/o pocos síntomas se deben utilizar inicialmente diuréticos para evitar el exceso de líquido en los pulmones y vigilarlos estrechamente, posponiendo la operación para más adelante.
La cirugía depende de la anatomía o de la presencia de tejido accesorio. En casos seleccionados con anatomía favorable se puede realizar dilatación de la válvula mitral con balón mediante cateterismo, lo que nos permitiría retrasar la cirugía mientras el niño sea muy pequeño.
DEFECTOS DEL SEPTO AURICULOVENTRICULAR:
Los defectos auriculoventriculares (AV) son cardiopatías congénitas caracterizadas por un defecto u orificio en el tabique interauricular e interventricular, que además presentarán una sola válvula para el lado derecho e izquierdo del corazón o una válvula parcialmente separada, en lugar de las dos válvulas originales.
Hay 3 tipos de defectos septales:
- Canal AV parcial o incompleto: con un defecto del tabique auricular.
- Canal AV transicional: con un defecto del tabique ventricular de tamaño pequeño o moderado además del defecto del tabique auricular.
- Canal AV completo: con un defecto del tabique de tamaño grande que incluye tanto las aurículas como los ventrículos y una única válvula auriculoventricular.
El defecto del septo auriculoventricular completo causa a menudo un cortocircuito de izquierda a derecha, lo que significa que parte de la sangre que ya ha recogido el oxígeno de los pulmones atraviesa el tabique y vuelve a los pulmones. Estos lactantes pueden desarrollar insuficiencia cardiaca, que provoca síntomas tales como respiración rápida, dificultad al comer, retraso en el crecimiento y sudoración, a las 4 a 6 semanas de edad. Al cabo del tiempo, puede desarrollar hipertensión pulmonar y conducir a una insuficiencia cardíaca.
El tratamiento de los defectos del tabique auriculoventricular generalmente es con cirugía y cuando el lactante tiene entre 2 y 4 meses de edad.
ENFERMEDAD DE EBSTEIN:
En la anomalía de Ebstein la válvula tricúspide está mal formada y adherida a la pared del ventrículo derecho, cerrándose a un nivel mucho más inferior de lo normal, siendo la aurícula derecha de un tamaño mucho mayor al normal porque parte del ventrículo derecho forma parte de ella debido a la anomalía de inserción valvular (ventrículo derecho atrializado).
La válvula tricúspide es disfuncionante existiendo diversos grados de insuficiencia y/o estenosis valvular, asociando además diversos grados de bajo desarrollo del ventrículo derecho y del árbol vascular pulmonar (más frecuente cuando la enfermedad es neonatal).
A nivel circulatorio, la sangre desoxigenada llega a la aurícula derecha y trata de pasar al ventrículo derecho a través de la válvula tricúspide, pero debido a la pequeñez del ventrículo derecho y a la insuficiencia tricúspide, es poca la sangre que llega a los pulmones, pasando el resto de sangre a través de la comunicación interauricular (CIA) hasta la aurícula izquierda, donde se mezcla con la sangre oxigenada que viene del pulmón y se vuelve sangre de mezcla. Esta sangre de mezcla pasa al ventrículo izquierdo, sale por la aorta y en parte se dirige a perfundir todo el cuerpo, ocasionando el color cianótico de estos niños. Desde la aorta, una cantidad variable de sangre pasa por el ductus a la arteria pulmonar y pulmones, supliendo en parte la falta de sangre que llega a través del ventrículo derecho.
La anomalía de Ebstein puede asociarse además a otras malformaciones cardíacas:
- La CIA o foramen oval amplio es la más frecuente.
- Nos podemos encontrar con diferentes grados de estenosis pulmonar o atresia pulmonar.
- Hasta uno de cada cuatro pacientes con Ebstein pueden tener anomalías en el sistema de conducción eléctrica.
Existen diferentes grados de afectación de la válvula tricúspide y del ventrículo derecho y, consecuentemente, las manifestaciones clínicas pueden ser muy variables:
- La forma neonatal, la anomalía de Ebstein puede presentarse como un cuadro muy grave con gran riesgo para la vida del recién nacido. En este periodo, se añade la hipertensión arterial pulmonar típica del neonato, ocasionando una mayor dificultad para que la sangre llegue en cantidad suficiente a los pulmones para oxigenarse (se asocia a diversos grados de bajo desarrollo del árbol pulmonar).
- Otra forma del lactante o preescolar-escolar, que generalmente están asintomáticos o son remitidos por un soplo cardiaco detectado en la exploración rutinaria o bien debutan con una arritmia, ya que asocian anomalías en el sistema eléctrico (preexcitación ventricular – Síndrome de Wolff-Parkinson-White). En otros, esta enfermedad puede manifestarse en forma de intolerancia al realizar esfuerzos físicos.
El tratamiento de las formas neonatales es vital el uso de prostaglandinas para mantener el Ductus abierto. Además de la medicación cardiológica, en cuadros graves podemos necesitar la ayuda de respiradores artificiales para que el paciente esté más estable. Si el neonato presenta cianosis grave sin respuesta al tratamiento o con obstrucción anatómica importante del ventrículo derecho, se debe valorar la cirugía cardíaca (corrección univentricular como si fuera ventrículo único).
Las formas tardías y asintomáticas no suelen requerir cirugía hasta la edad adulta, siendo la reparación valvular la mejor opción. Hay que recordar siempre el tratamiento de las posibles arritmias asociadas.
ATRESIA TRICUSPÍDEA:
Se produce por la no perforación de la válvula tricúspide, con diversos grados de bajo desarrollo del ventrículo derecho. Suele asociar un defecto septal ventricular y puede asociar anomalías en la salida de las grandes arterias, como trasposición de las mismas o bajo desarrollo / hipoplasia de la arteria pulmonar o la arteria aorta.
El tratamiento inicial dependerá de si existe obstrucción pulmonar o no, en caso afirmativo puede ser necesario realizar una fístula aorto pulmonar inicialmente para suplir el flujo del ductus; mientras en caso de no existir obstrucción pulmonar probablemente será necesario el cierre médico o quirúrgico ductal y la realización de un cerclaje o “banding” de la arteria pulmonar con el fin de evitar el hiperaflujo a los pulmones. En un segundo estadio se realizará anastomosis cavopulmonar superior (Glenn Bidireccional) antes del año de vida (entre los 4 y 8 meses) y a partir de los 2 años de vida se realizará la conexión cavopulmonar completa (Fontan).
A nivel de los ventrículos:
SÍNDROME DE CORAZÓN IZQUIERDO HIPOPLÁSICO:
Es una enfermedad que ocurre cuando partes del lado izquierdo del corazón no se desarrollan por completo. Como la válvula mitral, el ventrículo izquierdo y la válvula aórtica son hipoplásicas (a menudo con atresia aórtica), la sangre oxigenada que ingresa en la aurícula izquierda de los pulmones es derivada a través de la comunicación interauricular al corazón derecho, donde se mezcla con el retorno venoso sistémico desaturado. Esta sangre relativamente desaturada sale del ventrículo derecho a través de la arteria pulmonar hacia los pulmones y a través del conducto arterioso hacia la circulación sistémica.
El flujo sanguíneo sistémico se mantiene sólo a través del cortocircuido derecha-izquierda a través del ductus arterioso; por lo tanto, la supervivencia inmediata depende de la permeabilidad del ductus arterioso.
Los síntomas del síndrome de hipoplasia del corazón izquierdo aparecen cuando el ductus arterial comienza a cerrarse durante las primeras 24-48 h de vida. Luego, se instala con rapidez el cuadro clínico de shock cardiogénico (taquipnea, disnea, pulso débil, palidez, cianosis, hipotermia, acidosis metabólica, letargo, oliguria o anuria).
A menudo, se presenta un soplo sistólico suave no específico, así como hepatomegalia. La acidosis metabólica grave a menudo empeora si se administra oxígeno suplementario, lo que es característico del síndrome de corazón izquierdo hipoplásico.
El diagnóstico del síndrome del corazón izquierdo hipoplásico se sospecha clínicamente, sobre todo en los recién nacidos con acidosis metabólica que empeora después de recibir oxígeno; el oxígeno disminuye la resistencia vascular pulmonar y por lo tanto aumenta la proporción relativa de la salida del ventrículo derecho que fluye a los pulmones en lugar de fluir a través del conducto arterioso permeable al cuerpo. El diagnóstico se confirma por ecocardiografía.
Actualmente, la mayoría de los pacientes con síndrome de corazón izquierdo hipoplásico ahora son diagnosticados con ecografía prenatal o ecocardiografía fetal, lo que permite el inicio de la prostaglandina E1 y otras terapias apropiadas inmediatamente después del nacimiento y antes de que ocurra la hipoperfusión de los órganos.
TRATAMIENTO:
Se infunde prostaglandina E1 (PGE1) (en dosis inicial de 0,05 a 0,1 mcg/kg/min en perfusión continua intravenosa) para prevenir el cierre del conducto arterioso o reabrir uno cerrado. Los recién nacidos en estado grave con shock cardiogénico pueden requerir fármacos inotrópicos positivos (por ejemplo: milrinona), diuréticos para mejorar la función cardíaca y controlar el estado de volumen y generalmente requieren intubación traqueal y ventilación mecánica.
Como el oxígeno es uno de los vasodilatadores pulmonares más potentes, se ventila para alcanzar saturaciones sistémicas del 70-80%. Si el lactante requiere ventilación mecánica, puede controlarse la PCO2 en el rango normal o ligeramente elevado. La resistencia vascular sistémica se maneja evitando o minimizando el uso de fármacos vasoconstrictores (por ejemplo: adrenalina o dopamina en alta dosis). La milrinona puede ser beneficiosa porque puede provocar vasodilatación sistémica.
PROCEDIMIENTOS QUIRÚRGICOS:
En última instancia, la supervivencia requiere procedimientos quirúrgicos en varios tiempos que permiten que el ventrículo derecho funcione como el ventrículo sistémico y establecen una fuente controlada de flujo sanguíneo pulmonar.
- El tiempo 1, que se realiza durante la primera semana de vida, es el procedimiento de Norwood. Se secciona el tronco pulmonar, se cierra de forma distal con un parche, y se forma una neoaorta combinando la aorta hipoplásica y la arteria pulmonar proximal. Se liga el ductus arterioso. El flujo sanguíneo pulmonar se restablece mediante la inserción de una derivación de Blalock-Taussig-Thomas modificada del lado derecho o un conducto entre el ventrículo derecho y la arteria pulmonar (modificación de Sano). Por último, se amplía la comunicación interauricular.
- El tiempo 2, que se realiza a los 3-6 meses de edad, consiste en una operación bidireccional de Glenn o un procedimiento de hemi-Fontan. Estos procedimientos conectan la vena cava superior con la arteria pulmonar derecha, lo que permite que aproximadamente la mitad del retorno venoso sistémico evite la aurícula derecha y fluya directamente a los pulmones para su oxigenación. A diferencia del procedimiento de Glenn bidireccional, el hemi-Fontan no desinserta completamente la vena cava superior de la aurícula derecha.
- La tercera etapa, realizada entre los 18 y los 36 meses, es un procedimiento de Fontan modificado, en el cual se deriva el flujo de la vena cava inferior hacia la confluencia de la vena cava superior y la arteria pulmonar.
El riesgo de mortalidad en los niños con síndrome del corazón izquierdo hipoplásico es mayor en el primer año de vida. Alrededor del 90% de los pacientes que sobreviven a la lactancia vivirán hasta los 18 años. Como ocurre con otros niños con cardiopatías congénitas complejas, los sobrevivientes pueden presentar algún grado de alteración neuromadurativa, que puede deberse a alteraciones del desarrollo preexistentes del sistema nervioso central, hipoperfusión del sistema nervioso central o tromboembolias que se producen durante los procedimientos en múltiples tiempos.
En algunos lactantes con síndrome de hipoplasia del corazón izquierdo, en particular aquellos con disfunción grave de la válvula tricúspide o el ventrículo, el trasplante cardíaco se considera el procedimiento de elección; sin embargo, debe continuar con la infusión de PGE1 junto con manejo cuidadoso de la resistencia vascular pulmonar y sistémica hasta disponer de un corazón donante. Como la disponibilidad de corazones donantes es muy limitada, alrededor del 20% de los lactantes mueren mientras aguardan un trasplante. Tras el trasplante cardíaco, se requieren inmunosupresores.
Conexión ventriculoarterial:
ATRESIA PULMONAR CON SEPTUM INTERVENTRICULAR INTACTO:
En esta cardiopatía congénita la válvula pulmonar no se llega a formar adecuadamente durante el desarrollo fetal, y como resultado, no hay flujo desde el ventrículo derecho a la arteria pulmonar, pudiendo asociar grados más o menos importantes de hipoplasia de ventrículo derecho y de la válvula tricúspide, que puede estar afectada tanto en su forma como en su función.
El término “septo intacto” se refiere a que no hay ningún tipo de conexión/agujero entre los dos ventrículos. Por lo tanto, es necesario que exista un foramen oval permeable o una comunicación interauricular (CIA) para descomprimir la aurícula derecha.
Durante los primeros días de vida, el recién nacido precisará una fuente de flujo sanguíneo hacia los pulmones para poder oxigenarse, debido a que no dispone de flujo pulmonar procedente del ventrículo derecho. Esto se consigue gracias a que el ductus permanece abierto, ya sea de forma natural o gracias a la administración de prostaglandinas. En aquellos neonatos con una comunicación interauricular (Ya sea un foramen oval permeable o una CIA) restrictiva, se deberá realizar una atrioseptostomía con balón (Rashkind) para descomprimir la aurícula derecha.
Con los avances técnicos, el cateterismo terapéutico puede proporcionar en algunos casos seleccionados la reparación total sin necesidad de cirugía. El aporte de flujo pulmonar se consigue por el propio ductus, que se mantiene abierto gracias a la colocación de un stent ductal, y conectando el ventrículo derecho a la arteria pulmonar mediante la perforación de la válvula pulmonar.
Esta cardiopatía es grave y puede provocar alta mortalidad en el neonato, sobre todo en los casos con ventrículo derecho muy pequeño, debido a que muchos de estos niños tienen anomalías en el propio músculo cardiaco y la insuficiencia de la válvula tricúspide puede ser grave hemodinámicamente.
Pasado el periodo neonatal, si el ventrículo derecho crece, el pronóstico futuro es esperanzador y puede ser prácticamente normal. Si el ventrículo derecho no crece, la evolución es similar a la de los ventrículos únicos y la atresia tricuspídea.
DOBLE SALIDA DE VENTRÍCULO DERECHO:
En contraste con el corazón normal, en el que la aorta sale del ventrículo izquierdo, en la doble salida de ventrículo derecho (DSVD) la aorta sale del ventrículo derecho, de forma que ambos vasos (la arteria pulmonar y la aorta) salen del ventrículo derecho y ninguno sale del ventrículo izquierdo. Además, existe una comunicación interventricular (CIV) asociada.
De esta forma, la doble salida de ventrículo derecho (DSVD) implica dos anomalías asociadas:
- La aorta sale del ventrículo derecho junto con la arteria pulmonar.
- Existe siempre una CIV asociada.
Por otra parte, la DSVD engloba 4 grupos de patologías muy diferentes en cuanto a la fisiopatología, corrección quirúrgica y pronóstico, equiparando cada uno de estos grupos a otras patologías conocidas, respecto a las que siempre constituyen formas complejas o más graves:

DOBLE SALIDA DE VENTRÍCULO IZQUIERDO:
El ventrículo izquierdo de doble salida es una malformación cardíaca infrecuente que consiste en la conexión de la aorta y del tronco de la arteria pulmonar con el ventrículo morfológicamente izquierdo.
Existen diferentes variedades según la disposición de las arterias, su relación con la comunicación interventricular (CIV) y la existencia de estenosis pulmonar, siendo el tratamiento quirúrgico diferente en cada caso. La ausencia de CIV con hipoplasia severa del ventrículo es excepcional, mientras que la presencia de una CIV subaórtica y de un grado variable de estenosis pulmonar es la forma más frecuente.
TRONCO ARTERIOSO COMÚN:
Es la salida de una sola arteria desde ambos ventrículos. Suele asociar un defecto septal ventricular y diversos grados de malformación de las arterias pulmonares. La corrección quirúrgica se realizará en época neonatal precoz, y por lo general conlleva el cierre de la comunicación interventricular dejando el vaso truncal como neoaorta y desconectando las arterias pulmonares del vaso truncal y conectándose al ventrículo derecho mediante un conducto valvulado para tratar de “normalizar” la circulación.
Arterias pulmonares y subpulmonares:
ESTENOSIS PULMONAR:
La estenosis pulmonar es una estrechez en el tracto de salida del ventrículo derecho hacia los pulmones. Se localiza en el infundíbulo del ventrículo derecho (zona del ventrículo cercana a la arteria pulmonar), anillo pulmonar, válvula pulmonar o arteria pulmonar. El ventrículo derecho tiene que impulsar la sangre hacia el pulmón con mayor fuerza y a más presión para salvar el obstáculo de la estenosis pulmonar, generando con el tiempo hipertrofia del ventrículo derecho.
Dependiendo del grado de estenosis, los pacientes están asintomáticos si la estenosis pulmonar es leve o moderada, mientras que aquellos con estenosis severa pueden presentar disnea, fatiga, cianosis y clínica de insuficiencia cardíaca.
Algunos de estos recién nacidos necesitan que mantengamos el ductus abierto, mediante la administración de prostaglandinas, para asegurar flujo de sangre suficiente al pulmón.
Algunos síndromes asocian con frecuencia estenosis pulmonar: Síndrome de Noonan (aproximadamente en el 50% de estos pacientes), Síndrome de Leopard, Neurofibromatosis o Enfermedad Carcinoide del intestino.
Tipos de estenosis pulmonar:
- Valvular:
- Valvas elásticas.
- Valvas gruesas.
- Anillo pequeño/hipoplásico.
- Infundibular.
- Supravalvular.
Actualmente el tratamiento habitual o de elección sólo en la estenosis pulmonar de tipo valvular con valvas elásticas y estenóticas consiste en la apertura percutánea de la válvula pulmonar (valvuloplastia pulmonar) mediante cateterismo terapéutico. Se realiza con un catéter balón que se introduce por los vasos femorales hasta el corazón y dilata la válvula pulmonar. En las estenosis pulmonares supravalvulares, anulares o infundibulares el único tratamiento es el quirúrgico.
Arteria aorta y subaórticas:
ESTENOSIS AÓRTICA:
Se trata de la obstrucción a la salida de la sangre del ventrículo izquierdo que puede ser a 3 niveles:
- Subvalvular: por “debajo” de la válvula aórtica, pudiendo deberse a una membrana o a un rodete fibro-muscular
- Valvular: a nivel de la válvula aórtica, que suele ser displásica (mal desarrollada) y engrosada, pudiendo tener los 3 velos (la válvula aórtica es trivalva/tricúspide de forma normal) pero anormalmente desarrollados, sólo 2 velos (bicúspide) o incluso 1 velo (monocúspide).
- Supravalvular: por “encima” de la válvula aórtica, puede ser una obstrucción localizada o un hipodesarrollo de la aorta ascendente.
Se asocia muy comúnmente a anomalías genéticas como el Síndrome de Beuren-Williams. A su vez existen 2 formas clínicas de debut:
- Formas críticas neonatales: Debut con síntomas de insuficiencia cardiaca. Pulsos débiles en 4 miembros. Cardiomegalia y congestión pulmonar en la radiografía de tórax.
- Formas no neonatales: Asintomáticos. La radiografía de tórax suele ser normal, pudiendo encontrarse ligera dilatación de la aorta ascendente.
El tratamiento depende del nivel de la obstrucción, en los casos en los que la válvula sea la única afectada, se realiza cateterismo intervencionista mediante dilatación con balón (valvuloplastia), mientras que los otros casos requerirán reparación quirúrgica mediante circulación extracorpórea (CEC).
INTERRUPCIÓN DEL ARCO AÓRTICO:
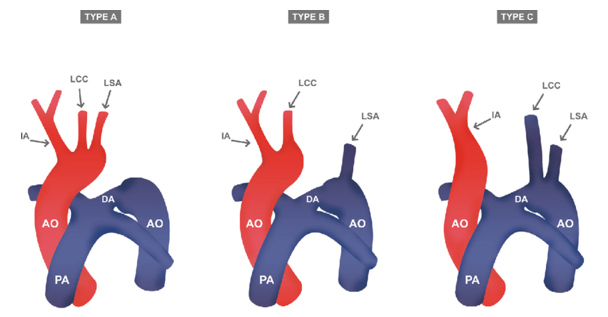
Ilustración 14. Fuente: Mavink. Tipos de arco aórtico. 2023.
Es una falta de continuidad entre la aorta ascendente y la descendente por lo que la sangre arterial sólo va a irrigar la aorta ascendente, es decir, la cabeza, cuello y extremidades superiores. La aorta descendente y con ella la circulación sistémica de la mitad inferior del cuerpo se va a rellenar con sangre venosa procedente de la arteria pulmonar a través del ductus arterioso, que será el encargado de mantener la circulación sistémica. Existen 3 tipos dependiendo del nivel al que se produzca la interrupción:
- Tipo A: la interrupción se produce tras el último tronco supraórtico.
- Tipo B: la interrupción se produce entre el segundo y tercer supraórticos.
- Tipo C: entre el primero y el segundo supraórticos.
Además, se asocian en un alto porcentaje a defectos septales interventriculares (CIV) y a otras cardiopatías como el truncus arterioso. También es frecuente la asociación con síndromes genéticos como el síndrome de Di George o Síndrome Velo-Cardio-Facial (CATCH 22), que asocian anomalías a otros niveles.
El cuadro clínico es el de shock cardiogénico brusco coincidiendo con la constricción del ductus arterioso. Los pulsos superiores serán débiles en las áreas que estén afectadas (siempre estarán disminuidos en miembros inferiores), es decir en una interrupción tipo B, por ejemplo, el pulso del brazo izquierdo estará disminuido/ausente y el del derecho estará conservado.
El tratamiento consiste inicialmente en la infusión de prostaglandinas para mantener abierto el ductus arterioso, para posteriormente realizar una corrección quirúrgica bajo CEC, reparando el arco aórtico mediante anastomosis directa o usando distintos materiales, además deberán repararse los defectos asociados que presente el paciente.
ANOMALÍAS CONGÉNITAS DE LA CIRCULACIÓN CORONARIA. SÍNDROME ALCAPA.
Las enfermedades de las arterias coronarias son muy raras en los niños, pero hay múltiples anomalías congénitas y adquiridas de las arterias coronarias que se pueden presentar en la edad pediátrica. Una de ellas es si la arteria coronaria que nace de la arteria pulmonar comúnmente se llama ALCAPA (por sus siglas en inglés).
La arteria coronaria izquierda nace erróneamente de la arteria pulmonar, y por ello lleva sangre desoxigenada a la pared muscular del ventrículo izquierdo y aurícula izquierda.
Al recibir sangre insuficientemente oxigenada, el corazón izquierdo no funciona con normalidad. Esta patología suele debutar hacia los 2 meses de vida, momento en el que ya han bajado las presiones pulmonares. Al disminuir la presión en la arteria pulmonar, la coronaria izquierda recibe sangre desoxigenada a baja presión, por lo que se ve comprometida la perfusión del miocardio y pueden aparecer signos graves de isquemia miocárdica.
En los casos graves, el paciente debe ser intervenido quirúrgicamente sin demora. La operación consiste en separar la arteria coronaria izquierda de la arteria pulmonar y hacer una anastomosis a la aorta, con lo que se restablece el flujo coronario normal de sangre oxigenada.
Hay algunos niños que espontáneamente, sin operación, superan la lactancia y son diagnosticados de esta lesión cuando tienen más de 6 meses – 1 año. En estos niños se han desarrollado colaterales que distalmente unen ambas coronarias, derecha e izquierda. Cuando esto ocurre, ambas arterias coronarias se constituyen en una gran fístula que une la aorta con la arteria pulmonar; el flujo coronario en esta situación va siempre de aorta (vaso con más presión) a la arteria pulmonar (vaso con menos presión).
En esta situación hay que operar a estos niños, conectando la arteria coronaria izquierda a la aorta, porque así se evita:
- Una pobre irrigación del corazón izquierdo, pues la sangre coronaria, aunque oxigenada, llega con escasez y con menor presión, al ser largo el recorrido desde la aorta hasta el corazón izquierdo.
- El paso inútil de sangre oxigenada a la arteria pulmonar y pulmones.
Enfermedades inflamatorias o infecciosas:
Enfermedad de Kawasaki:
La enfermedad de Kawasaki es una vasculitis de arterias de mediano calibre de etiología desconocida, que afecta principalmente a lactantes y preescolares con lesiones relevantes en piel, mucosas, ganglios linfáticos, articulaciones y corazón. La primera descripción fue realizada por Tomisaku Kawasaki en 1967, época en la cual se establecieron las bases para el diagnóstico que aún son vigentes.
A partir de su descubrimiento, la entidad ha sido reconocida en todo el mundo y en niños de todos los grupos raciales. Aunque es más prevalente en países asiáticos, especialmente en Japón, donde la incidencia ha ido en aumento hasta situarse en 330/100.000 niños menores de 5 años; En España se desconoce la incidencia general pero en 2017 se ha descrito una incidencia en Cataluña de 8/100.000 niños menores de 5 años.
La enfermedad se presenta, en la mitad de los casos, antes de los 2 años de vida, su pico de incidencia es entre los 13 y 24 meses de edad y, en un 80% aproximadamente, en menores de 4 años. Su frecuencia es mayor en el sexo masculino en una proporción de 1.5:1 a 1.7:1. Ha sido descrita una mayor incidencia, cerca de diez veces más grande, en hermanos de los niños que han padecido enfermedad de Kawasaki. En algunos países, esta patología ha rebasado a la fiebre reumática como primera causa de cardiopatía adquirida en la edad pediátrica.
FISIOPATOLOGÍA:
Se han propuesto algunos factores que pueden predisponer la aparición de la enfermedad, como enfermedades de vías respiratorias superiores o cuadros gastrointestinales, que habitualmente lo anteceden en 1 a 3 días. Diversos estudios han tratado de asociar la entidad con exposición a medicamentos, factores de polución ambiental o diversos tóxicos, entre ellos el mercurio, sin haberse demostrado una asociación.
Aunque se ha demostrado la elevación de todos los tipos de inmunoglobulinas, así como la presencia de complejos inmunitarios, la ausencia de consumo de complemento indica que la enfermedad de Kawasaki no es una enfermedad autoinmunitaria. Diversas citocinas proinflamatorias, como el factor de crecimiento endotelial vascular, el factor de necrosis tumoral y varias interleucinas, parecen desempeñar un importante rol en el proceso de la vasculitis.
Uno de los hallazgos más constantes en pacientes afectados por la enfermedad de Kawasaki es la hiperplaquetosis, que se piensa puede ser secundaria a una alteración del sistema reticuloendotelial por complejos inmunitarios. La presencia de otras alteraciones de la coagulación, como elevación del factor VIII y del fibrinógeno, aunada a la presencia de plaquetas hiperagregables, condiciona un estado de hipercoagulabilidad que pudiera ser condición determinante en la génesis de los problemas cardíacos que se observan en esta enfermedad.
MANIFESTACIONES CLÍNICAS:
El diagnóstico continúa siendo clínico, y los criterios propuestos por el Dr. Kawasaki fueron confirmados por diversas asociaciones médicas y son aceptados de forma mundial. La enfermedad de Kawasaki presenta tres fases clínicas: aguda, subaguda y período de convalecencia.
En la primera fase, con una duración promedio de entre 7 y 11 días, resaltan los siguientes síntomas y signos clínicos:
- Hiperemia conjuntival, que afecta primordialmente la conjuntiva bulbar, sin exudado o presencia de ulceraciones.
- Papilas linguales prominentes o "lengua en fresa" eritema labial, que progresa a inflamación, desarrollo de fisuras y sangrado.
- Exantema maculopapular de inicio en tronco y extremidades o de tipo escarlatiniforme.
- Fiebre elevada de hasta 40 °C, remitente con 2 a 4 picos por día (en niños no tratados la fiebre puede persistir más de 10 días, pero en pacientes tratados con ácido acetilsalicílico cede en 5 días aproximadamente y con gammaglobulina entre 24 y 48 h).
- Linfadenopatía cervical unilateral, que ocurre en el 50 a 70% de los casos (Para considerarse como criterio diagnóstico debe medir más de 1.5 cm).
- Las manos y los pies están edematosos, indurados, lo cual impide a los pacientes caminar o sostener objetos.
La fase subaguda se inicia con la desaparición de la fiebre, pero persisten:
- La irritabilidad.
- La anorexia.
- Hay descamación perianal, en manos y pies.
En un tiempo variable de 2 a 3 semanas, desaparece la gran mayoría de los signos de la enfermedad y da inicio la fase de convalecencia, que finaliza cuando se disipan todas las manifestaciones inflamatorias, lo que ocurre en buena parte de los casos a los 2 meses de iniciado el proceso.
Tanto en la fase aguda como en la subaguda, se pueden desarrollar lesiones a nivel cardíaco. Las lesiones cardíacas pueden ser:
- Miocarditis.
- Pericarditis.
- Alteraciones valvulares.
- Infarto de miocardio
Toda esta serie de alteraciones se presentan hasta en un tercio de los pacientes. Además, para profundizar:
- La miocarditis puede presentarse en un 20% de los pacientes en la fase aguda, manifestándose con taquicardia, signos de insuficiencia cardíaca, cardiomegalia y trastornos de la conducción.
- La alteración valvular más común afecta la válvula mitral, se observa en el 10% y se diagnostica mediante auscultación de un soplo sistólico regurgitante en el foco mitral.
- Las lesiones coronarias incluyen estenosis y dilataciones aneurismáticas, especialmente en niños menores de un año y en aquellos tratados con esteroides, siendo factores de alarma la fiebre prolongada, leucocitosis, velocidad de sedimentación globular elevada y títulos altos de tromboglobulina sérica.
- El infarto del miocardio, una complicación grave, ocurre principalmente en la fase subaguda debido a la trombosis en la luz del aneurisma coronario. Se manifiesta con síntomas como vómitos, palidez y dolor retroesternal, con cambios electrocardiográficos característicos y elevación de enzimas cardíacas.
- La artritis, dolor abdominal, hidrocolecisto, uretritis y meningitis aséptica son otras complicaciones asociadas.
DIAGNÓSTICO:
Enfermedad de Kawasaki completa:
Son necesarios la presencia de fiebre durante más de 5 días junto con 4 criterios clínicos o bien la fiebre junto con 3 criterios si el paciente presenta afectación cardiaca compatible.

Enfermedad de Kawasaki incompleta:
Se denomina enfermedad de Kawasaki incompleta cuando se cumple el criterio principal de fiebre persistente, junto con otros criterios clínicos que apoyan el diagnóstico, habiendo excluido otras enfermedades que pueden simular dicho proceso, pero sin cumplir los criterios necesarios para la enfermedad de Kawasaki completa. También será incompleta cuando se cumplen los criterios salvo la duración de la fiebre.
Los criterios diagnósticos convencionales deben ser empleados como una guía general, particularmente importante en la prevención de un sobrediagnóstico, si bien podrían fallar en el reconocimiento de aquellas formas incompletas de la enfermedad. Las formas incompletas son más frecuentes en pacientes más jóvenes, siendo vital una precoz identificación y tratamiento del proceso, pues presentan un mayor riesgo de desarrollo de anomalías coronarias.
El diagnóstico diferencial de la enfermedad de Kawasaki se debe realizar con otras enfermedades exantemáticas de la infancia (virosis o enfermedades mediadas por toxinas), reacciones inmunitarias u otras enfermedades reumatológicas menos frecuentes.
TRATAMIENTO:
- Inmunoglobulina intravenosa: el empleo está avalado por numerosos estudios que demuestran una disminución de los días de fiebre y mejoría del estado general del paciente. Asimismo, se ha comprobado que reducen la severidad y frecuencia de los aneurismas coronarios. La dosis a administrar es de 2 g/kg a pasar en 12 horas. Al inicio la infusión debe ser muy lenta y con vigilancia especial del enfermo. Velocidades de administración más elevadas favorecen la aparición de reacciones adversas (fiebre, escalofríos, náuseas, vómitos y raramente shock). Si el paciente presenta fallo cardiaco puede considerarse la infusión de 400 mg/kg/día durante 4 días consecutivos.
- Antiinflamatorios no esteroideos: ibuprofeno a dosis de 30-40 mg/kg/día o ácido acetilsalicílico (AAS) 30-50 mg/kg/día cada 6 horas, mientras dure la fiebre.
- AAS: 3-5 mg/kg/día en una sola dosis, una vez ceda la fiebre, por su efecto antiagregante plaquetario. Se debe tener en cuenta que el ibuprofeno antagoniza el efecto antiagregante del AAS.
- Omeprazol: 20 mg/día por vía intravenosa u oral.
- Además, en pacientes de alto riesgo se añadirán corticoides, generalmente: Metilprednisolona a 30/mg/kg/día (máximo 1 g) por vía intravenosa durante 3 días, posteriormente metilprednisolona, prednisolona o prednisona a 2 mg/kg/día por vía oral o intravenosa, con retirada progresiva según la evolución (Aunque existen distintas pautas).
- Vacunación: deben adaptar su calendario de vacunación y retrasar la administración de vacunas de virus vivos hasta 11 meses después de haber recibido la última dosis de inmunoglobulina intravenosa. También se recomienda la vacunación antigripal si está en tratamiento o se prevé que esté en tratamiento con AAS durante la época de la gripe.
Fiebre reumática y cardiopatía reumática:
La fiebre reumática es una enfermedad aguda de etiología autoinmune postinfecciosa en la que se presenta una respuesta sistémica inflamatoria generalizada que puede afectar articulaciones, sistema nervioso, corazón y piel. Ocurre en personas susceptibles que se exponen a algunas cepas reumatogénicas del estreptococo ß-hemolítico del grupo A. Para que aparezca la enfermedad es necesario que se combinen factores relacionados tanto al huésped y al agente causal como al medio ambiente. Su mayor importancia radica en que puede provocar lesiones valvulares residuales con alta morbimortalidad, especialmente en sujetos con carditis grave en el ataque inicial de fiebre reumática, o con recurrencias frecuentes. Se han descrito como agentes causales las cepas reumatogénicas del estreptococo ß-hemolítico del grupo A de Lancefield. Sin embargo, aunque las infecciones estreptocócicas son muy frecuentes en la población infantil, sólo un grupo pequeño de individuos desarrolla fiebre reumática (≤ 1%).
La incidencia mayor se encuentra entre los 5 y los 15 años, con pico máximo a los 8 a 9 años y descenso posterior. Este espectro de edad coincide con la de la faringoamigdalitis estreptocócica, la cual es más frecuente en edad escolar y disminuye en la adolescencia y la edad adulta. Se ha sugerido que las presentaciones más precoces están facilitadas por el ingreso temprano de los niños a la escuela. En cuanto al género, no hay diferencias con excepción de la corea de Sydenham, que se presenta más en la población femenina.
La secuela más significativa es la cardiopatía reumática, que es la cardiopatía adquirida más común en la infancia. Según la Organización Mundial de la Salud, aproximadamente 471.000 pacientes presentan un ataque de fiebre reumática aguda al año. De ellos, 336.000 son niños de 5 a 14 años y 95% provienen de países subdesarrollados.
De todos los casos de fiebre reumática aguda, entre el 55 y 60% desarrollarán cardiopatía reumática cada año si se trata de un solo ataque, y hasta el 80% de los pacientes padecerán más de una recurrencia o con carditis grave. Se reporta que 2.4 millones de niños de 5-14 años están afectados con cardiopatía reumática, 79% de los cuales viven en países en vías de desarrollo. Se reportan 492.000 muertes al año por cardiopatía reumática, de las cuales 468.000 ocurren en países subdesarrollados.
FISIOPATOLOGÍA:
Aún no se encuentran completamente aclarados todos los mecanismos inmunológicos involucrados en la presentación de los episodios de fiebre reumática. La historia natural inicia con la infección faríngea con estreptococo ß-hemolítico del grupo A, en la que se absorben productos de degradación que actúan como antígeno.
Diversos serotipos del estreptococo ß-hemolítico han sido asociados al desarrollo de fiebre reumática, aunque destacan el 1, 3, 5, 6, 14, 18 y 24. Dependiendo de la susceptibilidad del huésped y de la reumatogenicidad del agente causal, algunos pacientes desarrollan carditis grave o recurrencia del ataque agudo, lo cual se correlaciona estrechamente con las secuelas valvulares y el número de válvulas afectadas.
MANIFESTACIONES CLINICAS:
La fiebre reumática aguda puede presentarse con varios hallazgos clínicos diferentes dentro de una a cinco semanas (generalmente de dos a tres semanas) de una faringoamigdalitis por estreptococos del grupo A (GAS) (o pioderma estreptocócica en pacientes de regiones tropicales). Aquí se revisan las posibles manifestaciones mayores y menores. Estas manifestaciones se utilizan para el diagnóstico (Criterios de Jones revisados).
Las cinco manifestaciones principales (y el porcentaje de pacientes con cada una) son:
- Artritis (generalmente poliartritis migratoria que afecta predominantemente a las articulaciones grandes): 60 a 80 por ciento
- Carditis y valvulitis (p. ej., pancarditis) clínica o subclínica: 50 a 80 por ciento
- Afectación del sistema nervioso central (p. ej., corea de Sydenham): del 10 al 30 por ciento
- Nódulos subcutáneos: 0 a 10 por ciento
- Eritema marginado:
Las cuatro manifestaciones menores son:
- Artralgia
- Fiebre
- Reactantes de fase aguda elevados
- Intervalo PR prolongado en el electrocardiograma
Hay dos formas principales de presentación de la fiebre reumática aguda. La forma más común (aproximadamente entre el 70 y el 75 por ciento de los pacientes) es una enfermedad febril aguda con manifestaciones articulares y, a menudo, carditis. La forma menos común es un trastorno neurológico/conductual con corea de Sydenham. Las manifestaciones articulares suelen estar ausentes y la carditis, cuando está presente, suele ser subclínica.
DIAGNÓSTICO:
La reacción inflamatoria exudativa y proliferativa del tejido mesenquimatoso es más intensa en el miocardio, en el endocardio y en el pericardio. En el miocardio, produce un tipo de lesión muy característica que se considera patognomónica de fiebre reumática, que es el granuloma de Aschoff; éste es el resultado de la lesión a las fibras miocárdicas y el tejido conectivo circundante. Mide de 1 hasta 10 mm de largo y se ubica principalmente en el endocardio mural o en el intersticio miocárdico. Los componentes del granuloma, también conocidos como cuerpos de Aschoff, están formados por células de Aschoff, células de Anitschkow, células plasmáticas, linfocitos, material fibrinoide, edema, bandas colágenas fragmentadas y polimorfonucleares.
Los cuerpos de Aschoff tienen valor diagnóstico tanto de ataque agudo como de actividad reumática subclínica o como una lesión residual a un ataque previo. En la fase cicatrizal de los granulomas, sólo se encuentra tejido fibroso, en el que no es posible reconocer el carácter granulomatoso de la lesión. Estas áreas de fibrosis son de extensión variable, sobre todo en el miocardio del ventrículo izquierdo, y pueden contribuir a una disminución en la capacidad contráctil, hecho que puede ser muy significativo en algunos sujetos que, a pesar de someterse a cirugía valvular, evolucionan con falla ventricular.
En la miocarditis reumática, no sólo se encuentran las lesiones específicas señaladas previamente, sino que también existe un infiltrado inflamatorio difuso inespecífico con histiocitos, linfocitos y polimorfonucleares acompañados de edema intersticial y daño en las células miocárdicas; este proceso inflamatorio inespecífico es más importante que los cuerpos de Aschoff, y puede ser tan difuso en el intersticio que es el causante de diversos grados de insuficiencia cardíaca que podría conducir a la muerte. También se ve afectado el endocardio tanto mural como valvular. En el endocardio mural, el más alterado es el atrio izquierdo, el cual se toma áspero y grueso en algunas áreas que se conocen como placas de McCallum; pero fundamentalmente resulta afectado el endocardio valvular sobre los bordes de las valvas y sus cuerdas tendinosas, lo que constituye la valvulitis que puede producir grados variables de regurgitación, situación que contribuye a la dilatación cardíaca. Estas alteraciones pueden ser reversibles a un grado que, aunque estén presentes, no provoquen irregularidades hemodinámicas reconocibles por la clínica. No obstante, en la mitad de los casos, al cicatrizar o "curar" el proceso inflamatorio agudo, las valvas se engrosan, se retraen y se deforman, y las cuerdas tendinosas se acortan o las comisuras se fusionan, lo que da como resultado una lesión permanente, y se constituye así la cardiopatía reumática residual al ataque agudo de fiebre reumática. Después de algunos años, las valvas así alteradas pueden calcificarse.
Desde el punto de vista clínico, las válvulas del lado izquierdo del corazón son las más afectadas, y de ellas, la mitral más que la aórtica; la lesión mitral aislada, en nuestro medio, constituye entre el 60 y 75% de los casos, y la aórtica aislada, como lesión única, entre el 3 y 5%; las combinadas (mitroaórticas) representan entre el 20 y 30%.
En la edad pediátrica, la alteración valvular mitral residual al ataque reumático produce fundamentalmente regurgitación en un alto porcentaje de casos, y sólo alrededor de un 5% cursa desde un principio con estenosis, y un 30%, con doble lesión. Sin embargo, en el adulto este espectro cambia dramáticamente, pues los casos de insuficiencia mitral pasan a ser menos frecuentes y en cambio las estenosis conforman el grupo mayor junto con las dobles lesiones; esto probablemente se debe a nuevos ataques de actividad reumática y a una progresión en el grado de fibrosis o calcificación de la válvula y del aparato subvalvular. La lesión valvular tricuspídea sólo en el 10% de los casos es anatómica (90% son funcionales), y es muy rara la lesión de la válvula pulmonar.
La pericarditis reumática es muy común. Ambas hojas del pericardio se ven afectadas por la reacción inflamatoria. Su superficie serosa se torna roja, rugosa y cubierta por exudado fibrinoso, y pueden acumularse grados variables de líquido serosanguinolento, pero muy rara vez es abundante. Al cicatrizar, puede desarrollar fibrosis y adhesión de ambas hojas con obliteración parcial o total del saco pericárdico, pero sin la ocurrencia de pericarditis constrictiva. Las lesiones extracardíacas incluyen las articulaciones, los nódulos subcutáneos, el sistema nervioso central y el pulmón.
TRATAMIENTO:
Consiste en terapia con antibióticos, terapia antiinflamatoria, tratamiento de la insuficiencia cardíaca y comienzo de la atención continua (prevención secundaria y educación). Se recomienda la hospitalización para el manejo óptimo de la fiebre reumática aguda, especialmente para un episodio inicial, de modo que se puedan completar todas las pruebas, se pueda observar la respuesta al tratamiento y se puedan iniciar medidas preventivas a largo plazo con la educación adecuada para el paciente y sus cuidadores.
Los seis objetivos principales del tratamiento son:
- Erradicación del estreptococo betahemolítico del grupo A (GAS)
- Alivio sintomático de las manifestaciones agudas de la enfermedad (p. ej., artritis, fiebre)
- Manejar la enfermedad cardíaca reumática (RHD; por ejemplo, carditis, insuficiencia cardíaca), si está presente
- Manejar la corea, si está presente
- Profilaxis contra futuras infecciones por GAS para prevenir la progresión de la enfermedad cardíaca.
- Provisión de educación para el paciente y sus cuidadores.
- No existe ningún tratamiento que ralentice la progresión del daño valvular en el contexto de la fiebre reumática aguda.
Definición y clasificación de las miocardiopatías:
Una definición contemporánea de miocardiopatía es un trastorno del miocardio en el que el músculo cardíaco es estructural y funcionalmente anormal en ausencia de enfermedad de las arterias coronarias, hipertensión, valvulopatía y cardiopatía congénita suficiente para explicar la anomalía miocárdica observada. Las miocardiopatías incluyen una variedad de trastornos del miocardio que se manifiestan con diversos fenotipos estructurales y funcionales y frecuentemente son genéticos. Aunque algunos han definido la miocardiopatía para incluir enfermedades del miocardio causadas por causas cardiovasculares conocidas (como hipertensión, cardiopatía isquémica o valvulopatía), las definiciones actuales de miocardiopatía de las principales sociedades excluyen las enfermedades cardíacas secundarias a dichos trastornos cardiovasculares.
En 1980, la Organización Mundial de la Salud (OMS) definió las miocardiopatías como "enfermedades del músculo cardíaco de causa desconocida" para distinguir la miocardiopatía de la disfunción cardíaca debida a entidades cardiovasculares conocidas como hipertensión, cardiopatía isquémica o valvulopatía.
Como resultado, el grupo de trabajo de 1995 de la OMS/Sociedad Internacional y Federación de Cardiología (ISFC) sobre la definición y clasificación de las miocardiopatías amplió la clasificación para incluir todas las enfermedades que afectan el músculo cardíaco y tomar en consideración la etiología, así como la fisiopatología dominante. En esta clasificación de 1995, las miocardiopatías se definían como "enfermedades del miocardio asociadas con disfunción cardíaca". Se clasificaron según anatomía y fisiología en los siguientes tipos:
- Miocardiopatía dilatada (MCD)
- Miocardiopatía hipertrófica (MCH)
- Miocardiopatía restrictiva (MCR)
- Miocardiopatía arritmogénica (MCA)
- Miocardiopatías no clasificadas
En 2008, el grupo de trabajo de la European Society of Cardiology (ESC) sobre enfermedades del miocardio y del pericardio presentó una actualización de la clasificación de la OMS/ISFC en la que la miocardiopatía se definía como: "Un trastorno del miocardio en el que el músculo cardíaco es estructural y funcionalmente anormal en ausencia de enfermedad de las arterias coronarias, hipertensión, valvulopatía y cardiopatía congénita son suficientes para explicar la anomalía miocárdica observada". La clasificación ESC pretende ser particularmente útil en la práctica clínica diaria.
MIOCARDIOPATÍA DILATADA
La micocardiopatía dilatada (MCD) se caracteriza por dilatación y contracción alterada de uno o ambos ventrículos. La dilatación a menudo se vuelve grave e invariablemente va acompañada de un aumento de la masa cardíaca total (hipertrofia). Los pacientes afectados tienen función sistólica alterada y la presentación clínica suele ser con características de insuficiencia cardíaca.
La incidencia de micocardiopatía dilatada se ha estimado en cinco a ocho casos por 100.000 habitantes, con una prevalencia de 36 por 100.000. Estas cifras pueden subestimar la frecuencia del trastorno porque muchos pacientes con micocardiopatía dilatada tienen una expresión incompleta de la enfermedad, que pasa desapercibida. La evaluación con ECG y ecocardiograma de 767 familiares de 189 con micocardiopatía dilatada reveló enfermedad no reconocida en el 4,6 por ciento de los familiares. Además, la disfunción sistólica del ventrículo izquierdo puede ser más prevalente de lo que se estimaba anteriormente, como lo sugiere un estudio que encontró que el 14 por ciento de la población adulta de mediana edad y mayor tiene disfunción sistólica del ventrículo izquierdo (VI) asintomática.
La lista completa de causas de MCD es extensa. Las causas comunes incluyen virus y mutaciones genéticas, que ahora se reconoce que son relativamente comunes entre los pacientes con MCD idiopática.
Ilustración 15. Fuente: Miocardiopatía dilatada. EcuRed. 2019.
El ecocardiograma en la MCD muestra dilatación de la cavidad del VI (con una tendencia a que la forma de la cavidad se vuelva menos ovoide y más esférica), espesor de la pared normal o disminuido, engrosamiento deficiente de la pared y/o movimiento sistólico endocárdico hacia adentro reducido. Además de estos cambios en el VI, otros hallazgos incluyen agrandamiento de la aurícula izquierda y, con menos frecuencia, agrandamiento y disfunción del ventrículo derecho. En estos pacientes, las cuatro cámaras pueden estar dilatadas.
MIOCARDIOPATÍA HIPERTRÓFICA:
La MCH es un trastorno clínicamente heterogéneo causado por una variedad de mutaciones asociadas con la hipertrofia del VI y, ocasionalmente, del ventrículo derecho. El término "MCH" también se utiliza en un sentido más amplio en el sistema de clasificación de la AHA de 2006 y de la ESC de 2008 para incluir una variedad de afecciones (p. ej., ataxia de Fabry, Noonan, Friedreich) con aumento del grosor o masa de la pared ventricular no causada por condiciones de carga patológicas. (p. ej., hipertensión o valvulopatía).
El volumen del VI es normal o está reducido en la MCH y suele haber disfunción diastólica. En aproximadamente el 60 al 70 por ciento de los pacientes, la MCH es causada por mutaciones en genes de proteínas contráctiles sarcoméricas y se transmite como un rasgo autosómico dominante.
MIOCARDIOPATÍA RESTRICTIVA:
La miocardiopatía restrictiva (MCR) se caracteriza por ventrículos no dilatados con deterioro del llenado ventricular. Por lo general no hay hipertrofia, aunque las enfermedades infiltrativas (como la amiloidosis) y las enfermedades de almacenamiento (como la enfermedad de Fabry) pueden causar un aumento en el espesor de la pared del VI. La función sistólica suele permanecer normal, al menos en las primeras etapas de la enfermedad.
En el ecocardiograma bidimensional, la MCR se caracteriza por ventrículos no dilatados ni hipertrofiados (no engrosados) con agrandamiento biauricular de moderado a marcado, que es secundario a las presiones auriculares elevadas. El ecocardiograma Doppler tisular también es una herramienta de diagnóstico eficaz.
La MCR es mucho menos común que la MCD o la MCH fuera de los trópicos, pero es una causa frecuente de muerte en África, India, América del Sur y Central y Asia, principalmente debido a la alta incidencia de fibrosis endomiocárdica en esas regiones.
MIOCARDIOPATÍA ARRITMOGÉNICA:
La miocardiopatía arritmogénica (MCA) se define como un trastorno arritmogénico del músculo cardíaco con anomalías estructurales del miocardio y presentación clínica con arritmia que no se explica por una enfermedad cardíaca isquémica, hipertensiva o valvular. La presentación clínica puede ser con arritmia documentada (p. ej., fibrilación auricular, enfermedad de la conducción, taquicardia ventricular) o síntomas de arritmia.
La miocardiopatía arritmogénica del ventrículo derecho (ARVC) fue la primera y mejor caracterizada de las miocardiopatías arritmogénicas (MCA). La ARCV es una enfermedad del músculo cardíaco determinada genéticamente y caracterizada por arritmias ventriculares y una patología miocárdica específica. El miocardio de la pared libre del ventrículo derecho (y frecuentemente también del ventrículo izquierdo -VI-) es reemplazado por tejido fibroso y/o fibroadiposo, con células miocárdicas residuales dispersas. La función ventricular derecha es anormal, con acinesia o discinesia regional y, en casos graves, dilatación y disfunción global del ventrículo derecho.
MIOCARDIOPATÍAS NO CLASIFICADAS:
El término "miocardiopatía no clasificada" se incluyó en el sistema de clasificación ESC de 2008 para describir trastornos que no encajan fácilmente en ninguna de las categorías fenotípicas anteriores. Los ejemplos citados incluyen:
- No compactación del ventrículo izquierdo: La no compactación del VI, también llamada no compactación ventricular aislada, es una miocardiopatía poco común no clasificada con una pared miocárdica alterada.
- Miocardiopatía inducida por estrés: La miocardiopatía inducida por estrés, también llamada síndrome de balón apical, síndrome del corazón roto y miocardiopatía de takotsubo, es un síndrome cada vez más reportado, generalmente caracterizado por una disfunción sistólica transitoria de los segmentos apicales y/o medios del VI que a menudo es provocada por estrés.
- Miocardiopatía cirrótica: Si bien la miocardiopatía alcohólica es una causa de enfermedad cardíaca en pacientes con cirrosis, estudios experimentales y observacionales han encontrado que la cirrosis se asocia con disfunción miocárdica independientemente de la exposición al alcohol.
Pericarditis y enfermedades pericárdicas:
La pericarditis aguda se refiere a la inflamación del saco pericárdico.
Faltan en gran medida estudios epidemiológicos y se desconocen la incidencia y prevalencia exactas de la pericarditis aguda. Sin embargo, la pericarditis aguda se registra en aproximadamente entre el 0,1 y el 0,2 por ciento de los pacientes hospitalizados y en el 5 por ciento de los pacientes ingresados en el servicio de urgencias por dolor torácico no isquémico.
En los países desarrollados, a menos que exista una afección médica o quirúrgica aparente que se sepa que está asociada con la pericarditis, la mayoría de los casos de pericarditis aguda en pacientes inmunocompetentes se deben a una infección viral o son idiopáticos.
MANIFESTACIONES CLÍNICAS:
La pericarditis aguda puede presentarse con una variedad de signos y síntomas inespecíficos, según la etiología subyacente, incluyen:
- Dolor en el pecho: Típicamente agudo y pleurítico, mejora al sentarse e inclinarse hacia adelante.
- Roce pericárdico: Un sonido superficial áspero o chirriante que se escucha mejor con el diafragma del estetoscopio sobre el borde esternal izquierdo.
- Cambios en el electrocardiograma (ECG): Nueva elevación generalizada del segmento ST y depresión del PR, aunque no siempre produce los cambios descritos.
- Derrame pericárdico: Un derrame pericárdico es una característica común de la pericarditis, pero no es necesario para el diagnóstico.
Las características de la pericarditis aguda asociadas con un mayor riesgo incluyen:
- Fiebre (>38°C).
- Curso subagudo (sin inicio agudo de dolor torácico).
- Evidencia que sugiere taponamiento cardíaco (p. ej., compromiso hemodinámico).
- Un gran derrame pericárdico.
- Pacientes inmunosuprimidos e inmunodeprimidos.
- Uso de anticoagulantes.
- Trauma agudo.
- No mostrar mejoría clínica después de siete días de tratamiento con AINE y colchicina.
- Troponina cardíaca elevada, que sugiere afectación del miocardio.
Los pacientes que no presentan ninguna de estas características de alto riesgo pueden ser tratados de forma ambulatoria de forma segura.
DIAGNÓSTICO:
La pericarditis aguda se diagnostica por la presencia de al menos dos de los siguientes criterios:
- Dolor torácico típico.
- Roce pericárdico.
- Cambios característicos en el ECG.
- Derrame pericárdico nuevo o que empeora.
Estos criterios de diagnóstico son consistentes con las directrices de la Sociedad Europea de Cardiología de 2015 sobre enfermedades pericárdicas. En presentaciones atípicas, los hallazgos de apoyo adicionales incluyen evidencia de inflamación sistémica (p. ej., elevación de la proteína C reactiva) o inflamación pericárdica en una técnica de imagen como el contraste pericárdico en la tomografía computarizada o el edema pericárdico y el realce tardío con gadolinio en la resonancia magnética cardíaca.
El diagnóstico de pericarditis aguda generalmente se sospecha basándose en antecedentes de dolor torácico pleurítico característico y se confirma si hay un roce pericárdico. También se debe sospechar pericarditis en un paciente con fiebre persistente y derrame pericárdico o nueva cardiomegalia inexplicable.
TRATAMIENTO:
El tratamiento de la pericarditis aguda debe centrarse en la medida de lo posible en la etiología subyacente. En general, se supone que la mayoría de los casos de pericarditis "idiopática" son de etiología viral. Debido al curso relativamente benigno asociado con las causas más comunes de pericarditis (más del 80 por ciento de los casos). Como tal, la mayoría de los pacientes son tratados por una presunta causa viral con medicamentos antiinflamatorios no esteroides (AINE) y colchicina.
En la pericarditis viral o idiopática aguda, no se ha demostrado rigurosamente ningún tratamiento que prevenga secuelas graves, como el taponamiento cardíaco y la pericarditis constrictiva. Afortunadamente, sin embargo, estas complicaciones son raras.
- Tratamiento inicial:
Para casi todos los pacientes con pericarditis idiopática o viral aguda, recomendamos la terapia combinada con colchicina más AINE.
Está indicada una terapia específica apropiada para el trastorno subyacente en pacientes con causa identificada.
Los glucocorticoides deben usarse para el tratamiento inicial de la pericarditis aguda sólo en pacientes con contraindicaciones para los AINE, o para indicaciones específicas, y deben usarse al nivel más bajo de dosis efectiva.
- Tratamiento de reducción gradual:
Tras la resolución de los síntomas, reducimos la dosis del agente antiinflamatorio semanalmente en un intento de reducir la tasa de recurrencia posterior. La colchicina se continúa durante un total de tres meses.
Los pacientes con pericarditis aguda idiopática o viral tienen un buen pronóstico a largo plazo. El taponamiento cardíaco rara vez ocurre en pacientes con pericarditis idiopática aguda y es más común en pacientes con una etiología subyacente específica, como neoplasia maligna, tuberculosis o pericarditis purulenta. La pericarditis constrictiva puede ocurrir en aproximadamente el 1 por ciento de los pacientes con pericarditis idiopática aguda y también es más común en pacientes con una etiología específica.
PERICARDIOCENTESIS:
El drenaje de líquido pericárdico está indicado en los siguientes entornos clínicos:
- Taponamiento cardíaco: los pacientes con un derrame pericárdico que causa compromiso hemodinámico deben someterse a un drenaje urgente del derrame pericárdico con fines terapéuticos y, en algunos casos, diagnósticos.
- Pericarditis purulenta: esta afección suele presentarse con fiebre alta y taquicardia, con o sin dolor en el pecho. Se requiere un alto índice de sospecha, particularmente en pacientes con una infección conocida que puede extenderse al pericardio o con lesión previa del pericardio. Se requiere un tratamiento y diagnóstico urgentes.
La eliminación del líquido pericárdico se puede lograr mediante pericardiocentesis percutánea o mediante un procedimiento quirúrgico (drenaje quirúrgico abierto con o sin ventana pericárdica o ventana pericárdica toracoscópica asistida por video), que generalmente son muy eficaces para eliminar el líquido y aliviar los síntomas asociados con el compromiso hemodinámico. La elección del procedimiento para el drenaje del líquido pericárdico se basa en gran medida en si el derrame pericárdico es accesible para el drenaje percutáneo y si existe un sitio de sangrado cardíaco o aórtico crítico que requiera tratamiento quirúrgico.
La extracción de líquido pericárdico mediante pericardiocentesis o drenaje quirúrgico de un derrame pericárdico grande (generalmente con taponamiento cardíaco) rara vez se complica con inestabilidad hemodinámica aguda, shock cardiogénico y edema pulmonar, que se ha denominado síndrome de descompresión pericárdica. El tiempo de aparición varía desde inmediatamente después del procedimiento hasta 48 horas después.
Endocarditis infecciosa:
La endocarditis infecciosa es una infección del endocardio y/o de las válvulas cardíacas que implica la formación de trombos, que pueden dañar el tejido endocárdico y/o las válvulas. El proceso puede involucrar endocardio/endotelio nativo o material protésico. Aunque es poco común en niños, es importante identificar y tratar la endocarditis infecciosa debido a su importante morbilidad y mortalidad.
Las tasas de incidencia informadas de endocarditis infecciosa pediátrica en los Estados Unidos oscilan entre 0,3 y 3,3 por 100.000 personas por año. Las tasas son más altas entre los bebés menores de 1 año de edad en comparación con los niños mayores y los adolescentes. Las tasas más altas se observan en niños con cardiopatía congénita. Las tasas de EI pediátrica aumentaron durante la segunda mitad del siglo XX, probablemente debido a mejoras en la supervivencia de los niños con enfermedad coronaria y al mayor uso de catéteres venosos centrales (CVC).
MANIFESTACIONES CLÍNICAS:
La presentación clínica es variable y depende de la extensión de la enfermedad cardíaca local, el grado de afectación de otros órganos y el agente causal. Generalmente se clasifica como un proceso subagudo o agudo.
- Subaguda: la presentación subaguda se caracteriza por un curso prolongado de febrícula y síntomas inespecíficos que incluyen fatiga, artralgias, mialgias, escalofríos, pérdida de peso, intolerancia al ejercicio y diaforesis. La presencia de un conjunto de estos síntomas en un paciente con riesgo de endocarditis infecciosa (es decir, aquellos con enfermedad cardíaca preexistente o catéter venoso central permanente).
- Aguda: es una enfermedad fulminante y rápidamente progresiva. Estos pacientes suelen tener fiebre alta y gravemente enfermos. Se observa comúnmente una presentación aguda en pacientes con EI debida a S. aureus, que puede causar una rápida destrucción del tejido de la válvula cardíaca, formación de abscesos, fenómenos embólicos y un deterioro rápidamente progresivo del estado hemodinámico.
Los hallazgos clínicos de la endocarditis infecciosa corresponden a los fenómenos patológicos subyacentes de bacteriemia/fungemia, valvulitis, respuesta inmunológica y embolización.
Los factores de riesgo de endocarditis infecciosa, como enfermedad cardíaca preexistente, vías centrales permanentes, presencia de material protésico, bacteriemia persistente o infección con los organismos más asociados con endocarditis infecciosa, deben impulsar una evaluación temprana.
TRATAMIENTO:
En general, los principios de tratamiento de la endocarditis infecciosa en niños son los mismos que en los adultos. En pacientes con endocarditis infecciosa aguda, se deben obtener hemocultivos lo más rápido posible para poder iniciar la terapia antibiótica adecuada. Los pacientes con disfunción valvular asociada a endocarditis infecciosa que causa insuficiencia cardíaca sintomática y los pacientes con fiebre persistente y bacteriemia a pesar de la terapia antibiótica adecuada pueden ser candidatos para una intervención quirúrgica. Las razones más comunes para la intervención quirúrgica incluyen insuficiencia cardíaca congestiva, disfunción valvular progresiva y fenómenos embólicos.
Las estrategias para prevenir la endocarditis infecciosa en niños incluyen la higiene bucal para la prevención de enfermedades bucales y la profilaxis antimicrobiana para pacientes de alto riesgo cuando se someten a procedimientos invasivos.
Otras enfermedades cardiovasculares:
Arritmias en cardiología pediátrica:
En el pasado, el diagnóstico y tratamiento de las arritmias en edad pediátrica eran inferidos sólo a partir de la información obtenida de la experiencia con pacientes adultos.
Aunque las arritmias son más frecuentes en el paciente con corazón estructuralmente normal, la asociación con cardiopatía congénita es común y varía dependiendo del tipo de cardiopatía. La asociación más frecuente es el síndrome de Wolff-Parkinson-White (WPW) con la anomalía de Ebstein, encontrándose hasta en el 30% de los casos; en la transposición corregida de grandes arterias, es el bloqueo AV de diversos grados, con una frecuencia de hasta el 50%, siendo el más habitual el bloqueo de primer grado.
Se han descrito 3 tipos básicos de mecanismos electrofisiológicos: reentrada (el más frecuente), seguido por el de automatismo anormal y finalmente el de actividad desencadenada.
El mecanismo de reentrada consiste en la propagación del impulso eléctrico alrededor de un obstáculo de tipo anatómico o funcional, lo cual origina una recitación del miocardio con movimiento circular. Para que esto ocurra es necesario reunir tres condiciones:
a) dos vías de conducción
b) bloqueo unidireccional en una de las vías
c) una conducción lo suficientemente lenta en el circuito para posibilitar la recuperación del tejido y encontrar nuevamente al tejido excitable permitiendo el movimiento circular.
El ejemplo clásico de este mecanismo lo representa el síndrome de WPW, donde el mecanismo de reentrada ocurre en la unión AV; una de las vías es accesoria y la otra nodal. Este mecanismo también es el responsable del flutter auricular, la reentrada intranodal y algunas taquicardias ventriculares.
El automatismo anormal se basa en la despolarización diastólica espontánea, anormalmente inducida por una alteración patológica del tejido miocárdico. El potencial de membrana en reposo es menor al habitual, ocasionando mayor grado de despolarización de la membrana en reposo y por lo tanto un incremento en la frecuencia de descarga. Cualquier célula miocárdica es susceptible de poseer despolarización diastólica espontánea, tanto en ventrículos como en aurículas. Este mecanismo es el responsable de las taquicardias auriculares por foco ectópico y algunas taquicardias ventriculares en pacientes con daño miocárdico agudo (infarto, miocarditis).
La actividad desencadenada consiste en la generación de impulsos eléctricos repetidos originados por pospotenciales. Los pospotenciales son oscilaciones anormales del potencial de acción que, al alcanzar el umbral suficiente, dan lugar a la generación de un potencial de acción nuevo, el cual a su vez desencadena nuevos pospotenciales induciendo actividad eléctrica propagada. Existen dos tipos de pospotenciales, los tardíos y los precoces.
Los pospotenciales precoces tienen lugar durante las fases 2 ó 3 del potencial de acción. Existe relación directa de los pospotenciales con incremento en las corrientes de entrada de sodio o calcio, o disminución de las corrientes de salida de potasio, produciendo una prolongación del potencial de acción. Esta alteración del tejido miocárdico puede presentarse por alteraciones hidroelectrolíticas (hipokalemia), acidosis y fármacos, en respuesta a niveles altos de catecolaminas o en el tejido cardíaco lesionado, como en la hipertrofia y dilatación de cavidades cardíacas. La presencia de bradicardia o pausas puede favorecer la generación de pospotenciales precoces y por el contrario las frecuencias altas los inhiben. La torsades de pointes (TP) observada en los pacientes con QT largo congénito y adquirido se explica por este mecanismo.
Los pospotenciales tardíos aparecen al final de la repolarización y su origen está en un incremento anormal del calcio intracelular. Esta condición ocurre en la intoxicación por digitálicos, en respuesta a niveles elevados de catecolaminas y en corazones con hipertrofia o dilatación. En presencia de catecolaminas elevadas, existe una activación elevada de la adenilciclasa y por lo tanto un incremento en la entrada de calcio por los canales lentos.
En la intoxicación por digitálicos, la bomba Na/K está bloqueada, originando un incremento del sodio intracelular y posteriormente un intercambio de tres iones de sodio por uno de calcio, lo cual da origen a un incremento del calcio intracelular. A diferencia de los pospotenciales precoces, los tardíos se inducen con frecuencias rápidas. Este mecanismo ha sido observado en las taquicardias ventriculares idiopáticas, ritmos idioventriculares acelerados, taquicardia ventricular sensible a adenosina y en algunas taquicardias auriculares, en especial las originadas en el seno coronario.
BRADIARRITMIAS:
Las bradiarritmias son alteraciones regulares o irregulares del ritmo cardíaco con frecuencias cardíacas inferiores a las correspondientes para la edad. Estas alteraciones pueden deberse a problemas del automatismo cardíaco o a un bloqueo en la conducción sinoauricular o auriculoventricular.
El punto en el que se produce el retraso o bloqueo puede ubicarse en el tejido auricular, en el nodo AV o en sistema de His-Purkinje. Podemos encontrarnos ante dos posibles situaciones:
- La alteración se encuentra de manera primaria, es decir, desde la vida fetal o periodo neonatal. Dicho nodo no permite la conducción del estímulo eléctrico de manera congénita, por una anomalía en su desarrollo, como ocurre en algunas cardiopatías congénitas, o en el bloqueo auriculoventricular congénito por el daño ocasionado por el paso transplacentario de anticuerpos maternos (por ejemplo, en hijos de madres con Lupus Eritematoso Sistémico -LES-).
- La alteración puede suceder de manera secundaria, en etapas posteriores de la vida, por lesiones isquémicas, miocarditis, técnicas quirúrgicas, vías cardiacas patológicas…
DIAGNÓSTICO:
El método diagnóstico de elección es el electrocardiograma, mediante la identificación de la onda de despolarización auricular (onda P) y el complejo de despolarización ventricular (complejo QRS), así como la duración de los mismos y el intervalo de tiempo isoeléctrico existente entre ambos (segmento PR).
Los valores normales de duración del intervalo PR varían en función de la edad y la frecuencia cardíaca, así como la duración del complejo QRS varía con la edad. A lo largo de los años estos valores van aumentando hasta alcanzar los estándares de la edad adulta.
CLASIFICACIÓN BRADIARRITMIAS:
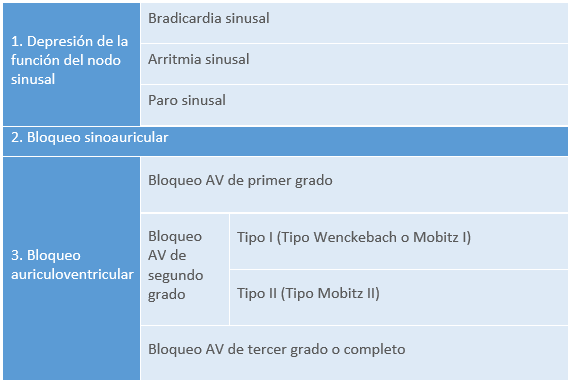
1. Depresión de la función del nodo sinusal
- Bradicardia sinusal: Fisiológica en la mayoría de las ocasiones, sin repercusión hemodinámica. Puede deberse a diferentes causas como: hipertonía vagal, hipertensión intracraneal, fármacos, hipotermia, hipoxia o puede ser secundaria a algunas cardiopatías congénitas. Generalmente tienen buen pronóstico, sin precisar tratamiento. Solo en casos sintomáticos con repercusión hemodinámica es necesario implantación de marcapasos para estimulación permanente.
- Arritmia sinusal: Al igual que en el caso anterior puede ser fisiológica. En los niños la más frecuente es la arritmia respiratoria. Cuando no es respiratoria, puede asociarse a determinadas cardiopatías congénitas o tras correcciones quirúrgicas. En el ECG se observa una variabilidad PP >0,12s con PR normal. Generalmente el pronóstico es bueno y no suelen requerir tratamiento.
- Paro sinusal: Se considera patológica la pausa superior a 3 segundos. En la mayoría de las ocasiones obedece a isquemia aguda, accidente cerebrovascular o intoxicación digitálica. El tratamiento, cuando es sintomático, es el implante de marcapasos.
2. Bloqueo sinoauricular:
Detención momentánea del marcapasos sinusal durante al menos un ciclo cardíaco completo. Si se alarga pueden aparecer latidos de escape desencadenados por focos ectópicos.
3. Bloqueo auriculoventricular:
El bloqueo auriculoventricular se define como la presencia de una conducción anormal del impulso eléctrico desde su salida del nodo sinusal (una vez que ha alcanzado la aurícula) hasta la despolarización de los ventrículos. Esto origina un retraso anómalo en la velocidad en la que acontece la conducción o incluso una ausencia de ésta.
- Bloqueo AV de primer grado: Las ondas P se siguen de complejos QRS, pero con un intervalo PR mayor del normal para la edad y frecuencia cardíaca del paciente. No suele producir síntomas ni deterioro hemodinámico. Es habitual en presencia de fármacos que interfieren en la conducción AV (por ejemplo, betabloqueantes o calcioantagonistas) o en situaciones de hipertonía vagal.
- Bloqueo AV de segundo grado: Algunas ondas P se siguen de complejos QRS, pero otras no. Existe conducción intermitente del impulso auricular. Se diferencian 2 subtipos:
- Tipo I (Tipo Wenckebach o Mobitz I): Se aprecia un alargamiento progresivo del intervalo PR hasta que hay una onda P que no conduce y posteriormente, tras ello, se reanuda el ciclo. Generalmente se asocian a un QRS estrecho, raramente progresando a un mayor grado de bloqueo, por lo que son de buen pronóstico y no necesitan tratamiento salvo que asocien sintomatología.
- Este tipo de bloqueo es fisiológico durante el sueño y en situaciones de hipertonía vagal. Sin embargo, cuando aparecen en presencia de cardiopatía estructural tienen mayor gravedad y peor pronóstico.
- Tipo II (Tipo Mobitz II): Antes de la onda P que no conduce no existe el alargamiento progresivo del PR propio del tipo I. Casi siempre se asocia con un complejo QRS ancho. Evoluciona con frecuencia a bloqueo completo y, cuando lo hace, el ritmo de escape suele ser inestable o insuficiente.
- Bloqueo AV de tercer grado o completo: Ninguna P se conduce a los ventrículos. Existe una disociación auriculoventricular.
TRATAMIENTO BRADIARRITMIAS:
El tratamiento de las bradiarritmias dependerá de la situación clínica y hemodinámica del paciente, en primer lugar, habrá que valorar la necesidad de iniciar medidas de RCP ante episodios de bradicardia extrema con compromiso hemodinámico. En otras ocasiones el tratamiento consistirá en perfusión de isoproterenol (simpaticomimético que actúa a nivel de los receptores beta adrenérgicos) y la colocación de un marcapasos, que puede ser temporal o definitivo.
En cuanto al tratamiento crónico resulta fundamental el seguimiento y observación de ese paciente para valorar la posible afectación miocárdica de la bradicardia.
TAQUIARRITMIAS:
El concepto de taquiarritmia implica un aumento del ritmo cardíaco, no necesariamente rítmico, causado por mecanismos no fisiológicos que pueden ser de diversos tipos y estar localizados en diversas zonas del corazón. El conocimiento de dichos mecanismos y su traducción gráfica, el ECG, es esencial para el diagnóstico y manejo adecuado de estos problemas.
CLASIFICACIÓN DE LAS TAQUIARRITMIAS:
La clasificación de las taquiarritmias se basa en la localización del mecanismo que da origen a la arritmia:

1. Auriculares (mecanismo de origen restringido a las aurículas):
a) Taquicardias auriculares focales y multifocales:
Forma de taquicardia rara, propia de neonatos y lactantes, en la que hay varios focos de activación auricular.
b) Flutter auricular:
El flutter auricular se da en dos situaciones: neonatos con corazón estructuralmente normal y en pacientes mayores con cardiopatía congénita y lesiones por cirugías previas (Flutter auricular perilesional). Línea de base con morfología en dientes de sierra (ondas F).
2. Auriculoventriculares (participan aurículas y ventrículos):
a) Taquicardias por reentrada AV por vía accesoria:
Las vías accesorias AV son tractos musculares anómalos situados en cualquier parte de los anillos fibrosos AV, que conectan el miocardio auricular y el ventricular.
Cuando la vía accesoria posee conducción anterógrada, parte del tejido ventricular se despolariza precozmente a través de la misma (preexcitación). Dicha despolarización es precoz (la velocidad de conducción de la vía accesoria es superior a la del nodo AV), por lo que se acorta el intervalo PR, y lenta (la despolarización del área preexcitada se realiza de miocardiocito a miocardiocito), produciendo un ensanchamiento característico de la porción inicial del QRS denominado onda delta. Así pues, PR corto, onda delta y QRS ancho constituyen las manifestaciones ECG de la preexcitación ventricular.
b) Taquicardia por reentrada intranodal
Forma de taquicardia muy rara antes de la edad escolar. La frecuencia aumenta con la edad. Implica la existencia de dos vías perinodales, una con velocidad de conducción lenta y período refractario corto (vía lenta) y otra con velocidad de conducción rápida y período refractario largo (vía rápida).
c) Taquicardia por reentrada AV permanente
Se trata de una taquicardia por reentrada mediada por un tipo de vía accesoria, localizada habitualmente en la región posteroseptal derecha, que posee unas características electrofisiológicas específicas. Causa que la taquicardia se inicie fácilmente y se mantenga durante largos períodos de tiempo. Esta taquicardia suele iniciarse en la infancia, tiene carácter incesante y puede pasar desapercibida, constituyendo un hallazgo incidental o debutando como insuficiencia cardíaca.
3. De la unión AV: se originan en la unión AV.
Se produce por la existencia de una zona de automatismo aumentado en la vecindad del haz de His. Existen dos tipos: una forma primaria, que puede ser de inicio precoz y de carácter incesante, y una secundaria, más frecuente, que se origina en el postoperatorio precoz de la cirugía cardíaca cuando se ha producido daño tisular en la unión AV (hemorragia, edema o inflamación).
4. Ventriculares: Taquicardia Ventricular:
Se define como 3 o más extrasístoles ventriculares a una frecuencia de 120-200 latidos/min. Los QRS son anchos y pueden ser monomórficos o pueden variar de forma fortuita (polimórficos). La Torsade de Pointes es una forma de taquicardia ventricular polimórfica, durante la cual hay cambios progresivos en la amplitud y polaridad del QRS.
Hipertensión arterial:
Clásicamente, la aparición de hipertensión arterial (HTA) en la infancia se ha considerado como un evento excepcional y siempre secundario a otra enfermedad. Sin embargo, en los últimos años, ha aumentado el número de publicaciones que centran su interés en la HTA primaria en la edad pediátrica. Si bien es más urgente detectar de forma temprana las formas secundarias, dado que éstas suelen ser más graves, a su vez es fundamental diagnosticar la HTA primaria en los niños lo más temprano posible.
En el año 2004, el National High Blood Pressure Education Program (NHBPEP) Working Group publica la última actualización sobre diagnóstico, evaluación y tratamiento de la HTA en la infancia y la adolescencia.
Prehipertensión arterial:
Se define en niños cuando la presión arterial sistólica (PAS) y/o la presión arterial diastólica (PAD) son ≥ p90, pero menores del p95 para edad, sexo y talla. Como en los adultos, los adolescentes con PA > 120/80mmHg también se considerarán prehipertensos, aunque para la talla ese valor sea menor del p90.
Hipertensión arterial:
Se define cuando el valor de PAS y/o PAD medido en al menos 3 ocasiones y en visitas separadas sea > p95 para edad, sexo y altura. Se distinguen a su vez 2 situaciones:
- HTA de estadio 1: si la PAS y/o la PAD se sitúa entre p95 y 5mmHg por encima del p99.
- HTA de estadio 2: si la PAS y/o la PAD es ≥ 5mmHg por encima del p99. Esta situación se denomina también crisis hipertensiva, ya que supone una amenaza para la función de los órganos vitales: si se presenta sin síntomas o con sintomatología menos grave, como vómitos o cefalea intensa, hablaríamos de urgencia hipertensiva, reservando el término emergencia hipertensiva para aquella situación que causa síntomas graves por afectación de órganos diana (encefalopatía hipertensiva, insuficiencia cardíaca congestiva, etc.). En ambas situaciones, el tratamiento ha de ser rápido, pero la última es una situación muy grave que requiere tratamiento urgente e ingreso en una unidad de cuidados intensivos pediátricos.
Aunque disponemos de tablas con rangos normales de presión arterial para niños y niñas según la edad y talla. Para el cálculo de percentiles se puede acceder a la página web: EndocrinoPED. En el apartado de antropometría, se introducen unos datos básicos del paciente (sexo, fecha de nacimiento, fecha de exploración, peso, talla y los valores de PAS y PAD) para obtener un informe endocrinológico con los percentiles a los que corresponde esa medición de presión arterial. En la siguiente tabla se adjunta un ejemplo:

Cuando la HTA es grave (crisis hipertensiva), la clínica estará determinada por la afectación del sistema vascular. Esta lesión es generalizada, pero los síntomas están determinados fundamentalmente por la afectación de 4 órganos diana:
- Sistema nervioso central (SNC): la encefalopatía hipertensiva se produce por un aumento de la presión arterial que sobrepasa los límites de la autorregulación cerebral. Potencialmente, es reversible si se controla la HTA. Aparece cefalea generalizada e intensa, vómitos y a veces convulsiones. Puede observarse edema de papila y/o hemorragias retinianas. En los casos más graves pueden producirse infartos lagunares, cuya clínica dependerá de su localización, e incluso una hemorragia intracerebral. Esta última es la complicación más grave y se asocia generalmente a cefalea intensa y síntomas neurológicos. Más del 90% se pueden complicar con hemorragias intraventriculares y posible hidrocefalia.
- Ocular: pueden producirse hemorragias retinianas, hemorragia vítrea y/o neuropatía isquémica óptica anterior.
- Cardiaco: si la HTA es crónica, se produce una hipertrofia progresiva del ventrículo izquierdo. Cuando se descompensa o en una situación aguda aparece clínica de insuficiencia cardíaca congestiva.
- Renal: la aparición de microalbuminuria y proteinuria será el primer indicador de lesión renal. Si la HTA no se controla, la afectación puede evolucionar a insuficiencia renal.
La crisis hipertensiva es la única situación en la que es urgente el inicio del tratamiento, aunque siempre evitando un descenso rápido por riesgo de hipoperfusión de órganos vitales. La cifra de PA no debe reducirse durante las primeras 8 horas más de un 25% de la reducción total planificada.
El método más seguro es la perfusión intravenosa continua de fármacos para asegurar un descenso controlado de la presión arterial y valorando según los casos el seguimiento con catéter arterial. El fármaco a usar dependerá fundamentalmente de las precauciones y las contraindicaciones en función del paciente. El labetalol, el nitroprusiato y la nicardipino intravenosa en perfusión continua son los 3 fármacos de elección.
En los casos en los que haya hipervolemia, habrá que asociar además restricción hídrica y diuréticos de asa: la furosemida en perfusión continua intravenosa sería el diurético de elección. Si no hay respuesta diurética, se valorará la instauración de una técnica de depuración extrarrenal urgente.
Hipertensión pulmonar:
La hipertensión pulmonar (HP) es una enfermedad caracterizada por una presión elevada de la arteria pulmonar (PAP), que puede provocar insuficiencia del ventrículo derecho (VD). En los niños, la HP se asocia más comúnmente con una enfermedad cardíaca o pulmonar subyacente. La HP puede asociarse con un riesgo considerable de morbilidad y mortalidad.
La HP se refiere a la presión elevada de la arteria pulmonar (PAP media >20 mmHg). La HP puede deberse únicamente a una elevación primaria de la presión en el sistema arterial pulmonar, a un aumento del flujo sanguíneo a través de la circulación pulmonar (p. ej., lesiones por cortocircuito sistémico-pulmonar) o a una elevación de la presión en las venas pulmonares.
Para niños y bebés >3 meses, la definición de HP es la misma que en adultos: presión media de la arteria pulmonar (PAP) >20 mmHg al nivel del mar. Esta definición se basa en el sexto World Symposium on Pulmonary Hypertension (WSPH) de 2018.
En los recién nacidos la resistencia vascular pulmonar (PVR) es alta en el útero y cae rápidamente después del nacimiento. La PAP normalmente alcanza los niveles adultos durante las primeras semanas de vida. Sin embargo, incluso si la PAP ha disminuido al ritmo habitual, el pulmón neonatal reacciona a los estímulos vasoconstrictores (p. ej., hipoxia alveolar) mucho más vigorosamente que el pulmón maduro, por lo que los factores estresantes provocan una respuesta mayor que en etapas posteriores de la vida. Además, en ocasiones se retrasa la transición neonatal a una circulación pulmonar de baja resistencia y, a pesar de tener pulmones sanos, la PAP media permanece elevada en ≥20 mmHg (a veces incluso suprasistémica). Estos recién nacidos asintomáticos requieren un seguimiento estrecho; sin embargo, en la mayoría de los casos, la HP se resuelve durante los primeros uno a tres meses y generalmente no se considera que tengan HP patológica a pesar de los niveles elevados de PAP.
- Lesiones de derivación cardíaca o enfermedad del corazón izquierdo: los pacientes con lesiones de derivación cardíaca sistémica a pulmonar pueden tener HP debido al aumento del flujo sanguíneo pulmonar (Qp) en lugar de enfermedad vascular pulmonar, per se. De manera similar, la enfermedad del corazón izquierdo que se asocia con una presión elevada de la aurícula izquierda (Lap; por ejemplo, insuficiencia ventricular izquierda, miocardiopatía, estenosis de la válvula mitral o aórtica u otras lesiones obstructivas del ventrículo izquierdo) puede causar HP debido al "retroceso" de presión (es decir, hipertensión venosa pulmonar). Los pacientes de estas categorías pueden en realidad tener vasos pulmonares sanos o anomalías vasculares pulmonares reversibles. Definir la HP únicamente sobre la base de la PAP no tiene en cuenta la cantidad de Qp o la presión venosa pulmonar como determinante de la PAP. Por el contrario, el PVR tiene en cuenta estas variables.
- Función del VD: el VD es el principal órgano terminal de interés en la HP. La PAP elevada es especialmente relevante en la medida en que afecta la función sistólica y diastólica del VD (es decir, su capacidad para generar flujo sanguíneo) en reposo y con ejercicio. Una PAP media que exceda considerablemente los 20 mmHg puede ser bien tolerada en un paciente cuyo VD está bien adaptado a la presión alta. Por el contrario, un aumento aparentemente menor en la PVR puede tener un impacto crítico en la función del VD en ciertos pacientes, incluso con niveles medios de PAP
TIPOS COMUNES DE HIPERTENSIÓN PULMONAR EN NIÑOS:
La HP pediátrica es una afección rara con una prevalencia estimada de aproximadamente 3 a 20 casos por millón de niños. La prevalencia varía según la edad, siendo mayor en lactantes
Los tipos más comunes de HP persistente/progresiva en niños son la HP asociada con cardiopatías congénitas, la HP debida a enfermedades pulmonares y la HP idiopática/hereditaria. Las formas transitorias de HP, como la HP persistente del recién nacido y la HP relacionada con una hernia diafragmática congénita, también son relativamente comunes.
- Hipertensión pulmonar persistente del recién nacido: suele ser de naturaleza transitoria.
- Cardiopatía congénita: sólo una pequeña minoría de pacientes con cardiopatía congénita desarrolla HP clínicamente significativa. Las dos categorías amplias de cardiopatías congénitas que pueden causar HP incluyen lesiones de derivación y enfermedades del corazón izquierdo asociadas con una presión auricular izquierda elevada (LAp).
- Derivación sistémica-pulmonar: por definición, la HP ocurre en cualquier defecto que, en virtud de su tamaño y ubicación, expone la circulación pulmonar a la presión arterial a nivel sistémico. Los defectos del tabique interventricular grandes son el ejemplo más común de esto. En los lactantes con este tipo de lesiones, el ventrículo derecho (VD) suele estar bien adaptado a la alta presión y, por tanto, la presión elevada de la arteria pulmonar (PAP), per se, tiene pocas consecuencias a corto plazo, aunque pueden presentar síntomas de insuficiencia cardíaca congestiva. Desde el punto de vista de la circulación pulmonar, la mayor importancia de los defectos de la derivación de alta presión no reparados es que, durante el primer o segundo año, el paciente puede desarrollar una alta resistencia vascular pulmonar (PVR) y una enfermedad vascular pulmonar hipertensiva, que puede ser irreversible y progresivo. La HP puede persistir y aumentar en pacientes después del cierre de derivaciones intracardíacas, especialmente cuando se cierran tarde. Por lo tanto, la reparación oportuna de los defectos de las derivaciones de alta presión es de gran importancia. Por el contrario, las comunicaciones interauriculares se asocian con cortocircuitos de baja presión (al menos inicialmente) y muy raramente provocan HP durante la infancia; Cuando se desarrolla HP, normalmente ocurre sólo después de las dos primeras décadas de la vida. A diferencia de la comunicación interventricular y el conducto arterioso persistente, el momento de la reparación de la comunicación interauricular (cuando está indicada) suele ser después del primer año de vida.
- Enfermedad del corazón izquierdo: las afecciones que aumentan la LAp (p. ej., enfermedad de la válvula mitral, falta de distensibilidad del ventrículo izquierdo) también pueden causar HP; sin embargo, estos no son comunes en la infancia.
- Estenosis de la vena pulmonar: la estenosis de la vena pulmonar es una causa poco común de HP. Es una enfermedad rara que puede ser idiopática o puede estar asociada con retorno venoso pulmonar anómalo total o parcial o prematuridad. Esta forma de HP es casi exclusivamente exclusiva de los pacientes pediátricos, siendo los bebés pequeños los más afectados.
- Enfermedad pulmonar: la displasia broncopulmonar es la entidad diagnóstica más notable en esta categoría. El mal desarrollo y la lesión adquirida de los vasos sanguíneos pulmonares son la base de la HP en este contexto, y el lecho vascular es especialmente propenso a la vasoconstricción con infección viral u otras tensiones. La mayoría de los pacientes con HP debido a displasia broncopulmonar sólo se ven afectados de forma leve a moderada, especialmente cuando están sanos, y la PAP generalmente disminuye con el crecimiento y el desarrollo.
- Muchos otros tipos de enfermedades pulmonares agudas y crónicas en niños pueden complicarse con la HP.
- Hernia diafragmática congénita.
- Enfermedad pulmonar intersticial.
- Síndrome de dificultad respiratoria aguda.
- Neumonía.
- Fibrosis quística.
- Hipertensión pulmonar idiopática/hereditaria: la HP idiopática y hereditaria se clasifican juntas porque son clínicamente indistinguibles. La HP hereditaria incluye pacientes con una mutación genética de HP conocida y aquellos con antecedentes familiares de HP. La HP idiopática se refiere a pacientes con HP en los que no se ha identificado una causa subyacente. Es probable que la HP hereditaria esté infradiagnosticada y algunos pacientes con HP idiopática pueden tener causas genéticas de su enfermedad.
- Síndromes: la HP se asocia con una gran cantidad de anomalías cromosómicas, síndromes y enfermedades multiorgánicas complejas. En datos de registros de HP pediátricos, entre el 12 y el 17 por ciento de los niños tenían síndromes cromosómicos o indefinidos subyacentes. El síndrome de Down es el trastorno más común en esta categoría; otros incluyen los síndromes de DiGeorge, Pierre-Robin y Noonan.
CARACTERÍSTICAS CLÍNICAS:
La presión de la arteria pulmonar (PAP) levemente o incluso moderadamente elevada puede no causar síntomas o solo de forma sutil, especialmente en personas sedentarias. Los síntomas pueden ser más notables si sobreviene una infección u otro factor estresante. En un estudio, el tiempo promedio desde la aparición de los síntomas hasta el diagnóstico fue de aproximadamente 17 meses.
El grado de los síntomas depende en gran parte como se adapta el VD al aumento de la carga de presión. La hepatomegalia y el edema periférico generalmente indican disfunción del VD y pueden no estar presentes incluso en casos de HP grave.
La ecocardiografía tiene una alta sensibilidad para identificar pacientes con HP clínicamente importante. El cateterismo cardíaco es el estándar de oro para el diagnóstico de HP, ya que proporciona la medida más precisa de la presión de la arteria pulmonar (PAP) y proporciona información valiosa adicional (p. ej., estimaciones del gasto cardíaco, presiones auriculares, respuesta a los vasodilatadores pulmonares).
La terapia dirigida, a veces denominada "terapia vasodilatadora pulmonar". Los agentes que se utilizan para la terapia dirigida a la HP incluyen:
- Bloqueadores de los canales de calcio (BCC; por ejemplo, nifedipino, amlodipino, diltiazem, pero no verapamilo)
- Inhibidores de la fosfodiesterasa tipo 5 (inhibidores de la PDE5; por ejemplo, sildenafilo, tadalafilo)
- Antagonistas de los receptores de endotelina (ARE; por ejemplo, bosentan, ambrisentan, macitentan)
- Análogos de prostaciclina (p. ej., epoprostenol, treprostinil, iloprost)
Los pacientes con HP grave refractaria al tratamiento médico tienen un alto riesgo de mortalidad. Las modalidades de tratamiento que se han utilizado con éxito variable en estos pacientes incluyen procedimientos de derivación de derecha a izquierda, soporte mecánico y trasplante de pulmón.
Procedimientos de derivación de derecha a izquierda: La creación de una abertura del tabique interauricular o de la arteria pulmonar (AP) a la comunicación aórtica para permitir la derivación de derecha a izquierda no es una intervención de rutina en el tratamiento de la HP pediátrica. Sin embargo, en pacientes con HP sintomática grave y refractaria, se pueden considerar estos procedimientos.
Los procedimientos que se han utilizado para generar derivaciones de derecha a izquierda en pacientes con hipertensión arterial pulmonar (PAH) incluyen la septostomía auricular con balón y la colocación de una derivación de Potts (anastomosis de lado a lado de la aorta descendente a la AP izquierda).
Soporte mecánico: El oxigenador de membrana extracorpórea (ECMO) se puede utilizar para reanimar a pacientes con HP que sufren un paro cardíaco y/o como soporte en espera de un trasplante de pulmón. Los dispositivos de asistencia pulmonar extracorpórea sin bomba (por ejemplo, oxigenador Novalung o Quadrox) también se han utilizado como puente para el trasplante de pulmón en pacientes con HP e insuficiencia grave del VD.
Trasplante de pulmón: es una opción de tratamiento para pacientes pediátricos con HP grave progresiva y deterioro del estado clínico a pesar del tratamiento. La HP es la afección más frecuente que conduce al trasplante de pulmón en niños de uno a cinco años y la segunda indicación más frecuente para pacientes pediátricos con trasplante de pulmón en general.
Insuficiencia cardíaca:
La insuficiencia cardíaca (IC) es un síndrome clínico consecutivo a la incapacidad del corazón y de los sistemas neurohormonales para mantener un gasto cardíaco que cubra los requerimientos metabólicos del organismo.
El sistema cardiovascular en el niño tiene una serie de características particulares: elementos contráctiles del corazón con menor desarrollo, inmadurez del sistema de conducción y una respuesta poco homogénea a las catecolaminas. El miocardio del neonato es inmaduro y alcanza la forma ordenada del miocardio del adulto de manera paulatina en la etapa de lactante. En el corazón neonatal, sólo un tercio del área del miocito tiene elementos contráctiles, situación que condiciona una menor masa efectiva contráctil y explica la respuesta inadecuada para elevar el gasto cardíaco al incrementar la precarga. Por todo lo anterior, el corazón neonatal tiene una limitación estructural que se hace evidente al utilizar inotrópicos y obtener una mínima mejoría en el gasto cardíaco. El corazón inmaduro del neonato y el lactante cuenta con una reserva cardíaca limitada y es muy dependiente de la frecuencia cardíaca. Aunado a lo anterior, las frecuencias cardíacas elevadas propias de esta edad producen una disminución en el tiempo de llenado ventricular y en la perfusión coronaria, lo que, sumado a un incremento en el consumo de oxígeno, condiciona estrés miocárdico.
El sistema reticular sarcoplásmico del miocardio neonatal tiene una mayor dependencia de la concentración de calcio extracelular en comparación con el miocardio adulto. Puesto que el calcio intracelular juega un papel central en la contractilidad miocárdica en los neonatos y lactantes, resulta indispensable la presencia de niveles sanguíneos normales para aumentar el gasto cardíaco. La incapacidad de manejar el volumen y la presión son los dos denominadores que actúan en la insuficiencia cardíaca y pueden presentarse de forma aislada o combinada. La sobrecarga de volumen es producto de una comunicación que permite un cortocircuito entre las dos circulaciones; este cortocircuito puede ser intracardíaco o extracardíaco. Otras alteraciones que determinan sobrecarga de volumen incluyen la insuficiencia de las válvulas atrioventriculares o sigmoideas y, finalmente, cuando hay dilatación del corazón producto de una alteración en las miofibrillas, como en las cardiomiopatías, por trastornos del ritmo o de la conducción cardíaca. Cuando existen problemas en el vaciamiento de alguno de los ventrículos, puede ser debido a obstrucción antes, a nivel valvular o después de las válvulas sigmoideas, o bien por aumento en las resistencias periféricas, como ocurre en la hipertensión sistémica y pulmonar.
El 82 % de los casos de IC en la edad pediátrica se produce debido a Cardiopatías Congénitas (CC) tanto nativa como reparada o intervenida. En el caso de las CC, al tratarse de una patología congénita, algunos de los factores de riesgo que se han asociado al desarrollo de estas patologías son el control inadecuado de diabetes mellitus materna, tanto antes de la concepción como durante el embarazo, la rubéola o la exposición a agentes teratogénicos, entre otros. Además, la existencia de anomalías cromosómicas conocidas o no pueden desencadenar la aparición de malformaciones cardíacas en neonatos El niño con insuficiencia cardíaca necesita más aporte de oxígeno y mayor presión de llenado ventricular para mantener un gasto cardíaco óptimo. Los mecanismos que utiliza el sistema cardiovascular para compensar el exceso de trabajo cardíaco incluyen el aumento del volumen circulante, de glóbulos rojos, del gasto por latido y de la frecuencia cardíaca, así como hipertrofia y dilatación de las cavidades cardíacas. Sin embargo, el crecimiento del corazón no es suficiente para dar una respuesta adecuada al incremento de la precarga o presión de llenado.
En la insuficiencia cardíaca existen otros aspectos a considerar, entre los que destacan el transporte de oxígeno, las alteraciones bioquímicas y los mecanismos de adaptación de la función cardíaca. En la edad pediátrica, como consecuencia de un gasto cardíaco elevado en reposo, la adaptación a una sobrecarga volumétrica es limitada. Tanto la dilatación como la hipertrofia ventricular son mecanismos importantes de compensación para mantener un gasto cardíaco adecuado. Sin embargo, el hecho de mantener una presión sistólica adecuada en una cámara dilatada implica un crecimiento de la tensión de la pared y consecuentemente un mayor consumo de oxígeno.
La hipertrofia ventricular, como respuesta a una carga impuesta al ventrículo, es otro mecanismo compensador para mantener el gasto adecuado. Esta respuesta varía de acuerdo a la sobrecarga impuesta al ventrículo. Con la hipertrofia ventricular, tanto el endocardio como el miocardio ventricular sufren isquemia debido a que el número de capilares que suplen las fibras hipertrofiadas no es suficiente para un aporte adecuado de oxígeno.
Otro mecanismo compensador importante a considerar es el renal: debido a la reducción del flujo renal, existe retención de agua y sodio en un intento por mantener el volumen intravascular y la perfusión renal. La retención de sodio en el túbulo distal y los colectores se debe a la acción de la aldosterona, en respuesta al aumento de la angiotensina II circulante. Este potente vasoconstrictor actúa como el estímulo más importante para la liberación de aldosterona de la glándula adrenal.
El péptido natriurético tiene un papel importante en mantener el volumen y presión arterial adecuado; este péptido se eleva en la insuficiencia cardíaca en la edad pediátrica y es liberado cuando se distienden las aurículas. Su nivel tiene una relación estrecha con el incremento del flujo pulmonar, con la presión atrial izquierda y con la presión arterial pulmonar. Su liberación produce una variedad de efectos, como son el aumento de la diuresis y la vasodilatación, e interactúa con otros reguladores del volumen circulante como la renina, la angiotensina y la vasopresina.
MANIFESTACIONES CLÍNICAS:
En lactantes y niños pequeños, la presentación típica de la IC se caracteriza por dificultad en la ingesta de alimento (desde periodos de ingesta elevados hasta intolerancia). También se pueden presentar síntomas como cianosis, taquipnea, taquicardia sinusal y diaforesis.
La sintomatología que caracteriza la IC en niños mayores y adolescentes consiste fundamentalmente en presencia de fatiga, dificultad respiratoria, taquipnea e intolerancia al ejercicio. Aparecen con menos frecuencia otros síntomas como dolor abdominal, oliguria o edema en extremidades inferiores. El fallo de los mecanismos compensatorios (activación del sistema nervioso simpático y la estimulación del sistema renina-angiotensina-aldosterona) promueve la progresión de la IC, de modo que la presentación de la sintomatología es más severa o incluso se produce en reposo.
Para valorar la severidad de la IC en niños se emplea habitualmente la Clasificación de Ross modificada. Esta clasificación estaría indicada para la evaluación de niños menores de 6 años, mientras que la New York Heart Association (NYHA) podría emplearse en mayores de 6 años.

Tumores cardíacos:
Las neoplasias cardíacas y pericárdicas primarias son raras; Además pueden ser asintomáticas o simular otras anomalías cardiovasculares más comunes, como arritmia, insuficiencia cardíaca congestiva, insuficiencia valvular o soplos. La presentación clínica y el pronóstico de los pacientes con estas lesiones varían según la ubicación de la lesión y el tipo histológico. La prevalencia de tumores cardíacos primarios informada en estudios de autopsia de pacientes de todas las edades es aproximadamente del 0,001% al 0,03%. La mayoría de los tumores cardíacos primarios que se manifiestan en niños son benignos, siendo el rabdomioma la neoplasia más común durante la vida fetal y la infancia, seguido del teratoma, fibroma y hemangioma. El tumor cardíaco pediátrico primario maligno más común es el sarcoma, que incluye sarcoma indiferenciado, rabdomiosarcoma y fibromiosarcoma.
En los últimos años, el diagnóstico de tumores cardíacos se ha visto facilitado por el uso de imágenes cardíacas no invasivas. La ecocardiografía es la modalidad de evaluación de primera línea. La resonancia magnética cardíaca y, en menor grado, la tomografía computarizada, se utilizan para la caracterización del tejido y para la evaluación del tamaño, la extensión y el efecto fisiológico.
TRATAMIENTO:
Los rabdomiomas tienden a involucionar con el tiempo, por lo que la cirugía está indicada sólo en caso de compromiso hemodinámico por obstrucción del flujo sanguíneo en las vías de entrada o salida ventricular, o cuando existan arritmias refractarias. Debe recordarse que muchos de estos pacientes se asocian con esclerosis tuberosa; por lo tanto, se requiere para su adecuada atención de un equipo multidisciplinario. Los pacientes con bloqueo AV completo necesitarán colocación de marcapasos definitivo, así como la ablación con radiofrecuencia en pacientes con rabdomiomas y taquicardia supraventricular.
No se ha documentado aún la regresión en caso de fibroma cardíaco, por lo que debe valorarse la extirpación quirúrgica. Por la alta incidencia de embolia que tienen los mixomas y por la potencial obstrucción valvular, estos tumores deben ser extirpados aun en ausencia de síntomas. Los tumores pericárdicos, sobre todo el teratoma, deben resecarse por el riesgo de transformación maligna y taponamiento cardíaco. Si se comprueba la malignidad de un tumor, debe considerarse el uso de quimioterapia o radioterapia.
La cirugía es necesaria para evitar muerte súbita en casos de lesiones obstructivas y arritmogénicas. En casos de tumoraciones cardíacas no resecables, el trasplante cardíaco puede ser una opción a considerar.
2.5 PROCESO DE ATENCIÓN DE ENFERMERÍA: NANDA-NOC-NIC
A continuación, se muestran unos Diagnósticos de Enfermería clasificados dentro de los Patrones Funcionales de Marjory Gordon. Estos NANDA se asocian a una serie de Resultados (NOC) y de Intervenciones (NIC) a modo de conceptualización, debido a que un Proceso de Atención de Enfermería es dinámico y, además, evoluciona a lo largo del tiempo, según cambia la situación del paciente en el proceso de salud-enfermedad. De esta forma, debemos determinar las intervenciones a realizar en cada una de sus etapas, de forma prioritaria, para satisfacer las necesidades alteradas.

PATRÓN 1- Percepción-Manejo de la salud.
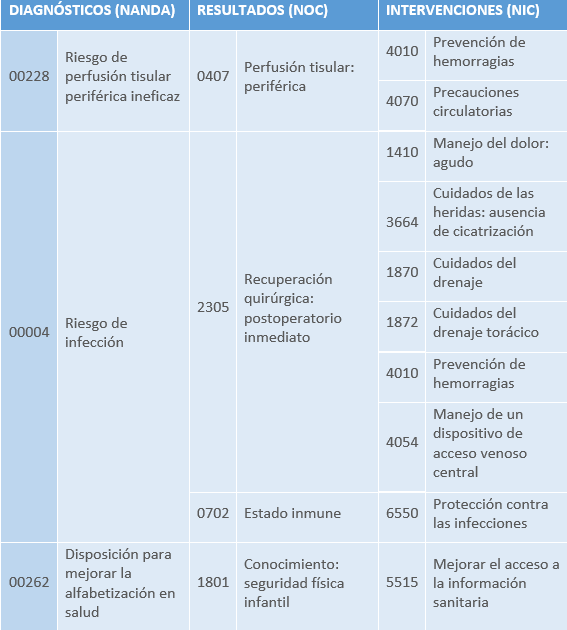
PATRÓN 2- Nutricional-Metabólico.
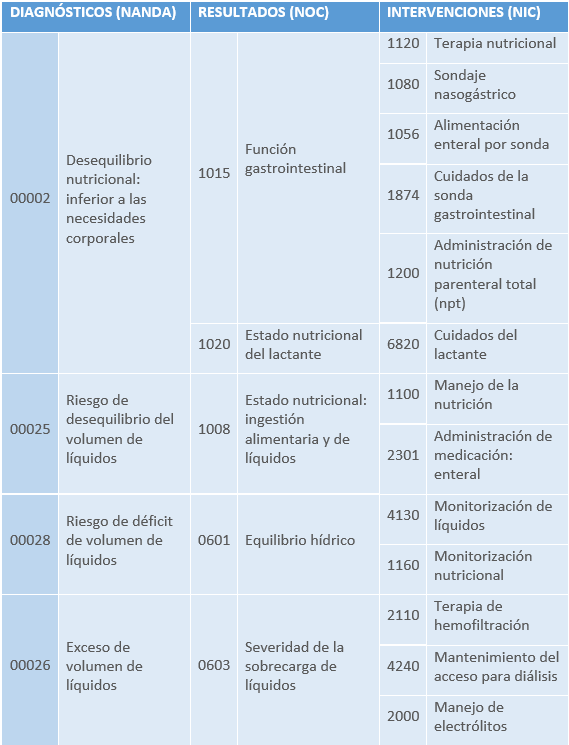
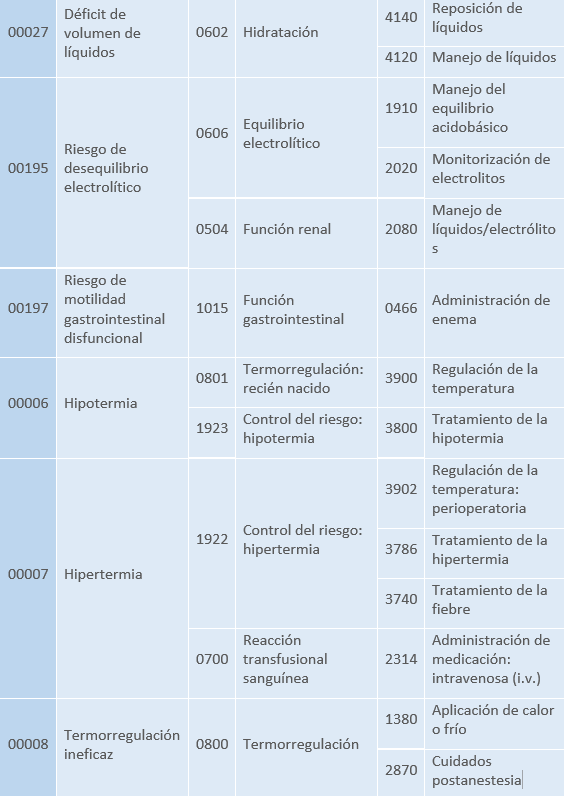
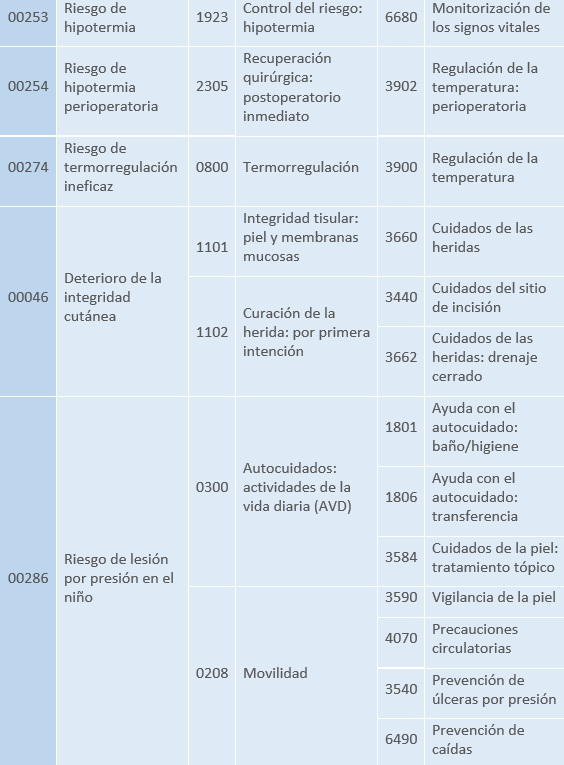
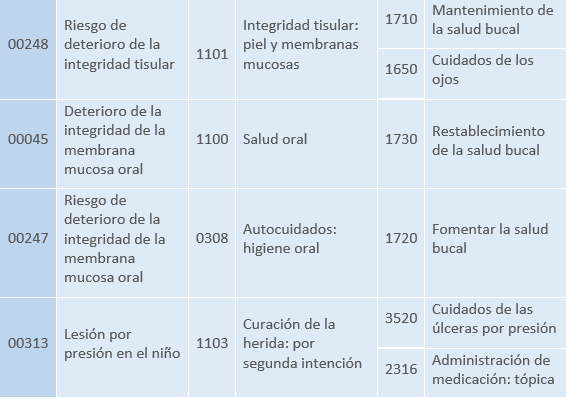
PATRÓN 3- Eliminación.
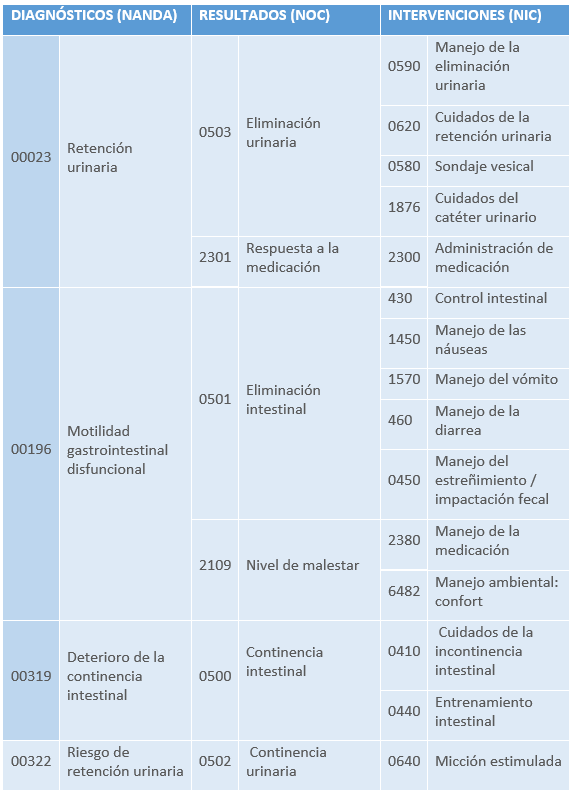
PATRÓN 4- Actividad ejercicio.
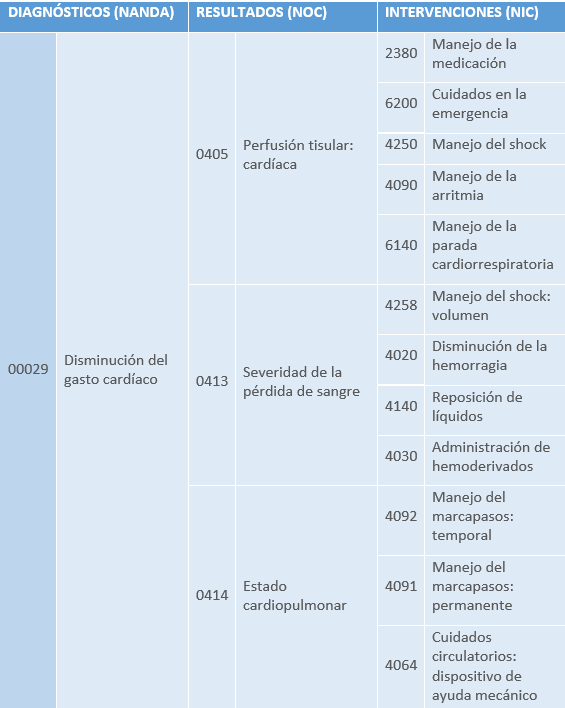
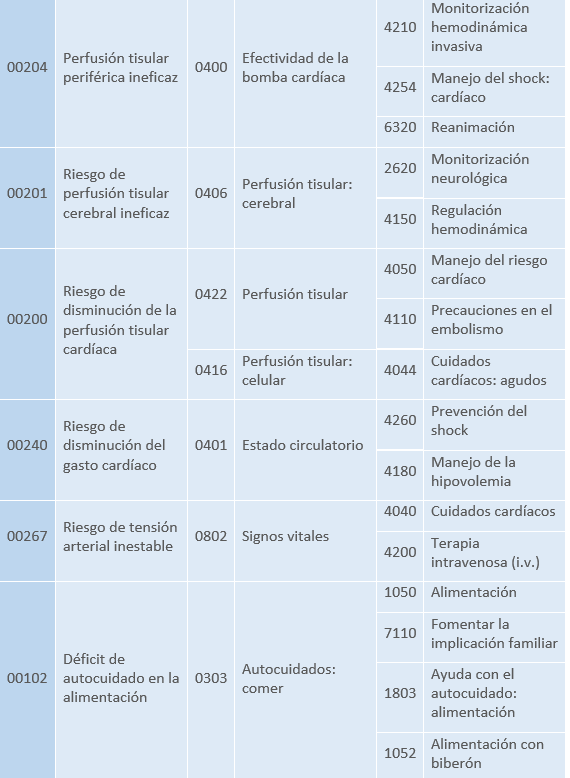
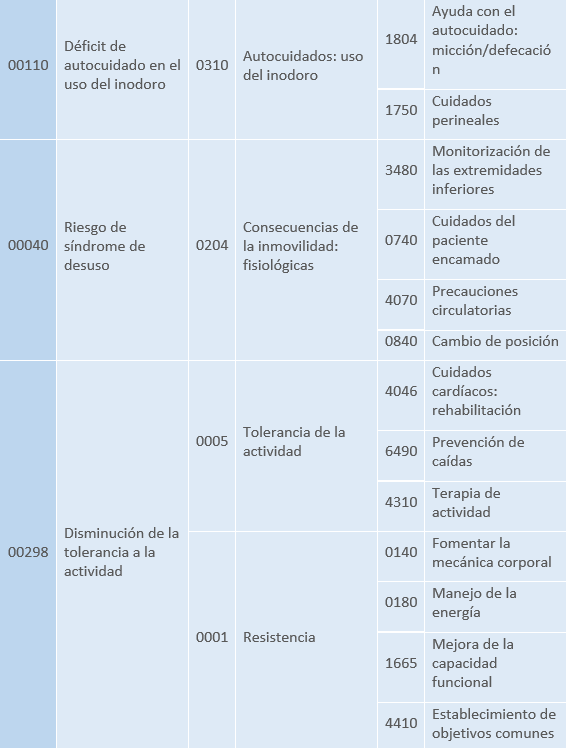
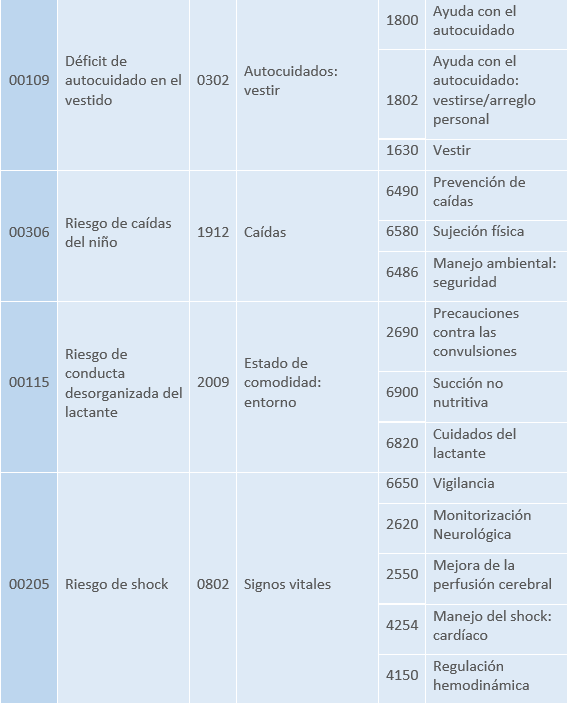
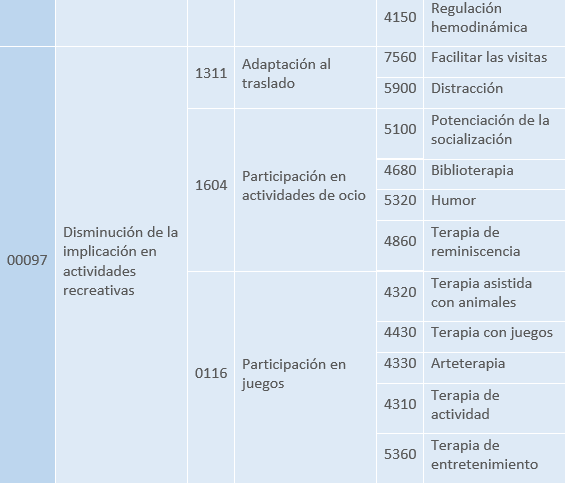
PATRÓN 5- Sueño-Reposo.
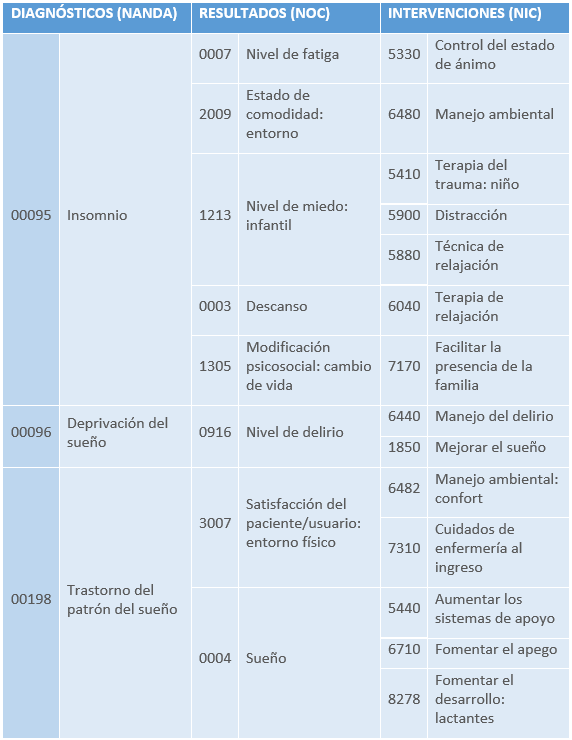
PATRÓN 6- Cognitivo-Perceptivo.
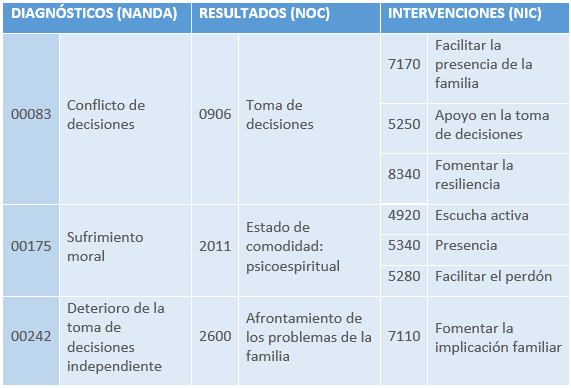
PATRÓN 7- Autopercepción-Autoconcepto.
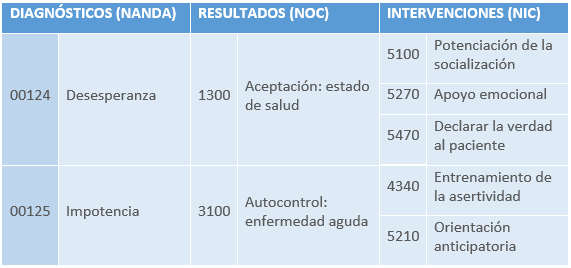
PATRÓN 8- Rol-Relaciones.
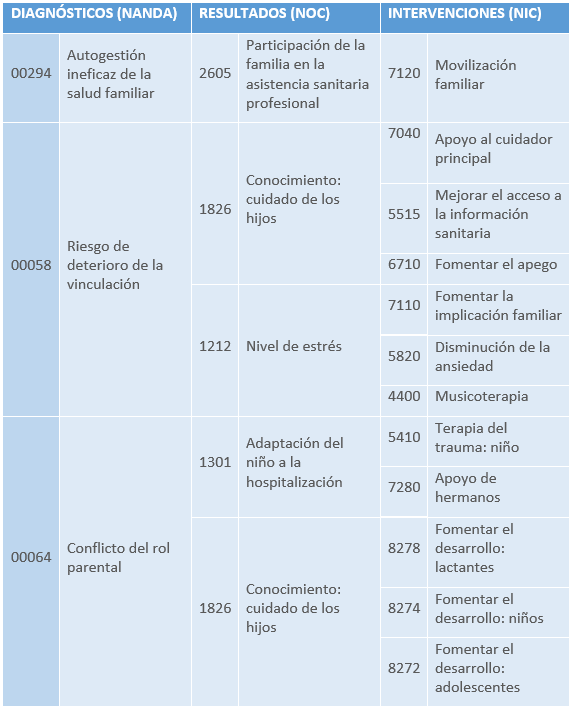
PATRÓN 9- Sexualidad-Reproducción.
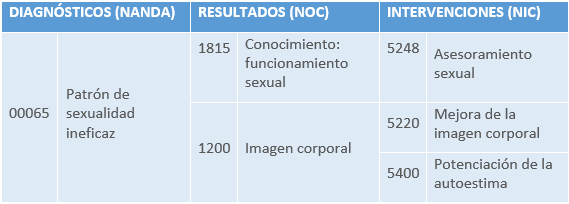
PATRÓN 10- Afrontamiento-Tolerancia al estrés.
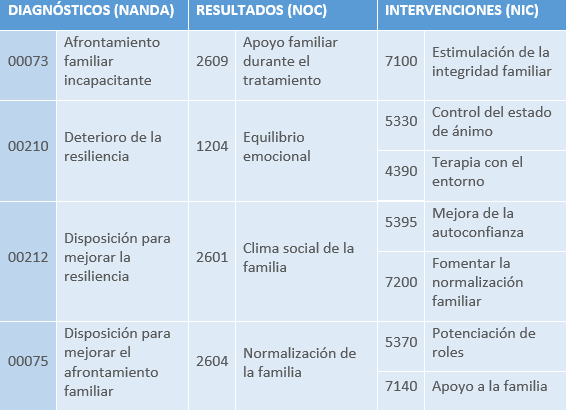

2.6 CUIDADOS CARDIOVASCULARES: PROCEDIMIENTOS Y TÉCNICAS:
Monitorización hemodinámica:
La corrección quirúrgica de una cardiopatía congénita supone una alteración de la hemodinámica previa de un paciente que se habrá de adaptar a la nueva situación fisiológica.
La anestesia general combinada con la circulación extracorpórea sumará efectos sobre los determinantes del transporte de oxígeno, existiendo una situación de necesidad adaptativa continua en las primeras horas. Es en este periodo donde existe el riesgo de producir un bajo gasto y por ello es esencial anticiparse a las posibles complicaciones con una adecuada monitorización del estado hemodinámico del paciente.
Este control se fundamenta en una estrecha vigilancia por personal de enfermería adecuadamente capacitado y entrenado, en colaboración con un médico intensivista que observe atentamente la evolución del paciente. La exploración clínica, si bien fundamental, se verá limitada por los soportes ventilatorios y la sedación, habiendo de complementarse con ayudas técnicas mediante dispositivos de monitorización de diferente invasividad. En este sentido, la valoración objetiva del Gasto Cardíaco (GC) en niños es compleja debida al decreciente uso del catéter de la arteria pulmonar. La monitorización básica se centra en el electrocardiograma y en la medición de presiones.
La monitorización avanzada basada en la ecocardiografía como principal instrumento se complementa con nuevos dispositivos tecnológicos. De especial interés para el control hemodinámico del paciente cardiópata intervenido son la termodilución transpulmonar (TDTP) y la espectroscopia cercana al infrarrojo (NIRS).
Monitorización hemodinámica básica:
ELECTROCARDIOGRAMA:
La obtención de las derivaciones I, II, IlI mediante electrodos adhesivos a piel y su registro continuo en el monitor de cabecera permite el estricto conocimiento de la frecuencia cardíaca y confirmar la existencia de un ritmo sinusal. El volcado de datos a la central de monitorización permite análisis de ondas, eventos y alarmas a lo largo del tiempo, posibilitando el análisis de tendencias.
Para el diagnóstico más preciso de arritmias y alteraciones electrocardiográficas será preciso realizar un electrocardiograma completo de 12 derivaciones. Especial interés para el diagnóstico y control de las arritmias auriculares tiene la obtención de un electrocardiograma atrial mediante el registro a través de los electrodos epicárdicos temporales colocados en el tiempo quirúrgico.
PRESIÓN ARTERIAL NO INVASIVA:
El registro de la presión arterial es fundamental para conocer la presión de perfusión de los órganos. Mantener la presión arterial en un rango en función de la edad, la cardiopatía y la situación clínica será un objetivo básico del postoperatorio. La referencia de la presión media (PAM) para la edad sería 40, 45, 50-60 y 65-75 mmHg para neonato, lactante, niño y adolescente, respectivamente. La presión de perfusión tisular (PPT) se calcula restando a la PAM la presión venosa central (PVC). Sobre todo, en cardiopatías con fallo derecho es muy probable que la PVC sea elevada, por lo que habrá de conseguirse una PAM mayor que permita mantener la PPT. La hipotensión ha de ser resuelta de forma inmediata ya que genera una alteración en la perfusión de los órganos que puede conducir a graves secuelas o incluso a la muerte. Sin embargo, hemos de recordar que la presión arterial no es sino una determinación derivada de 2 factores independientes que son el gasto cardíaco y la resistencia sistémica. Por ello, habrá siempre de ser manejada junto con la estimación del gasto, manteniendo ambos en límites adecuados.
Asimismo, la hipertensión ha de evitarse por las complicaciones que asocia: inducción de fallo cardíaco por aumento de postcarga, riesgo de hemorragia, lesión cerebral, etc.
El método básico de monitorización de la PA es el registro no invasivo mediante manguito. Esta medición es adecuada cuando no existen situaciones de bajo gasto, hipotensión o arritmias.
El tamaño del manguito:
Medir el perímetro del brazo en el punto medio (entre hombro y codo). Apuntar el perímetro y elegir el manguito más adecuado (que contenga la medida del perímetro del brazo dentro del rango indicado en el mismo manguito). Los tamaños de manguito más comunes en edad pediátrica son: 17-22, 22-32 y 32-42cm. La elección adecuada del tamaño es crucial, ya que un manguito menor del adecuado sobrestimará los valores de PA y viceversa.
Existen comercializados manguitos pediátricos de diferentes tamaños (anchura y longitud). Se recomienda que la longitud del manguito debe cubrir el 80-100% del perímetro del brazo, y la anchura del manguito el 40-50% del perímetro del brazo.
Se colocará el manguito de presión con la marca en zona anterior del codo (2-3 cm por encima de la fosa antecubital) con el brazo apoyado a la altura del corazón. El manguito debe de estar igualmente ajustado por su parte superior como inferior, pero dejando pasar el dedo del explorador por estos bordes.
PRESIÓN ARTERIAL INVASIVA:
Debido a las limitaciones, en situación postquirúrgica lo adecuado es disponer de una línea arterial que permitirá además la extracción de muestras para gasometría. Para monitorización invasiva se utiliza habitualmente la arteria femoral o radial (umbilical en neonatos), manteniendo un sistema de lavado continuo con suero heparinizado (1 Ul/ml) a ritmo de 1-2 ml/h. Las manipulaciones habrán de ser mínimas para evitar infecciones, sangrados y trombos, habiendo de manejarse asépticamente como una vía central.
Una ventaja adicional del sistema invasivo es la posibilidad de análisis de la onda de pulso. La forma de la onda, con especial atención a la elevación de la sístole y la posición del punto dicroto nos informan de la contractilidad cardíaca y el estado de resistencias. Una onda de escasa pendiente indica fallo de contractilidad, un punto dicroto tardío y poco elevado se relaciona con vasodilatación.
PRESIÓN VENOSA CENTRAL:
La presión venosa central (PVC) se puede registrar de manera continua mediante la inserción de un catéter a la entrada de la vena cava superior en la aurícula derecha a través de la vena yugular interna o de la subclavia. También es posible emplazar un catéter largo desde la vena femoral en posición supradiafragmática.
Imprescindible para la obtención de mediciones de la SvO2 central, su utilidad para estimación de la volemia es escasa y más aún en el escenario del postoperatorio. La PVC ha sido desechada como estimación de precarga, recomendándose otras monitorizaciones adicionales (ecografía, TDTP).
PRESIÓN DE LA ARTERIA PULMONAR:
Si bien el uso de un catéter de inserción percutánea tipo Swan-Ganz para la medición de la presión pulmonar y para el cálculo del gasto cardíaco está prácticamente erradicado de la práctica pediátrica, hay circunstancias que aconsejan monitorizar la presión pulmonar mediante la colocación de un catéter intraoperatorio. Su indicación fundamental es el diagnóstico y manejo de la hipertensión pulmonar. También nos permite obtener muestras para gasometría para valorar la presencia de un shunt izquierda-derecha significativo (SvO2 elevadas).
PRESIÓN AURÍCULA IZQUIERDA:
La colocación de un catéter intraoperatorio que nos permita monitorizar la presión de la aurícula izquierda (valor normal 4-12 mmHg), es especialmente útil en situación de hipertensión pulmonar (registros bajos), patología mitral o fallo del ventrículo izquierdo (registros elevados). Debido a los riesgos de infección y sangrado, su uso se reserva para indicaciones restringidas. El taponamiento cardíaco inducirá una elevación simultánea de la PAl y la PVC.
PRESIÓN INTRAABDOMINAL:
La presencia de fuga capilar, anasarca y ascitis puede ocasionar un aumento de la presión abdominal que interfiera en la hemodinámica ocasionando un síndrome compartimental abdominal. La medición de la presión intraabdominal (PIA) a través de un catéter vesical nos ayudará a plantear la necesidad de una paracentesis o una apertura abdominal. Presiones superiores a 15-20 mmHg pueden ser significativas en situaciones de inestabilidad clínica.
Monitorización hemodinámica avanzada:
La monitorización hemodinámica avanzada consiste en el uso de dispositivos para obtener datos objetivos del gasto cardiaco y sus determinantes, la predicción de la respuesta al aumento de la volemia y la valoración del edema pulmonar. Debido a su invasividad, coste o necesidad de formación específica se reservan para los pacientes en situación de shock o sometidos a situaciones de especial riesgo de alteración hemodinámica (cirugía cardiaca, ventilación mecánica, politraumatizados, administración de vasopresores…).
ECOCARDIOGRAFÍA-DOPPLER:
La ecografía es una herramienta imprescindible para valorar la presencia de lesiones residuales, derrame pericárdico, calcular la función contráctil (fracción de eyección del ventrículo izquierdo), la sincronía y la hipovolemia (colapso inspiratorio de a vena cava). La función sistólica del VD se calcula valorando el movimiento del plano anular de la válvula tricúspide (TAPSE). Además, se puede obtener el gasto cardíaco mediante el cálculo del volumen sistólico (GC= Vs x frecuencia cardíaca). El Volumen Sistólico se obtiene multiplicando el área de la válvula aórtica por el área bajo la curva Doppler obtenida en el tracto de salida del ventrículo izquierdo. Esta técnica no está exenta de subjetividad, viéndose influenciada por la angulación en la adquisición de las imágenes y por la asunción de un porcentaje fijo de distribución de flujo entre el territorio coronario-braquiocefálico y la aorta descendente (30/70), por lo que no debiera ser tomada como absoluta, sino en relación al estado del paciente y sobre todo es útil para valorar la evolución o respuesta del paciente a la terapia.
La ecografía torácica también nos será útil para valorar el edema pulmonar mediante la abundante presencia de líneas B (imágenes hiperecogénicas lineales en forma de láser que emergen desde la pleura en modo perpendicular) y la presencia de derrames pleurales.
SATURACIÓN VENOSA DE OXÍGENO:
Se denomina saturación venosa mixta a la que se obtiene del análisis de sangre obtenida de la arteria pulmonar, recogiendo el territorio de la cava superior, inferior y el seno coronario. La necesidad de inserción de un catéter en dicha localización hace que en la práctica se utilice la saturación venosa central (SvcO2), mediante una muestra obtenida de la aurícula derecha a través de una vía venosa yugular, subclavia o femoral. Este valor estima el balance entre el aporte y el consumo tisular de oxígeno y, aunque se relaciona con el GC, ambos reflejan aspectos diferentes de la hemodinámica y son determinantes en el cálculo del consumo de O2.
Su valor normal es del 70%. Desciende en situación de: anemia, hipoxemia, bajo gasto o aumento de las demandas tisulares. Un valor aumentado puede ser igualmente patológico en relación a fallo mitocondrial celular con incapacidad de metabolizar el oxígeno a pesar de una elevada oferta, esto puede ocurrir en situación de vasoplejia postquirúrgica. La diferencia con la saturación arterial de oxígeno (SaO2 - SvO2) es más útil para interpretar la situación hemodinámica en pacientes hipoxémicos, siendo un valor superior al 25% compatible con bajo gasto cardíaco. Habitualmente la SvO2 medida en la vena cava superior es menor a la del territorio de la cava inferior por el mayor consumo de O2 cerebral. Sin embargo, en situación de shock el descenso inicial de la perfusión esplácnica, conservándose la del territorio cerebral, invierte esta relación. Así, la valoración conjunta de muestras de la vena cava superior e inferior puede ser útil en la detección y manejo del bajo gasto.
Habitualmente se utiliza el análisis en gasómetro de muestras obtenidas a través de catéteres para valorar la SvO2, aunque existen sondas de fibra óptica que permiten el registro continuo.
GASTO CARDÍACO MEDIANTE TERMODILUCIÓN TRANSPULMONAR
El método de termodilución transpulmonar (TDTP) ha sido validado para medir el GC y es aplicable en pediatría. El sistema se fundamenta en la detección de la caída de temperatura en el circuito arterial sistémico (femoral) tras la inyección de un volumen conocido de suero salino enfriado en una vía central. Para que la medición sea correcta no debe recircular la sangre y el flujo ha de ser constante. Por ello, en la práctica, las lesiones cardíacas residuales (insuficiencia valvular, cortocircuitos) y las arritmias invalidan su uso, por lo que en muchas ocasiones el paciente postoperado cardíaco no es susceptible de su uso.
El sistema, además, ofrece datos sobre la volemia y la estimación del edema pulmonar, que, si bien se incluyen en los algoritmos de pacientes adultos, aún no pueden darse como establecidos en la infancia. Además, dada la heterogeneidad en relación con el cambio en la conformación corporal con el crecimiento, estas cifras podrían ser muy variables desde la lactancia a la adolescencia.
ESPECTROSCOPIA CERCANA AL INFRARROJO
La monitorización mediante “espectroscopia cercana al infrarrojo" (Near InfraRed Spectroscopy, NIRS) consiste en la colocación de un sensor sobre la piel para medir la saturación de oxígeno de la hemoglobina (Hb) del lecho venoso-capilar regional (rSO2) basado en que la Hb oxigenada absorbe más el espectro de luz de 800-850 nm, mientras que la reducida lo hace en el rango de 650-800 nm. La mayoría de la Hb en los tejidos se encuentra en el lecho venoso, por lo que la medición refleja preferentemente este compartimento a diferencia de la pulsioximetría. Los cambios en el registro reflejan cambios en la demanda o suministro metabólico de la región explorada, en relación al GC y al contenido arterial de O2.
Su uso como sensor de perfusión cerebral ha sido ampliamente difundido. Aunque se han intentado establecer valores de normalidad, el NIRS representa, más que un valor absoluto, un proceso dinámico. Un descenso del rSO significará perfusión disminuida, incremento en la extracción de O2, metabolismo elevado o bien un estancamiento circulatorio. Valores altos pueden indicar incremento de perfusión, metabolismo disminuido o menor extracción de O2.
Como se ha comentado previamente, conocer el balance entre la oferta y el consumo de oxígeno es fundamental para establecer que se está consiguiendo un adecuado suministro a los tejidos. La espectroscopia nos permite un sistema sencillo, continuo y de nula invasividad para poder explorar diferentes territorios.
El análisis de la saturación venosa mixta o central ha sido el parámetro clásico para conocer esta situación de forma global. Sin embargo, sería más interesante poder detallar la realidad en cada uno de los territorios del organismo, ya que la adaptación a la situación de bajo gasto obliga a la redistribución del flujo sanguíneo. En esta línea, una monitorización del territorio esplácnico, el primero en "sacrificarse" en situación de bajo gasto, nos permitiría anticipar una situación de riesgo antes de que se detectase en la SvcO2. Los valores renales basales suelen ser 15-20% mayores a los cerebrales debido a que el riñón es un órgano de alto flujo y escasa extracción en situación de gasto adecuado. Debido a que la SvcO2 refleja un promedio de las diferentes regiones del organismo, puede ser poco sensible al inicio de situaciones patológicas. Por ello es interesante mejorar la monitorización global con un examen regional que incluya diversos órganos o territorios.
Tener en cuenta que el estándar de oro para la monitorización hemodinámica en cuidados críticos pediátricos es un tema abierto.
2.7 PRUEBAS DIAGNÓSTICAS EMPLEADAS EN LA EDAD PEDIÁTRICA
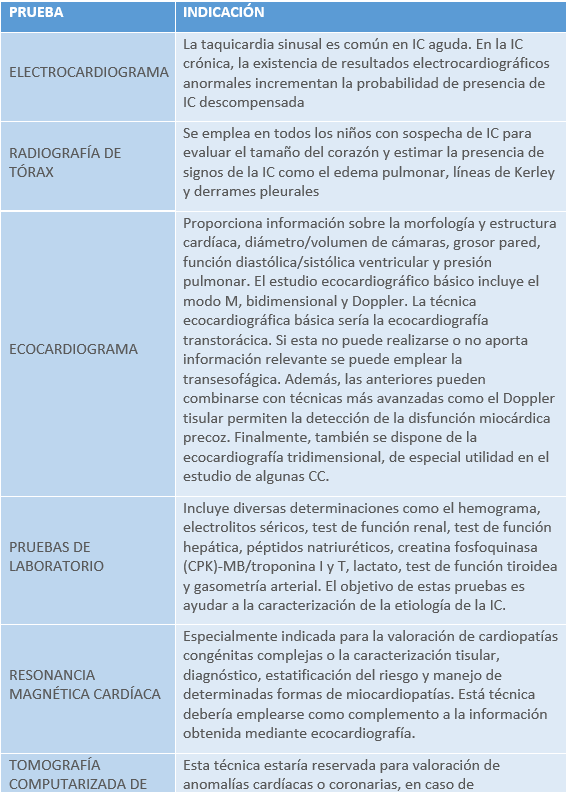

2.8 CATETERISMO TERAPÉUTICO
El papel del estudio hemodinámico pediátrico ha evolucionado significativamente a lo largo del tiempo. Los importantes avances en técnicas no invasivas desde la década de los 80 (ecocardiografía transtorácica, transesofágica, ecocardiografía 3D, angio TC y cardioresonancia) han disminuido significativamente las indicaciones con fines diagnósticos, en cambio, cada vez son más los procedimientos que se realizan con fines terapéuticos.
La evaluación diagnóstica hemodinámica preoperatoria no se realiza de forma rutinaria en la mayoría de defectos cardíacos congénitos, tales como defectos tipo canal auriculoventricular, comunicación interauricular, comunicación interventricular, tetralogía de Fallot, ventrículo derecho de doble salida, coartación de aorta, ventrículo izquierdo hipoplásico, transposición de grandes vasos, etc. Mediante ecocardiografía se puede establecer claramente el situs cardíaco, conexiones venosas y arteriales, anatomía septal, severidad de estenosis o insuficiencias valvulares, tamaño de arterías pulmonares, origen de arterias coronarias, anatomía de arco aórtico, etc., con el grado de exactitud requerido para realizar un tratamiento quirúrgico adecuado.
TÉCNICA:
Previamente a la realización del estudio hemodinámico es imprescindible un conocimiento completo de la historia clínica, una planificación del procedimiento a realizar y ofrecer una información adecuada y comprensible al paciente, padres o tutores legales.
En los días previos se obtendrá el consentimiento informado, consulta con el servicio de anestesia, así como una evaluación completa del estado clínico actualizado del paciente. De forma rutinaria se hará un hemograma, bioquímica y función renal. Se solicitará sangre en pruebas cruzadas, en caso de estudios terapéuticos, y el resto de pruebas serán variables según la patología del paciente y técnica a realizar. Normalmente estará a dieta absoluta mínimo 6 horas previo al procedimiento.
Tras la sedación o anestesia general, se prestará especial atención a la posición del paciente, para que esta sea óptima para la obtención de imágenes, y se tendrá especial cuidado en mantener una adecuada temperatura corporal. A continuación, se procede a la canalización de vía o vías a utilizar seguido de la anticoagulación con heparina.
En caso de realizar un cateterismo intervencionista se debe administrar profilaxis de endocarditis. Normalmente, seguiremos la pauta, si no existen antecedentes de alergia a betalactámicos se administrará cefazolina 30 mg/kg, tres dosis, cada 8 horas, la primera dosis antes de realizar el procedimiento.
La información obtenida durante el estudio hemodinámico y el cateterismo podríamos resumir en dos tipos:
- Una funcional, obtenida a través de la medición de presiones y saturación de oxígeno en las cámaras cardíacas y grandes vasos (presiones anómalas, gradientes de presión, gasto cardíaco, áreas valvulares, cuantificación de cortocircuitos anómalos, resistencias vasculares, etc.).
- Otra es anatómica, mediante la inyección de un volumen ajustado al peso de contraste yodado a una determinada velocidad y presión.
Una vez finalizado el estudio debe realizarse hemostasia cuidadosa en la zona de acceso vascular. En los niños, la forma más habitual de realizarla, actualmente, es la compresión manual. El error más frecuente al comprimir es hacerlo a nivel de la punción en la piel, cuando debe realizarse en la zona de punción del vaso, que habitualmente está 1-2 cm superior al sitio de punción en la piel. Existen una serie de dispositivos para cierre arterial mediante sutura percutánea (Perclose® y Angio-Seal®) que acortan el tiempo de realización de hemostasia, aunque solo puede utilizarse en adolescentes y adultos.
COMPLICACIONES:
En general las complicaciones del cateterismo cardíaco son pocas, pero potencialmente graves, por lo que es esencial una adecuada y cuidadosa planificación del procedimiento y prever las complicaciones.
Los efectos adversos mayores varían ampliamente dependiendo del procedimiento a realizar, edad, peso y estado clínico del paciente. En un reciente estudio se recogen las complicaciones en cateterismos diagnósticos y terapéuticos con una incidencia de 1.072 efectos adversos en 665 pacientes de un total de 14.790 cateterismos, lo que representa el 4,5% de todos los procedimientos.
En otros estudios, las complicaciones se relacionan principalmente con la edad, peso, estado clínico previo, necesidad de drogas vasoactivas, ventilación mecánica, complejidad de la cardiopatía y tipo de procedimiento a realizar.
Las complicaciones producidas en la zona de punción, aunque frecuentes, habitualmente son leves y no van más allá de pequeños sangrados autolimitados o pequeños hematomas. No obstante, es importante recordar que se relacionan con el tamaño del introductor empleado y con las punciones arteriales. Este tipo de complicaciones vasculares, son las que más frecuentemente se observan tras el procedimiento y en la Unidad de Cuidados Intensivos. Se debe tener especial cuidado y vigilancia de las zonas de acceso vascular en las horas posteriores a la realización del cateterismo. En caso de sangrado significativo debe procederse a la retirada del vendaje compresivo y realizar nueva compresión, visualizando la zona de punción en piel.
Entre las complicaciones vasculares más graves destacamos el hematoma retroperitoneal, la oclusión arterial y el pseudoaneurisma. Las fístulas arteriovenosas se desarrollan de forma tardía y ocurren generalmente tras el alta del paciente.
El sangrado retroperitoneal puede variar clínicamente desde ser asintomático hasta un cuadro de hipovolemia grave. Debe sospecharse en un paciente con acceso vascular femoral, generalmente arterial, que desarrolle anemia aguda o inestabilidad hemodinámica no explicada. En niños grandes y adultos un sangrado subcutáneo importante también puede llevar a este cuadro, aunque en general es más fácil de detectar.
La oclusión arterial también puede ocurrir sobre todo en niños pequeños o cuando son necesarios introductores grandes para el tamaño del paciente. Provoca frialdad, palidez y pérdida de pulsos distales. En lactantes y neonatos es frecuente una pérdida transitoria del pulso, con buena perfusión, y no precisa tratamiento. Ante la sospecha de un evento arterial es obligada la realización de un Doppler arterial para establecer la vascularización del miembro, localizar la oclusión, determinar la circulación colateral e identificar el trombo, si existiese. Si este estudio no es concluyente o si se planifica una intervención quirúrgica, está indicado la realización de un angio-TC. En caso de no recuperación de pulso, se debe realizar tratamiento con heparina sódica. Si la perfusión del miembro está comprometida debe iniciarse tratamiento con fibrinolíticos. Rara vez es necesario el tratamiento quirúrgico o la trombectomía percutánea, aunque no deben retrasarse en casos de tratamiento ineficaz o cuando existen contraindicaciones para recibir tratamiento fibrinolítico.
El pseudoaneurisma se manifiesta como una masa palpable que puede ir aumentando de tamaño y el diagnóstico se realiza por ecografía. Cuando son de tamaño pequeño se pueden trombosar espontáneamente. Los de mayor tamaño pueden tratarse mediante compresión directa, con o sin inyección de trombina guiada por ecografía. La cirugía se reserva cuando fracasan estos tratamientos previos o hay compromiso arterial del miembro inferior.
Las fístulas arteriovenosas son menos frecuentes y más tardías. Clínicamente se detectan por la aparición de frémito y soplo en la zona de la punción. Su diagnóstico también es ecográfico. Las de pequeño tamaño pueden cerrarse espontáneamente, aunque hay que seguirlas para confirmarlo. Las de mayor tamaño precisan tratamiento quirúrgico.
PROCEDIMIENTOS MÁS FRECUENTES REALIZADOS POR CATETERISMO:
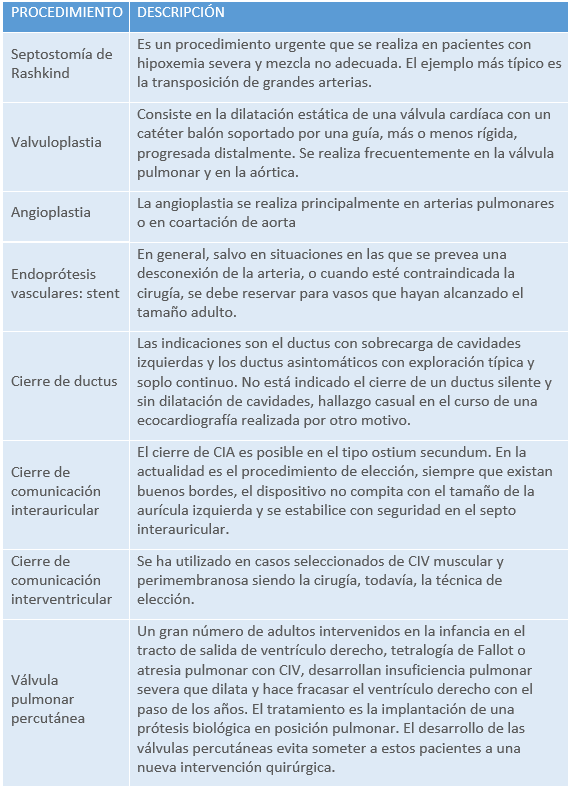
2.9 CUIDADOS DE ENFERMERÍA EN EL POSTOPERATORIO DE CIRUGÍA CARDIOVASCULAR
El personal de enfermería desempeña un importante papel en la recepción del paciente tras la cirugía cardíaca. Durante el postoperatorio, los cuidados de enfermería deben estar principalmente dirigidos hacia la identificación y resolución de las complicaciones potenciales. La enfermería, en su condición de cuidadora a pie de cama, se convierte en este contexto en un profesional clave en la atención a estos pacientes. Por ello, es importante que las enfermeras que tratan a estos pacientes tengan un buen conocimiento de:
- Las cardiopatías congénitas y su fisiopatogenia.
- La cirugía cardíaca para la corrección de anomalías y la nueva fisiología tras la intervención.
- Las complicaciones que pueden aparecer después de una cirugía extracorpórea (CEC).
2.10 PREPARACIÓN EN LA UNIDAD DE CUIDADOS INTENSIVOS DE PEDIATRÍA (UCIP)
Conocimiento del paciente que vamos a recibir: La información preoperatoria debe incluir las características del paciente y su cardiopatía, por lo que se registran datos de:
- Nombre, número de historia clínica, edad y peso del paciente.
- Diagnóstico y tratamiento previo.
- Tipo de intervención prevista.
Descripción de la preparación del box:
Preparación del monitor. Además de las mediciones básicas de cualquier ingreso en UCIP, módulos y cables de: ECG/FR, pulsioximetría (SpO2) y presión arterial no invasiva (PANI), se añadirán tantos módulos de presión como necesitemos (normalmente se utilizan dos, rotulados correctamente, presión arterial invasiva (PA) y presión venosa central (PVC).
En algunos casos será necesario la monitorización de otros parámetros: presión de aurícula izquierda (PAI), presión de arteria pulmonar (PAP), temperatura central, CO2 espirado, BIS, etc.
Una vez preparados los módulos, se elegirá perfil adecuado según paciente y se ajustarán las alarmas según las características del paciente.
En ocasiones se monitorizan otros parámetros externos al monitor como NIRS (Near-infrared spectroscopy).
Preparación de los soportes ventilatorios:
Preparación del Ambú® y válvula inspiratoria-espiratoria con su alargadera para una toma de O2 (comprobación de buen funcionamiento) y mascarilla adecuada al tamaño del paciente.
Comprobación de las tomas de gases (oxígeno y aire).
Conocer el soporte ventilatorio que precisa el paciente: En el postoperatorio inmediato normalmente: Ventilación mecánica (VM): Elección del respirador, conexión a las tomas de gases, selección del tamaño de las tubuladuras según el peso (valorar la necesidad de tubuladuras con humidificación pasiva o activa), realización del control preliminar, programación de los parámetros y comprobación del funcionamiento.
Ocasionalmente, puede precisar aporte de óxido nítrico que requiere preparación del aparato y colocación en VM.
Colocación de sondas de aspiración de secreciones adecuadas al tamaño del número del tubo endotraqueal que porte el paciente.
Preparación y comprobación de las tomas de aspiración:
Comprobar el buen funcionamiento de las tomas de aspiración.
Conocer el número de tomas necesarias (aspiración de secreciones, aspiración de drenajes pericárdicos, pleurales, mediastínicos).
Preparación de bombas de infusión:
El número de bombas de infusión dependerá de las perfusiones que precise, habitualmente se utilizan para: sueroterapia, drogas vasoactivas (a dosis adecuadas según peso del paciente), sedoanalgesia y otros fármacos.
Colocación de presurizadores (normalmente 2), en algunos centros hospitalarios se utilizan bombas de infusión con sueros heparinizados para mantenimiento de las diferentes presiones (PA, PAI, PAP).
Preparación de tubos de analítica:
Bioquímica, estudio de coagulación, hemograma, gases arteriales y venosos, etc.
Preparación de la cama para su traslado a quirófano de cirugía cardíaca:
- Hay diferentes formas de actuación según el centro hospitalario.
- Colocación de monitor de transporte con módulos de ECG, SpO2 y presión invasiva o no invasiva.
- Colocación del respirador de transporte.
- Colocación y preparación de las bombas de infusión continúa solicitadas por el anestesista o bombas de infusión vacías.
- Colocación de los presurizadores necesarios.
2.11 RECEPCIÓN DEL PACIENTE
Objetivo:
Disponer de una perfecta coordinación para disminuir al máximo el tiempo de recepción del paciente para el establecimiento de la monitorización hemodinámica y demás controles con ánimo de reducir los riesgos para el paciente. Para ello seguiremos el protocolo del centro que puede ser similar a este:
Recepción del paciente en UCIP:
Personal necesario:
- 2 Enfermeras (1 de ellas es la encargada del paciente) y, en ocasiones, un EIR.
- 1 TCAE.
- Adjunto UCIP y normalmente un MIR.
- Anestesista y cirujano.
- 2 Celadores de quirófano.
Secuencia en la transferencia:
- Conexión del paciente a Ventilación Mecánica, descartar problemas mecánicos de entrada de aire, vigilar movimientos torácicos, comprobar correcta fijación del TET y comprobación del balón del TET.
- Colocación de la cama a 30°.
- Monitorización de parámetros: FC, FR, CO2 espirado, SpO2, PA, PNI, PVC y calibración de los transductores de presión.
- Personal que atiende a la transferencia (no realiza ninguna otra actividad mientras se produce el traspaso de información):
- Enfermera que lleva al niño.
- Adjunto UCIP + MIR que lleva al niño.
- Anestesista y cirujano.
- El resto de personal (Enfermera, TCAE y EIR) pueden ir trabajando sobre el paciente (conexión de drenajes, analítica, etc.).
- Información por parte de Anestesia.
- Información de la intervención por parte de Cirugía cardíaca: Informe quirúrgico.
- Plan de objetivos (Pruebas complementarias, medicación, inicio de dieta, extubación y observaciones especiales).
El paciente queda a cargo del personal de UCIP:
- Completar la monitorización: NIRS, sensor BIS, temperatura central, etc.
- Comprobación del correcto funcionamiento de los tubos de drenaje.
- Conexión de perfusiones:
- Drogas vasoactivas por una luz del catéter venoso central (CVC), en caso de necesidad de cambiar la perfusión se realizará con doble bomba con especial vigilancia para evitar descompensaciones hemodinámicas.
- Perfusión, expansores y medicación por la otra luz del CVC.
- Sedoanalgesia.
- Sueros heparinizados para mantenimiento de catéteres (PA, PAI, etc.).
- Comprobación y fijación de sonda vesical y sonda nasogástrica.
- Control de apósitos de herida quirúrgica y catéteres.
- Extracción de la analítica.
- Solicitud de radiografía de tórax.
- Realización ECG de 12 derivaciones.
- Sujeción del paciente.
Protocolo de acogida:
- Comprobar la identificación del paciente (pulsera).
- Aplicar las precauciones estándar.
- Presentarse a la familia y orientarla en el entorno. Facilitar información oral y escrita. Entregar el folleto con la normativa de la unidad.
- Mantener confidencialidad de los datos.
2.12 PRIORIZACIÓN DE LOS CUIDADOS DE ENFERMERÍA
Durante el postoperatorio, los cuidados de enfermería tienen una doble vertiente:
- Valoración del paciente y plan de cuidados de enfermería.
- Detección precoz de posibles complicaciones.
La función de la enfermería es la valoración continua y objetiva del paciente para detectar y anticiparse a posibles complicaciones y para ello tenemos que ir vigilando diferentes parámetros:
1. Parámetros hemodinámicos:
El control hemodinámico es primordial en la valoración del paciente postoperado de cirugía cardíaca. Se debe conocer:
- Constantes vitales según la edad.
- Los tratamientos que se administran y sus efectos.
- Establecer unos límites de alarma de los parámetros adecuados.
- Identificar las alarmas de riesgo.
- Los principales parámetros hemodinámicos que debemos controlar son: frecuencia cardíaca (FC), frecuencia respiratoria
- (FR), presión arterial (PA), temperatura, saturación O2 (SpO2), presión venosa central (PVC) y gasto cardíaco (GC)
- Frecuencia cardíaca (FC):
Vigilar tanto la frecuencia cardíaca como el electrocardiograma, detectando y valorando las siguientes alteraciones:
- Bradicardia.
- Taquicardia.
- Arritmias.
Acciones de enfermería:
- Manejo adecuado de inotrópicos y sedación.
- Evaluar condiciones clínicas como perfusión periférica, relleno capilar, color y temperatura de la piel.
- Evitar hipoxia.
- Manejo de vía aérea.
- Mínima estimulación.
- Manejo del dolor y del estrés. Realización de la Escala del dolor según edad, y una vez por turno. Dependiendo de los centros hospitalarios se realizan diferentes escalas: escala FLACC, numérica, etc.
- Control de la temperatura: fármacos y medidas físicas.
- Control del sangrado y anemia.
- Identificar las arritmias en el monitor.
- Comprobar si hay repercusión hemodinámica
- Disponer de marcapasos y desfibrilador.
- Frecuencia respiratoria (FR):
Valorar el estado respiratorio del paciente.
Acciones de enfermería:
- Vigilar la frecuencia, ritmo, profundidad y esfuerzo de las respiraciones.
- Controlar el esquema de respiración: taquipnea, bradipnea, apnea, distrés, etc.
- Presión arterial (PA):
Valorar los cambios relacionados con la presión sanguínea del paciente.
Acciones de enfermería:
- Control del dolor y de estrés (control de sedoanalgesia).
- Control ambiental.
- Manejo de inotrópicos.
- Manejo del CVC.
- Manejo de hipotensores.
- Agrupar actividades para minimizar la manipulación.
- Temperatura:
El control de la temperatura es una actividad importante en el postoperado de cirugía cardíaca ya que variaciones de la misma pueden repercutir en el estado hemodinámico. A veces, se emplea termómetro central.
- Pulsioximetría (SpO2):
Es una medición no invasiva del oxígeno transportado por la hemoglobina.
Acciones de enfermería:
- Comprobar correcta colocación de la sonda de pulsioximetría ya que el sensor puede dar falsas mediciones en caso de hipotermia, por mala perfusión, shock, anemia, etc.
- Valorar la hipoxemia.
- Valorar hiperoxia en niños con oxigenoterapia.
- Presión venosa central (PVC):
Es un indicador de la volemia intravascular, la distensión ventricular y la presión intratorácica.
La medición se realiza por una luz del CVC, habitualmente por la luz distal, que en ocasiones se puede utilizar para perfusiones y medicación. - Acciones de enfermería:
- Vigilar colocación adecuada del transductor de presión, realizar calibraciones si precisa.
- Parar, momentáneamente, el ritmo de perfusiones y/o fármacos para realizar una correcta medición.
2. Soporte ventilatorio:
Dependiendo del soporte respiratorio que precise el paciente se realizaran diferentes acciones de enfermería.
- Con ventilación mecánica invasiva (VM):
- Observar si se producen alteraciones en los parámetros ventilatorios.
- Observar si se producen efectos adversos a la ventilación mecánica.
- Comprobar alarmas del respirador, incluida temperatura de humidificación de aire espirado.
- Controlar la lesión de la mucosa bucal.
- Documentar todos los cambios de los ajustes del ventilador y las respuestas del paciente.
- Asegurar la presencia del equipo de emergencia (Ambu® conectado a O2 y equipo de aspiración).
- Cuidados del tubo endotraqueal (TET):
- Registrar tamaño del TET y vigilar/registrar el número en el que está fijado.
- Asegurar/Verificar la correcta fijación y cambio de esparadrapos según protocolo de cada unidad.
- Comprobación de la presión de pneumotaponamiento para evitar neumonía asociada a la VM (la presión debe estar entre 20 y 30 cmH2O).
- Correcta sedación.
- Aspiración de secreciones según protocolo.
3. Cuidados y manejo de las vías venosas:
Los pacientes postoperados de cirugía cardíaca son portadores de varios catéteres: arterial, CVC, catéteres periféricos, por ello dentro de los cuidados de enfermería están el control y la manipulación de estos accesos.
- Acciones de enfermería:
- Higiene de manos previa manipulación de cualquier catéter.
- Manipulación aséptica.
- Vigilar permeabilidad.
- Vigilar posibles extravasaciones.
- Vigilar puntos de inserción del catéter y coloración del miembro portador.
- Cambio de apósito según precise.
- Cambio de equipos de perfusiones según protocolo.
- Utilizar soluciones desinfectantes en el cambio de perfusiones.
- Mantenimiento de un ritmo de infusión correcto.
- Identificación de las medicaciones que se están pasando por cada luz.
- Extracción de muestras con las medidas asépticas pertinentes.
4. Cuidados y manejo de los equipos de infusión:
La vigilancia constante de las infusiones se debe realizar para evitar la inestabilidad hemodinámica.
- Acciones de enfermería:
- Etiquetado correcto de las medicaciones y de sus líneas.
- Control del ritmo de las infusiones.
- Colocar perfusiones de inotrópicos en bombas de presión.
- Prever el final de las infusiones sobre todo de inotrópicos para realizar su cambio a doble bomba y evitar
posibles alteraciones hemodinámicas.
- Conocer las compatibilidades de las medicaciones.
- Administración de medicaciones y/o perfusiones:
1. Inotrópicos por una luz del CVC, si es posible infundir por separado, normalmente por la luz proximal.
2. Sueroterapia y medicaciones por otra luz del CVC.
3. Sedación y analgesia por otra luz del CVC o vía periférica.
4. Correcciones de iones por CVC.
5. Cargas de volumen o hemoderivados por vía periférica o una luz del CVC.
- Dependiendo de la situación hemodinámica del paciente puede precisar medicaciones en perfusión continua, siendo necesario canalización de nuevos catéteres (diurético, insulina, amiodarona, etc.).
- Fármacos vasoactivos e inotrópicos más frecuentemente utilizados:
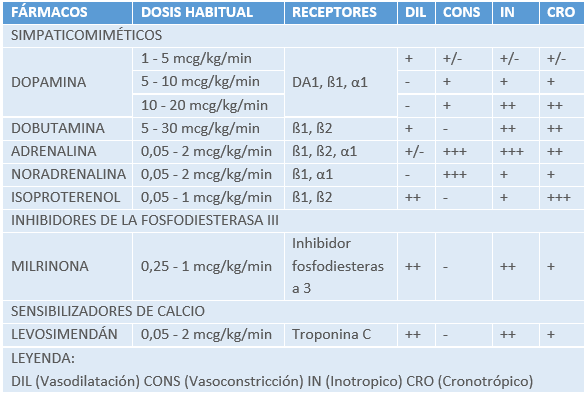
5. Cuidados de los drenajes:
Estos pacientes también son portadores de drenajes pericárdico, pleural o ambos.
- Acciones de enfermería:
- Asegurarse de que están conectados a aspiración y a la presión correcta.
- Fijarse en el punto de inserción para detectar posibles signos de infección.
- Vigilar las conexiones de los tubos de drenaje.
- Vigilar la permeabilidad del drenaje.
- Observar/registrar el volumen, cada quince minutos las dos primeras horas.
- Observar las fugas de aire.
- Valorar características del drenaje:
1. Si es hemático más de dos días habrá un sangrado activo.
2. Si el sangrado es mayor o igual a 10 cc/kg/h es una urgencia.
3. Si es lechoso, quilotórax.
6. Cuidado de la herida quirúrgica:
Es importante la vigilancia de la herida (bordes, exudado) para evitar posibles complicaciones.
- Acciones de enfermería:
- Observar apósito en la recepción del paciente. Si el apósito está manchado de sangre rotular para valorar su evolución.
- Cambiar el apósito cuando precise.
- Realizar la cura de forma aséptica y valorar los posibles signos de infección, dehiscencia o cualquier otro problema.Si el paciente llega con el tórax abierto estricta vigilancia (vigilar abombamiento) y no manipulación.
7. Cuidados de la sonda vesical (SV) y diuresis:
La medición de diuresis es importante en estos pacientes, así como el control del balance hídrico.
- Acciones de enfermería:
- Controlar periódicamente la eliminación urinaria, incluyendo la frecuencia, consistencia, olor, volumen y color, si procede.
- Vigilar características de la orina.
- Medir diuresis.
- Remitir al médico si se producen signos y síntomas de infección del tracto urinario.
- Observar si hay signos y síntomas de retención urinaria.
- Protocolo de manipulación de SV para evitar infecciones.
8. Cuidados del marcapasos:
En ocasiones, por problemas del ritmo cardíaco es necesario la utilización de un marcapasos temporal externo.
- Acciones de enfermería:
- Vigilar los cables de marcapasos y su correcta colocación.
- Revisar su correcto funcionamiento y tener una pila de recambio por si se necesita.
- Revisar la programación.
- Vigilar en el ECG cuando está en ritmo de marcapasos.
- Vigilar el lugar de colocación del marcapasos para evitar caídas.
9. Cuidados neurológicos:
Valoración del estado neurológico del paciente, si está despierto se le realizará Escala de Glasgow. Si está sedado y/o relajado, control de pupilas y colocación de un sensor BIS o NIRS.
10. Además, se realizará una valoración integral del paciente teniendo en cuenta:
- Autocuidados.
- Riesgo de caídas.
- Riesgo de deterioro de la integridad cutánea.
- Dolor.
- Deterioro de la movilidad física.
- Familia.
2.13 OXIGENACIÓN POR MEMBRANA EXTRACORPÓREA (ECMO)
El soporte circulatorio mecánico se ha convertido en los últimos años en una herramienta habitual dentro del manejo de pacientes con fallo cardíaco y/o respiratorio grave refractario a las terapias convencionales. En el ámbito pediátrico existen dos tipos: los dispositivos de asistencia ventricular externa (VAD, ventricular assist device) que ofrecen exclusivamente soporte hemodinámico, y la oxigenación por membrana extracorpórea (ECMO, extracorporeal membrane oxygenation) que puede además ofrecer soporte respiratorio. La experiencia con balón de contrapulsación intraórtica en la edad pediátrica es muy limitada.
El primer caso de ECMO cardíaca con éxito fue en 1972 en un niño de 2 años que tras ser sometido a una cirugía correctora de una transposición de los grandes vasos mediante técnica de Mustard fue soportado con ECMO durante 36 horas por Robert Bartlett. A lo largo de las últimas décadas las indicaciones de ECMO en el paciente con patología cardíaca se han ido ampliando y la técnica ha ido cambiando con la utilización de distintas bombas y circuitos. Además, el número de centros en los que se aplica este procedimiento está aumentando. La ELSO (Extracorporeal Life Support Organization) ha registrado desde enero de 1989 hasta julio de 2016 un total de 78.397 pacientes sometidos a ECMO, 23.874 por patología cardíaca.
La ECMO o ECLS (Extracorporeal Life Support) es una terapia que utiliza un "bypass" cardiopulmonar parcial (ECMO veno arterial) o un circuito pulmonar en serie (ECMO veno venoso) para dar soporte cardíaco y/o pulmonar por un tiempo (comúnmente de 1 a 4 semanas). Esta terapia proporciona tiempo para descanso pulmonar y/o cardíaco y con ello la posibilidad de recuperación. Se desarrolló a principios de la década de los setenta desde la técnica de circulación extracorpórea (CEC) utilizada en cirugía cardíaca. Se indica a pacientes adultos, pediátricos y neonatales con fallo respiratorio y/o cardiaco grave, potencialmente reversible, que no responden a terapia convencional.
COMPONENTES DEL SISTEMA:
- Cánulas:
Son cánulas de poliuretano reforzadas con anillos de acero inoxidable, que presentan flexibilidad y resistencia al acodamiento, son radiopacas y permiten altos flujos.
- Venosas: De salida del paciente, conectada a un circuito de tubos que conectara con la entrada al sistema.
- Arteriales o de retorno: De entrada en el paciente, conectado con circuito de tubos que salen del dispositivo.
Se seleccionarán en función de la superficie corporal del paciente, así como el calibre del vaso que se va a canular, pero siempre se intentará elegir la de mayor calibre posible para asegurar el flujo adecuado y las mínimas resistencias al flujo.
Cuando la canulación es femoral, es frecuente añadir una cánula de perfusión del miembro, dado que se puede producir una isquemia distal al ocluir totalmente la arteria femoral, esta cánula mantiene la perfusión de la extremidad inferior. - Líneas:
Sistema de tubos que conectan las cánulas del paciente con la bomba y el oxigenador. Las líneas también son dos: Línea venosa (Color azul) y la línea arterial o de retorno (Color rojo). - Consola:
Es la encargada del control hemodinámico del sistema, suministra la fuerza electromotriz a la bomba, regula su potencia, es decir la velocidad de rotación de la centrífuga, registra la información aportada por el sensor externo colocado en la línea de salida y por los demás sensores hemodinámicos, bioquímicos y de seguridad implantados en el circuito. Cada tipo de bomba funciona con su propia consola, que como mínimo nos indicará las revoluciones por minuto (RPM) y el flujo en litros por minuto (LPM).
- Bomba centrífuga:
La bomba centrífuga proporciona la energía necesaria para impulsar la sangre a través del circuito, generando presiones negativas en la línea y cánula venosas, que da lugar al flujo de sangre hacia la bomba, y presión positiva en la línea y cánula arteriales que permite el retorno de sangre al paciente.
Estas bombas generan flujo laminar no pulsátil y son de naturaleza no oclusiva. Modificando la precarga y la postcarga conseguiremos el flujo o gasto cardíaco deseado en cada paciente. Todo esto se controla a través de un sensor de flujo.
En general son bombas de flujo continuo, de levitación magnética, (el rotor está suspendido magnéticamente, no contiene soportes que lo fijen a la carcasa), este hecho diferencial con otras bombas centrifugas, hace que haya menos fricción entre los elementos formes de la sangre, generando menos producción de calor y por tanto disminuyendo las posibilidades de hemólisis y la formación de trombos. - Oxigenador de membrana:
El oxigenador se compone de una fase gaseosa y una fase sanguínea, separadas por una membrana, que en el caso de los que se utilizan actualmente en ECMO son de polimetilpenteno (PMP) impermeables al plasma que favorece su uso continuado durante varios días manteniendo un intercambio gaseoso de calidad, evita las fugas de plasma y previene la formación de microburbujas. La transferencia de gas desde la fase gaseosa a la sanguínea, o viceversa, es motivada por difusión, que es el movimiento de los átomos o moléculas de un gas desde las regiones de más alta concentración a las regiones de concentración más baja. - Mezclador de gas o caudalímetro:
Por medio de este dispositivo, formado por un mezclador de gases que regula la proporción de oxígeno/aire y un caudalímetro que regula el flujo de esta mezcla que entra en el oxigenador, se lleva a cabo el aporte de oxígeno adecuado. El aporte de oxígeno y la eliminación de dióxido de carbono (CO2) son relativamente independientes. El control de la eliminación de CO2 se realiza variando el flujo de gas del mezclador; si se aumenta el flujo de gas aumentamos la eliminación de CO2 al disminuir la presión parcial de CO2 en la fase gaseosa, muy similar a la respiración profunda del pulmón y viceversa. El control del aporte de oxígeno se lleva a cabo aumentando o disminuyendo la proporción de oxígeno del gas suministrado por el mezclador.
- Intercambiador de calor:
Los oxigenadores además van provistos de un circuito por donde circula agua a una temperatura variable, permitiendo enfriar o calentar la sangre en contacto con dicho sistema. La sangre que circula por el circuito va perdiendo calor en su recorrido, por lo que debe mantenerse en normotermia.
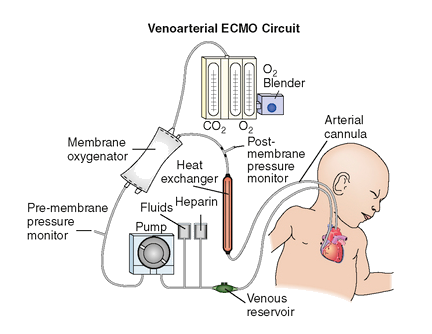
Ilustración 16. Fuente: Pike N, Klee L, Zemetra B. Circuito de oxigenación por membrana extracorpórea venoarterial. Nurse Key. 2023.
INDICACIONES:
De manera general, la ECMO está indicada en casos de fallo cardíaco y/o respiratorio agudo potencialmente reversibles, pero con elevada mortalidad a pesar de una máxima optimización de la terapia convencional (de manera muy teórica se aconseja considerar el soporte ECMO si la mortalidad esperada es del 50%, e indicarla si la mortalidad esperada es del 80%). También se puede indicar como puente a trasplante o a otro tipo de soporte mecánico que se pueda mantener a largo plazo.
OBJETIVOS:
Asegurar un flujo sanguíneo adecuado para suplir las necesidades del metabolismo celular en pacientes con un gasto cardíaco inadecuado. Para ello se precisará de una ECMO venoarterial (ECMO VA). El flujo sanguíneo variará de 60 a 100 ml/kg/min (en ocasiones hasta 150 ml/kg/min) en función de si se consigue o no una adecuada perfusión, valorada por signos clínicos (diuresis, frecuencia cardíaca) y analíticos (saturación venosa mixta, lactato, equilibrio ácido-base).
Asegurar una adecuada oxigenación y lavado de CO2 en pacientes con disfunción pulmonar. Si el paciente mantiene un gasto cardíaco adecuado, puede instaurarse una ECMO venovenosa (ECMO VV). La oxigenación correcta, asumiendo un gasto cardíaco y hematocrito adecuados, se conseguirá habitualmente con una saturación arterial de 02 entre 80-90%, aunque dependerá del diagnóstico del paciente y la configuración del circuito y deberá monitorizarse mediante el equilibrio ácido-base arterial y el lactato. La PaCO, es fácilmente controlable con un correcto flujo de gas y sangre a través del oxigenador.
Prevenir las complicaciones relacionadas con otras terapias. Se pretende evitar o disminuir el daño pulmonar producido por una ventilación mecánica agresiva, los efectos hemodinámicos negativos relacionados con la ventilación mecánica y la presión intratorácica elevada, así como el aumento del estrés miocárdico y el daño en órganos diana que producen las altas dosis de inotrópicos y vasoconstrictores. También se utiliza la ECMO para facilitar otras terapias, como cateterismos cardíacos complejos, intervenciones sobre la vía aérea o el mantenimiento de órganos en donantes para trasplante.
MODOS DE ECMO:
- ECMO veno-venoso (VV):
Está indicado para el soporte del fallo respiratorio, con función cardiaca adecuada con o sin inótropicos. Generalmente se drena sangre desde la vena femoral y se devuelve oxigenada a la aurícula derecha vía yugular derecha.
Se considera que el soporte es adecuado cuando la SaO2 > 85% y la SvO2 > 60%, en ventilación apneica. Esto generalmente se consigue con flujos de sangre de 120 ml/kg/ min para neonatos y 60-80 ml/kg/min para niños y adultos.
La situación hemodinámica depende exclusivamente del propio paciente y de la medicación e infusiones que se le administren.
- ECMO VV con cánula de doble lumen:
Indicado para el soporte de fallo respiratorio, con función cardiaca adecuada con o sin inótropicos. Se utiliza una cánula de doble lumen insertada vía yugular derecha, por un lumen la sangre es drenada desde la vena cava superior (VCS) e inferior (VCI), pasa por el oxigenador y es devuelta por el otro lumen a la aurícula derecha para seguir por válvula tricúspide. Da más independencia al paciente para rehabilitación y tiene un acceso central menos.
- ECMO veno-arterial (VA):
Permite soporte en fallo cardiaco severo. Sin embargo, la ECMO VA puede proporcionar soporte tanto pulmonar como cardíaco. La sangre es drenada desde la aurícula derecha vía vena yugular interna derecha, vena femoral o directamente de la aurícula derecha (central) y es retornada, a través de una cánula carotídea derecha, femoral o aórtica.
Tras la entrada en ECMO el flujo de sangre se incrementa progresivamente hasta conseguir una SaO2 > 95%, una SvO2 > 70% y una correcta perfusión distal, que a nivel analítico se traduce en un lactato normal y ausencia de acidosis metabólica. En general esto puede requerir un flujo de sangre de hasta 2,4-2,8 L/min/m2 (100-150 ml/kg/min en neonatos, 80 ml/kg/min en niños y 60 ml/kg/min en adultos).
Cuando la contractilidad miocárdica está muy afectada esto puede no ser posible, pudiéndose requerir una asistencia aún mayor.
La situación hemodinámica depende del flujo sanguíneo (el flujo de la bomba más el gasto cardíaco nativo) y las resistencias vasculares. Como la onda de pulso es menor, la presión arterial media también será menor a la habitual para la edad del paciente (40-50 mmHg para neonatos y lactantes, 50-70 mmHg para niños y adultos).
Incluso podemos constatar ausencia de onda de pulso si la contractilidad miocárdica está muy deprimida y la presión sistólica del ventrículo izquierdo (VI) es insuficiente para abrir la válvula aórtica (perdiéndose la eyección nativa). Aun en esta situación, la perfusión sistémica puede ser adecuada. Si la SvO2, es > 70% la entrega de O2 a los tejidos es suficiente, aunque la presión arterial se mantenga en el límite bajo. Es más, incrementar la poscarga puede ser contraproducente para el VI.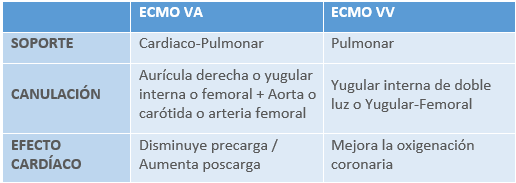
- INSERCIÓN DE CÁNULA PARA ECMO E INICIO DE SOPORTE:
Se realiza en la unidad de cuidados intensivos o en el quirófano. El paciente debe estar bajo sedoanalgesia y relajación muscular. Hay técnicas para canulación tanto veno-arterial, veno-venosa y central. Para conseguir un acceso vascular óptimo deben tenerse en cuenta las siguientes consideraciones:
- Se debe disponer de una cánula venosa que permita obtener un flujo sanguíneo adecuado. El diámetro interno de la cánula venosa limita el flujo máximo (considerando que existe una volemia adecuada), por lo que se intenta colocar la de mayor grosor posible. En ocasiones se necesita colocar una segunda cánula venosa de drenaje para adecuar el flujo. El tamaño de la cánula arterial determina la resistencia en el circuito.
- La canulación para ECMO VA puede ser central o periférica y realizada de forma quirúrgica o percutánea. La canulación central o transtorácica requiere la participación de cirujanos cardiovasculares, realizándose a través de una esternotomía. Si la ECMO se plantea a la salida de CEC o en el postoperatorio inmediato la canulación transtorácica es la óptima, colocando la cánula venosa en la aurícula derecha y la arterial en la aorta ascendente. Tiene mayor riesgo de sangrado y mediastinitis, pero permite colocar cánulas de mayor tamaño que facilitan mejores flujos.
- La canulación en pacientes pediátricos fuera del postoperatorio de cirugía cardíaca es generalmente periférica (cervical o femoral) y habitualmente la realiza el cirujano por disección. En la EMO VA la cánula venosa se inserta a través de la yugular derecha y debe llegar a la aurícula derecha, y la cánula arterial se inserta a través de la carótida en el arco aórtico. La canulación arterial, sobre todo la cervical, presenta más riesgo de accidente cerebrovascular. Los vasos cervicales se pueden reparar en el momento de la decanulación y no es necesario ligarlos. En niños mayores de 10-15 kg se pueden utilizar los vasos femorales, pero al insertar cánulas más finas y largas en ocasiones se necesitan cánulas adicionales tanto para el drenaje venoso como para la perfusión arterial distal del miembro.
- En la ECMO VV se puede utilizar una cánula de doble luz que se inserta a través de la yugular derecha, cuyos orificios de drenaje deben quedar en vena cava inferior y superior y los de retorno dirigidos hacia la válvula tricúspide, con lo que se disminuye la recirculación. Si para ECMO VV se canulan dos venas una es la yugular derecha y otra la femoral. Es preferible utilizar la cánula femoral como cánula de drenaje y la yugular interna de retorno, pero en niños menores de 10-15 kg puede que no se consiga suficiente drenaje y puede ser necesario invertir la posición, con lo que aumenta la recirculación. En niños mayores la canulación puede ser percutánea. En todos los casos es necesario comprobar la posición de las cánulas con radiografía y ecocardiografía. En el momento de retirar las cánulas es posible reconstruir los vasos, sin necesidad de ligarlos.
Una vez canulado el paciente se iniciará la asistencia hasta conseguir el soporte completo o suficiente para la estabilización del paciente. El soporte completo en general es equivalente al gasto cardiaco en ECMO VA, considerando que en situaciones de demanda metabólica elevada y/o de vasoplegia pueda requerir flujo más alto. Se determinarán las revoluciones necesarias de la bomba para el flujo requerido en condiciones de pre y post carga óptimas. Este va a depender fundamentalmente de la volemia, la resistencia dada por la cánula venosa y presión de la unidad circuito/paciente. Al iniciar la asistencia puede requerir de aporte de volumen significativo, proporcional al SIRS (Síndrome de Respuesta Inflamatoria Sistémica, por su sigla en inglés Sistemyc Inflamatory Response Syndrome) que se genera por el contacto con el circuito nuevo, mediado por citoquinas, con aumento de reactantes de fase aguda y permeabilidad capilar aumentada.
En ECMO VV los flujos de inicio son similares, pero hay que considerar que la bomba nativa (corazón) se debe hacer cargo del flujo ECMO a través de un gasto cardiaco equivalente e incluso un poco mayor al flujo del ECMO, para evitar sobrecarga derecha.
MANEJO DE LA TERAPIA ECMO RELACIONADO CON EL PACIENTE:
- Manejo ventilatorio:
Tanto en ECMO VV como en VA el paciente debe manejarse con parámetros ventilatorios de protección pulmonar, típicamente los siguientes: FR más bajas de las correspondientes a la edad del paciente, Ti largos, PEEP 5-15 cmH20, FiO2 35-40 % (para mantener oxigenación coronaria, que depende del gasto cardíaco nativo), PIP 20-25 cmH20 en modalidades de presión, Vt 2-4 ml/kg en modalidades de volumen. En pacientes en ECMO VA por patología cardíaca y con el pulmón relativamente conservado, se suelen utilizar FR algo más altas y Vt 4-6 ml/kg. Si no se consigue un intercambio gaseoso sistémico adecuado con estos parámetros (SaO2 < 95% en ECMO VA o < 85% en ECMO W, o paCO2 > 40) se debe optimizar el intercambio gaseoso a nivel del circuito.
Modalidad ventilatoria. El paciente puede ser ventilado en cualquier modalidad, ya sea de presión o de volumen. Una vez el pulmón empieza a recuperarse, se recomienda mantener al paciente lo más despierto posible y favorecer la respiración espontánea asistida con modalidades de soporte.
En pacientes en ECMO VA como soporte cardíaco y con la función pulmonar conservada, o en ECMO VV como puente a trasplante pulmonar, especialmente en adultos, puede valorarse un manejo con el paciente extubado y en ventilación espontánea.
En caso de neumotórax, si es pequeño y no tiene repercusión clínica sobre el paciente ni sobre la ECMO, deberá tomarse una conducta expectante por el alto riesgo de sangrado asociado a la colocación de un tubo de drenaje pleural. Aun así, su evolución deberá monitorizarse estrechamente y, en caso de que su tamaño aumente progresivamente o produzca compromiso hemodinámico, deberá drenarse.
Terapias coadyuvantes. Las maniobras de reclutamiento pulmonar pueden utilizarse una vez que ha pasado la fase de inflamación aguda, vigilando siempre que el aumento progresivo de la PEEP no interaccione con los flujos del circuito. También existen varias publicaciones sobre la seguridad y los beneficios de la posición en prono de pacientes en ECMO. Dado el colapso pulmonar y la estrategia ventilatoria de protección pulmonar que implica volúmenes bajos, se pueden observar acumulación de secreciones y desreclutamiento pulmonar. En general se recomienda realizar fisioterapia respiratoria a todo paciente en ECMO.
- Anticoagulación:
El anticoagulante ideal para un sistema extracorpóreo, es decir, aquel que inhiba la coagulación dentro del circuito, pero evitando sangrados en el paciente, y cuya actividad sea fácilmente monitorizado, no existe. En su defecto se continúa utilizando la heparina no fraccionada (HNF). Su efecto se monitoriza mediante el tiempo de coagulación activado (ACT), el tiempo de tromboplastina parcial activado (TTPa), los niveles de antifactor Xa y el tromboelastograma (TEG).
Cada centro con ECMO desarrolla sus propios protocolos para el manejo y monitorización de la anticoagulación basándose en la literatura publicada, los protocolos de otros centros con ECMO, las guías de la ELSO y su propia experiencia. A continuación, destacamos algunas de las recomendaciones de la ELSO.
En la mayoría de centros los pacientes reciben un bolo de HNF de 50-100 UI/kg en el momento de la canulación.
Posteriormente, cuando el ACT disminuye < 300 seg se inicia una infusión continua de HNF a 10-20 Ul/kg/h, excepto en casos de sangrado excesivo o en pacientes que acaban de tener una cirugía cardíaca, en los que se demorará el inicio de la anticoagulación. El objetivo es mantener el ACT entre 180-220 seg, excepto en pacientes con riesgo de sangrado o sangrado activo, en los que se disminuirá el ACT hasta 150-180 seg.
Si se controla el TTPa, éste debe mantenerse entre 60-80 segundos (para un nivel de anticoagulación estándar en pacientes sin sangrado). El método de referencia para la monitorización de la heparina es el antifactor Xa, cuyo rango para una correcta heparinización se sitúa entre 0,3-0,6 UI/ml.
El uso de los nuevos anticoagulantes orales (argatrobán, bivalirudina y lepirudin), inhibidores directos de la trombina, quedaría restringido a aquellos pacientes con trombopenia inducida por heparina, entidad muy poco frecuente en pediatría, en los que el uso de HNF quedaría contraindicado. Existe experiencia limitada con la administración de bivalirudina por vía parenteral en perfusión continua en situaciones de resistencia a la heparina, pero se debe utilizar con precaución por su vida media muy corta y el riesgo de producir trombosis en zonas de estancamiento de sangre.
La ECMO produce un consumo muy elevado de plaquetas. Se recomienda mantener cifras de plaquetas por encima de 80.000/mm en pacientes sin sangrado y > 100.000/mm en pacientes que sangran y en neonatos. Las indicaciones de transfusión de plasma son: hipofibrinogenemia < 150 mg/dL o INR > 1,5. Si existe solo déficit de fibrinógeno se puede administrar concentrado de este factor.
- Drogas vasoactivas:
El paciente en soporte ECMO VA estable requiere de mínimo apoyo vasoactivo. Al ser el ECMO la bomba de la unidad paciente circuito y no el corazón, no siempre requiere de apoyo inotrópico. En casos de hipertensión pulmonar o disfunción diastólica se podrá apoyar con milrinona. En caso de hipertensión arterial dispone de variedad de fármacos, en general se inicia manejo con infusión continua de un vasodilatador como Nitroprusiato de Sodio.
El paciente en soporte ECMO VV en cambio va a requerir de competencia de bomba nativa, para lo cual puede requerir de inotrópicos si esta está comprometida. Algunos protocolos recomiendan disponer de bombas de infusión de adrenalina y noradrenalina preparadas y conectadas a catéter venoso central para emergencias.
- Apoyo nutricional:
Es necesario mantener un adecuado soporte nutricional en los pacientes sometidos a ECMO, ya sea mediante nutrición enteral, o mediante nutrición parenteral en aquellos pacientes con bajo gasto cardíaco que puedan tener comprometida la perfusión intestinal.
- Antibioterapia y prevención de infecciones:
Para la canulación se recomienda, además de la técnica estéril habitual, administrar una dosis única de una cefalosponina de primera generación (como cefazolina) 30 minutos antes de la incisión quirúrgica. Hay evidencia de que la antibioterapia profiláctica para Gram positivos de la piel disminuye el riesgo de mediastinitis en pacientes con tórax abierto. Los pacientes tratados con ECMO durante más de 2 semanas, aquellos soportados por fallo cardiaco o aquellos con tórax abierto tienen mayor riesgo de desarrollar infecciones fúngicas, por lo que algunos centros administran profilaxis antifúngica en estos casos.
La ELSO no recomienda la realización de cultivos seriados del paciente y del circuito, ya que no hay suficiente evidencia científica.
- Soporte renal:
En los pacientes en ECMO es importante mantener un adecuado balance de fluidos, que en muchas ocasiones se consigue simplemente con la utilización de diuréticos. Aun así, hasta un 50% necesitan iniciar una técnica de depuración extrarrenal, ya sea a través de una vía venosa insertada ya en el paciente o, lo que resulta más habitual y más seguro en estos pacientes, conectando el aparato de hemofiltración directamente al circuito.
- Sedoanalgesia y monitorización neurológica:
El paciente en ECMO precisa de sedación y analgesia como cualquier otro paciente crítico, aunque conseguir el efecto óptimo de estos fármacos puede suponer un reto, ya que hay que tener en cuenta que el volumen de distribución está aumentado y que algunas drogas pueden ser secuestradas por los componentes poliméricos del circuito, disminuyendo su biodisponibilidad. La infradosificación de estos fármacos puede perpetuar el dolor, la agitación, la asincronía con el ventilador y conllevar la extubación o decanulación accidental. El sobretratamiento, en cambio, se asocia con prolongación de la ventilación mecánica, infecciones relacionadas con la asistencia sanitaria, delirio, aumento de la estancia hospitalaria y mayor probabilidad de aparición de síntomas de abstinencia. Los relajantes musculares se utilizan durante la canulación, pero deben evitarse posteriormente.
La monitorización neurológica se basa en la evaluación clínica periódica (evaluación pupilar, así como examen neurológico exhaustivo haciendo ventanas de sedación). En algunos centros se utiliza la oximetría tisular cerebral y el índice biespectral.
En pacientes con fontanela abierta se debe realizar ecografía transfontanelar periódicamente. En caso de aparición de focalidad neurológica se valorará realizar una TC craneal.
COMPLICACIONES:
Los pacientes sometidos a ECMO tienen riesgo de desarrollar múltiples complicaciones. Un mayor tiempo en ECMO se relaciona con una mayor probabilidad de aparición de estas complicaciones, que pueden aparecer tanto en el circuito como en el paciente. Es muy importante para minimizarlas tanto la monitorización continua del circuito y el paciente como la formación y entrenamiento del personal sanitario que atiende a estos niños. A continuación, se resumen las complicaciones más frecuentes.
- Trombosis
La formación de trombos en el circuito es la complicación mecánica más frecuente. Si son pequeños y están en la zona venosa del circuito existe poco riesgo para el paciente y el circuito. Suelen aparecer en las zonas de estasis del flujo de sangre en el oxigenador, pero si no producen alteración en su función se debe mantener la observación. También aparecen frecuentemente pequeños coágulos o acúmulo de fibrina en los tubos y conectores del circuito. Cuando aparecen se debe aumentar la anticoagulación y vigilar la aparición de hemólisis.
Cuando la aparición de trombos en el circuito causa problemas de malfuncionamiento o hemólisis o existe riesgo elevado de embolismo, se debe cambiar el circuito (en su totalidad o solo el oxigenador).
- Embolismo aéreo
No es una de las complicaciones más frecuentes reportadas en el registro de la ELSO (4%), pero si puede ser grave. Pueden aparecer desde pequeñas burbujas de aire en el lado venoso del circuito hasta una importante embolia aérea hacia el paciente. La zona de mayor riesgo de entrada de aire en el circuito es en la que existe presión negativa, desde el drenaje venoso del paciente hasta la bomba. También existe riesgo de entrada de aire cuando aparece cavitación de las cánulas venosas por hipovolemia o porque hagan pared en el vaso o aurícula. Como sistema de prevención se debe considerar la utilización de un detector de burbujas de aire que alerte y pueda opcionalmente parar la bomba. Ante la presencia significativa de aire en el circuito es necesario parar la asistencia de ECMO, determinar el origen de ese aire y, tras la resolución, reiniciar de nuevo la asistencia.
- Fallo en el oxigenador
La formación de coágulos en el oxigenador, que determinan una mala difusión de gases y hemólisis, es la causa más frecuente por la que es necesario cambiarlo. Los oxigenadores de fibra de polimetilpenteno presentan menos complicaciones que los de membrana siliconada.
- Problemas con las cánulas y decanulación accidental
Durante la canulación pueden aparecer complicaciones vasculares, como desgarro de la vena y disección de la arteria. Durante la asistencia también se pueden dar complicaciones en relación con las cánulas, como obstrucciones, determinadas por trombosis o acodamiento.
La decanulación accidental es una complicación muy grave y habitualmente prevenible. Si se produce determina hemorragia y embolismo aéreo que puede llevar a la muerte del paciente. Una vez colocadas las cánulas y confirmado su adecuado posicionamiento se deben fijar y marcar la profundidad en el sitio de inserción. En ocasiones es necesario aumentar la sedación y limitar la movilidad para prevenir el desplazamiento de las cánulas.
- Fallo de bomba
Los equipos de ECMO deben disponer de sistemas manuales para mantener la asistencia hasta el cambio de bomba.
- Alteración en el intercambiador de calor
La monitorización frecuente de la temperatura del paciente y el circuito minimizará las complicaciones producidas por malfuncionamiento o desconexión del intercambiador de calor.
- Sangrado
La hemorragia menor en ECMO es frecuente, debido a la heparinización, la disfunción plaquetaria y la activación de la fibrinólisis. Suele aparecer en la zona quirúrgica o zona de inserción de cánulas o catéteres y se controla con medidas locales, administración de hemoderivados, disminución de la dosis de heparina y revisión de la zona quirúrgica si es el caso. Si el sangrado es muy abundante o generalizado puede tener un difícil control, debiéndose valorar la administración de antifibrinolíticos y, en casos excepcionales (por el riesgo elevado de coagulación del circuito) y nunca simultáneamente, factor VII activado.
- Neurológicas
Según el registro de la ELSO el 20% de los pacientes tratados con ECMO tienen alguna forma de alteración neurológica. La hemorragia y el infarto cerebral son complicaciones mayores y determinan una importante morbimortalidad. Su frecuencia puede disminuir si se previene el tromboembolismo y el exceso de anticoagulación. Estas complicaciones pueden estar determinadas por la situación del paciente previa a la entrada en ECMO. En caso de hipotensión refractaria, hipoxemia o parada cardíaca, acelerar el inicio de la ECMO puede disminuir el riesgo neurológico.
- Hemólisis
Es una complicación frecuente, pero si es leve no determina consecuencias importantes. Si es grave se asocia a fallo multiorgánico y aumento de mortalidad. Cuando existe una hemólisis excesiva con niveles de hemoglobina libre > 50 mg/dl de forma mantenida, se recomienda cambiar el circuito de ECMO.
DESCENSO DE LA ASISTENCIA Y DECANULACIÓN:
El descenso de la asistencia en ECMO se realiza cuando existe una resolución o clara mejoría del proceso que motivó su indicación.
En el caso de ECMO VA se inicia el descenso cuando aparecen los signos de recuperación de la función ventricular. Se observa un aumento de la pulsatilidad en la onda de presión arterial y aumento del CO2 espirado. La función cardíaca se monitoriza con ecocardiografía. Se disminuye progresivamente el flujo de sangre y gas. A medida que se disminuye la asistencia en ECMO se debe optimizar el soporte ventilatorio. Al iniciar el descenso de la asistencia algunos centros indican milrinona o levosimendán, y previa a la retirada definitiva de la asistencia inician adrenalina en perfusión. Al bajar el flujo de sangre es necesario aumentar la anticoagulación por el riesgo de trombosis del circuito. Antes de la retirada definitiva de la asistencia, se debe hacer una prueba clampando (cerrando) las cánulas arterial y venosa.
Durante este tiempo se debe prestar atención a la oxigenación, frecuencia cardíaca, tensión arterial, presiones de llenado y función cardíaca medida por ecocardiografía. Las cánulas se deben lavar cada 5-10 minutos durante la prueba de retirada o el perfusionista puede colocar un puente entre ellas.
Si la prueba es favorable se puede realizar la retirada definitiva de la asistencia y decanulación.
En el caso de ECMO VV la retirada se realiza disminuyendo el flujo de gas y la FiO2 del oxigenador adecuando el soporte ventilatorio en el paciente. Si las condiciones son favorables se llega a cerrar el flujo de gas del oxigenador.
En pacientes con ECMO VA, si no es posible la retirada y la situación respiratoria lo permite, se debe valorar la instauración de asistencia ventricular de medio y/o largo plazo como puente a la recuperación o como puente al trasplante cardíaco.
PRONÓSTICO:
El registro de la ELSO recoge, hasta Julio de 2016, un total de 23.874 pacientes soportados con ECMO por causa cardiaca, de los cuales 6.475 han sido neonatos, 8.374 pacientes pediátricos y 9.025 adultos. La supervivencia al alta hospitalaria va desde el 41% en neonatos y adultos hasta el 51% en niños, todavía lejos de las cifras para ECMO respiratorias (58% de supervivencia al alta en niños y adultos, 74% en neonatos).
De entre los diferentes diagnósticos, la supervivencia parece ser mayor en general en todos los grupos de edad para las miocarditis y miocardiopatías (50-70%) frente a las cardiopatías congénitas o el paro cardíaco (30-45%). Y entre las complicaciones reportadas con mayor frecuencia se encuentran la necesidad de inotrópicos, el sangrado en la zona quirúrgica y la necesidad de hemofiltración.
2.14 DISPOSITIVOS DE ASISTENCIA VENTRICULAR (DAV) DE LARGA DURACIÓN
Los dispositivos de asistencia ventricular (DAV) actúan como una bomba, generando un flujo circulatorio (específico según el dispositivo considerado), que permite sustituir parcial o totalmente la función del corazón en situaciones de fallo cardíaco grave (agudo o crónico), que no responde a otros tratamientos. La bomba se encuentra conectada al ventrículo izquierdo mediante una cánula de entrada y otra de salida de flujo que la conecta a la aorta ascendente. Finalmente, un cable conecta la bomba a la consola externa con un microprocesador que controla el funcionamiento de la bomba y recoge información procedente de esta. La energía necesaria para el funcionamiento del sistema es suministrada bien a través de dos baterías, o con una batería y corriente eléctrica. El almacenamiento de datos del sistema y el ajuste de parámetros de la consola externa se realiza a través un ordenador de pantalla táctil provisto de un software específico. Los DAV han experimentado un rápido desarrollo desde su aparición y han mejorado su seguridad, aumentando su durabilidad y reducido su tamaño.
El tipo de soporte que pueden proporcionar dichos dispositivos, bien sea univentricular o biventricular, el cual está determinado fundamentalmente por el tipo de canulación realizada, o dicho de otro modo, por cuáles son los vasos (o cámaras cardíacas) a los cuales se conecta el dispositivo. Así, para proporcionar asistencia ventricular izquierda (DAVI) la bomba de sangre a emplear se conecta por un lado a la aurícula izquierda (Al) o al ventrículo izquierdo (VI) y por otro a la aorta. Para proporcionar, en cambio, asistencia ventricular derecha (DAVD) se conecta el dispositivo a la aurícula derecha (AD) y a la arteria pulmonar (AP). Para proporcionar asistencia biventricular (DAVB) se combinan en el mismo paciente dos dispositivos, uno para asistencia derecha y otro para asistencia izquierda con las conexiones ya mencionadas. Finalmente, existe un tipo especial de asistencia biventricular, el llamado corazón artificial total (CAT), cuya singularidad consiste en que para su implante se recurre a la extirpación del corazón nativo, siendo este sustituido por el CAT.
El soporte con DAV se plantea fundamentalmente como un soporte a largo plazo. La modalidad más empleada en el soporte de larga duración es el DAVI (81%), seguida del DAVB (15%), siendo el DAVD (2%) y el CAT (3%) unas indicaciones excepcionales.
En los años 80 se desarrolló la primera generación de DAV para adultos que se encuentran ampliamente implementados en la práctica clínica diaria. Sin embargo, la introducción de estos dispositivos en pacientes en edad pediátrica ha sido más paulatina debido a limitaciones técnicas en la adaptación de los dispositivos existentes, la complejidad anatómica de las CC y limitaciones reguladoras en la evaluación del dispositivo en una población pequeña y heterogénea. Actualmente, existen diversos DAV que se emplean en población pediátrica. Sin embargo, la literatura se refiere con mayor frecuencia a los dispositivos de soporte temporal como puente a la recuperación o trasplante y en raras ocasiones a la indicación de terapia de destino.
CLASIFICACIÓN:
Existen diversos tipos de dispositivos según sus características.
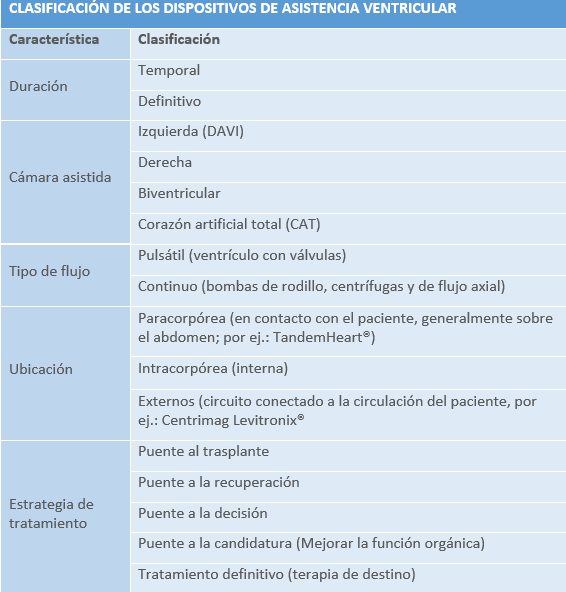
En edad pediátrica, los DAV pulsátiles son empleados en soporte izquierdo, derecho y biventricular. Entre estos dispositivos destacan, el DAV paracorpóreo Berlin Heart EXCOR® (Berlin Heart, Inc.), referenciado en la literatura con mayor frecuencia, y el dispositivo paracorpóreo e implantable Thoratec VAD (Thoratec Corporation).
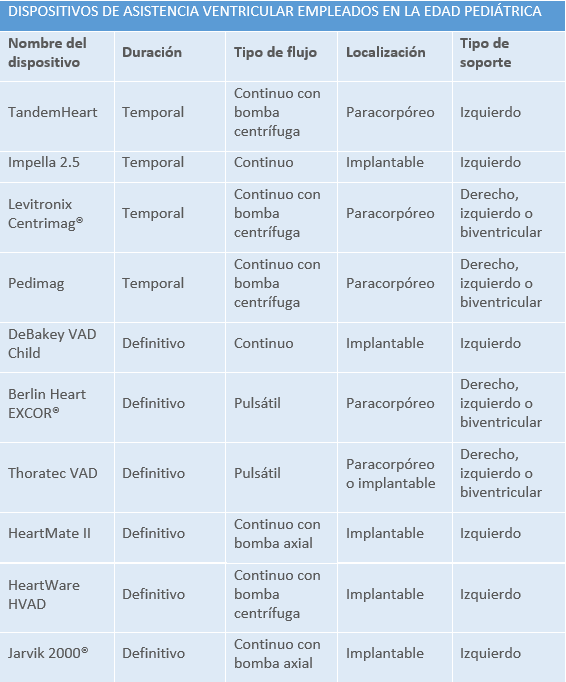
DISPOSITIVO DE FLUJO PULSÁTIL DE LARGA DURACIÓN:
El dispositivo EXCOR® de Berlin Heart es una bomba neumática de colocación paracorpórea capaz de bombear la práctica totalidad del gasto cardíaco. Puede proporcionar soporte univentricular o biventricular en función de si se colocan una o dos bombas neumáticas. Es un dispositivo de empleo a medio-largo plazo, de localización paracorpórea, que proporciona un flujo pulsátil y apto para cualquier tamaño/edad del paciente.
La selección del tamaño de la bomba neumática (10, 15, 25, 30, 50 o 60 ml) depende del tamaño del paciente. Para determinar el tamaño del ventrículo o ventrículos a implantar es preciso determinar primero el flujo sanguíneo que será necesario proporcionar (2,2 a 3 L/min/m2) para después calcular qué tamaño de ventrículo puede proporcionar
dicho flujo con una frecuencia entre 70-80 latidos por minuto.

Ilustración 17. Fuente: EXCOR Pediátrico. Berlin Heart. 2018.
La colocación de las cánulas y bombas, así como su puesta en funcionamiento se realiza en quirófano, dado que el procedimiento se realiza a través de una esternotomía media bajo circulación extracorpórea (CEC).
La terapia antitrombótica requiere de un cuidado muy minucioso y una adaptación individual a cada paciente en particular. Existen variaciones del manejo antitrombótico entre los distintos centros en lo que se refiere tanto a la duración de cada una de las fases (heparina sódica vs enoxaparina/anticoagulantes orales) como a los instrumentos de monitorización empleados (TTPa, actividad anti-Xa, tromboelastograma, agregometría). Ninguna técnica de monitorización es perfecta, siendo la monitorización multimodal probablemente la más indicada. Por otro lado, tan importante o más que la monitorización bioquímica/biológica es la monitorización clínica del estado del dispositivo (mediante inspección varias veces al día) y la integración de los hallazgos observados con los resultados del laboratorio, la terapia en curso y la situación clínica del paciente. Es preciso destacar el gran impacto que tiene la aparición de cualquier estado proinflamatorio en el equilibrio del sistema hemostático, desequilibrando la balanza hacia un estado protrombótico que en ocasiones puede ser incontrolable mediante la medicación anticoagulante/antiagregante. Por ello, cualquier causa de inflamación, infecciosa o no infecciosa debe ser abordada con agresividad, dadas las graves consecuencias que pueden tener los fenómenos tromboembólicos, que son la principal causa de morbimortalidad una vez superada la fase postoperatoria inicial.
En España, según el informe del Registro ESPAMACS (Registro Nacional Español de Asistencia Mecánica Circulatoria, octubre 2014-mayo 2016) realizado en 18 centros, se implantaron 3 DAV de larga duración (Berlin Heart EXCOR®) como puente a trasplante en población pediátrica (6 %) durante este período (2 de ellos menores de 2 años). En el último registro ESPAMACS publicado, correspondiente al periodo comprendido entre el 1 enero del 2017 y el 31 de diciembre de 2018 no se registraron los DAV empleados en población pediátrica. Según la Organización Nacional de Trasplantes (ONT), durante el 2019 se incluyeron en urgencia 0 para trasplante cardíaco por presentar asistencia ventricular (incluyendo ECMO) a 19 pacientes.
SUPERVIVENCIA:
El empleo de DAV de larga duración se indica fundamentalmente como puente al trasplante (64% de pacientes entran en lista de trasplante en el momento del implante y un 29% reciben soporte con DAV con la intención de ser evaluados y eventualmente colocados en lista de trasplante), la indicación de terapia de destino es infrecuente (7%). La supervivencia a los 6 meses del implante se sitúa actualmente en el 81% y ha supuesto una reducción de la mortalidad en lista de trasplante cardíaco superior al 50%.
ASPECTOS ÉTICOS, SOCIALES O LEGALES:
Un estudio que analiza los aspectos éticos-legales derivados de la desactivación de los DAVI con indicación de terapia de destino en población pediátrica a través de una revisión narrativa de la literatura, y recogió la perspectiva de los clínicos sobre la desactivación del soporte ventricular en este tipo de población. Algunos autores no consideran la desactivación del dispositivo como una forma de eutanasia ya que el fallecimiento del paciente sobreviene como consecuencia de la progresión natural de la enfermedad. Mientras que otros tienen la opinión contraria, considerando que este procedimiento sólo debe ofrecerse a pacientes en una situación cercana a la muerte. Los autores de la revisión concluyen en la necesidad de elaborar documentos en los que se recojan los aspectos éticos, sociales y legales de la desactivación de DAVI en población pediátrica desde el punto de vista de todos los agentes implicados, es decir, clínicos, familiares/cuidadores, en los que se incluyan, además, planes de actuación para guiar todo el proceso.

Ilustración 18. Fuente: Menon A. EXCOR® Active. Berlin Heart. Wirtchaftsforum. 2023.
2.15 TRASPLANTE CARDIACO
El trasplante cardíaco supone una alternativa terapéutica eficaz para el tratamiento de pacientes con insuficiencia cardíaca terminal. En los últimos años, la mejora en las técnicas quirúrgicas, terapias inmunosupresoras y profilaxis infecciosa han logrado un importante incremento en la supervivencia de los pacientes.
Cada año aumenta el número de pacientes pediátricos en lista de trasplante cardiaco. En España, según datos de la Organización Nacional de Trasplantes, durante el año 2010 estuvieron en lista de espera de trasplante cardiaco 399 pacientes, de los cuales 31 (7,8%) fueron pacientes pediátricos. La mortalidad de los adultos en lista de espera fue del 3,8%, la más baja desde el año 1993. En cambio, la mortalidad de los niños en lista de espera fue del 9,3%, una mortalidad inferior a la de países como Estados Unidos (19%) pero lejos de las cifras del adulto y, lo que es más importante, una cifra que apenas se ha modificado en los últimos años. En cuanto al trasplante cardiaco urgente se refiere (pacientes en lista de trasplante con dispositivos de asistencia ventricular [DAV] o pacientes en shock cardiogénico que requieren fármacos vasoactivos o ventilación mecánica), el tiempo en lista para los pacientes infantiles fue superior al de los adultos. Más del 50% de los casos infantiles estuvieron en lista urgente más de 20 días mientras que el 87% de los adultos recibieron el trasplante en menos de 10 días. Así pues, el mayor tiempo de espera y la mayor mortalidad de los pacientes pediátricos en lista de trasplante cardiaco pone de manifiesto la necesidad de mejorar en el campo de la asistencia ventricular pediátrica.
INDICACIONES:
La indicación para el trasplante cardíaco en la infancia es la insuficiencia cardíaca terminal de cualquier origen y en la que no existe ninguna opción terapéutica posible.
La escasez de donantes de la edad pediátrica junto con la necesidad de idoneidad de peso donante-receptor, determina estancias prolongadas en lista de espera y con ello un manejo pretrasplante complejo en unidades especializadas con alta necesidad de dispositivos de asistencia ventricular.
CONTRAINDICACIONES:
Las contraindicaciones absolutas para el trasplante son: hipoplasia de arteria o venas pulmonares e hipertensión pulmonar irreversible.
Se consideran contraindicaciones relativas las alteraciones genéticas, cromosómicas o malformaciones que limiten la supervivencia o los beneficios potenciales del trasplante, sepsis activa, fallo multiorgánico y evaluación neurológica con mal pronóstico. Las causas de exclusión del receptor son cada vez más revisadas y deben individualizarse en cada caso.
SELECCIÓN DEL DONANTE:
La correcta selección del donante condiciona el éxito del trasplante en gran medida. La elección del donante viene condicionada por el peso del mismo y del receptor, aceptándose un tamaño de hasta 3 veces el peso del receptor. El tiempo estimado de isquemia del órgano debe ser tenido en cuenta en función de las condiciones en las que esté esperando el receptor. Tiempos mayores de 4 horas se asocian con peor pronóstico.
Se elige un donante del mismo grupo sanguíneo que el receptor, si bien, ante la escasez de donantes en menores de 1 año, en los que la inmadurez de su sistema inmunológico determina una mejor tolerancia del injerto, se están realizando trasplantes ABO incompatibles con resultados óptimos en el seguimiento a medio plazo.
CARACTERÍSTICAS DEL CORAZÓN TRASPLANTADO
El corazón trasplantado presenta unos problemas específicos que precisan de la adecuación de los cuidados postoperatorios.
Los principales son la denervación, la isquemia y el aumento en la poscarga del ventrículo derecho.
- Denervación:
La respuesta del corazón trasplantado está alterada:
- No responde con taquicardia cuando se produce hipotensión por hipovolemia, vasodilatación o disminución de la contractilidad, por pérdida del reflejo barorreceptor.
- No responde con aumento de la frecuencia cardíaca y contractilidad ante el dolor o la ansiedad. La frecuencia cardíaca aumentará solamente cuando se incrementen las catecolaminas circulantes.
- Solamente responde a fármacos vasoactivos que tienen acción directa sobre el corazón, como la adrenalina, el isoproterenol y la dobutamina. Los receptores alfa y beta están intactos.
- La respuesta a betabloqueantes es igual que la del corazón inervado.
- No responde a fármacos que actúan a través del sistema nervioso parasimpático, como la atropina.
- Los vasodilatadores arteriales tienen más efecto porque no se produce taquicardia refleja.
- Isquemia:
El corazón trasplantado sufre una isquemia generalizada a pesar de una técnica óptima de preservación miocárdica. Dicha isquemia causa un descenso de la complianza diastólica y de la contractilidad de ambos ventrículos por lo que en el postoperatorio inmediato se van a necesitar presiones de llenado altas y perfusión de fármacos inotrópicos y cronotrópicos.
- Poscarga del ventrículo derecho:
El ventrículo derecho del donante es el que más sufre, presenta mayor disfunción tras la isquemia y va a padecer una poscarga elevada por el árbol vascular pulmonar del receptor. El volumen latido de ese ventrículo derecho normal (no hipertrofiado) desciende de forma significativa con pequeños aumentos de la poscarga. La eyección del ventrículo derecho reducida disminuye la precarga del ventrículo izquierdo, reduciendo el gasto cardíaco y el flujo sanguíneo pulmonar; por lo que las medidas terapéuticas para disminuir la poscarga del ventrículo derecho son cruciales en el postoperatorio inmediato.
CUIDADOS POSTOPERATORIOS:
- Hemodinámico:
Los cuidados del postoperatorio inmediato sólo varían ligeramente de los de otras cirugías cardíacas con circulación extracorpórea. El principal objetivo del manejo hemodinámico es mantener un adecuado gasto cardíaco a pesar del tiempo de isquemia sufrido por el corazón y de su denervación.
Para cumplir el objetivo de mantener un adecuado gasto cardíaco en estas condiciones debemos:
Mantener una buena precarga: favorece la distensibilidad y disminuye la necesidad de fármacos inotrópicos.
Mantener una FC en el límite alto de lo normal para la edad del niño y en ritmo sinusal. En algunas ocasiones puede ser preciso el empleo de marcapasos en cuando hay disfunción sinusal o bloqueo AV. Para asegurar el cronotropismo del corazón denervado se suele emplear una infusión continua de isoproterenol 0.01-1 mcg/kg/min; que se mantiene durante los primeros 3-5 días.
Favorecer una adecuada contractilidad con fármacos inotrópicos: dopamina, dobutamina o adrenalina. El levosimendán, sensibilizante del calcio, se emplea como inotrópico por sus ventajas como vasodilatador coronario y sobre la función diastólica.
Disminuir la poscarga de ambos ventrículos: milrinona beneficiosa por su efecto inotrópico y vasodilatador pulmonar y sistémico. Vasodilatadores pulmonares selectivos como óxido nítrico inhalado a 10-20 ppm, así como sildenafilo y bosentán en el caso de que sean necesarios por hipertensión pulmonar.
En caso de fracaso ventricular grave pueden utilizarse dispositivos de asistencia ventricular o ECMO.
- Respiratorio:
La ventilación mecánica debe ser poco agresiva con PIP y PEEP bajas para disminuir la presión media de la vía aérea (y con ello proteger el VD). La extubación debe realizarse tras asegurar la estabilidad hemodinámica. Son complicaciones frecuentes las atelectasias, broncoespasmo y la parálisis diafragmática.
- Renal:
La insuficiencia renal es un problema frecuente en los niños trasplantados. Algunos pacientes la presentan desde antes de la intervención por bajo gasto y posteriormente se puede ver agravada por los inhibidores de la calcineurina, en especial el tacrolimus. Ante disfunción renal grave y oligoanuria se deben instaurar técnicas de depuración extrarrenal, preferiblemente hemodiafiltración venovenosa continua.
- Neurológico:
Una sedoanalgesia adecuada es fundamental en estos pacientes para minimizar el consumo miocárdico. Si la inestabilidad hemodinámica es importante, se puede considerar la relajación neuromuscular con monitorización estricta de la sedoanalgesia.
INMUNOSUPRESIÓN:
El tratamiento inmunosupresor es fundamental en estos pacientes para evitar el rechazo. El período de mayor riesgo es el primer año y en especial la primera semana postrasplante.
Existen múltiples protocolos de inmunosupresión. Lo difícil en ellos es llegar al equilibrio entre la ausencia de rechazo y la aparición de efectos adversos.
Como regla general se emplea una triple terapia durante los primeros 3-6 meses postrasplante (inhibidor de la calcineurina + antiproliferativo + corticoides) y posteriormente se suspenden los corticoides manteniendo biterapia.
- Terapia de inducción
Su uso es electivo y las últimas publicaciones no lo relacionan con una menor incidencia de rechazo, pero sí permite la introducción posterior y más lenta de los inhibidores de la calcineurina, siendo interesante en pacientes con insuficiencia renal o alteraciones neurológicas. La terapia de inducción recomendada son los anticuerpos anti-CD25, el basiliximab, que se administra a 12 mg/m2/día (máximo 20 mg) los días 0 y +4 postrasplante.
En pacientes de alto riesgo inmunológico (sensibilizado, politransfundido, en asistencia, etc.) la timoglobulina es el fármaco de elección. Se administra 1,5 mg/kg/día intravenosa durante 5 días con el objetivo de mantener los linfocitos en cifras de 200-500/mm3.
- Terapia de mantenimiento
- Inhibidores de la calcineurina
Tacrolimus: es el más usado en la actualidad (58% de los pacientes trasplantados en la edad pediátrica) debido a los efectos estéticos secundarios de la ciclosporina (hirsutismo, hiperplasia gingival). Se relaciona, como el resto de inmunosupresores, con la aparición de tumores e infecciones oportunistas. Entre sus efectos adversos destaca la insuficiencia renal y la diabetes.
Se debe iniciar entre los 3-5 días postrasplante de forma oral o por sonda nasogástrica a una dosis de 0,1 mg/kg/día dividido cada 12 horas, siempre que existan ruidos intestinales. En caso de que la administración oral no sea posible se puede administrar de forma intravenosa en infusión continua a 0,025 mg/kg/día.
La dosis se va modificando en función de los niveles valle del fármaco. El objetivo durante el primer mes es mantener niveles entre 10-12 ng/ml; en los siguientes 5 meses entre 8-10 ng/ml y posteriormente entre 5-10 ng/ml.
Ciclosporina: actualmente se reserva para pacientes que no pueden utilizar tacrolimus (por ejemplo, en gastropatías eosinofílicas o trastornos neurológicos), pero su efectividad frente al rechazo es igual que la del tacrolimus.
La dosis inicial a administrar es de 5-10 mg/kg/día cada 12 horas con una dosis de mantenimiento posterior de 2-6 mg/ kg/día. Si la vía oral no puede utilizarse se puede administrar en forma de infusión intravenosa continua. La dosis se modifica para alcanzar niveles objetivo en sangre entre 200-300 ng/ml durante los primeros 3-6 meses; posteriormente se consideran óptimos niveles entre 80-120 ng/ml.
- Antiproliferativos:
Micofenolato de mofetilo: es el fármaco más empleado en combinación con el tacrolimus. La dosis recomendada es 600 mg/m2 (20-40 mg/kg) cada 12 horas vía oral o intravenosa comenzando con una dosis previa al inicio de la cirugía. Aunque se pueden medir niveles del fármaco no son muy fiables. Sus efectos adversos más frecuentes son diarrea, leucopenia y neutropenia. Si leucocitos < 4.000/ mm3 se debe reducir la dosis o suspender si neutropenia < 1.500/mm3.
Azatioprina: queda relegado a aquellos niños que no toleran el micofenolato. Sus efectos adversos más importantes son: mielosupresión, pancreatitis, hepatotoxicidad y vómitos. Dosis: 1-3 mg/kg/día vía oral.
Sirolimus: ha demostrado efecto protector contra el desarrollo de enfermedad vascular del injerto y es una alternativa al tacrolimus en los casos de insuficiencia renal severa. Sus efectos adversos son anemia, leucopenia, trombocitopenia, hipertensión, hiperlipidemia, artralgias, edemas y úlceras orales. Dosis: 1 mg/m2 una vez al día para obtener niveles entre 4-8 ng/ml.
- Corticoides:
Las pautas empleadas son variables. Su administración se inicia intraoperatoriamente en la fase de inducción a 10 mg/kg en el momento de la esternotomía y 10 mg/kg en el desclampaje aórtico. En el postoperatorio inmediato se administra 1 mg/kg cada 6 horas el día +1, y se continúa con 1 mg/kg/día en una sola dosis desde el día +2. Posteriormente se disminuye la dosis hasta su retirada a los 3-6 meses, si no existe rechazo.
RECHAZO:
El rechazo agudo sigue siendo un importante problema clínico en los niños trasplantados, aunque su incidencia y mortalidad ha disminuido en los últimos años debido principalmente al mejor manejo del tratamiento inmunosupresor.
Su incidencia es mayor durante el primer año postrasplante, especialmente en los 3 primeros meses; la incidencia actual de rechazo agudo durante el primer año es de 16%. Los episodios de rechazo agudo más allá del primer año (rechazo tardío) ensombrecen el pronóstico a largo plazo.
- Rechazo celular agudo
Este tipo de rechazo consiste en una respuesta inmunológica mediada por células T contra el injerto.
La clínica del rechazo al inicio es muy inespecífica: fiebre, vómitos, diarrea, anorexia, irritabilidad, posteriormente pueden aparecer signos de disfunción diastólica (disnea, edemas, etc.) e incluso signos de bajo gasto asociado a disfunción sistólica. Asimismo, la inflamación miocárdica puede manifestarse con voltajes bajos en el ECG, o actuar como desencadenante de taquiarritmias auriculares, ventriculares, bradiarritmias y bloqueo AV. En la ecocardiografía se puede objetivar edema de la pared miocárdica, disfunción diastólica, derrame pericárdico de nueva aparición, insuficiencia de las válvulas auriculoventriculares, dilatación del VI y finalmente, disfunción sistólica.
El gold standard de los métodos diagnósticos para detectar rechazo agudo, al igual que en los adultos, es la biopsia endomiocárdica. La mayoría de los rechazos se diagnostican en pacientes asintomáticos en las biopsias de seguimiento, sin embargo, se trata de una técnica invasiva, y en los receptores menores de 1 año (< 10 kg) existe mayor riesgo de complicaciones.
Ante la sospecha de rechazo agudo, se debe iniciar tratamiento, aun cuando no se disponga de la posibilidad de realización de biopsia endomiocárdica. El tratamiento depende del grado de rechazo. La presencia de rechazo no hace necesario el cambio en la terapia inmunosupresora de mantenimiento del paciente.
- Rechazo humoral mediado por anticuerpos
Es un rechazo menos frecuente. Se trata de un proceso inflamatorio dependiente de células B, que producen anticuerpos dirigidos contra el endotelio vascular del injerto, lo que condiciona disfunción y vasculopatía del injerto.
Su aparición es más frecuente durante el primer mes postrasplante; y puede ser muy precoz, incluso en la primera semana si el receptor estaba sensibilizado; pero también puede presentarse de forma tardía meses o años tras el trasplante.
Debe sospecharse cuando exista disfunción del injerto con biopsia que no presente rechazo celular pero también, ante cambios sutiles de la ecocardiografía como edema o hipertrofia de pared. El diagnóstico se realiza por la sospecha clínica, la medición de anticuerpos en sangre y los cambios histopatológicos e inmunohistoquímicos en la biopsia.
- Rechazo crónico o enfermedad vascular del injerto
La alteración principal es una obstrucción progresiva de los vasos coronarios. El tratamiento es sintomático donde se debe valorar el retrasplante, la revascularización coronaria con stent y el cambio de inmunosupresión a everolimus asociado a inhibidores de la calcineuria.
INFECCIÓN:
El mayor riesgo de infección ocurre en el primer mes postrasplante debido a infecciones relacionadas con la asistencia sanitaria y con la cirugía (neumonía, mediastinitis o infección relacionada con el catéter). Pasado ese tiempo, durante los siguientes 6 meses del trasplante las infecciones oportunistas (citomegalovirus, Pneumocystis jirovecii y candidiasis) pueden aparecer, al igual que en pacientes imunodeprimidos.
La infección por citomegalovirus (CMV) es la infección viral más frecuente, siendo de mayor riesgo los niños receptores con serología de CMV negativa que reciben un órgano de donante CMV positivo.
El tratamiento como profilaxis habitual es: Trimetoprim-sulfametoxazol, Ganciclovir, Valganciclovir o Inmunoglobulina anti-CMV y Nistatina.
2.16 REHABILITACIÓN CARDÍACA
La guía de la Sociedad Interamericana de Cardiología (SIAC) de 2024 sobre rehabilitación cardiorrespiratoria (RCR) en pacientes pediátricos con cardiopatías congénitas tiene como objetivo reunir y evaluar toda la evidencia relevante actualmente disponible con la finalidad de unificar criterios y alentar la implementación de programas de RCR para esta población en Latinoamérica y otras partes del mundo.
La actividad física en la infancia es crucial para un adecuado desarrollo social, intelectual y físico y prevenir enfermedades crónicas no transmisibles como obesidad, hipertensión arterial, hipercolesterolemia, resistencia a la insulina, síndrome metabólico y enfermedades cardiovasculares.
Según las actuales recomendaciones de la Organización Mundial de la Salud, la población pediátrica debe realizar actividad física de intensidad moderada a vigorosa 60 minutos al día todos los días y ejercicios de fuerza 3 veces por semana para lograr cambios metabólicos significativos.
La mayoría de los niños con CC presentan una capacidad funcional (CF) disminuida con mayor riesgo de morbimortalidad a mediano plazo, atribuible a causas centrales (menor gasto cardiaco por disfunción miocárdica o incompetencia cronotrópica) y periféricas (afección del músculo esquelético, inadecuada perfusión tisular…)
PROGRAMAS DE REHABILITACIÓN CARDIORRESPIRATORIA Y MUSCULAR
Se requiere un equipo multidisciplinar. Se compone de varias etapas:

La población objetivo consiste en quienes cumplan los criterios de inclusión y exclusión, que serán evaluados por el equipo de rehabilitación para iniciar los programas de rehabilitación cardiorrespiratoria (PRCR).
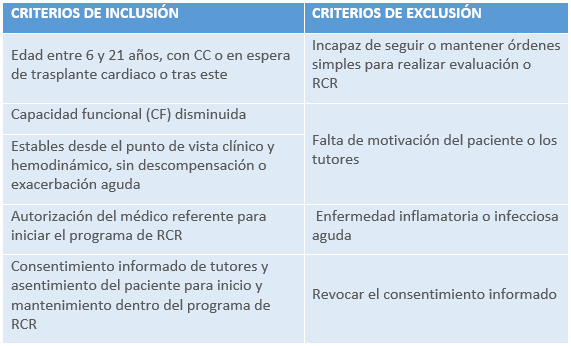
FASES DE LA IMPLEMENTACIÓN DE PROGRAMAS DE REHABILITACIÓN CARDIORRESPIRATORIA EN NIÑOS Y ADOLESCENTES
Los PRCR se basan en 3 pasos: realizar una adecuada evaluación inicial para una estratificación de riesgo, establecer límites de seguridad, minimizar efectos adversos y cuantificar el impacto positivo del programa finalizado.
- Paso 1
Anamnesis completa: cardiopatía subyacente, tipo de intervenciones quirúrgicas y cateterismos, comorbilidades no cardiacas, medicamentos, síntomas y signos gatillados por ejercicio físico.
- Paso 2
Se deben realizar pruebas complementarias para la estratificación del riesgo:
- ECG en reposo y Holter de arritmias de 24 h.
- Ecocardiograma transtorácico.
- Prueba de los 6 minutos de marcha.
- Prueba de esfuerzo convencional o prueba de esfuerzo con análisis de gases o cardiopulmonar (PECP).
Se debe realizar una estratificación del riesgo (bajo, moderado o alto), ubicar al paciente en uno de los 3 niveles de intensidad de entrenamiento y, posteriormente, incorporarlo al PRCR.
Actualmente se realizan programas híbridos: primero entrenamiento y capacitación del paciente y tutores en el hospital, para luego continuar con actividades en casa, lo cual logra aceptación, adherencia y buenos resultados. Los pacientes con riesgo alto deben realizar su RCR hospitalaria totalmente monitorizada por el riesgo que conlleva y solo aquellos en riesgo de bajo a moderado pueden terminar su RCR domiciliaria.
- Paso 3
Al inicio se mantendrá una reunión con el paciente y tutores para explicar el esquema de evaluación y entrenamiento. Se firmará un consentimiento informado explicando posibles efectos adversos durante la RCR. Debe existir un registro de las actividades planificadas para el seguimiento y modificación.
Programación de la actividad física
Se recomienda utilizar el acrónimo FITT (frecuencia, intensidad, tiempo y tipo de ejercicio físico) para la prescripción del ejercicio.
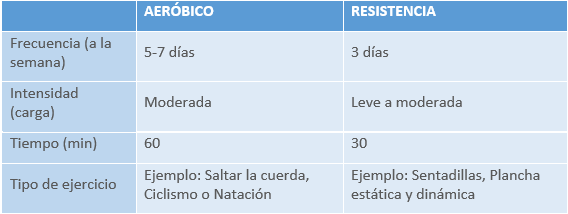
- Paso 4
Realizar periódicamente (cada semana o cada mes) una revaluación del tipo de entrenamiento, la técnica y la carga de trabajo para ajustar según las modificaciones.
Al finalizar el PRCR, se realiza un seguimiento para evaluar que los beneficios alcanzados al alta se mantienen. Se sugiere controlar a los 3, 6 y 12 meses desde el alta.
REHABILITACIÓN DOMICILIARIA Y TELERREHABILITACIÓN
Esta debe realizarse con supervisión presencial de un familiar y con un profesional al cargo a distancia. Sin embargo, solo las personas con una estratificación del riesgo bajan o moderada podrán realizar esta modalidad. La evaluación y la prescripción individual inicial deben ser presenciales para enseñar la correcta técnica del ejercicio y los signos y síntomas de alarma, y luego puede ser a distancia.
El número de sesiones semanales, su duración y la del programa, así como el intervalo entre evaluaciones, son similares a los de la RCR ya descrita. Se mantiene el acrónimo FITT para ejercicios aeróbicos y de resistencia. Los ejercicios pueden realizarse en cinta, en bicicleta, mediante actividades lúdicas que utilicen el propio peso corporal o materiales domésticos para peso extra.
- Papel del fisioterapeuta
El fisioterapeuta debe estar presente durante todas las fases del PRCR. Se inicia en el posoperatorio inmediato para el destete de la ventilación mecánica, la fisioterapia respiratoria, la movilización precoz y el ejercicio físico ligero, según las condiciones clínicas y hemodinámicas del paciente. El objetivo es prevenir complicaciones respiratorias y tromboembólicas, disminuir los días de ventilación mecánica y de estadía en la unidad de cuidados intensivos y hospitalización, conseguir el alta en las mejores condiciones físicas y promover la educación para el inicio precoz de la RCR.
- Papel del psicólogo
Una comunicación eficaz con el personal de salud es una pieza fundamental en los PRCR, así como un abordaje y tratamiento de la salud mental que fomente la aceptación y el compromiso del paciente y su familia, motivando los comportamientos saludables.
CONCLUSIÓN:
La RCR en niños y adolescentes con CC es una herramienta aún desconocida, infrautilizada pero absolutamente indispensable para que tanto ellos como su familia expresen su máximo potencial en todas las diferentes áreas del individuo y mejorar la integración a la escuela, la universidad y la sociedad en general.
2.17 ASPECTOS PSICOLÓGICOS DEL NIÑO CON CARDIOPATÍA CONGÉNITA
Hablar de los aspectos emocionales de los niños con cardiopatía congénita es un tema realmente amplio y variado: algunos de estos niños son completamente asintomáticos, otros tienen limitaciones graves; algunos requieren múltiples cirugías, otros nunca las necesitarán; algunos exigen de una atención médica constante, otros sólo cierta observación y consultas anuales de control; algunos requieren muchos medicamentos, otros sólo alguno o ninguno; en algunos su enfermedad es evidente físicamente, en otros nadie supondría que tienen un defecto cardíaco.
Sin embargo, por muy variadas que puedan ser las manifestaciones de la enfermedad, existen temores universales y características emocionales en estos niños y sus familias. Asimismo, la reacción emocional del niño a su enfermedad dependerá en mayor medida de su nivel de angustia, de la angustia de sus padres, de su propia historia y su personalidad, que del diagnóstico.
El significado del corazón es de todos conocido: el corazón es el motor de la vida, el ritmo de la salud, ¿cuántos padres no se han emocionado al escuchar el latido del corazón de su bebé en su primer ultrasonido? Así es como, por medio del corazón, el bebé se ha vuelto real, su latido es la señal de su presencia viva.
Con los adelantos médicos y tecnológicos, los niños con cardiopatía congénita tienen hoy, más que nunca, una expectativa de vida y salud mucho mayor a la que tenían hace algunas décadas. Pero la "reparación" de su enfermedad no es siempre el fin de del libro, no sólo por las lógicas preocupaciones que tendrá el adulto con cardiopatía congénita, sino porque lo que en el quirófano puede solucionarse en unas horas, no queda totalmente resuelto en la vida emocional, ni esto ocurre con la misma rapidez.
EL NIÑO CON CARDIOPATÍA CONGÉNITA:
La enfermedad es un episodio habitual en la vida de todos los niños. Los episodios agudos permiten a los niños experimentar la regresión a la dependencia y después recuperar su salud y su vida anterior. Los niños con enfermedades crónicas y congénitas, sin embargo, han nacido ya con un padecimiento y requerirán de mucho tiempo para poder resolverlo, es decir, hay que aprender a vivir con ello. El desarrollo del concepto de sí mismos estará relacionado a su enfermedad y su vida cotidiana también. Su familia tendrá que aprender a vivir con ello y desplegar todas sus capacidades y habilidades para contender con la enfermedad y poder ayudar al niño.
La adaptación a la enfermedad no puede predecirse de manera lineal y existen variaciones significativas con respecto al nivel de adaptación que cada niño puede lograr. La adaptación debe comprenderse en términos de asumir que cada niño tendrá una respuesta individual y única basada en su particular concepción del mundo y cada niño parte de este modelo mental para predecir su vida y adaptarse a lo que ocurre en ella. Es debido a esta gran variabilidad que la enfermedad crónica tiene diferentes efectos en diferentes personas, y es por ello de vital importancia el conocer a cada niño y su familia, no sólo para cuantificar el impacto de la enfermedad en ellos, sino para facilitar la creación de intervenciones terapéuticas efectivas.
CONSTRUCCIONES ACERCA DEL TRATAMIENTO:
El concepto que se tiene del tratamiento depende de la comprensión de la naturaleza de la enfermedad; si es necesario o adecuado llevarlo a cabo dependerá de que se haya entendido de forma íntegra el diagnóstico. Depende también de la manera en la que el tratamiento afecta al niño. El tratamiento puede ser visto entonces como algo necesario, adecuado o como algo erróneo y agresivo.
Por lo general, los niños nos enseñan una lección de vida y fortaleza ante las circunstancias adversas; sin embargo, la enfermedad y hospitalización pueden dejar secuelas emocionales que hay que identificar para poder manejarlas.
LA FAMILIA:
Los niños son parte de un núcleo familiar y es imposible evaluarlos y tratarlos separados de éste. Bien decía Winnicott que no hay niño sin su madre; pues esto es equiparable a decir que no hay niño sin su familia.
El proceso de adaptación del niño a su enfermedad va en paralelo al proceso de adaptación de su familia a ella. Una relación familiar armoniosa con capacidad de comunicación y oportunidad de expresar los sentimientos son factores que fortalecen y protegen a los niños; en cambio, los conflictos familiares, particularmente entre los padres, son uno de los predictores más efectivos de problemas emocionales en los niños, ya sean o no enfermos.
Independientemente del número de dificultades emocionales o prácticas que tienen que resolver, algunas de estas familias logran llevar a cabo su vida muy cerca de la normalidad y evaluar de manera realista los efectos que la enfermedad tiene sobre su hijo; otras familias, en cambio, se verán rebasadas por la situación y la enfermedad se convierte en una especie de autoridad que rige todas las actividades de la familia, casi siempre limitándolas.
El nacimiento de un niño enfermo obliga a los padres a renunciar a muchas de sus ilusiones y a elaborar la pérdida del bebé que esperaban para poder aceptar al bebé que recibieron. El futuro del niño y su bienestar se convierte en la principal preocupación de los padres. El nacimiento de un niño enfermo provoca en los padres una revolución psicológica ante la incongruencia entre las expectativas y la realidad y la materialización del peor de sus temores. Buscarán la causa de lo ocurrido y se sentirán culpables de ello preguntándose qué habrán hecho para causar la enfermedad. En parejas con conflictos previos, el culparse el uno al otro mermará aún más la relación familiar.
Muchas son las preocupaciones que estos padres tienen con respecto al futuro de su hijo, particularmente los tratamientos necesarios para resolver la enfermedad, su pronóstico, la afectación que tendrá en la vida cotidiana del niño, la calidad que tendrá su vida y también las preocupaciones de índole económica, que es una realidad práctica y palpable. Es muy importante promover la comunicación de tal manera que estas dudas tengan respuesta y en lo posible responderlas cuando se presenten.
La manera en la que los padres responden e interactúan entre sí y con su hijo son determinantes en la formación de su autoconcepto, la confianza en sí mismos y los otros y el despliegue de sus relaciones sociales. Si un niño se siente valioso para su familia, esta sensación de valor se convertirá en la base sobre la cual el niño responderá a lo que le ocurra.
Muchos niños desarrollan sentimientos de culpabilidad por causar a sus padres angustia, dificultades o exigencias económicas. El egocentrismo natural y esperable del niño opera en estos casos en su contra y la preocupación por el dolor de los padres se convierte en una carga difícilmente tolerable. Cuando identificamos esta dinámica, es muy importante comunicarla a los padres para que puedan desmentir esta creencia y realizar una intervención de manera que los padres se conviertan en la autoridad y guía en la vida del niño.
La relación entre hermanos es una relación intensa, conviven mucho tiempo juntos, viven y despiertan juntos, comparten padres y casa, juegos, a veces juguetes y otros miembros de la familia. Es una relación compleja porque pueden ser protectores, cariñosos y solidarios, y a la vez agresivos, resentidos o hasta crueles.
La rivalidad fraterna es un fenómeno natural y universal en las familias. La llegada de un hermano despierta siempre temores de sustitución o desplazamiento, todos los hermanos se han quejado más de una vez que al otro se le da más, algo más bonito, más atención, más cariño, etcétera; sea cierto o no, esta vivencia es real para ellos. Esta sensación de quedarse en desventaja puede verse acrecentada al tener un hermano que requiere mayor atención y tiempo que un hermano sano.
Algunas de las reacciones emocionales más comunes en los hermanos del niño enfermo son:
- Preocupación por lo que su hermano sufre.
- Miedo a la muerte de su hermano.
- Celos de la atención recibida por el enfermo.
- Culpa. Tiene su origen en la rivalidad fraterna y está relacionada con el hecho de haber albergado sentimientos agresivos o de rechazo hacia su hermano.
Informar a los hermanos de lo que ocurre, qué es la enfermedad, qué ocurrirá para tratarla, qué medidas se tomarán en el futuro, es muy importante. Asimismo, incluirlo en esta nueva dinámica resulta vital: se debe evitar la sensación de separación y aislamiento y no hay que olvidar que los hermanos están también preocupados y angustiados por lo que le ocurrirá al enfermo. Es recomendable ofrecerles explicaciones adecuadas para la edad y promover visitas al hospital.
EL HOSPITAL:
Toda estancia en el intrahospitalaria es una fuente de angustia tanto para el niño como para su familia, y requiere de una reorganización que puede ser emocionalmente difícil. En el hospital, los niños se enfrentan a un ambiente poco predecible y a los reglamentos institucionales, están rodeados de personas que probablemente no conocen, angustiados por los procedimientos a los que serán sometidos y se encontrarán en un estado de relativa inmovilidad y en un ambiente desconocido.
Los niños que ya han sido hospitalizados previamente recuerdan de manera inevitable eventos desagradables o dolorosos de sus anteriores estancias.
Conocer tanto al niño como a la familia es una función primordial del psicólogo de enlace y le permite proporcionar soluciones y respuestas a dudas y temores. Al entrevistar a los niños y sus familias, es importante recabar información con respecto a la historia de la enfermedad identificando cuál es la interpretación que el niño y la familia hacen de esta, sus síntomas y la información que han obtenido. La relación comprende también el desarrollo de una alianza de trabajo en la que la familia se sienta apoyada y comprendida y promover la confianza en el personal médico. Es importante enfatizar que la familia es una parte importante del equipo de trabajo con el objeto de crear un ambiente de respeto y confianza mutuos.
La actitud general de las familias de pacientes hospitalizados es de agrado y cooperación frente al psicólogo, porque abre un espacio de expresión de ideas y comprensión de sentimientos. Entrevistarse periódicamente con los padres y con el niño permite crear un ambiente en el que se ventilan dudas, temores, posibles soluciones, y se permite crear una estrategia en la cual la estancia hospitalaria sea lo más llevadera posible, se identifiquen las fortalezas del niño y la familia y que éstas se pongan en juego para recurrir a ellas y poder recuperarse.
En el hospital, los padres son un modelo a seguir para el niño: si se muestran confiados, el niño confiará, si se muestran angustiados, el niño reaccionará de la misma manera. Dentro del hospital, todos debemos reconocer el esfuerzo que la familia hace por tolerar y manejar sus temores, por desplegar actitudes de ayuda a su niño y por apegarse a las rutinas hospitalarias.
En situaciones difíciles, recurrir al humor puede ser una buena medida para descargar la angustia y poder reírnos de nosotros mismos. El ser ocurrentes, contar o recordar situaciones graciosas, hacer parodias, imitar voces o personas, tomar fotografías divertidas puede ayudarnos a recuperarnos de los malos ratos.
Una de las principales funciones del psicólogo en la sala pediátrica es la de la preparación previa para los procedimientos médicos y la hospitalización misma, con el objetivo de que ésta sea lo menos traumática posible. La preparación para la hospitalización y el tratamiento debe incluir:
- Proporcionar información al niño (de acuerdo a su edad y con el vocabulario adecuado).
- Alentar la expresión emocional y promover la adaptación.
- Establecer una relación de confianza con el psicólogo y con el personal hospitalario.
Al proporcionar información se atenúan las fantasías de los niños y disminuye la ansiedad; dando la información necesaria, prevenimos también malas interpretaciones. La imaginación puede llevar a los niños a desarrollar fantasías terroríficas que serán mucho más atemorizantes que lo que ocurre en la realidad.
El comprender los aspectos psicológicos de la enfermedad y los sentimientos despertados por la hospitalización hará que los niños se sientan más comprendidos y los padres entiendan la conducta de su hijo, dándole así espacio y tiempo para ventilar sus temores y evitando que recurra a defensas rígidas o al aislamiento.
La preparación tiene como objetivo atenuar fantasías, dar salida a las emociones y encaminar el proceso de elaboración, además de llegar a la cirugía con menor ansiedad y tratar de prevenir cicatrices emocionales y alteraciones en el autoconcepto y esquema corporal.
Cuando hablamos con un niño de lo que le ocurrirá, hay que hacerlo de manera honesta: conocer malas noticias puede ser difícil, pero no hay nada peor que el ocultamiento y la evasión. Cuando un niño es hospitalizado, debemos evitar las sorpresas, los niños necesitan sentir que pueden confiar en los adultos que los están cuidando y tienen derecho a saber lo que les ocurrirá.
En la preparación psicológica, las metas clínicas se concentran en:
- La eliminación de defensas patológicas y la elección de otras más adaptativas.
- El análisis y corrección de ideas distorsionadas.
- La preparación para los procedimientos.
- La prevención del trauma postoperatorio y la adaptación al hospital.
- Los procedimientos y la separación de la familia.
Al proporcionarle información al niño es importante considerar lo siguiente:
- Determinar lo que el niño ya sabe.
- La información que ya ha obtenido de su médico y la que le proporcionaremos para su cuidado emocional debe ser discutida primero con los padres; ellos pueden darnos información valiosa y a su vez el poder de decisión acerca de qué, cuánto y cómo decírselo.
- Tener en cuenta aspectos como su edad, nivel de desarrollo y diagnóstico.
- Proporcionar la información al ritmo que sea más cómodo para el niño, ir por pasos, dejar que el niño nos guíe en este sentido.
- Es importante utilizar un lenguaje llano, comprensible, y si su edad lo permite, explicar la terminología médica. Proporcionar información debe ser un proceso cálido, no solemne y, si es posible, hacerlo de manera creativa.
- Dar información de forma ordenada, estructurada y clara, especificando el orden en el que ocurrirán las cosas. Observar la reacción del niño ante cada parte de esta información.
- Darle tiempo suficiente para comentar juntos lo conversado y despejar dudas. Darle al niño una participación activa para hablar, dibujar, moldear, preguntar.
- Utilizar dibujos, esquemas, maquetas, fotos, videos, muñecos para jugar y material hospitalario al dar información.
- Llevar al niño al lugar físico donde ocurrirán los procedimientos y la hospitalización.
- Tener la certeza de que lo ha entendido.
- Actualizar constantemente la información.
- Tener en cuenta a los pacientes que acuden de otras partes del mundo: cultura, religión, idioma…
- Desarrollar un ambiente interdisciplinario de cooperación. Registrar las entrevistas con el niño y su familia.
Una buena preparación ayuda al niño a organizar sus pensamientos, sentimientos y acciones acerca de un evento antes de que éste ocurra. Le da al niño la oportunidad de ensayar mentalmente lo que piensa que le ocurrirá y a sentir lo pertinente, es decir, preocuparse, imaginar cosas, pensar en preguntas, hablar de sus dudas, obtener respuestas. La preparación proporciona a los niños y a sus padres una sensación de mayor control de la situación ante la cual frecuentemente se sienten impotentes.
Algunos padres piensan que la preparación puede ser contraproducente porque mientras menos sepan los niños, estarán menos ansiosos, o porque piensan que no es necesario preocuparlos. Debemos recordar a esos padres que no hay miedo más desorganizador que el miedo a lo desconocido, y que, si el niño no obtiene información, llenará esas lagunas con fantasías. En la mayoría de las ocasiones, no es necesario entrar en detalles acerca de los procedimientos, pero es beneficioso para los niños conocer de manera general qué les ocurrirá, explicar por qué es necesario el procedimiento, lo que sentirán, dónde ocurrirá, quién estará, etcétera.
Los niños no preparados viven de manera traumática los procedimientos y sufren elevados niveles de ansiedad, además de que padecen cada minuto en el hospital porque no pueden desplegar sus capacidades de adaptación. La preparación es también importante para poder comunicarles a los niños lo que se espera de ellos, por ejemplo, quedarse quietos un momento para cierto procedimiento. No hay que decirle a un niño que necesita ser valiente (de hecho ya lo es) o que no llore, puede hacer el ruido que quiera si es capaz de cooperar en ese momento.
EL PSICÓLOGO DE ENLACE:
Muchos miembros del hospital pueden ayudar a los niños en el cuidado emocional durante su enfermedad u hospitalización, pero los profesionales de la salud mental tienen a su favor un mayor conocimiento de este aparato y el entrenamiento necesario para poner en juego este conocimiento, diseñar técnicas e intervenciones terapéuticas, traducir síntomas en explicaciones e identificar los conflictos para encontrarles solución.
El proceso de ayudar a los niños se refiere básicamente a comunicarse de manera efectiva con ellos. Implica saber escuchar y llegar juntos a la comprensión de un problema, en este caso su enfermedad. Implica a su vez ayudar a los niños a desarrollar ellos mismos estrategias para superar las dificultades, y echar a andar sus capacidades para contender y manejar de la mejor manera lo que les sucede.
Ayudar al niño enfermo u hospitalizado implica enseñarle a compartir lo que ocurre en su interior, sus miedos, ideas, pensamientos, sentimientos, y hacerlos sentir comprendidos. El objetivo principal de este proceso es capacitar al niño a desarrollar sus propias estrategias de solución y, en consecuencia, ayudarse a sí mismo y sentirse en mayor control de lo que ocurre.
Ayudar a un niño significa darle la oportunidad de expresar lo que vive y siente, explorarlo de manera amplia y diseñar objetivos a alcanzar. Implica indagar sus percepciones y construcciones acerca de su enfermedad y su mundo, y ayudar a clarificarlas y, si es necesario, cambiarlas cuando no son útiles o son falsas.
Ambos podrán en juego en esta relación sus habilidades y capacidades, así como sus preocupaciones e inteligencia, de manera que la hospitalización sea para el niño lo menos traumática posible.
CONCLUSIONES:
Al trabajar con los niños con cardiopatía congénita y sus familias, debemos apegarnos al principio de que deben ser respetados en todos sentidos y que su perspectiva debe ser tomada en cuenta ante cualquier procedimiento y decisión. Los niños enfermos y sus familias merecen ser tratados con dignidad y consideración. Aun cuando en múltiples ocasiones no podemos evitarles el dolor tanto físico como emocional, no cometamos el error de subestimar su fortaleza.
Lo que nos toca hacer es proporcionar a los niños un espacio para hablar, dibujar y jugar, y nosotros por nuestra parte escuchar atenta, muy atentamente lo que nos dicen y actuar en consecuencia.
El objetivo de trabajar con la familia es disminuir la centralidad y protagonismo del niño enfermo: todos los miembros de la familia son igualmente importantes y todos tendrán diferentes necesidades. El disminuir su centralidad ayuda al niño enfermo a sentirse parte de su familia, no la causa o el determinante de la angustia, y les permite a todos desplegar sus propias capacidades en el proceso de volver a encontrar la salud. Las cicatrices emocionales siempre llevan mucho más tiempo de elaboración que las físicas.
El psicólogo de enlace tiene una función integradora, de elaboración y comunicación, y busca favorecer el reconocimiento de los aspectos emocionales, las reacciones psicológicas a la enfermedad y el establecimiento de estrategias de solución buscando siempre el bienestar emocional de los niños enfermos.
BIBLIOGRAFÍA
- Adewale L. Anatomy and assessment of the pediatric airway. Pediatric Anesthesia 2009;19:1-8.
- Aicardi J. Diseases of the nervous system in childhood. 1992;115:0.
- Alonso AR, Molina C, Amores M. Patología pulmonar crónica. Pedi ía ntegral atr I 2021:101
- Álzate Gallego ED, Correa Salazar S. Caracterización clínica y sociodemográfica de pacientes pediátricos con sospecha de ingestión o aspiración de cuerpo extraño. Departamento de Cirugía 2016.
- Anta MZ. Semiología respiratoria. Pediatría Integral 2016;6:63.
- Aragonés Manzanares Rocío, Rincón Ferrari Maria Dolores. Manual de Cuidados Intensivos para Enfermería. España: Panamericana; 2020.
- Ares MIA. Técnicas y procedimientos para enfermería en urgencias pediátricas. : Editorial Médica Panamericana; 2019.
- Aroca Á, Polo L, Bret M, López-Ortego P, González Á, Villagrá F. Drenaje venosa pulmonar anómalo total. Técnicas y resultados. Cirugía Cardiovascular 2014 -04;21(2):90.
- Asenjo CA, Pinto RA. Características anátomo-funcional del aparato respiratorio durante la infancia. Revista Médica Clínica Las Condes 2017;28(1):7-19.
- Attie F, Calderón Colmenero J, Zabal Cerdeira C, Buendía Hernández A. Cardiología pediátrica. Médica Panamericana; 2013.
- Barrio MI, Antelo C. Enfermedad respiratoria. Anales de Pediatría Continuada 2008;6(2):59-64.
- Benito Javier. Urgencias Pediátricas. España: Panamericana; 2019.
- Casado Flores J, de Quero Masía PG, Fernández YL. iii curso intensivo para residentes de cuidados intensivos Pediátricos. 2011.
- Cases GS, Aragonés C, Toya AA, Carreño GM, Peiró M. Dispositivos y guía de administración vía inhalatoria. Rev OFIL 2017;27(1):31-46.
- Cid JL. Manual de cuidados intensivos pediátricos. : Publimed; 2019.
- Cooper LT. Definition and classification of the cardiomyopathies. UpToDate 2022.
- Drake RL, Vogl AW, Mitchell AM. Gray. Anatomía para estudiantes. Elsevier Health Sciences; 2020.
- Del Arco FS. Manual de ventilación mecánica para enfermería. : Editorial Médica Panamericana; 2017.
- De la Hoz GV, Aedo IF, Peña SB. Manual práctico de enfermería de cuidados intensivos: guía rápida para estudiantes de enfermería en prácticas. : Servicio Editorial de la Universidad del País Vasco; 2020.
- Desiderio MJZ, Llerena MFC, Morán BAV, Soledispa MMD. Proceso de atención en enfermería en niños y niñas con enfermedades respiratorias. Dominio de las Ciencias 2022;8(3):52-65.
- Donoso A, Arriagada D, Contreras D, Ulloa D, Neumann M. Monitorización respiratoria del paciente pediátrico en la Unidad de Cuidados Intensivos. Boletín médico del Hospital Infantil de México 2016;73(3):149-165.
- Drake RL, Vogl AW, Mitchell AM. Gray. Anatomía para estudiantes.: Elsevier Health Sciences; 2020.
- Fernández JB, Paniagua Calzón N. Diagnóstico y tratamiento de la bronquiolitis aguda en urgencias. Protoc diagn ter pediatr 2020;1:63-73.
- Galindo CG, Hernández SSF, Pérez-Redondo CN. Diferencias anatomofuncionales y endoscópicas entre la vía aérea del niño y la del adulto. Revista del Instituto Nacional de Enfermedades Respiratorias 2007;20(2):142-148.
- García-Hernández AL, García-Hernández MN. Plan de cuidados pediátrico individualizado en lactante con proceso respiratorio agudo. Ene 2022;16(2).
- Gómez Guzmán E, Tejero Hernández MA, Pérez Navero JL. Tratamiento actual de la insuficiencia cardiaca pediátrica. Cardiocore 2013 -01;48(1):12.
- González Brabin A., García Teresa M.A., García-Salido A. Oxigenoterapia. Pediatría Integral 2021; XXV (1): 37 – 43 .
- Gordon N. Neurological problems in childhood.: Butterworth-Heinemann; 2013.
- Guerrero-Fernández J, Sánchez AJC, Bonis ACB, Suso JM, Domínguez JR. Manual de diagnóstico y terapéutica en Pediatría. ; 2018.
- Herramienta online para la consulta y diseño de Planes de Cuidados de Enfermería. NNNConsult. Elsevier. 2015.
- Hockenberry MJ, Rodgers CC. Wong. Enfermería Pediátrica.: Elsevier; 2019.
- Imazio M. Acute pericarditis: Treatment and prognosis. UpToDate 2024.
- Imazio M. Acute pericarditis: Clinical presentation and diagnosis. UpToDate 2023.
- La web de las Cardiopatías Congénitas. Available at: https://cardiopatiascongenitas.net/.
- Laso EL, González MEM. Tumores cerebrales infantiles, semiología neurológica y diagnóstico. Protocolos diagnósticos y terapias en neurología pediátrica 2022;1:151-158.
- López-Herce J, Carrillo Á. Ventilación mecánica: indicaciones, modalidades y programación y controles. Anales de Pediatría Continuada 2008;6(6):321-329.
- Madrid PCCA. Servicio de Neurología. Hospital Infantil Universitario Niño Jesús. Universidad Autónoma de Madrid. Madrid. anna. duat@ salud. madrid. org.
- Martínez-Serrano A, Martínez-Campos P, Seijoso-González L, Ruiz-Rojo H. Revisión narrativa de la técnica de los lavados nasales en pediatría. Enfermería Clínica 2021;31(3):189-194.
- Martinón-Torres, F., de la Rosa, I. I., Sanmartín, M. F., Menor, E. G., & Sánchez, J. M. Ventilación de alta frecuencia. In Anales de Pediatria (Vol. 59, No. 2, pp. 172-180). Elsevier Doyma.(2003, January).
- Medina Perez M, Lichtenberger JP, Huppmann AR, Gomez M, Ramirez Suarez KI, Foran A, et al. Cardiac and Pericardial Neoplasms in Children: Radiologic-Pathologic Correlation. Radiographics 2023 -09;43(9): e230010.
- Menchón, N. M., Palacios, E. I., & i Alapont, V. M. Ventilación mecánica en el estado asmático. In Anales de Pediatría (Vol. 59, No. 4, pp. 352-362). Elsevier Doyma. (2003, January).
- Millet, P. R., & Bonet, J. M. Intubación, sedación y adaptación a la ventilación mecánica. In Anales de Pediatría (Vol. 59, No. 5, pp. 462-472). Elsevier Doyma. (2003, January).
- Monge RMB, Corullón SC, Fernández AJA. Tos húmeda: bronquitis bacteriana persistente, enfermedad supurativa bronquial y bronquiectasias. Protocolos diagnósticos y terapéuticos en Neumología pediátrica 2017.
- Mullen MP. Pulmonary hypertension in children: Classification, evaluation, and diagnosis. UpToDate 2023.
- O´Brien SE. Infective endocarditis in children. UpToDate 2023.
- Orive FJP, Fernández YML, UCIP EMA. Oxigenoterapia de alto flujo. Anales de Pediatría Continuada 2014;12(1):25-29.
- Oyagüez-Ugidos PP, Blanco-Gómez I, García-González M, Alonso-Álvarez ML. Papel de la unidad de cuidados intensivos pediátricos en la evaluación y soporte del paciente con patología de la vía aérea.¿ Cómo lo hacemos? 2018.
- Pastor D, Perez S, Rodriguez J. Fracaso respiratorio agudo y crónico. Oxigenoterapia. Protocolo, diagnostico, terapia pediatrica 2017;1:369-399.
- Pérez CV, Navarro TA, Aurrecoechea BD, Valcarce MÁF. Monográfico Respiratorio (1). 2015.
- Pérez LO, Álvarez JA, Pérez RP. Faringoamigdalitis aguda y sus complicaciones.
- Perin F, Rodríguez Vázquez del Rey MM, Carreras Blesa C. Cardiología pediátrica para residentes de pediatría. Educatori; 2023.
- Puñal Riobóo J, Varela Lema L. Efectividad y seguridad del dispositivo de asistencia ventricular izquierda (DAVI) como terapia de destino en edad pediátrica. Ministerio de Sanidad 2020.
- Protocolos diagnósticos y terapéuticos en Pediatría | Asociación Española de Pediatría.
- Redondo, P. Clasificación de las anomalías vasculares (tumores y malformaciones): características clínicas e historia natural. In Anales del sistema sanitario de Navarra (Vol. 27, pp. 09-25)(2004). Gobierno de Navarra. Departamento de Salud.
- Rey CC, García MG, Flecha IC, Breña PP. Infecciones respiratorias virales. Protocolos de Infectología Asociación Española de Pediatría Sociedad Española de Infectología Pediátrica 2011:189-204.
- Rosner MJ. Cerebral perfusion pressure: Link between intracranial pressure and systemic circulation. In: J.H. (ed), editor. Cerebral Blood Flow. Physiological and Clinical Aspects New York: McGraw-Hill Company; 1987. p. 425-448.
- Rubio F, Melgosa M. Hipertensión arterial. Anales de pediatría continuada 2009;7(2):70–8.
- Sánchez T, Concha I. Estructura y funciones del sistema respiratorio. Neumologia pediatrica 2018;13(3):101-106.
- Sánchez De Toledo J, Balcells J. Asistencia ventricular pediátrica: una realidad asistencial con un futuro alentador. Anales de Pediatría 2012 -03;76(3).
- Steer AG, A. Acute rheumatic fever: Clinical manifestations and diagnosis. UpToDate 2024.
- Steer AG, A. Acute rheumatic fever: Treatment and prevention. UpToDate 2024.
- Snell RS. Neuroanatomía clínica. : Ed. Médica Panamericana; 2007.
- Silverthon DE. Fisiología humana: un enfoque integrado. 4th ed. Madrid: Panamericana; 2008.
- Sánchez-Manubens J. Enfermedad de Kawasaki. Protoc diagn ter pediatr. 2020(2):213–224.
- Talamillo T. Manual básico para enfermería en electroencefalografía. Enfermería Docente [Internet] 2011;94:29-33. [Acceso: 23/09/2017]. Disponible en: http://www.juntadeandalucia.es/servicioandaluzdesalud/huvvsites/default/files/revistas/ED-094-07.pdf.
- Torres EB, Pérez CA. Anomalías vasculares. Pediatr Integral. 2021;25:128. e1-128. e22.
- Toro-Moreno AC, Serna-Velez L, Gallego-González D, Jaramillo-Jaramillo LI, Martínez-Sánchez LM, Álvarez-Hernández LF. Tumores de sistema nervioso central en pediatría: Presente y futuro del abordaje diagnóstico. Revista Ecuatoriana de Neurología 2017;26(3):283-288.
- Tuñón AL. Ingesta-aspiración de cuerpo extraño. Protoc diagn ter pediatr 2020;1:339-355.
- Valderrama P, Carugati R, Sardella A, Flórez S, de Carlos Back I, Fernández C, et al. Guía SIAC 2024 sobre rehabilitación cardiorrespiratoria en pacientes pediátricos con cardiopatías congénitas. Revista Española de Cardiología 2024.
- Victor Monreal E, Yuri Zuleta M, Ema Reyes S, Evelyn Palominos L. ECMO PEDIÁTRICO. UNA PUESTA AL DÍA. Neumología pediátrica 2020;14(1):34–40.
- Vergnaud E, Terzi E, Blauwblomme T, Naggara O, Boulouis FG, Meyer PG. Malformaciones vasculares cerebrales en niños. EMC-Pediatría 2023;58(2):1-12.
- Zamorano AV, Méndez MP. Bronquiolitis aguda: tratamiento de la insuficiencia respiratoria. Neumología Pediátrica 2020;15(1):251-256
